培元颗粒质量初步研究
黄依鸣,李宛蓉,王 键,2,桂双英,2,3
(1.安徽中医药大学,安徽 合肥 230012;2.新安医学教育部重点实验室,安徽 合肥 230012;3.安徽省中医药科学院药物制剂研究所,安徽 合肥 230012)
·方药研究·
培元颗粒质量初步研究
黄依鸣1,李宛蓉1,王键1,2,桂双英1,2,3
(1.安徽中医药大学,安徽 合肥230012;2.新安医学教育部重点实验室,安徽 合肥230012;3.安徽省中医药科学院药物制剂研究所,安徽 合肥230012)
[摘要]目的建立培元颗粒的质量标准。方法采用薄层色谱法对培元颗粒中人参、黄芪、淫羊藿进行定性鉴别,采用高效液相色谱-蒸发光散射检测法测定培元颗粒中人参皂苷Rb1与黄芪甲苷的含量。色谱柱为Phenomenex C18(250 mm×4.6 mm,5 μm),流动相为乙腈-水(梯度洗脱),流速为1.0 mL/min,柱温为30 ℃。蒸发光散射检测器的漂移管温度为100 ℃,雾化温度为30 ℃。结果薄层色谱法能检出人参、黄芪、淫羊藿,斑点清晰,且阴性对照无干扰;人参皂苷Rb1和黄芪甲苷分别在2.46~20.5 μg/mL、1.54~7.69 μg/mL范围内与峰面积线性关系良好,平均加样回收率分别为96.84%、97.58%,RSD分别为1.15%、1.34%。结论所建立的方法操作简单,重复性好,可以用于培元颗粒的质量控制。
[关键词]培元颗粒;质量标准;薄层色谱法;高效液相色谱法
培元颗粒是根据新安医家汪机的“培本固元”理论,在孙一奎“壮元汤”的基础上加减而成[1-3],由人参、黄芪、淫羊藿等中药组成,具有固本培元、温阳益气之功效。原方为汤剂,本课题组采用现代提取与制剂技术研制了培元颗粒[4]。为更好地控制制剂质量,本试验开展培元颗粒的质量研究。
1 仪器与试药
1.1仪器Agilent 1260型高效液相色谱仪:包括G1312C二元泵、G1316A柱温箱、G1329B自动进样器、二极管阵列检测器G4212B、ChemStation色谱工作站; SHB-Ⅲ循环水式多用真空泵:河南省郑州长城科工贸有限公司;DNP-9052型电热恒温培养箱:上海市三发科学仪器有限公司;UV757CRT紫外分光光度计:上海精科有限公司;DZF-2002真空干燥箱:上海浦东荣丰科学仪器有限公司。
1.2材料人参、黄芪、淫羊藿等饮片购于安徽省亳州药材市场,经安徽中医药大学周建理教授鉴定均为合格饮片;培元颗粒(自制);阴性样品溶液(自制);薄层层析用硅胶G板、H板:山东省青岛海洋化工厂。人参皂苷Rb1对照品(批号 110704-201223)、人参皂苷Re对照品(批号 110754-201324)、淫羊藿苷对照品(批号 110737-200415)、黄芪甲苷对照品(批号 110781-200613):中国食品药品检定研究院。
2 方法与结果
2.1薄层鉴别[5-8]
2.1.1人参的薄层鉴别取本品颗粒5 g,研细,加氯仿40 mL回流1 h,弃去氯仿液,药渣挥干溶剂,加入水2 mL搅拌湿润,加入水饱和正丁醇20 mL,振摇,取正丁醇液蒸干,加甲醇2 mL使溶解制成样品溶液;另取缺人参阴性颗粒5 g,同法制成阴性样品溶液;取人参皂苷Rb1、人参皂苷Re对照品,加甲醇制成1 mg/mL的混合对照溶液。分别精密吸取上述3种溶液各5 μL,点于硅胶G薄层板上,采用氯仿-乙酸乙酯-甲醇-水(15∶40∶22∶10)下层液展开,以10%硫酸乙醇溶液为显色剂,105 ℃加热至斑点清晰,日光灯检视。结果在与对照品相应的位置上,3批样品溶液显示相同颜色的斑点,而阴性样品无干扰,结果见图1。
2.1.2黄芪的薄层鉴别[9]取本品颗粒5 g,研细,加甲醇40 mL回流1 h,滤过,滤液采用中性氧化铝柱(100~200目)纯化:以40%甲醇洗脱,收集洗脱液100 mL,蒸干后加水40 mL使溶解;以水饱和正丁醇(1∶1)萃取2次,收集正丁醇液,用水洗涤2次;收集正丁醇层,蒸干,残渣加甲醇1 mL使溶解制成样品溶液;另取缺黄芪阴性颗粒5 g,同法制成阴性样品溶液;取黄芪甲苷对照品适量,加甲醇制成1 mg/mL的对照品溶液。分别吸取上述3种溶液各10 μL,点于硅胶G板上,采用氯仿-甲醇-水(13∶7∶2)下层液展开,以10%硫酸乙醇溶液,105 ℃加热至斑点清晰,日光灯和紫外光灯(365 nm)下检视。结果在与对照品相应的位置上,3批样品日光下显示相同的棕褐色斑点;紫外光灯(365 nm)下显示相同的橙黄色荧光斑点,而阴性样品无干扰。结果见图2。
2.1.3淫羊藿的薄层鉴别取本品颗粒5 g,研细,加水60 mL,超声处理20 min,滤过,滤液加水饱和正丁醇振摇提取2次,每次20 mL,正丁醇层以氨水洗涤2次,收集正丁醇液蒸干,残渣加甲醇1 mL使溶解,制成样品溶液;另取缺淫羊藿阴性颗粒5 g,同法制成阴性样品溶液;取淫羊藿苷对照品适量,加甲醇制成0.23 mg/mL的对照品溶液。分别吸取上述3种溶液各10 μL,点于硅胶H板上,采用乙酸乙酯-丁酮-甲酸-水(10∶1∶1∶1)展开,以三氯化铝溶液为显色剂,紫外灯(365 nm)下检视。结果在与对照品相应的位置上,3批供试品显示相同颜色的斑点,而阴性样品无干扰。结果见图3。
2.2含量测定[10-11]
2.2.1色谱条件色谱柱:Phenomenex C18(250 mm×4.6 mm,5 μm);流动相:乙腈-水,梯度洗脱;流速:1.0 mL/min;柱温:30 ℃;漂移管温度:100 ℃;雾化温度:30 ℃;进样量:20 μL。
2.2.2对照品溶液的制备精密称取人参皂苷Rb1、黄芪甲苷对照品,加甲醇分别制成0.820 mg/mL人参皂苷Rb1、0.308 mg/mL黄芪甲苷的混合对照品溶液,摇匀,即得。

注:1-3为培元颗粒样品,4为人参皂苷Rb1、Re对照品,5为阴性样品。图1 人参薄层色谱图 注:1-3为培元颗粒样品,4为黄芪甲苷对照品,5为阴性样品。图2 黄芪薄层色谱图 注:1-3为培元颗粒样品,4为淫羊藿苷对照品,5为阴性样品。图3 淫羊藿薄层色谱图
2.2.3供试品溶液的制备取本品颗粒10.0 g,精密称定,置具塞锥形瓶中,精密加入纯化水80 mL,密塞,称定质量,超声20 min,冷却后称定质量,以纯化水补足减失的质量,滤过,以水饱和正丁醇(1∶0.5)萃取4次,合并正丁醇液,以10%氨水洗涤2次,每次25 mL,收集正丁醇液蒸干,以50%甲醇溶解定容至5 mL,微孔滤膜(0.22 μm)滤过,取续滤液,即得。
2.2.4阴性样品溶液的制备分别取缺人参阴性样品和缺黄芪阴性样品,依法制备阴性样品溶液。
2.2.5系统适应性试验分别精密吸取对照品溶液、供试品溶液、阴性样品溶液各10 μL,按“2.2.1”项下色谱条件依法测定。结果在对照品色谱相应位置上,供试品溶液具有相同保留时间的色谱峰,阴性样品在此峰位无吸收。见图4。
2.2.6线性关系考察分别精密吸取混合对照品溶液3、5、10、12、15、20、25 μL,注入液相色谱仪中,按“2.2.1”项下色谱条件依法测定,记录峰面积。以峰面积的自然对数值(y)对进样量的自然对数值(x)进行线性回归,得人参皂苷Rb1的回归方程为y=1.283 5x+5.023 6(r=0.999 3),黄芪甲苷的回归方程y=1.508 9x+5.207 7(r=0.999 4)。结果表明,人参皂苷Rb1和黄芪甲苷分别在2.46~20.5 μg/mL、1.54~7.69 μg/mL范围线性关系良好。
2.2.7精密度试验精密吸取混合对照品溶液10 μL,连续进样6次,按“2.2.1”项下色谱条件依法测定,记录峰面积,计算RSD,结果人参皂苷Rb1与黄芪甲苷的RSD分别为0.98%、1.10%,表明该方法精密度良好。
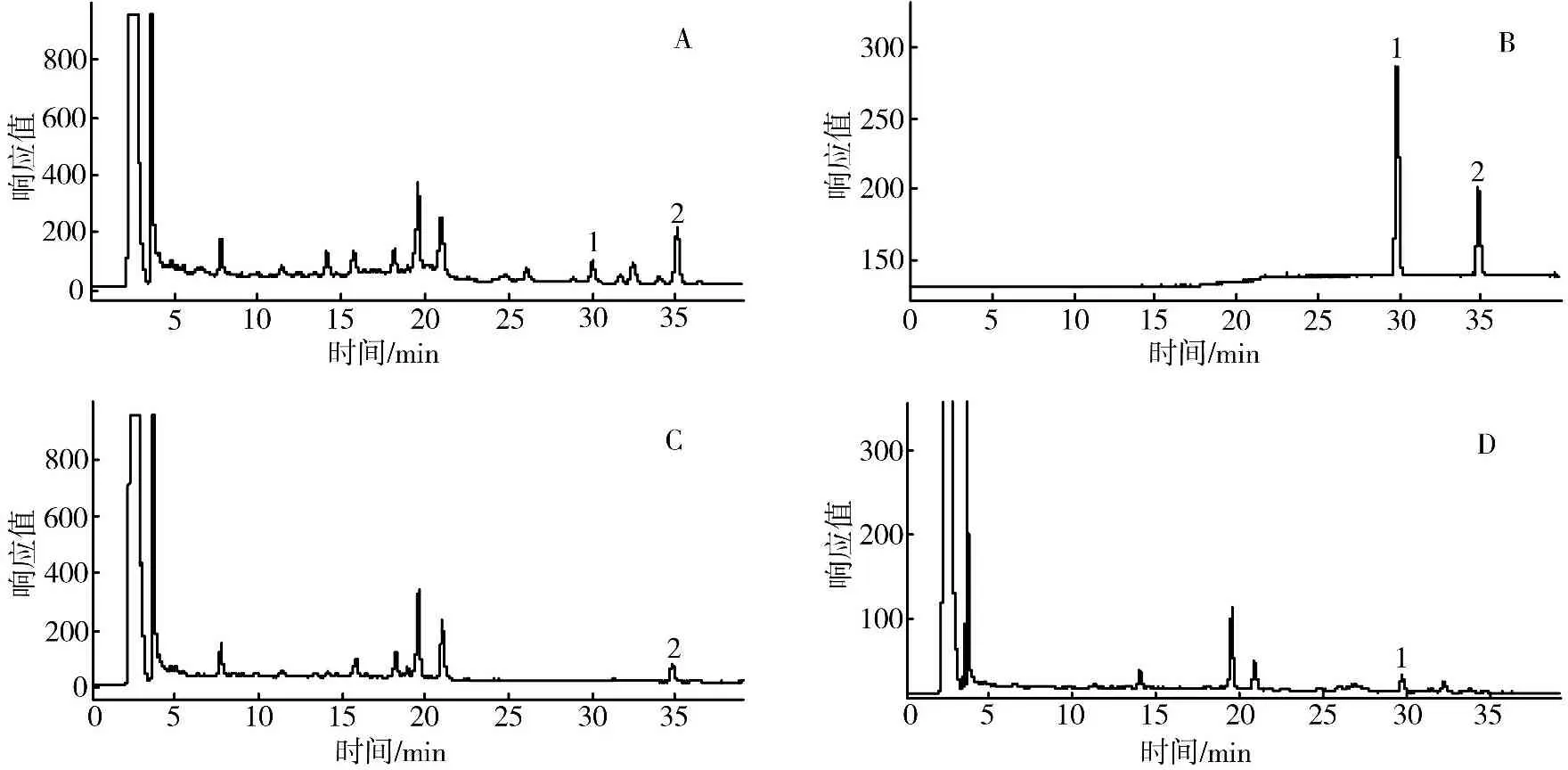
图4 样品(A)、对照品(B)、缺人参样品(C)和缺黄芪样品(D)的高效液相色谱图(1.人参皂苷Rb1;2.黄芪甲苷)
2.2.8重复性考察取同一批样品6份,按“2.2.3”项下方法制备样品溶液,依法测定人参皂苷Rb1与黄芪甲苷的峰面积,计算其RSD分别为1.30%、1.53%,表明本方法重复性良好。
2.2.9稳定性试验 取同一供试品溶液,分别于0、4、8、12、24 h进样,依法测定人参皂苷Rb1与黄芪甲苷的峰面积,计算其RSD分别为1.85%、2.14%,表明供试品溶液在24 h内基本稳定。
2.2.10加样回收率试验取已知含量的同一批样品5.0 g,6份,精密称定,分别加入人参皂苷Rb1与黄芪甲苷对照品溶液适量,按“2.2.3”项下方法制备样品溶液,测定人参皂苷Rb1和黄芪甲苷的含量,计算加样回收率,结果见表1。结果人参皂苷Rb1与黄芪甲苷的平均回收率分别为96.84%、97.58%,RSD分别为1.15%、1.34%,表明该方法准确可行。

表1 加样回收率试验结果
2.2.11样品测定分别取自制的10批培元颗粒10 g,精密称定,按“2.2.3”项下方法制备10批样品溶液,分别吸取样品溶液与混合对照品溶液各10 μL,依法测定峰面积,计算各批样品的人参皂苷Rb1与黄芪甲苷含量,结果见表2。
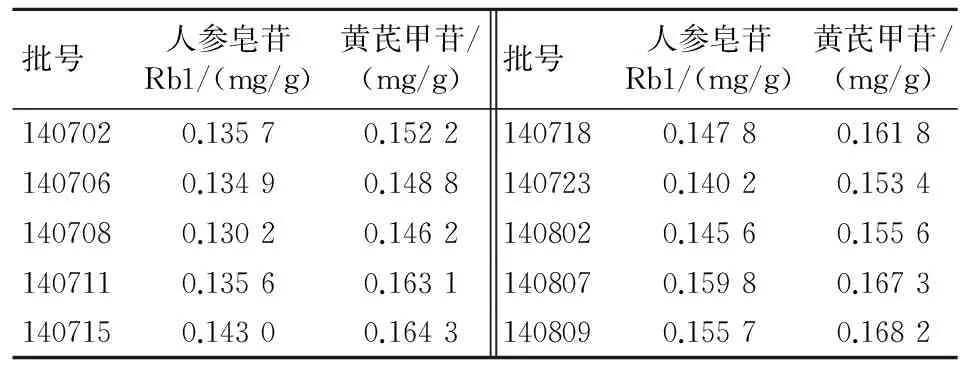
表2 10批样品含量测定结果
3 讨论
3.1超声时间的确定在含量测定中,本试验采用超声提取法制备供试品溶液,考察超声时间的长短对色谱峰的影响。结果超声10 min的样品色谱峰强度较小,而超声20 min和30 min无明显差异,因此,本实验选用超声提取20 min。
3.2流动相的选择在含量测定中,考察了以乙腈-水、甲醇-水、甲醇-0.1%甲酸水为流动相对人参皂苷Rb1和黄芪甲苷分离度的影响。结果表明,选用甲醇-水、甲醇-0.1%甲酸水为流动相时色谱峰分离度不高,而选择乙腈-水溶液作为流动相,各色谱峰分离度高且色谱峰基线平稳。因此,本实验选用乙腈-水溶液作为流动相。
3.3梯度洗脱本实验采用超声提取法制备供试品溶液,超声提取所得的供试品成分复杂,选用梯度洗脱能使人参皂苷Rb1和黄芪甲苷两个化合物峰型好,出峰时间早,分离度高。
参考文献:
[1]张倩,牛淑平.新安医家汪机、孙一奎“固本培元”学术流派研究[J].中医学报,2012,27(6):697-699.
[2]王键,黄辉,蒋宏杰.新安固本培元派扶阳理论与临床应用研究[J].安徽中医药大学学报,2014,33(1):15-18.
[3]张倩,牛淑平.孙一奎壮元汤医案选介[J].中医文献杂志,2012(4):35-37.
[4]李宛蓉,桂双英,王举涛,等.复方培元颗粒的提取工艺研究[J].安徽中医药大学学报,2015,34(4):78-81.
[5]国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2010:8,283-284,306-308.
[6]李琼,曾锐,杨学森.参芪胶囊质量标准研究[J].时珍国医国药,2014,25(1):100-102.
[7]杨荣艳,王倩,刘晓秋,等.清毒祛痨丸的薄层色谱鉴别及没食子酸的含量测定[J].中国现代中药,2010,12(8):33-36.
[8]刘薇.益气固摄浓缩丸中黄芪及陈皮的薄层色谱法定性鉴别[J].湖北医药学院学报,2014,33(2):163-164.
[9]阮建兵,邹文哲,金学平.类风湿胶囊质量控制研究[J].中国现代中药,2013,15(4):320-323.
[10]唐露,李希,冯建安,等.HPLC-ELSD法测定舒络颗粒中黄芪甲苷、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].实用中医药杂志,2012,28(11):964-967.
[11]陈祖云,石凌云,黄勇,等.HPLC-ELSD法测定脑通颗粒中黄芪甲苷和人参皂苷Rb1的含量及稳定性[J].中国药房,2011,22(23):2164-2166.
基金项目:科技部十二五科技支撑计划项目(2012BAI26B03)
作者简介:黄依鸣(1994-),女,硕士研究生
通信作者:桂双英,guishy0520@126.com
[中图分类号]R283[DOI]10.3969/j.issn.2095-7246.2016.04.020
(收稿日期:2015-08-28;编辑:张倩)
A Preliminary Study of Quality Control of Peiyuan Granule
HUANGYi-ming1,LIWan-rong1,2,WANGJian1,2,GUIShuang-ying1,2,3
(1.AnhuiUniversityofChineseMedicine,AnhuiHefei230012,China; 2.KeyLaboratoryofXin’anMedicine,MinistryofEducation,AnhuiHefei230012,China; 3.InstituteofPharmaceutics,AnhuiAcademyofChineseMedicine,AnhuiHefei230012,China)
[Abstract]ObjectiveTo establish a quality standard for Peiyuan Granule. MethodsThe qualitative identification of Panax ginseng, Astragalus membranaceus, and Herba Epimedii in Peiyuan Granule was performed by thin-layer chromatography (TLC), and the content of ginsenoside Rb1 and astragaloside in Peiyuan Granule was determined by high-performance liquid chromatography-evaporative light-scattering detection. The analysis was carried out on a Phenomenex-C18column (250 mm × 4.6 mm, 5 μm) with a mobile phase of acetonitrile-water for gradient elution at a flow rate of 1.0 mL/min and a column temperature of 30 ℃. The evaporative light-scattering detector was used at a drift tube temperature of 100 ℃ and an atomizing temperature of 30 ℃. ResultsThe TLC spots of Panax ginseng, Astragalus membranaceus, and Herba Epimedii were clear without interference from the negative control. A good linear relationship with peak area was achieved when the concentrations of ginsenoside Rb1 and astragaloside ranged within 2.46-20.5 μg/mL and 1.54-7.69 μg/mL, and the average recovery rates were 96.84% and 97.58%, respectively, with relative standard deviations of 1.15% and 1.34%. ConclusionThe established method is simple and repeatable to effectively control the quality of Peiyuan Granule.
[Key words]Peiyuan Granule; Quality standard; Thin-layer chromatography; High-performance liquid chromatography

