硅氧烷硫化体系对药用氯化丁基橡胶塞性能的影响
代高峰,黄环宇,刘民英,赵清香,梁明伟
(1.郑州翱翔医药科技股份有限公司,河南 登封 452483;2.郑州大学,河南 郑州 450001)
药用丁基橡胶(IIR)胶塞由于具有较好的气密性、耐热性、耐酸碱性、化学惰性和较高的内在洁净度等特点[1-3],很快取代了天然橡胶(NR)胶塞用于医药包装领域。国外早在20世纪六七十年代就实现了药用胶塞的丁基化,我国也于21世纪初完成了药用胶塞的丁基化[4-5]。如今世界上90%以上的药用胶塞是以IIR为基材生产的。因此,药用胶塞的丁基化已成为全球性不可逆转的趋势。
我国使用药用IIR胶塞已有10余年的历史,所生产的药用IIR胶塞能够满足普通药品的包装需求,但还不能满足一些敏感药剂,如头孢粉针制剂、酸碱性较强制剂等相容性的要求。据报道,IIR胶塞与头孢菌素的相容性较差是造成头孢曲松钠等头孢类产品在有效期内澄清度不合格的主因[6]。国家药监部门对此高度重视,下发了《关于进一步加强使用丁基胶塞的头孢类注射剂监督管理的通知》,中国医药包装协会也下发了关于督促加强药用IIR胶塞质量管理的文件。IIR胶塞与药物相容性差是由从IIR胶塞中迁移到药品中的可提取物与浸出物造成的。因此有必要开发特殊的无锌无硫的硫化体系,以便从根本上避免和减少药用IIR胶塞中的可提取物与浸出物,特别是影响药品相容性的可提取物与浸出物,这也是医药和药品包装材料行业研究的热点和前沿课题。
本工作采用以γ-氨乙基-氨丙基-三乙氧基硅烷为硫化剂的无锌无硫硫化体系制备氯化丁基橡胶(CIIR)胶塞,研究硅氧烷硫化体系的硫化机理及其对CIIR胶料硫化特性、CIIR胶塞提取液澄清度以及CIIR胶塞与头孢类药品相容性的影响。
1 实验
1.1 主要原材料
CIIR,牌号Exxon Chlorobutyl 1066,埃克森美孚化工公司产品;γ-氨乙基-氨丙基-三乙氧基硅烷,南京裕德恒精细化工有限公司产品;头孢曲松钠和注射用头孢替安,福南京海晨药业股份有限公司产品;普通CIIR胶塞和覆聚四氟乙烯膜CIIR胶塞,规格为20-B,郑州翱翔医药科技股份有限公司产品;进口CIIR胶塞,美国西氏公司产品。
1.2 主要设备和仪器
S(X)K-160A型开炼机,上海橡胶机械厂产品;TCY-V-22-2-S-PCD型模压成型机,东毓油压机械股份有限公司产品;UR2010-SD型无转子硫化仪,中国台湾优肯科技股份有限公司产品;GT-7001-F2-PC型微电脑拉力机,中国台湾高铁科技股份有限公司产品;WQF-510A型傅里叶转换红外光谱仪,北京瑞利分析仪器有限公司产品;SHH-250SD型药品稳定性试验箱,重庆永生实验仪器厂产品。
1.3 试样制备
1.3.1 CIIR胶塞
基本配方:CIIR 100,炭黑 0.3,煅烧高岭土 80,钛白粉 4,活性剂 3,硫化剂 变量。
CIIR胶塞的制备:按照配方要求称取配合料在开炼机上进行混炼,用无转子硫化仪测定胶料的t90,根据t90在模压成型机上进行硫化,然后除边清洗包装备用。
1.3.2 CIIR胶塞提取液
取质量约为20 g的CIIR胶塞若干个,放在烧杯中,加入10倍于CIIR胶塞质量的纯化水浸没,煮沸5 min,然后放冷,用纯化水冲洗,每次用10倍于CIIR胶塞质量的纯化水,共冲洗5次。移置于500 mL锥形瓶中,加10倍于CIIR胶塞质量的纯化水,置高压灭菌器中,在30~50 min内升温至(121±2)℃,保持60 min,于20~30 min内冷却至室温,移出,即得供试品提取溶液;并同时制备空白对照溶液。供试品提取溶液和空白对照溶液均需放置24 h后才能观察试验液的澄清度。
1.4 性能测试
1.4.1 硅氧烷的交联结构
采用傅里叶转换红外光谱仪(ATR法)进行测试分析,在4 000~500 cm-1范围内扫描,扫描次数为32,分辨率为4 cm-1,得到CIIR和用硅氧烷硫化的CIIR胶塞的衰减全反射红外光谱。
1.4.2 硫化特性
采用无转子硫化仪测试,测试条件为:温度185 ℃,时间 15 min。
1.4.3 CIIR胶塞提取液的澄清度
采用YB-Ⅱ型澄明度检测仪观察CIIR胶塞提取液的澄清度,并与标准澄清液进行对比。
1.4.4 CIIR胶塞与药品的相容性
药瓶为洁净的玻璃瓶,并与CIIR胶塞相匹配;药粉为生产厂家直接提供的抗生素,每瓶装量为0.5 g;药瓶放置在温度为60 ℃的药品恒温稳定性试验箱中;药瓶倒立(使药粉与胶塞充分接触)置于恒温箱中,时间为10 d;取出并冷却至室温,且每瓶注入5 mL纯水;用标准澄清液与药液相进行对比。
2 结果与讨论
2.1 硅氧烷硫化CIIR的机理
CIIR和用硅氧烷硫化的CIIR胶塞的红外光谱如图1所示。

图1 CIIR和CIIR胶塞的红外光谱
从图1可见,与CIIR相比,CIIR胶塞在3 445 cm-1处有一宽谱带,1 089 cm-1处有一吸收峰。3 445 cm-1处的宽谱带与—NH—的伸缩振动有关,也可能与氢键键合的—Si—OH有关;1 089 cm-1处的吸收峰与—Si—O—Si—有关[6]。这说明硅氧烷硫化的CIIR胶塞存在着—NH—和—Si—O—Si—结构。由此可见,硅氧烷硫化CIIR的机理是硅氧烷中氨基(—NH2)与CIIR中氯原子发生烷基化反应,硅氧键[—Si(OC2H5)3]发生水解缩合反应,从而形成碳氮和硅氧交联键。
硅氧烷硫化CIIR的机理如图2所示。

图2 硅氧烷硫化CIIR的机理
2.2 硅氧烷用量对CIIR胶料硫化特性的影响
由于硫和氧化锌对CIIR胶塞质量有不良影响[7-9],因此采用以硅氧烷为硫化剂的无锌无硫的硅氧烷硫化体系能从根本上避免和减少CIIR胶塞中的可提取物与浸出物。
硫化剂用量对CIIR胶料硫化特性的影响如表1所示。
从表1可以看出:随着硫化剂用量的增大,胶料的硫化程度明显增大,硫化速度加快,ts2和t90缩短;当硫化剂用量为1.5和2份时,硫化程度几乎不变;当硫化剂用量为2.5份以上时其硫化程度又逐渐增大。这一点与聚合物材料的应力屈服现象类似,但机理完全不同。
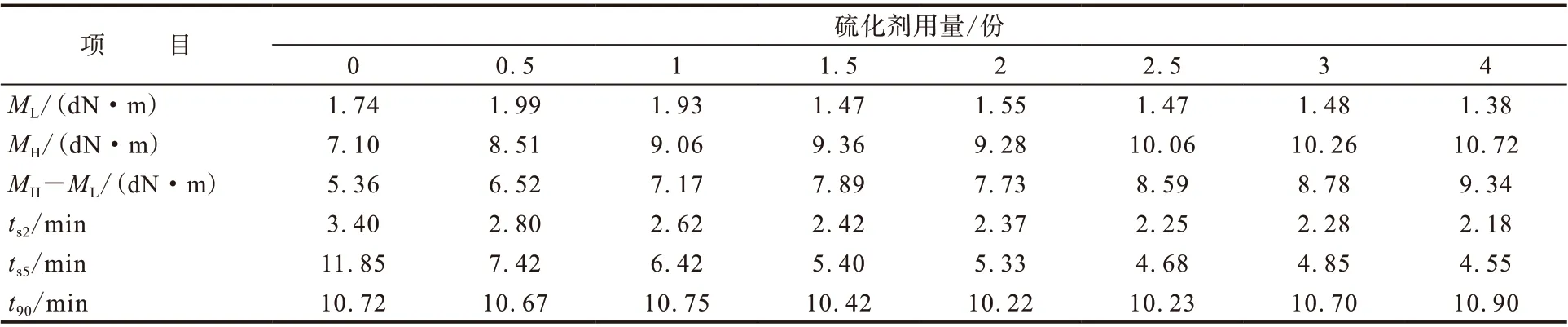
表1 硫化剂用量对CIIR胶料硫化特性的影响
这种现象的机理可能是:作为硫化剂的硅氧烷可以视为一种烷基化剂,能够通过烷基化反应与CIIR中的氯原子作用,从而交联CIIR。另一方面,硅氧烷也可以作为偶联剂与无机物高岭土反应[10]。因此当硅氧烷用量较小时就不可能生成最多的交联键,当硫化剂达到一定用量时,CIIR中的氯原子已反应完毕,交联密度也“暂时”达到最大,此时的硫化程度几乎不变。再增大硫化剂的用量,则过量的硫化剂与无机物高岭土反应而使模量增加,此时硫化程度明显增大。这也从另一方面证明了硅氧烷硫化CIIR的机理是烷基化反应和水解缩合反应。
但是,如果硅氧烷用量太大,硅氧烷中可能只有一个氨基参与交联反应,这样也会增加CIIR胶塞中的可提取物与浸出物。这种推断也可通过测定CIIR胶塞提取液的澄清度得到证实。因此恰当地控制硅氧烷的用量是采用此硫化体系硫化CIIR的关键。
2.3 硫化剂用量对CIIR胶塞提取液澄清度的影响
CIIR胶塞在生产过程中必须加入多种化学助剂,而且还需要经过高温硫化过程,因而不可避免地会在胶塞内残存一些未被化学键合的反应剩余物以及一些不参与反应的物质、热分解产物和硫化生成物,这些物质大多数是有机物。在高温灭菌(一般灭菌条件为121 ℃灭菌30或60 min)时,这些物质也是CIIR胶塞中可提取物与浸出物的一种或几种,其不可避免地会迁移到胶塞表面。这些有机物不溶于水,从而使萃取液浑浊。因此可以通过测定CIIR胶塞高温萃取液的澄清度(也称浊度)来评价CIIR胶塞配方的合理性。
硫化剂用量对CIIR胶塞提取液澄清度的影响如图3所示。

图3 硫化剂用量对CIIR胶塞提取液澄清度的影响
从图3可以看出,随着硫化剂用量的增大,CIIR胶塞提取液的浊度先由大变小,然后再由小变大。当硫化剂用量为2份时,CIIR胶塞提取液的浊度最小(小于0.5级);当硫化剂用量为1.5份时,CIIR胶塞提取液的浊度较小(小于0.5级);不加硫化剂时,CIIR胶塞提取液的浊度最大(大于2级);当硫化剂用量为3和4份时,CIIR胶塞提取液的浊度基本相当,且均较大(大于1级并小于2级)。
通过上述CIIR胶塞提取液澄清度的对比可以发现,硅氧烷存在一个最佳用量,多用、少用或不用均会使CIIR胶塞提取液的浊度变大;硅氧烷可明显减小CIIR胶塞提取液的浊度,这也证实了过量的硅氧烷也会增加CIIR胶塞中的可提取物与浸出物。
2.4 硅氧烷硫化的CIIR胶塞对药品相容性的影响
注射用头孢替安和头孢曲松钠分别为第2代和第3代头孢菌素类抗生素,国内CIIR胶塞能满足注射用头孢曲松钠相容性的要求,但是还不能满足注射用头孢替安相容性的要求,其所用的CIIR胶塞都是覆膜CIIR胶塞或进口CIIR胶塞,因此用这两个药品来评价硅氧烷硫化的CIIR胶塞质量。药品与CIIR胶塞的高温加速相容性试验条件和结果如表2所示[11]。
从表2可以看出,硅氧烷硫化的CIIR胶塞能够满足注射用头孢替安和头孢曲松钠相容性的要求,优于普通CIIR胶塞,与覆膜CIIR胶塞和进口CIIR胶塞相当。因此用硅氧烷硫化的CIIR胶塞可以替代价格昂贵、工艺复杂的覆膜CIIR胶塞和进口CIIR胶塞。
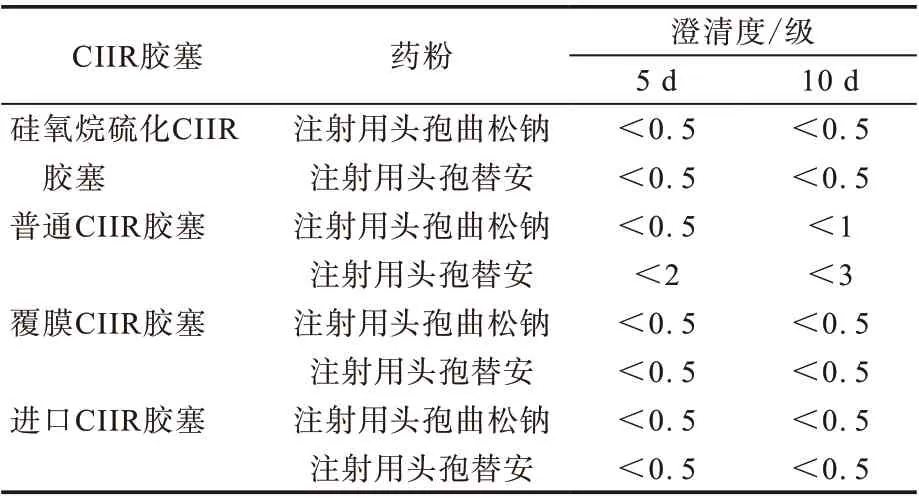
表2 硅氧烷硫化CIIR胶塞对头孢菌素相容性的影响
3 结论
(1)硅氧烷硫化体系是CIIR有效的无锌无硫硫化体系。
(2)采用硅氧烷硫化CIIR时有一个最佳用量,当硅氧烷用量为2份时,CIIR胶塞中的可提取物与浸出物最少,胶塞提取液的浊度最小。
(3)用硅氧烷硫化的CIIR胶塞能够满足注射用头孢替安和头孢曲松钠相容性的要求,达到了覆膜CIIR胶塞和进口CIIR胶塞的水平,可以替代价格昂贵、工艺复杂的覆膜CIIR胶塞和进口CIIR胶塞使用。

