干扰素α序贯替比夫定治疗HBeAg阳性慢性乙型肝炎的疗效及安全性
王秀珍,刘雪峰,张长
(温州医科大学附属温岭医院 感染科,浙江 温州 317500)
干扰素α序贯替比夫定治疗HBeAg阳性慢性乙型肝炎的疗效及安全性
王秀珍,刘雪峰,张长Δ
(温州医科大学附属温岭医院 感染科,浙江 温州 317500)
目的 探索干扰素α(interferon-α,IFN-α)序贯替比夫定治疗乙型肝炎e抗原(hepatitis B e antigen,HBeAg)阳性慢性乙型肝炎的疗效和安全性。方法 选取2008年8月~2013年9月温州医科大学附属温岭医院肝炎门诊档案94例慢性乙型肝炎患者,其中聚乙二醇干扰素α-2a(pegylated interferon α-2a,peg-IFN-α-2a)序贯替比夫定45例;同期单用替比夫定初始治疗49例作对照组,观察生化应答、病毒学应答、病毒学突破、血清学应答。结果 经替比夫定32个月的治疗,累计HBV DNA<100 IU/mL者实验组88.9%(40/45),优于对照组44.9%(22/49),(P<0.05);2组HBeAg阴转率和HBeAg血清学转换率实验组53.3%(24/45)和51.1%(23/45)均优于对照组各为24.5%(12/49),(P<0.05);2组病毒学突破实验组6.7%(3/45)明显低于对照组34.7%(17/49)(P<0.05),显示peg-IFN-α-2a序贯替比夫定治疗慢性乙型肝炎具有协同抗病毒作用。结论 干扰素序贯替比夫定治疗慢性乙型肝炎不仅抗病毒疗效高,而且安全性良好。
慢性乙型肝炎;e抗原;干扰素α;替比夫定
通过大量关于慢性乙型肝炎病程中免疫功能的变化及急性乙型肝炎与慢性乙型肝炎免疫功能差异的研究,发现抗病毒免疫应答功能缺陷是慢性乙型肝炎的重要特征,因此导致病毒长期存在而无法被彻底清除。目前国内外学者认为最合理的方案可能是将药物抗病毒治疗与免疫治疗有机序贯的联合起来[1-4],只有使机体产生有效的抗病毒免疫应答,才能真正达到临床完全控制病毒复制甚至清除病毒的目的。温州医科大学附属温岭医院感染科对94例阳性慢性乙型肝炎患者用peg-IFN-α-2a治疗应答欠佳患者序贯应用替比夫定优化治疗,现将结果报告如下。
1 资料与方法
1.1 一般资料 94例HBeAg阳性慢性乙型肝炎患者选自2008年8月~2013年9月温州医科大学附属温岭医院肝炎门诊档案,45例聚乙二醇干扰素α-2a(pegylated interferon a-2a,peg-IFN-α-2a)治疗应答欠佳等原因停药即序贯替比夫定优化治疗(下称实验组),年龄24~35岁,平均(29.89±5.18)岁,病程9~18年,平均病程(14.91±2.52)年。peg-IFN-α-2a治疗后应答情况,干扰素失效22例,干扰素严重不良反应6例,干扰素抵抗4例,前C区变异1例,另外12例peg-IFN-α-2a有效[其中乙肝病毒基因(hepatitis B virus DNA,HBV DNA)<100 IU/mL 7例,下降>2 lg IU/mL 5例,HBeAg血清学转换1例,滴度下降6例],因生育、经济等原因改替比夫定序贯治疗。同期49例单用替比夫定初治患者作为对照组,年龄24~38岁,平均(31.84±7.37)岁,病程9~17年,平均(14.04±2.81)年。2组患者基线特征比较,差异无统计学意义,见表1。本试验入选患者均知情同意,并研究获得医院伦理委员会批准。

表1 2组患者病毒学基线特征Tab.1 Baseline characteristics of virologic between two groups (±s)
纳入标准:诊断符合2010中华医学会肝病学分会和中华医学会感染病学分会联合修订的《慢性乙型肝炎防治指南》[5];①年龄18~69周岁;②HBeAg阳性,HBeAb阴性;③符合抗病毒指征;④签署知情同意书。
排除标准:18周岁以下69周岁以上;排除肝硬化失代偿期及其他慢性肝病;排除严重肾功能不全、慢性充血性心力衰竭患者。
1.2 方法
1.2.1 研究方法:实验组组停用peg-IFN-α-2a(上海罗氏制药有限公司,国药准字J20120075)后即改用替比夫定(北京诺华制药有限公司,规格600mg,国药准字H20070028)600mg,1次/天口服,治疗32个月;对照组组单用替比夫定600mg,1次/天口服,治疗32个月。疗效评价标准参照慢性乙型肝炎防治指南[5]。
1.2.2 观察指标:治疗前和治疗中1~3个月检测血常规、甲状腺功能、肝功能、肌酸磷酸激酶和肌红蛋白等。肝功能采用美国Abbott公司Aeroset全自动生化分析仪及配套试剂;HBV标志物每3个月检测一次,采用美国Abbott公司Axsym型抗原抗体定量分析仪及微粒子酶免疫试剂,HBeAg>1.0S/CO为阳性,HBeAb<1.0S/CO为阳性;HBVDNA采用上海罗氏公司荧光定量PCR检测仪,检测下限<2lgIU/mL,试剂由湖南圣湘公司提供;HBV聚合酶RT区基因序列检测,血清标本送杭州迪安医学检验中心以德国Qlagen公司Pyromark-Q96ID测序仪进行耐药基因测序。
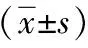
2 结果
2.1 2组患者疗效比较 患者生化应答(ALT复常)、病毒学应答(HBV-DNA阴转)、病毒学突破(HBV-DNA突破)、HBeAg阴转率和HBeAg血清学转换率,2组比较差异有统计学意义(χ2=8.688,20.217,11.001,8.259,7.113,P<0.05)。HBsAg血清学转换率,2组比较差异无统计学意义。见表2。

表2 2组患者疗效比较[n(%)]Tab.2 Comparison of efficacy between two groups [n(%)]
2.2 停药后复发率 实验组与对照组各有11例获得HBV DNA、HBeAg、ALT完全应答后停药,随访96周,再复发:实验组为9.09%(1/11),对照组为36.4%(4/11),差异无统计学意义。
2.3 安全性 患者治疗中,肌酸磷酸激酶及其同工酶和肌红蛋白升高,每1~2 w监测1次,发现肌酸激酶升高者实验组为40.0%(18/45),对照组为55.1%(27/49),肌酸激酶升高6倍者实验组为6.7%(3/45),对照组为6.1%(3/49),2组比较差异均无统计学意义。三项同时升高者实验组为13.3%(6/45),对照组为12.2%(6/49),2组比较差异无统计学意义。没有发生中毒性肌炎和周围神经炎等病例。
3 讨论
干扰素α(interferon-α,IFN-α)是具有广谱抗病毒、抗肿瘤、抑制细胞增殖和免疫调节作用的细胞因子,抗HBV治疗优点主要表现为疗程明确,没有病毒变异和耐药,HBeAg、乙肝表面抗原(hepatitis B surface antigen,HBsAg)阴转率或转换率高,缺点是直接抗病毒能力弱,不良反应多,使用不便等。核苷(酸)类药物的优缺点恰好与之相反,抑制HBV-DNA疗效好,速度快,使用方便,不良反应少,疗程长,易发生病毒变异和耐药(除恩替卡韦),HBeAg、HBsAg阴转率偏低等。IFN-α主要是调节免疫,兼抗病毒作用,核苷(酸)类药物是直接抗病毒,2组作用机制不同,不存在相互竞争抑制,从理论上分析,两者序贯治疗应该能达到协同作用。因此近年来许多临床研究试图通过不同组合,取长补短,以期取得更好的疗效[6-9]。
文献报道HBsAg自发清除率每年约1%~3%[5],核苷(酸)类药物虽可抑制HBV复制,但拉米夫定、阿德福韦酯、恩替卡韦及替比夫定治疗1年的HBeAg血清学转换率分别为16、12、21及22.5%,HBsAg转阴率均<2%,且以白种人为主[5]。普通IFN治疗亚裔人群HBeAg血清学转换率约为12%~22%,peg-IFN-α治疗1年HBeAg血清学转换率提高到32%,但HBsAg血清学转换率为3%[10]。本研究采用peg-IFN-α-2a序贯替比夫定治疗HBeAg阳性慢性乙型肝炎,HBeAg血清学转换率达51.1%,HBsAg血清学转换率为6.7%,抗病毒疗效得到明显提高(P<0.05)。特别是6例对peg-IFN-α-2a发生严重不良反应者,5例(83.3%)出现HBeAg血清学转换,是否由于药物反应剧烈导致机体更快进入免疫清除期,值得进一步探索。
文献报告HBeAg血清学转换同疾病的临床缓解密切相关,因此被定为HBeAg阳性慢性乙型肝炎的有限治疗目标[11-15]。本研究结果显示实验组ALT复常、HBeAg阴转率和血清转换率均优于对照组(P<0.05)。同时实验组HBV-DNA突破明显低于对照组(P<0.05),疗效优于梁雪松等及孙海霞等[16-17]报告,证明IFN-α序贯替比夫定的作用机制存在互补性,可能有相加或协同作用[18]。
IFN-α联合替比夫定治疗慢性乙型肝炎可增加患者周围神经病变的发病风险[19-20],临床研究已被叫停。本文观察结果显示IFN-α应答欠佳或不良反应等原因序贯应用替比夫定优化治疗安全性良好,没有增加不良反应发生率,但抗病毒疗效明显提高,是值得推荐的一种治疗方法。
[1] Zoulim F.Assessment of treatment efficacy in HBV infection and disease[J].J Hepatol,2006,44(1):95-99.
[2] 王贵强.从慢性乙型肝炎免疫和病原学特点探讨临床治疗策略[J].中华传染病杂志,2007,25(7):385-387.
[3] 王福生,陈威巍. 肝脏免疫与慢性乙型肝炎抗病毒治疗[J].中华肝脏病杂志,2008,16(2):81-83.
[4] Shi Y,Wu YH,Shu ZY,et al.Interferon and lamivudine combination therapy versus lamivudine monotherapy for hepatitis B e antigen-negative hepatitis B treatment:a meta-analysis of randomized controlled trials[J].Hepatobiliary Pancreatic Dis Int,2010,9(5):462-472.
[5] 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010版)[J].中华传染病杂志,2011,29(2):65-80.
[6] 赵刚德,谢青.干扰素在病毒性肝炎治疗中的联合应用[J].中华肝脏病杂志,2011,19(1):5-7.
[7] 何智敏,任姗,金怡,等.干扰素应答不佳或不耐受的慢性乙型肝炎患者序贯应用替比夫定的临床观察[J].北京医学,2014,36(12):1008-1011.
[8] 李晓鹤,何清,曾丽娇,等.HBeAg阳性慢性乙肝患者干扰素疗效欠佳序贯核苷类似物治疗的疗效观察[J].中华实验和临床病毒学杂志,2015,29(1):5-7.
[9] 侯爱芳,张荣,李汾香.干扰素α-2b与替比夫定序贯疗法治疗HBeAg阳性慢性乙型肝炎疗效观察[J].临床医药实践,2014,23(12):917-919.
[10] Lau GK,Piratvisuth T,Luo KX,et al. Peginterferon Alfα-2a,lamivudine ,and the combination for HBeAg-positive chronic hepatitis B[J].N Engl J Med,2005,352(26):2682-2695.
[11] Chu CM,Liaw YF.Predictive factors for reactivation of hepatitis B following hepatitis B e antigen seroconversion in chronic hepatitis B [J].Gastroenterology,2007,133(5):1458-1465.
[12] Lin SM,Yu ML,Lee CM,et al. Interferon therapy in HBeAg positive chronic hepatitis reduces progression to cirrhosis and hepatocellular carcinoma[J].J Hepatol,2007,46(1):45-52.
[13] European Association For the Study of the Liver. EASL Clinical Practice Guidelines:management of chronic hepatitis B virus infection[J].J Hepatol,2012,57(1):167-185.
[14] Liaw YF,Leung N,Kao JH,et al.Asian -Pacific consensus statement on the management of chronic hepatitis B:a 2008 update[J].Hepatol Int,2008,2(3):263-283.
[15] Keeffe EB,Dieterich DT,Han SH,et al. A treatment algorithm for the management of chronic hepatitis B virus infection in the United States:2008 update [J].Clin Castroenterol Hepatol,2008,6(12):1315-1341.
[16] 梁雪松,李成忠,尹伟,等.聚乙二醇干扰素-α-2a治疗24周应答不佳的乙型肝炎e抗原阳性的慢性乙型肝炎患者优化治疗分析[J].中华传染病杂志,2014,32(5):280-284.
[17] 孙海霞,杨小安,张烨琼,等.聚乙二醇干扰素α-2a序贯替比夫定治疗HBeAg阳性慢乙肝的短期疗效与安全性[J].中华实验和临床病毒学杂志,2014,28(3):213-215.
[18] Hou J,Yin YK,Xu D,et al. Telbivudine versus lamivudine in Chinese patients with chronic hepatitis B:Results at 1 year of a randomized, double-blind trial[J].Hepatology,2008,47(2):447-454.
[19] 郑日亮,袁云.替比夫定与聚乙二醇干扰素α-2a联用导致感觉神经病二例[J].中华神经科杂志,2009,42(7):475-478.
[20] 刘敏,易为,蔡晧东.替比夫定及干扰素相关肌炎及周围神经病[J].药物不良反应杂志,2010,12(2):130-131.
(编校:师维康)
Efficacy and safety of interferon-α sequential telbivudine in the treatment of HBeAg-positive chronic hepatitis B
WANG Xiu-zhen, LIU Xue-feng, ZHANG ChangΔ
(Department of Infectious Diseases, The Affiliated Wenling Hospital of Wenzhou Medical University, Wenzhou 317500, China)
ObjectiveTo explore the efficacy and safety of sequential telbivudine (LDT) therapy following interferon-α(IFN-α) in hepatitis B e antigen (HBeAg) positive chronic hepatitis B patients.Methods94 chronic hepatitis B patients in our hospital hepatitis clinic archives from August 2008 to September 2013 were divided into two groups, 45 patients treated with LDT following IFN-α due to unsatisfactory response to peginterferon-α-2a(peg-IFN-α-2a)treatment in the sequential group and 49 patients treated with LDT initially in the controlled group. In the sequential group, 22 patients failed to respond to IFN-α treatment, 4 patients obtained IFN-resistance, 6 patients developed severe side effects, 1 patients had pre-C mutation and 12 patients switched to LDT due to economic factors or fertility requirement. The biochemical response and virological response, virological breakthrough and serological response were observed. Chi-square test was adapted for data analysis.ResultsAfter 32.35 months of LDT therapy, 88.9%(40/45) patients had with HBV-DNA <100 IU/mL in the experiment group compared with 44.9%(22/49) patients in the control group (P<0.05). The rates of HBeAg loss and HBeAg seroconversion in the experiment group were 53.3%(24/45) and 51.1%(23/45) respectively, which were significantly higher than that of the control group, 24.5% (12/49) and 24.5% (12/49) (P<0.05). 6.7% (3/45) patients developed virological breakthrough in the sequential group compared with 34.7%(17/49) in the control group (P<0.05). Above results suggested the synergistic antiviral activity between peg-IFN-α-2a and LDT.ConclusionSequential LDT therapy following peg-IFN-α-2a is better efficacy and safety compared with treating patients with LDT alone initially.
chronic hepatitis B; HBeAg; interferon α; telbivudine
10.3969/j.issn.1005-1678.2016.12.047
王秀珍,女,本科,副主任医师,研究方向:感染病学,E-mail:wxzwyh@163.com;张长,通信作者,男,本科,主任医师,研究方向:感染病学,E-mail:yx0571yx@163.com。
R512.6+2;TQ929.1
A
——以《推销员之死》对话选段为例

