Sysmex HISCL5000化学发光分析仪检测乙型肝炎标志物性能评价
鄂建飞,刘利洪,陈宗耀,王登朝,叶 敏,袁成良
(四川省德阳市人民医院检验科 618000)
Sysmex HISCL5000化学发光分析仪检测乙型肝炎标志物性能评价
鄂建飞,刘利洪,陈宗耀,王登朝,叶敏,袁成良△
(四川省德阳市人民医院检验科618000)
目的评价Sysmex HISCL5000化学发光免疫分析仪(以下简称HISCL5000分析仪)对乙型肝炎血清标志物检测的分析性能。方法用HISCL5000分析仪进行HBsAg、HBsAb、HBeAg、HBeAb、HBcAb检测,根据美国临床和实验室标准化协会(CLSI)颁布的EP系列文件对仪器分析性能进行评价。结果HISCL5000分析仪检测HBsAg、HBsAb、HBeAg、HBeAb、HBcAb低浓度和高浓度两个浓度批内不精密度变异系数(CV)%分别为1.24%、1.05%、2.56%、2.27%、2.19%、1.95%、2.37%、1.43%、2.49%、1.29%;总不精密度CV%分别为2.32%、1.74%、3.12%、2.45%、2.94%、2.96%、3.02%、1.82%、3.21%、1.54%。HBsAg检测线性r2=0.976 5,HBsAb检测线性r2=0.951 6,两者r2均大于0.95。HISCL5000分析仪和e601分析仪HBsAg检测结果比对:r2=0.982 2,HBsAb检测结果比对:r2=0.974 8。HISCL5000分析仪与ELISA两种方法检测HBsAg、HBsAb、HBeAg、HBeAb、HBcAb结果的符合率分别为99.6%(550/552)、93.5%(516/552)、99.6%(550/552)、94.9%(524/550)、92.0%(508/552)。HISCL5000分析仪检测HBsAg携带污染X=0.070 8,3SD(L-L)=0.106 2,X<3SD(L-L)。HISCL5000分析仪检测HBsAg、HBsAb下限分别为0.006 IU/mL、0.213 6 mIU/mL。结论HISCL5000分析仪检测乙型肝炎血清标志物的精密度、线性范围、比对结果、携带污染、检测下限均达到要求,能满足临床需求。
乙型肝炎病毒;磁微粒化学发光酶免疫分析法;血清学标志物;性能评价
乙型肝炎病毒(HBV)感染是世界范围内的严重公共卫生问题之一,约5%的世界人口为HBV携带者。当前国内HBV的感染率比较高,乙型肝炎血清学标记物(HBV-M)是临床实验室最主要的检测项目[1]。ELISA仍是目前大多数临床实验室定性检测HBV-M的常规方法,其检测结果常作为临床诊断和治疗慢性乙型肝炎的依据之一[2],但是,近年来越来越多的临床实验室将磁微粒化学发光酶免疫分析法用于HBV-M检测。本实验室按美国临床和实验室标准化协会(CLSI)EP系列文件的要求,对Sysmex HISCL5000全自动化学发光免疫分析仪进行性能验证,现报道如下。
1材料与方法
1.1标本来源所有检测标本均来自2015年3~6月本院检测HBV-M的门诊和住院患者。
1.2仪器与试剂采用日本Sysmex HISCL-5000全自动化学发光免疫分析仪(以下简称HISCL5000分析仪,磁微粒化学发光酶免疫分析法)及其配套试剂;德国COBAS e601 全自动免疫分析仪(以下简称e601分析仪,电化学发光免疫分析法)及其配套试剂;瑞士TECAN全自动酶免疫分析仪(以下简称TEACN分析仪,酶联免疫吸附试验),试剂为上海科华生物工程股份有限公司产品,标准物质来自北京康彻思坦生物公司。
1.3方法每日对仪器进行保养,且质控品检测结果均在控制范围内。采用HISCL5000分析仪、e601分析仪及TECAN分析仪检测乙型肝炎表面抗原(HBsAg)、乙型肝炎表面抗体(HBsAb)、乙型肝炎e抗原(HBeAg)、乙型肝炎e抗体(HBeAb)、乙型肝炎核心抗体(HBcAb),严格按仪器及试剂说明书进行操作。结果判读:ELISA检测时,HBsAg、HBsAb、HBeAg样品吸光度(OD)值大于或等于临界(Cut-off)值为阳性,HBeAb、HBcAb样品OD值小于Cut-off值为阳性;HISCL5000检测时,HBsAg≥0.03 IU/mL,HBsAb≥5.0 mIU/mL,HBeAg≥1.0 C.O.I,HBeAb≥50 Inh%,HBcAb≥1.0 C.O.I为阳性。
1.3.1精密度试验每天分析1个批次,取2个浓度的标本,每天每个浓度的标本重复测定4次,连续测定5 d,计算批内不精密度和总不精密度,评价方案按EP15-A2进行[3]。
1.3.2线性试验HBsAg、HBsAb线性试验参照EP6-A2进行[4],选择高于仪器检测上限的标本,用HISCL专用稀释液进行稀释,以原始标本为1.0,按照0.9、0.8、0.7、0.6、0.5、0.4、0.3、0.2、0.1进行稀释,0.1以下对倍稀释,直至检测值低于仪器检测下限,计算决定系r2是否大于0.95。
1.3.3比对试验选择40个浓度覆盖仪器线性范围的标本,按EP9-A2进行HISCL5000分析仪及e601分析仪HBsAg、HBsAb定量检测结果比对[5];另选择患者血清标本进行HISCL5000分析仪及ELISA检测HBsAg、HBsAb、HBeAg、HBeAb、HBcAb结果比对,计算结果符合率。
1.3.4携带污染取高浓度标本(H)和低浓度标本(L)各一份,将高浓度标本分成 10 份,低浓度标本分成11份,21份标本按顺序:L1、L2、L3、H1、H2、L4、H3、H4、L5、L6、L7、L8、H5、H6、L9、H7、H8、L10、H9、H10、L11连续测定,选出高值对低值干扰组(H-L)与低值对低值干扰组(L-L)两组数值,分别计算均值(Mean)和标准差(SD),要求X=Mean(H-L)-Mean(L-L),X<3SD(L-L)验证通过。
1.3.5检测下限用HISCL专用稀释液将已知浓度的低浓度标本(HBsAg C1校准品0.25 IU/mL,HBsAb C1校准品10 mIU/mL)对倍稀释成5个浓度系列作为验证材料,每个浓度重复检测20次,计算CV%,CV%<20%的最低浓度即为定量检出限。
1.3.6检测结果频数图选取常规标本1 642份,潜在干扰标本120份:孕妇标本16份,注射过疫苗标本6份,黄疸标本10份,脂血标本10份,溶血标本10份,HIV阳性标本4份,梅毒阳性标本10份,丙肝阳性标本10份,ANA阳性标本16份,弓形虫感染标本4份, EB病毒阳性标本4份,风疹抗体阳性4份, RF阳性标本16份。
1.4统计学处理采用SPSS17.0软件进行数据处理及统计学分析,计数资料以例数或百分率表示,组间比较采用配对χ2检验,P<0.05为差异有统计学意义。
2结果
2.1HISCL5000分析仪精密度验证结果(1)批内不精密度:HISCL5000分析仪检测HBsAg、HBsAb、HBeAg、HBeAb、HBcAb低浓度和高浓度两个浓度批内不精密度分别为:1.24%、1.05%、2.56%、2.27%、2.19%、1.95%、2.37%、1.43%、2.49%、1.29%;(2)总不精密度:HISCL5000分析仪检测HBsAg、HBsAb、HBeAg、HBeAb、HBcAb低浓度和高浓度总不精密度分别为:2.32%、1.74%、3.12%、2.45%、2.94%、2.96%、3.02%、1.82%、3.21%、1.54%,见表1。
2.2HISCL5000分析仪检测HBsAg、HBsAb的线性分析HBsAg检测线性r2=0.976 5,回归方程为Y=205.72X-480.29;HBsAb检测线性r2=0.951 6,回归方程为Y=78.521X-240.85,两者r2均大于0.95。
2.3比对结果(1)HISCL5000分析仪及e601分析仪HBsAg检测比对结果:r2=0.982 2,回归方程为Y=0.727 3X+0.153 3; HISCL5000分析仪及e601分析仪HBsAb检测比对结果:r2=0.974 8,回归方程为Y=0.731X-5.842。(2)HISCL5000分析仪与ELISA两种方法检测552例患者血清标本HBsAg、HBsAb、HBeAg、HBeAb、HBcAb结果的符合率分别为99.6%(550/552)、93.5%(516/552)、99.6%(550/552)、94.9%(524/550)、92.0%(508/552);两种方法检测HBsAg、HBeAg的结果差异无统计学意义(P>0.05),HBsAb、HBeAb、HBcAb的结果差异有统计学意义(P<0.05),见表2。用HISCL5000分析仪检测552例患者血清标本HBsAb、HBeAb、HBcAb阳性率分别为62.0%(342/552)、25.7%(142/552)、61.2%(338/552),阳性率明显高于ELISA,两种方法阳性率比较差异有统计学意义(P<0.05),见表3。
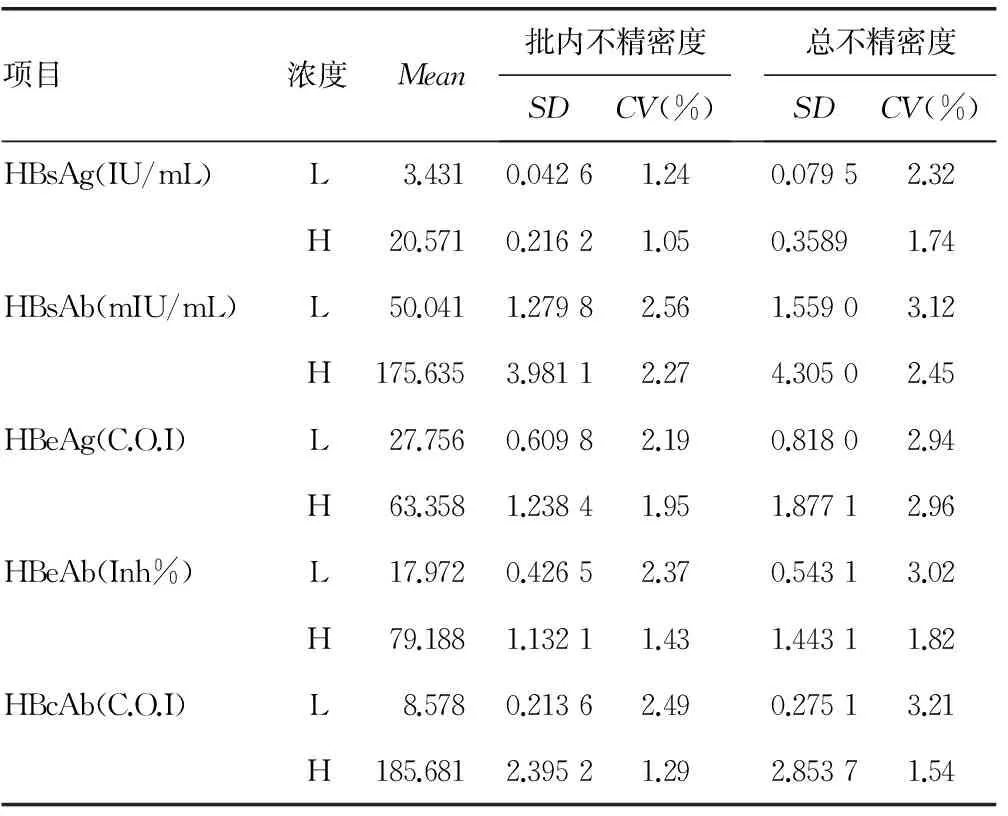
表1 HISCL5000分析仪精密度验证结果
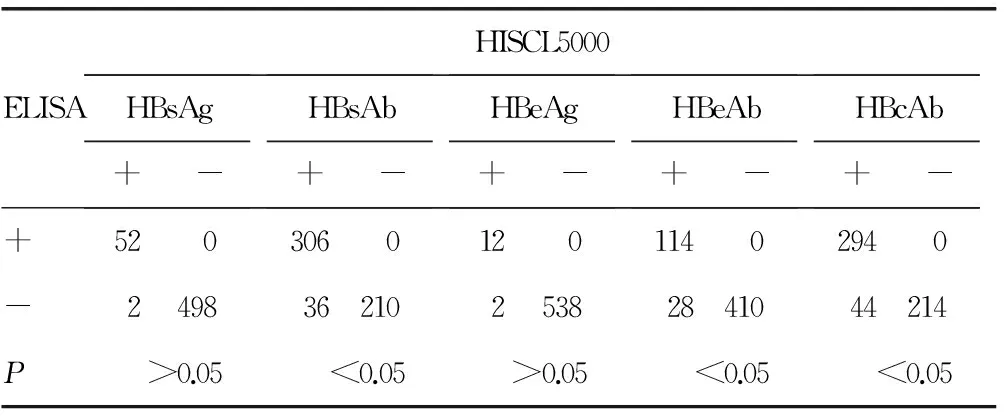
表2 HISCL5000分析仪与ELISA检测HBV-M结果
2.4HISCL5000分析仪检测HBsAg携带污染检测结果携带污染HISCL5000分析仪检测HBsAg携带污染X=0.070 8,3SD(L-L)=0.106 2,X<3SD(L-L),符合相应的要求。
2.5HISCL5000分析仪检测下限分析HISCL5000分析仪检测HBsAg、HBsAb下限分别为0.006 IU/mL、0.213 6 mIU/mL,明显低于试剂说明书0.03 IU/mL和5.0 mIU/mL,见表4。
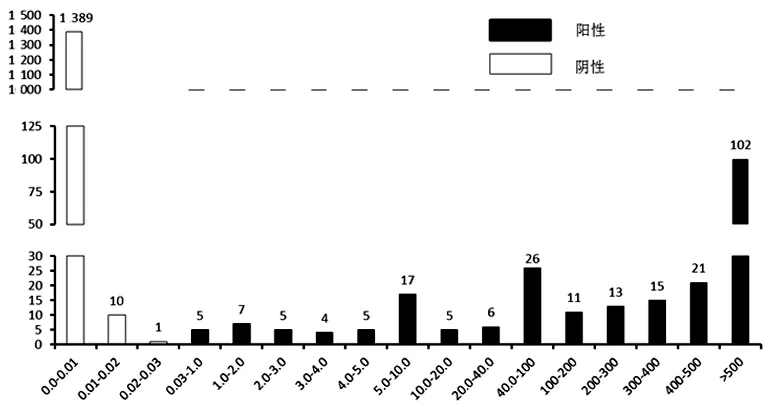
注:HBsAg标本浓度(IU/mL)。
图1HISCL5000检测1 642例患者HBsAg结果分布情况
2.6HISCL5000分析仪检测HBsAg结果分布HISCL5000分析仪检测1 642患者HBsAg,其中结果小于或等于0.01 IU/mL 1 389例,占阴性标本的99.2%(1 389/1 400),大于或等于5.0 IU/mL 216例,占阳性标本的89.3%(216/242),见图1。
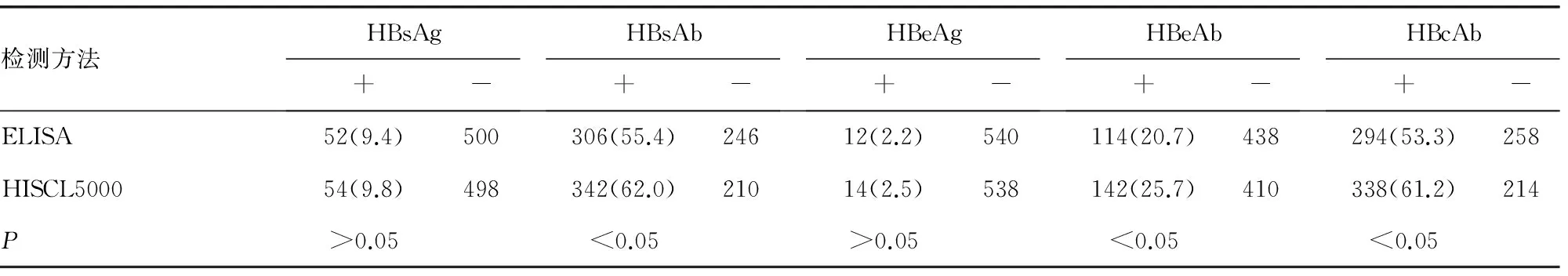
表3 HISCL5000分析仪与ELISA检测HBV-M阳性率的比较[n(%)]
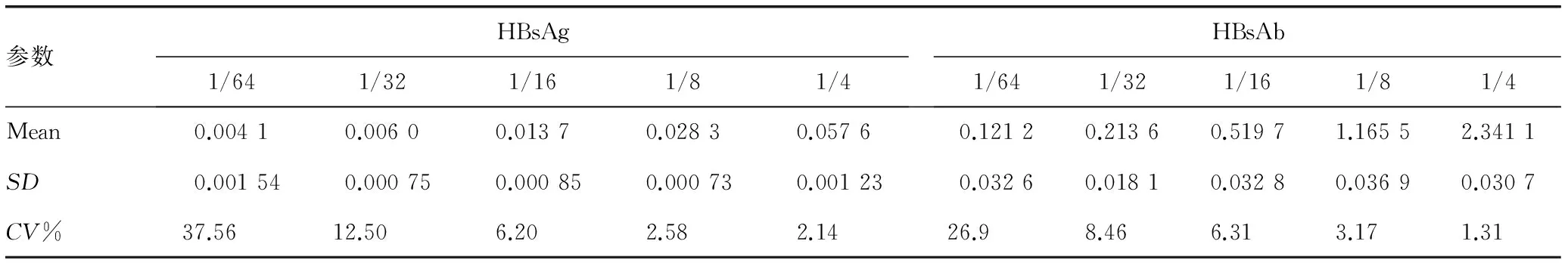
表4 HISCL5000分析仪HBsAg、HBsAb检测下限结果
3讨论
乙型肝炎是由HBV感染引起的,HBV是一种有包膜的DNA病毒,能感染肝脏并引起肝细胞坏死和炎症。HBV感染可分为慢性和急性感染,可以表现为无症状感染、轻度感染、严重感染,甚至罕见的爆发性肝炎[6]。纵向调查发现慢性乙型肝炎患者在不进行治疗超过5年会增加8%~20%的概率发展为肝硬化[7-11]。上述患者出现肝硬化时发生肝功能代偿不全的概率每年增加约20%,同时乙型肝炎相关性肝癌的发生率也很高,1%~5%不等[12]。不进行治疗的患者出现失代偿性肝硬化预后极差,5年生存率为15%~40%[10,12-13]。据世界卫生组织报道,全球约有2.4亿人为HBV携带者,非洲和亚洲的感染率最高。慢性乙型肝炎感染者肝硬化和肝癌的风险很高,每年约65万人死于HBV感染所致的肝衰竭、肝硬化和原发性肝细胞癌[14]。因此世界卫生组织呼吁各国采取更多措施防止新的感染,并确保已感染人被诊断和治疗。
HBV-M检测是诊断HBV感染和判断病毒复制的重要指标之一[15]。临床检验中检测HBV-M的方法较多,按照检测技术不同分为定性检测和定量检测两大类,前者主要包括金标法和ELISA,后者主要包括化学发光法、电化学发光免疫分析、时间分辨荧光免疫分析等。HBV-M的准确检测对于乙型肝炎的流行病学监测和诊断有着十分重要的作用,所以好的检测方法非常重要。
ELISA操作简单、经济实惠,通过在检测过程中直接进行标准量化质控,保证了检测结果的相对有效性。此外,ELISA如引入生物素和亲和素系统或采用化学发光等技术,其灵敏度还可进一步提高。但ELISA技术有其局限性,因试验中假阳性或假阴性结果是不能完全避免的。除方法和试剂本身对检测结果性能的影响外,ELISA检测结果的可靠性比较易受检测过程中操作误差的影响,如加样和加试剂的重复性、孵育温度的均衡性、孵育时间的长短、标本溶血等都可能影响检测结果。因此,检测中尽管使用符合要求的方法和试剂,也应注意检测过程中其他因素对检测结果的影响。磁微粒化学发光酶免疫分析具有高灵敏度和高特异度,试剂安全、稳定及检测快速等优点,因此近年来基于此技术的全自动检测设备发展迅速,被广泛应用于临床。
HISCL5000分析仪采用磁微粒化学发光酶免疫检测技术,与传统的化学发光分析法相比,HISCL5000检测HBV-M有6个新的特点:(1)以磁性微粒作为包被载体,碱性磷酸酶作为标记物,金刚烷类衍生物作为高敏发光底物,发光强度为3-(2-螺旋金刚烷)-4-甲氧基-4-(3-磷氧酰)-苯基-1,2-二氧环乙烷二钠盐的4倍以上,能够检测出低浓度的标本,提高检出率利于早期发现病毒感染,避免了假阴性造成的漏诊。(2)创新的B/F分离技术:通过在集磁/清洗后,加入去磁/分散磁珠的步骤,使得磁微粒重新均匀分散在液相中,并重复4次,这样夹杂在微粒间的非特异性反应物能够彻底释放清洗液中,直到完全清除,最大限度排除干扰,保证结果准确可靠。(3)HISCL5000分析仪高敏发光法第一步捕获待测物时,没有磁珠参与,为液相(均相)反应。布朗运动颗粒越小,温度越高,反应速度更快,结合更充分,所以孵育时间大大缩短。所有待测物被完全捕获后,生物素化的抗原抗体结合物,再同包被链霉亲和素的磁珠结合,因此HISCL5000分析仪检测HBV-M 5项只需要90 μL标本量,检测时间只需要17 min。(4)通过切换滤镜,确保浓度由低到高的宽检测线性范围,大大降低了标本稀释的频率,为实验室节省人力、时间及试剂成本,操作更方便。(5)一次性加样吸头和过滤薄膜擦拭双重保障,最大限度地降低携带污染。(6)HISCL5000分析仪可在运行过程中随时更换试剂盒、消耗品和冲洗液,体现HISCL5000分析仪的高度智能化和人性化。因此HISCL5000分析仪具有定量跟踪分析、高灵敏度、高特异度、检测快速、操作简单及标本用量少的优点,可提供实时、动态的检测结果,有效指导临床诊断和治疗。
本研究结果显示,HISCL5000分析仪检测批内和总不精密度CV%均小于15%,符合厂商要求,说明仪器检测重复性好,结果稳定。标本中被测物质的浓度在仪器检测线性范围内时,所测结果是可信的,即更接近于被测物质的真值,HISCL5000分析仪检测HBsAg、HBsAb的线性范围,r2分别为0.976 5、0.951 6,均大于 0.95。保证检测结果的一致性是实验室管理中实现质量目标的重要依据,即对同一份标本进行相同项目检测,不同检测方法所获得的结果应相互符合。本研究按EP9-A2文件对HISCL5000 分析仪及e601分析仪定量检测HBsAg、HBsAb的结果进行比对分析,二者检测结果r2分别为0.982 2、0.974 8均大于0.95,说明二者定量检测HBsAg、HBsAb具有较好一致性。本研究结果显示,磁微粒化学发光酶免疫法与ELISA对HBsAg、HBsAb、HBeAg、HBeAb、HBcAb符合率分别为99.6%、93.5%、99.6%、94.9%、92.0%,检测结果具有较好的一致性,高于相关报道的符合率[16],其原因可能在于不相符的结果主要出现在临界值浓度标本。大量研究显示,磁微粒化学发光酶免疫法对临界值标本的检出率及结果准确性均优于ELISA[17-18]。由此可见,ELISA与磁微粒化学发光酶免疫法对临界值标本的检测结果存在差异,就方法学和自动化程度而言,磁微粒化学发光酶免疫法优于ELISA。HISCL5000分析仪检测HBsAg携带污染X=0.070 8,小于L-L组3SD(0.106 2),说明HISCL5000分析仪可以有效避免交叉污染,保证检测结果的准确性。本研究显示HISCL5000分析仪对HBsAg、HBsAb的检测下限分别为0.006、0.213 6 mIU/mL,均能满足临床需求,同时HISCL5000分析仪检测1 642患者HBsAg,≤0.01 IU/mL 1 389例,占阴性标本99.2%(1 389/1 400),HBsAg≥5.0 IU/mL16例,占阳性标本89.3%(216/242),说明HISCL5000分析仪能有效区分阴性和阳性标本。以上均说明磁微粒化学发光酶免疫法定量检测结果能更好地用于患者病情监测和疫苗接种效果评价,HISCL5000能为临床乙型肝炎的诊断、治疗和全程动态监测提供准确的科学依据。
综上所述,HISCL5000分析仪具有灵敏度高、特异性强、线性范围宽、携带污染低、检测快速、标本用量少、自动化程度高等优点,可以很好地满足临床诊断要求。
[1]方志红.临床检验中乙型肝炎病毒检测方法的应用评价[J].国际检验医学杂志,2012,33(13):1648-1649.
[2]王宇明,周吉军,程林.乙型肝炎病毒血清学标记物定量检测方法比较[J].中华肝脏病杂志,2011,19(11):812-814.
[3]Clinical and Laboratory Standards Institute.EP15-A2 Evaluation of precision performance of quantitative measurement methods[S].Wayne,PA,USA:CLSI,2008.
[4]National committee for clinical laboratory.EP6-A Evaluation of the linearity of quantitative measurement procedures[S].Wayne,PA,USA:NCCLS,2003.
[5]National committee for clinical laboratory.EP9-A2 Method comparison and bias estimation using patient samples[S].Wayne,PA,USA:NCCLS,2002.
[6]Lavanchy D.Hepatitis B virus epidemiology,disease burden,treatment,and current and emerging prevention and control measures[J].J Viral Hepat,2004,11(2):97-107.
[7]McMahon BJ.The natural history of chronic hepatitis B virus infection[J].Semin Liver Dis,2004,24(Suppl 1):17-21.
[8]Hoofnagle JH,Doo E,Liang TJ,et al.Management of hepatitis B:summary of a clinical research workshop[J].Hepatology,2007,45(4):1056-1075.
[9]Lok AS,McMahon BJ.Chronic hepatitis B[J].Hepatology,2007,45(2):507-539.
[10]Ganem D,Prince AM.Hepatitis B virus infection-natural history and clinical consequences[J].N Engl J Med,2004,350(11):1118-1129.
[11]Fattovich G.Natural history and prognosis of hepatitis B[J].Semin Liver Dis,2003,23(1):47-58.
[12]Fattovich G,Stroffolini T,Zagni I,et al.Hepatocellular carcinoma in cirrhosis:incidence and risk factors[J].Gastroenterology,2004,127(Suppl):S35-S50.
[13]Hadziyannis SJ,Papatheodoridis GV.Hepatitis B e antigen-negative chronic hepatitis B:natural history and treatment[J].Semin Liver Dis,2006,26(2):130-141.
[14]World Health Organization.Guidelines for the prevention,care and treatment of persons with chronic hepatitis B infection[S].Geneva:WHO,2015.
[15]中华医学会肝病学分会感染病学分会.慢性乙型肝炎防治指南[J].中华肝脏病杂志,2005,13(12):881-891.
[16]邓俊.两种方法检测乙型肝炎病毒的对比分析[J].检验医学与临床,2013,10(3):303-304.
[17]谭璐.化学发光微粒子免疫分析法与酶联免疫法测定乙肝标志物的比较[J].实用学杂志,2008,15(3):294-295.
[18]Peng J,Cheng LM,Yin BT,et al.Development of an economic and efficient strategy to detect HBsAg:Application of gray-zones in ELISA and combined use of several detection assays[J].Cliniea Chimica Acta,2011,412(23/24):2046-2051.
Performance evaluation of Sysmex HISCL5000 in detecting HBV markers
EJianfei,LIULihong,CHENZongyao,WANGDengchao,YEMin,YUANChengliang△
(DepartmentofClinicalLaboratory,thePeople′sHospitalofDeyangCity,Deyang,Sichuan618000,China)
ObjectiveTo analyze performance of Sysmex HISCL5000 chemical luminescence immunity analyzer in detecting HBV markers.MethodsEvaluate the accuracy,linearity,carry pollution,the comparison results and detection limit of HISCL5000 according to Clinical and Laboratory Standards Institute(CLSI)documents.ResultsInter-inaccuracy of HISCL5000 in detecting HBsAg,HBsAb,HBeAg,HBeAb and HBcAb with low and high concentrations were 1.24%,1.05%,2.56%,2.27%,2.19%,1.95%,2.37%,1.43%,2.49%,1.29% respectively;Total-inaccuracy were 2.32%,1.74%,3.12%,2.45%,2.94%,2.96%,3.02%,1.82%,3.21%,1.54% respectively.The linearity of HBsAg and HBsAb were 0.976 5 and 0.951 6,the both greater than 0.95.The comparison result of HISCL5000 and e601 in HBsAg and HBsAb were 0.982 2 and 0.974 8.Coincidence of HISCL5000 and ELISA in HBsAg,HBsAb,HBeAg,HBeAb,HBcAb were 99.6%(550/552),93.5%(516/552),99.6%(550/552),94.9%(524/550),92.0%(508/552) respectively.The carry pollution of HISCL5000 when detecting HBsAg wasX=0.070 8,3SD(L-L)=0.106 2,X<3SD(L-L).Meanwhile detection limit in HBsAg and HBsAb were 0.006 IU/mL,0.213 6 mIU/mL.ConclusionHISCL5000 is suitable for clinical application with good precision,accuracy,linearity,carry pollution,the comparison results and detection limit.
hepatitis B virus;magnetic particle chemiluminescence enzyme immunoassay;serological markers;performance evaluation
2016-01-28修回日期:2016-03-18)
鄂建飞,男,主管检验师,主要从事临床免疫学研究。△
,E-mail:13568235628@163.com。
10.3969/j.issn.1673-4130.2016.12.020
A
1673-4130(2016)12-1647-04
·论著·

