糖尿病前期患者自主神经功能改变分析
黄菊香 李中健
郑州大学第二附属医院心电图科 郑州 450014
糖尿病前期患者自主神经功能改变分析
黄菊香李中健△
郑州大学第二附属医院心电图科郑州450014
【关键词】糖尿病前期;自主神经功能;心脏
糖尿病前期是由正常状态转为糖尿病的过渡,主要包括空腹血糖受损(impaired fasting glucose,IFG)和葡萄糖耐量减退(impaired glucose tolerance,IGT)。心脏自主神经病变是糖尿病严重的并发症之一,发生率高达25%~40%[1]。但一直缺乏简单、快捷、方便的客观指标评价心脏自主神经功能变化情况。本研究选用动态心电图分析软件,评价自主神经功能状态的指标心率减速力(DC)和心率变异性(HRV)评估糖尿病前期人群自主神经功能改变情况,并分析其相关因素。
1资料与方法
1.1一般资料选择2015-01—2015-11到我院进行健康体检者330例,男185例,女145例;平均年龄(53±17)岁。参照2009年ADA糖尿病诊疗指南[2]中糖尿病前期的诊断标准,根据葡萄糖耐量试验结果,将受试者分为血糖正常组(对照组)215例:空腹血糖(FPG)<6.1 mmol/L且餐后2 h血糖(2 h PG)<7.8 mmol/L;糖尿病前期组(研究组)115例:FPG<61 mmol/L,同时2 h PG≥7.8 mmol/L但<11.1 mmol/L。排除继发性血糖升高、已诊断为糖尿病的患者。
1.2方法
1.2.1葡萄糖耐量试验:试验前3 d,嘱所有受试者禁食咖啡、饮酒及吸烟,实验前禁食至少>10 h,避免剧烈活动和精神刺激。用75 g(无水葡萄糖)葡萄糖耐量试验负荷后2 h血糖水平代替餐后2 h血糖值。清晨抽取患者空腹血标本后,将75 g含水葡萄糖粉溶于200~300 mL水中,要求患者3~5 min内喝完,从患者服用第一口开始计时,于服后2 h抽取静脉血检测血糖。
1.2.2胰岛素抵抗指数计算方法:胰岛素抵抗指数=空腹血糖水平(FPG,mmol/L)×空腹胰岛素水平(FINS,mIU/L)/22.5。
1.2.3DC与HRV测量方法:所有受试者均采用美国DMS豪华版动态心电图监测仪行24 h动态心电图检查,记录完毕后回放数据,利用分析软件并进行人工校正后计算出DC 值和HRV指标。
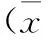
2结果
2.12组胰岛素抵抗指数(HOMA-IR)、DC、HRV值比较与对照组比,研究组DC较低,HOMA-IR较高,差异有统计学意义(P<0.05);研究组HRV指标(SDNN、rMMSD、pNN50)均低于对照组,差异有统计学意义(P<0.05)。见表1。
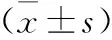
表1 2组HOMA-IR、DC、HRV值比较
2.2胰岛素抵抗指数与心率变异性各指标相关性分析Pearson相关分析显示,胰岛素抵抗指数与SDNN、rMMSD、pNN50呈负相关(r=-0.617、r=-0.356、r=-0.278,P< 0.01)。
3讨论
2003年美国糖尿病协会(American Diabetes Association,ADA)提出了“糖尿病前期”这一全新的概念,为糖尿病的防治提供了新的契机。调查显示,我国糖尿病前期患病率约为15.15%,未采取干预或治疗的情况下,该类人群35%~63%的人可转为糖尿病[3]。鉴于糖尿病发病率及由糖尿病引起的一系列并发症的发生率逐年增高,我们越来越多关注糖尿病前期的防治和干预,这对预防糖尿病的发生具有重要意义。
自主神经病变是糖尿病的并发症之一,但糖尿病前期是否有自主神经紊乱,一直缺乏明确的量化标准。近几年来,动态心电图中的DC、HRV值被用于评价自主神经系统的平衡状态,并得到临床学者的认可。为此,本研究应用动态心电图分析软件中DC、HRV两项指标,定性、定量分析糖尿病前期自主神经功能变化情况。
本研究结果显示,与对照组相比,研究组DC值较低,我们认为糖尿病前期患者迷走神经兴奋性减弱;心率变异性的3个指标SDNN、rMMSD、pNN50 也均较对照组降低,故我们认为糖尿病前期患者交感神经张力增高,迷走神经张力降低,二者的平衡状态遭到破坏,提示糖尿病前期存在自主神经功能失调。同时Pearson相关分析显示,胰岛素抵抗指数与SDNN、rMMSD、pNN50呈负相关,提示糖尿病前期自主神经调节功能障碍与胰岛素抵抗有关。
Sanyal等[4]在链脲霉素诱导的糖尿病大鼠的早期研究中发现,心脏迷走神经末梢递质已减少,表明心脏自主神经调节功能的损害在血糖调节初始受损时就已经存在。血糖升高可引起胰岛素抵抗、凝血功能障碍、纤维蛋白溶解系统功能异常、血管内皮细胞功能紊乱等病理变化,均可导致自主神经调节障碍。另有研究[5]显示,糖尿病前期人群,随着血糖增高,胰岛素抵抗程度不断加重,HRV的变化也越来越明显。胰岛素抵抗是糖尿病前期重要的病理生理机制,随着胰岛素抵抗作用不断加重,可导致炎症介质、氧化应激及糖基化产物释放增多,造成电解质及机体代谢紊乱,成为导致心脏自主神经调节障碍的致病基础;同时又伴有儿茶酚胺分泌增高,引起交感张力增高,压力感受器及心脏迷走神经张力受抑制,最终导致自主神经功能失衡。
综上所述,糖尿病前期患者已存在心脏自主神经功能障碍,对该类人群进行血糖监测,并检测、评估其心脏自主神经功能状态,及时采取相应干预措施,纠正自主神经功能紊乱,对降低糖尿病发病率及防止或延缓心脏自主神经调节功能损害具有重要意义。
4参考文献
[1]Beltrand J,Caquard M,Arnoux JB,et al.Glucose metabolism in 105 children and adolescents after pancreatectomy for congenital hyperinsulinism[J].Diabetes Care,2012,35(2):198-203.
[2]American Diabetes Association.Diagnosis and classification of diabetes mellitus[J].Diabetes Care,2010,3(1):S62-69.
[3]吴文炎.糖尿病前期的转归、危害及干预政策[J].中华全科医学,2010,8(1):88-90.
[4]Sanyal SN,Wada T,Yamabe M,et al.Synaptic degradation of cardiac autonomic nerves in streptozotocin-induced diabetic rats[J].Pathopysiology,2012,19(4):299-307.
[5]Wineles RM,Fowler MB.Insulin-resistant cardiomyopathy clinical evidence,mechanisms,and treatment options[J].J Am Coil Cardiol,2008,51(8):93-102.
(收稿2016-02-23)
通讯作者:△李中健,郑州大学第二附属医院心电图科;E-mail:lizhongjian56@126. com
【中图分类号】R747.9
【文献标识码】B
【文章编号】1673-5110(2016)12-0093-02

