亚低温血液净化技术对瓣膜病术后心源性休克患者炎症因子的影响*
肖红艳,刘 彬,许卫江,李 颖,危 宇,任海波
(武汉亚洲心脏病医院ICU,武汉 430022)
亚低温血液净化技术对瓣膜病术后心源性休克患者炎症因子的影响*
肖红艳,刘彬△,许卫江,李颖,危宇,任海波
(武汉亚洲心脏病医院ICU,武汉 430022)
[摘要]目的通过血液净化(CBP)技术控制不同的温度,对比观察常温和亚低温CBP对心脏瓣膜病术后心源性休克患者炎症因子水平的影响。方法将符合入选标准的95例患者分为常温CBP组(NT组,47例)和亚低温CBP组(HT组,48例),对比观察两组患者不同时间点的肿瘤坏死因子α(TNF-α)及白细胞介素(IL)-6、IL-8水平及临床结果。结果两组患者入选时各观察指标比较差异无统计学意义(P>0.05);与治疗前比较,治疗后两组患者TNF-α、IL-6、IL-8水平均明显下降(P<0.05),但HT组治疗后各个时间点下降幅度均高于NT组(P<0.05);急性生理与慢性病Ⅲ(APACHE Ⅲ)评分HT组在治疗后24 h较NT组低,且HT组在住ICU 时间、机械通气时间、CBP时间、病死率均低于NT组(P<0.05)。结论亚低温CBP通过清除炎症因子及抑制其产生,能更有效的减轻炎症反应。
[关键词]休克,心源性;亚低温;血液净化;炎症因子
体外循环术后由于缺血再灌注损伤、外科创伤、内毒素作用、血液与体外循环机的管道接触等诱发的炎症反应,激活机体的中性粒细胞、内皮细胞、血小板等引起肿瘤坏死因子α(TNF-α)及白细胞介素(IL)-6、IL-8等多种炎症因子的释放能形成逐级放大的瀑布样效应,导致全身炎症反应综合征,使得心血管功能进一步恶化,并引起多器官功能障碍、急性呼吸窘迫综合征等,导致病情进一步恶化,严重影响心脏外科患者的康复,因此抑制术后炎症反应就显得尤为重要。本研究旨在对比不同温度血液净化(continuous blood purification,CBP)治疗对术后心源性休克患者的炎症因子水平的影响。
1资料与方法
1.1一般资料采取前瞻性随机对照分组研究方法,选择2011年1月至2014年12月在本院行心脏瓣膜病置换术的心脏瓣膜病变患者,入选标准:(1)择期在全身麻醉低温体外循环下行心脏直视手术;(2)术前不合并冠状动脉粥样硬化性心脏病;(3)有Swan-Ganz导管监测;(4)术后出现心源性休克[心源性休克的诊断标准,血压小于90/60 mm Hg,且心输出量指数(cardiac index,CI)<2.5 L·min-1·m-2];(5)符合《CBP标准操作规程》并行CBP治疗的。排除标准:(1)术后存在围术期心肌缺血;(2)术后二次手术创伤的;(3)患者及家属不愿意接受该临床研究的。将符合上述标准的95例患者按照随机数字表,随机化分为常温治疗组47例(NT组),亚低温治疗组48例(HT组),两组患者临床资料,见表1。
1.2方法
1.2.1治疗方法患者术前留置尿管、桡动脉测压管,经颈内静脉放置三腔静脉管、Swan-Ganz(Edwards Lifesciences 7.5F)5腔导管,术毕放置心包纵隔引流管送ICU 监护;所有患者入ICU后取仰卧位,床头高30°,持续镇静、肌肉松弛、呼吸机辅助通气,使用Philip监护仪持续监测心电,Swan-Ganz导管接心排仪(Edwards LifesciencesTM Vigilance Ⅱ)监测;对符合CBP标准[1]的采用Seldinger技术经股静脉建立血管通路,使用GAMBRO-PRISMAFLEX型血液滤过机、CM-100型聚砜膜血滤器行连续性静脉-静脉血液滤过(CVVH)模式治疗,置换液采用改良的Port配方,稀释无抗凝生理盐水冲管法,置换液量35 mL·kg-1·h-1,血流量200 mL/min,连续24 h不间断。两组除温度外,其余治疗均相同,NT组采用血滤机加温,维持温度在36.5~37.3 ℃,HT组则不加温或将回血端管路置于冰水中,控制温度在34.0~35.0 ℃。
1.2.2记录指标统计两组入选时的临床资料和入选后6、12、24、48 h的血清TNF-α、IL-6、IL-8水平及急性生理与慢性病Ⅲ(APACHEⅢ)评分,并记录两组最终的住ICU 时间、机械通气时间、CBP时间及病死率。

2结果
2.1两组患者治疗前后各临床指标比较两组患者治疗前各临床指标、炎症因子水平及APACHE Ⅲ评分比较,差异无统计学意义(P>0.05),见表1。与治疗前比较,治疗后两组患者的血清炎症因子TNF-α、IL-6、IL-8水平均明显下降(P<0.05),但HT组治疗后各个时间点的炎症因子水平下降的幅度均高于NT组(P<0.05);APACHE Ⅲ评分HT组在治疗后24 h较NT组低(P<0.05),见表2。
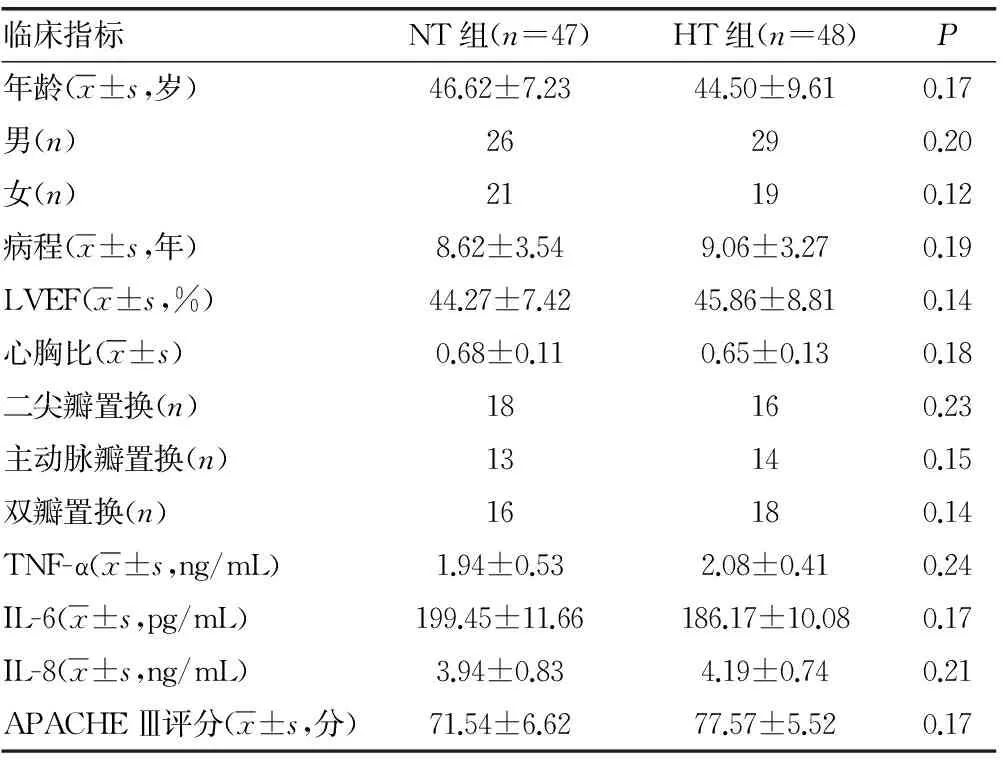
表1 两组患者治疗前临床一般资料比较
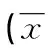
表2 两组患者治疗不同时间点各临床观察指标比较±s)
a:P<0.05,与同组0 h比较;b:P<0.05,与NT组比较。
2.2两组患者总的住ICU时间、机械通气时间等指标比较HT组在住ICU 时间、机械通气时间、CBP时间、病死率均低于NT组,且差异有统计学意义(P<0.05),见表3。
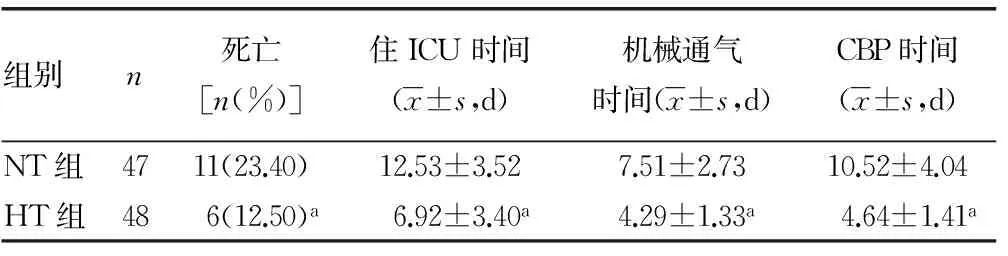
表3 两组临床预后的比较
a:P<0.05,与NT组比较。
3讨论
有报道显示重症心瓣膜病围术期病死率高达11.9%[2],而术后心源性休克是心瓣膜置换术后的主要死亡原因[3]。术后并发心源性休克的原因除了与术前心功能状态及术中心肌保护有关之外,与术后的全身炎症反应有密切关系。心脏体外循环手术后,由于手术创伤、应激反应及缺血再灌注损伤、血液接触异物管道等原因引起全身炎症反应,激活中性粒细胞并介导释放多种炎症介质,其中以TNF-α、IL-6、IL-8的表达水平升高为主[4-5], TNF-α、IL-6、IL-8在心脏手术围术期表达水平的变化国内外已有多家心脏中心进行过研究[6],在本组心脏瓣膜病变术后并发心源性休克患者中,以上3种炎症介质均显著升高。TNF-α被认为是参与炎症反应中最早、最重要的炎症细胞因子,它可以使血管内皮细胞通透性增加、血管内皮功能失调、全身血管阻力降低、发热、低血压、血液浓缩、代谢性酸中毒和循环休克;已有动物实验表明,TNF-α可以导致左心室功能的异常,造成持续的心肌收缩功能障碍[7]。IL-6则是急性期反应蛋白合成和炎性细胞积聚的主要因素,为炎症介质释放的第二高潮中的主要因子,能促进炎性因子的进一步释放,IL-6的升高和体外循环术后的心功能不全相关,可在早期敏感的反映组织损伤情况[8],有研究报道,释放或抗IL-6治疗可在一定程度上减轻体外循环后心肌缺血再灌注损伤[9]。IL-8是一种趋化性细胞因子,它的血浆水平被认为是严重组织损伤的标志,主要介导细胞毒和局部炎症有关的免疫应答辅助抗体生成,可以导致中性粒细胞脱颗粒并分泌释放弹性蛋白酶,导致内皮细胞损伤,使得微循环淤滞,器官功能障碍,组织损伤坏死[10]。因此,减轻炎性反应及通过清除炎症因子降低其在体内的血清浓度将有助于心脏术后患者循环功能的好转。在本组研究中NT组通过CBP治疗后TNF-α、IL-6、IL-8水平都有一定程度的下降,而且临床病情出现好转,APACHE Ⅲ评分下降,这与CBP减低心脏前负荷、改善内环境有关,同时因以上3种炎症因子均属于小分子物质,能通过CBP吸附和滤过方式有效的清除,改善其对心血管的抑制作用。但是决定血浆细胞因子血清浓度水平的关键性因素是细胞因子的生成与清除之间的平衡。在实验室研究中,亚低温已被证实能减少细胞炎性相关因子及氧自由基的生成和释放[11-12]。在本研究中,HT组与NT组除温度外其他治疗均一致,但HT组通过实施亚低温治疗后,检测的各个时间点的炎症因子水平下降的幅度均高于NT组,APACHE Ⅲ评分HT组在治疗后24 h较NT组更低,在住ICU 时间、机械通气时间、CBP时间、病死率方面也均低于NT组,说明通过亚低温CBP能更有效的降低炎症因子的水平,减轻炎症因子对组织器官的损害,同时亚低温通过降低基础代谢率,降低全身氧耗,改善氧供需失衡关系,从而改善临床的预后。
因此,本研究在瓣膜病术后难以纠正的心源性休克患者中,采用亚低温CBP清除炎症因子及减少炎症因子的产生,以减少其对心血管及其他组织器官的生物学效应,可改善临床预后。
参考文献
[1]陈香美,丁小强,刘伏友,等.血液净化标准操作规程[M].北京:人民军医出版社,2010:83-84.
[2]王立成,张向立,马为民,等.重症心脏瓣膜病的围术期处理[J].中国临床医生杂志,2008,36(9):35-36.
[3]丁凯,周华富,覃家锦,等.心瓣膜置换术后患者围术期死亡原因分析[J].中国胸心血管外科临床杂志,2011,18(1):80-82.
[4]Bayram H,Erer D,Iriz E,et al.Comparison of the effects of pulsatile cardiopulmonary bypass,non-pulsatile cardiopulmonary bypass and off-pump coronary artery bypass grafting on the inflammatory response and S-100beta protein[J].Perfusion,2012,27(1):56-64.
[5]Allan CK,Newburger JW,Mcgrath E,et al.The relationship between inflammatory activation and clinical outcome after infant cardiopulmonary bypass[J].Anesth Analg,2010,111(5):1244-1251.
[6]孙卓祥,陈廷.婴幼儿体外循环过程中炎症反应的变化[J].济宁医学院学报,2011,34(3):183-184.
[7]吴滨,吴自荣.肿瘤坏死因子-α与心脏疾病[J].生命的化学,2004,24(1):63-66.
[8]Stoney WS.Evolution of cardiopulmonary bypass[J].Circulation,2009,119(21):2844-2853.
[9]来薛,刘恩顺,孙增涛.慢阻肺与白细胞介素6研究进展[J].中国实用医药,2010,5(17):237-239.
[10]苗雪,官杰.IL-8的研究进展[J].齐齐哈尔医学院学报,2011,32(22):3693-3695.
[11]Rim KP,Kim K,Jo YH,et al.Effect of therapeutic hypothermia according to severity of sepsis in a septic rat model[J].Cytokine,2012,60(3):755-761.
[12]Kawamura N,Schmeichel AM,Wang Y,et al.Multiple effects of hypothermia on inflammatory response following ischemia-reperfusion injury in experimental ischemic neuropathy[J].Exp Neurol,2006,202(2):487-496.
doi:·经验交流·10.3969/j.issn.1671-8348.2016.18.031
基金项目:武汉市卫计委临床医学科研基金资助项目(WX13C48)。
作者简介:肖红艳(1978-),副主任医师,硕士研究生,主要从事心脏重症医学方面的研究。△通讯作者,E-mail:liubin02161@sina.com。
[中图分类号]R459.7
[文献标识码]B
[文章编号]1671-8348(2016)18-2546-03
(收稿日期:2015-12-25修回日期:2016-03-01)

