Fenton法预处理高浓度焦化废水的影响因素与动力学研究
殷旭东

摘 要:采用Fenton预处理高浓度焦化废水,以COD和挥发酚为评价指标,通过正交和单因素实验研究了废水初始pH值、H2O2量、[Fe2+]/[H2O2]和反应时间对处理效果的影响,同时对反应过程的动力学进行了探讨。结果表明:同时降解COD和挥发酚的最佳控制条件是pH值为3、H2O2投加量为170 mL/L、Fe2+/H2O2摩尔比为1:80、反应时间为20 min,此时COD和挥发酚的去除率分别达到80%和95%以上;COD的降解反应符合一级动力学方程规律,相关系数R2=0.991 5,反应速率常数为0.446 9 min-1。
关 键 词:Fenton法;高浓度焦化废水;正交试验;动力学
中图分类号:X 703 文献标识码: A 文章编号: 1671-0460(2016)04-0673-04
Abstract: Fenton process was applied to oxidize high concentration coking wastewater. Using removal efficiencies of COD and volatile phenol as evaluation index, through orthogonal experiment and single factor experiment, effect of operating conditions such as initial pH,hydrogen peroxide concentration, molar ratio of Fe2+/H2O2 and reaction time on treatment result was investigated, the optimal reaction conditions were determined, and the dynamics of the reaction process was discussed. The results show that, when pH value is 3, H2O2 dosing quantity is 170 mL/L, Fe2+/H2O2 is 1:80, the reaction time is 20 min, the degradation rates of COD and volatile phenol are more than 80% and 95% ,respectively. COD degradation reaction follows the first-order kinetic reaction equation, and the correlation coefficient R2 is 0.991 5, the reaction rate constant is 0.446 9 min -1.
Key words: Fenton process; High concentration coking wastewater; The orthogonal experiments; Dynamics
高浓度焦化废水具有以下特点[1-3]:①有机物浓度高,可高达几万乃至几十万mg/L;②成分复杂,含大量难降解有机物、无机物、重金属等;③色度较高,有刺激性气味。高浓度焦化废水对环境有着很强的毒害和危害性,降低此种废水对环境的危害具有重要意义。因为该废水各种污染物指标浓度较高,必须对其进行预处理到一定程度后,才可进入到生化阶段。
目前,国内外对高浓度焦化废水预处理的方法主要有[4-7]:物理法、化学法、物理化学法。Fenton试剂法属于物理化学法中的一种,该方法利用Fe2+和H2O2反应生成·OH自由基,利用其氧化性来处理难降解有机污染物,氧化速率快,被广泛的应用于各种高浓度废水处理[8]。
本研究拟采用Fenton法处理广东省某化工厂排放的高浓度焦化废水,通过正交和单因素实验研究废水初始pH值、H2O2量、[Fe2+]/[H2O2]和反应时间对处理效果的影响,并分析其反应过程的COD降解动力学,为高浓度焦化废水的预处理技术提供一定的参考和指导。
1 实验部分
1.1 实验仪器及用水
六联磁力加热搅拌器(江苏省金坛市友联仪器研究所,HJ-6型)、pH酸度计(上海仪电科学仪器股份有限公司,PHS-25型)、电子分析天平(梅特勒-托利多,AB204-E 型)、5管标准COD消解器(姜堰市国瑞分析仪器厂,HCA-100型)、紫外可见分光光度计(上海精密科学仪器有限公司,752N型)。高浓度焦化废水取自广东省某化工厂,COD为25 000~30 000 mg/L,BOD5为2 500~2 800 mg/L,氨氮为4 000~5 000 mg/L,挥发酚为1 300~1 500 mg/L,氰化物为10~20 mg/L,pH为7~9,色度为1 500~2 500(倍)。
1.2 分析测试方法
pH测定-玻璃电极法;COD测定-重铬酸钾法;挥发酚测定-4氨基安替比林直接光度法;COD和挥发酚的降解动力学采用一级动力学方程拟合:
1.3 实验方法
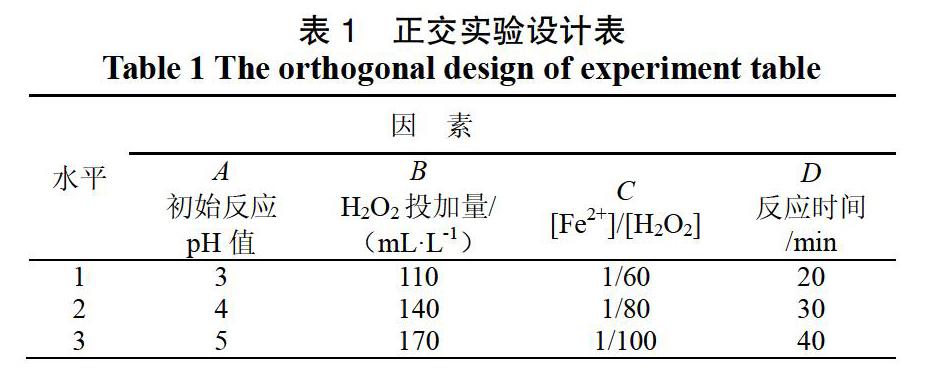
正交实验:选定废水初始pH值分别为3、4、5;H2O2投加量分别为110、140、170 mL/L;Fe2+/H2O2摩尔比分别为1/60、1/80、1/100;反应时间分别为20、30、40 min;采用L9(34)正交实验确定各影响因素的重要性和最佳反应条件。
单因素实验:取1 000 mL水样,分别考察不同H2O2投加量、初始pH值、Fe2+/H2O2摩尔比、反应时间对废水的COD和挥发酚的去除效果。每个实验条件下,待充分反应后用NaOH将水样的pH调至11左右,取水样测定COD和挥发酚浓度。
2 结果与讨论
2.1 正交实验
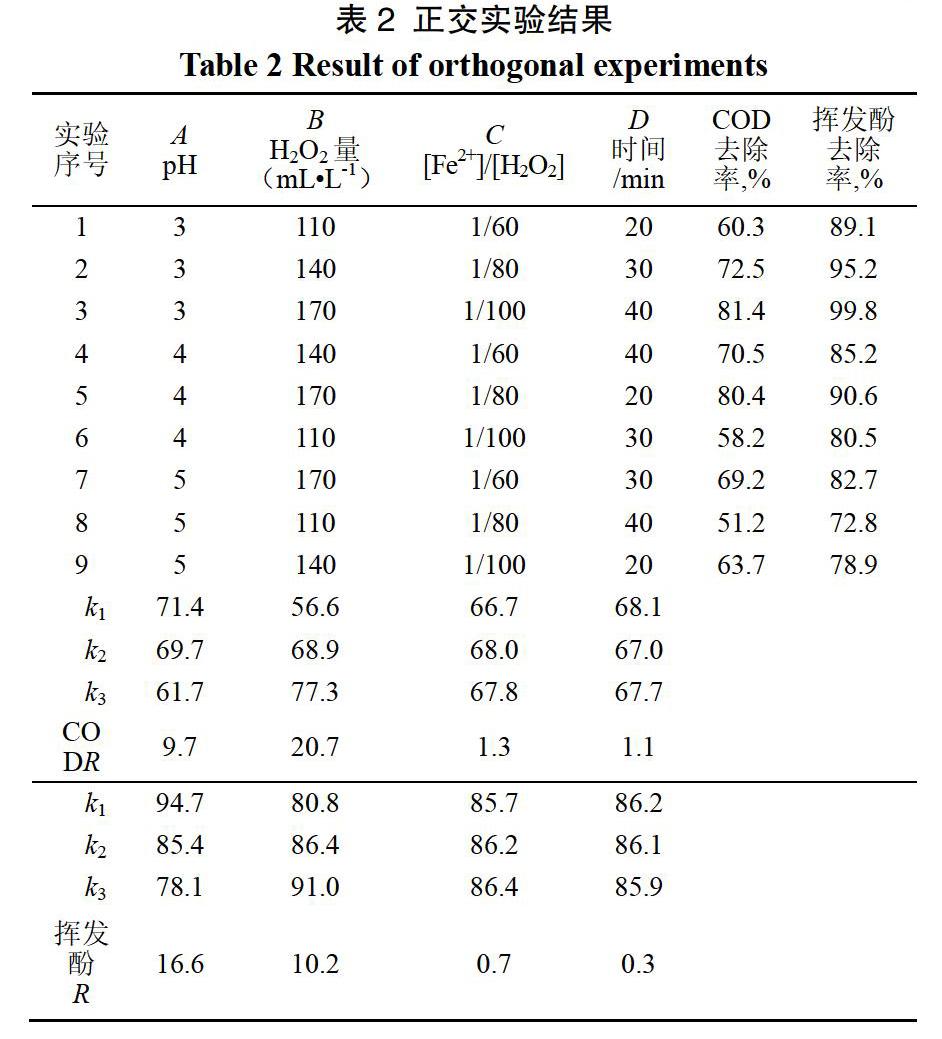
正交实验设计表和实验结果见表1和表2。
由表2可知,决定COD去除率高低的影响因素优先顺序为H2O2投加量、初始pH值、Fe2+/H2O2摩尔比、反应时间,得到最佳工艺参数组合为A1B3C2D1;决定挥发酚去除率高低的影响因素优先顺序为初始pH值、H2O2投加量、Fe2+/H2O2摩尔比、反应时间,得到最佳工艺参数组合为A1B3C3D1。根据污水处理投入最小化,处理效果最优化原则,得出最佳工艺组合为A1B3C2D1,即pH值为3、H2O2投加量为170 mL/L、Fe2+/H2O2摩尔比为1∶80、反应时间为20 min。
2.2 单因素实验
2.2.1 最佳H2O2投加量的确定
根据2.1的正交实验结果,取5个体积为1 000 mL的水样,实验过程中均保持pH值为3、Fe2+/H2O2摩尔比为1∶80、反应时间为20 min,考察H2O2投加量分别为70、100、150、200、250 mL/L时对COD和挥发酚去除效果的影响,实验效果见图1。该批实验原水的COD为27 791 mg/L,挥发酚为1 382 mg/L。
图1表明,当H2O2 投加量小于150 mL/L时,伴随H2O2 投加量的增加,系统反应产生的·OH也逐步增多,氧化能力逐步提高,所以COD和挥发酚去除率呈现增加的趋势;当H2O2 投加量大于150 mL/L时,过量的H2O2 会与·OH反应生成HO2·,·OH的产生量并没有继续增加,这时COD和挥发酚去除率呈现平稳的趋势。因此确定H2O2的最佳投加量为150 mL/L,此时COD和挥发酚的去除率分别达到81.3%和99.8%。
2.2.2 最佳初始pH值的确定
结合2.2.1的实验结果,取6个体积为1 000 mL的水样,实验过程中均控制H2O2投加量为150 mL/L,Fe2+/H2O2摩尔比为1/80、反应时间为20 min,考察废水pH值分别为2、3、4、5、6和7时对COD和挥发酚去除效果的影响,实验效果见图2。该批实验原水的COD为25 860 mg/L,挥发酚为1 320 mg/L。
图2表明,当pH之小于3时,COD和挥发酚的去除率逐渐增加,这是因为随着pH值的降低,Fe2+的催化性能减弱;当pH之大于3时,COD和挥发酚的去除率逐渐减小,这是因为较高的pH一方面会抑制·OH的产生,另一方面会使铁离子形成氢氧化物沉淀,影响其利用率[9]。所以在pH值为3时,效果最好,COD和挥发酚的去除率分别达到81.4%和95.2%。
2.2.3 最佳Fe2+/H2O2摩尔比的确定
结合2.2.1和2.2.2的实验结果,取5个体积为1 000 mL的水样,实验过程中均控制初始反应pH值为3、H2O2的投加量为150 mL/L、反应时间为20 min,考察Fe2+/H2O2摩尔比分别为1/40、1/80、1/100、1/120、1/140时对COD和挥发酚去除效果的影响,实验效果见图3。该批实验原水的COD为25 400 mg/L,挥发酚为1 313 mg/L。
图3表明,当Fe2+/H2O2摩尔比小于1/80时,COD和挥发酚去除率逐渐增大,这是因为过低Fe2+/H2O2摩尔比不利于·OH的产生;当Fe2+/H2O2摩尔比大于1/80时,COD和挥发酚去除率逐渐减小,这是因为过高的Fe2+/H2O2摩尔比,会使·OH利用率减小[10]。结合处理成本的问题可知,最佳的Fe2+/H2O2摩尔比为1/80,此时效果最好,COD和挥发酚的去除率分别达到74.5%和96.1%。
2.2.4 最佳反应时间的确定
结合2.2.1、2.2.2和2.2.3的实验结果,取4个体积为1 000 mL的水样,实验过程中均控制初始反应pH值为3、H2O2的投加量为150 mL/L、Fe2+/H2O2摩尔比为1/80,考察反应时间分别为10、20、40、60 min时对COD和挥发酚去除效果的影响,实验效果见图4。该批实验原水的COD为28 762 mg/L,挥发酚为1 426 mg/L。
图4表明,随着反应时间的进行,COD和挥发酚去除效果呈现先增加后趋于平稳的趋势。反应进行20 min时,COD和挥发酚去除效果最好,分别达到80.1%和96.8%。
2.3 稳定运行实验
采用各单因素研究的最佳条件下,即H2O2的投加量为150 mL/L,pH值为3,Fe2+/H2O2摩尔比为1/80,反应时间为20 min,在常温下进行5次重复性实验。实验结果表明:COD去除率在78%~82%之间,挥发酚的去除率均在95%以上,对COD和挥发酚的去除效果较高,具有良好的重复性,同时B/C比从0.1提高到0.34。
2.4 COD动力学分析
根据雷庆铎的研究成果[11],采用一级动力学方程拟合不同反应时间下COD的降解过程。动力学分析以综合指标COD为研究对象,根据出水COD浓度随时间的变化,对COD降解进行动力学分析。
由图4可知,在20 min后出水COD基本达到稳定,结合最佳单因素条件选取H2O2的投加量为150 mL/L,pH值为3,Fe2+/H2O2摩尔比为1/80,分析反应时间为0、5、10、15、20 min时刻的COD降解情况,用C0表示原水COD浓度,Ct表示上述不同时刻的出水COD浓度,以-ln(Ct/C0)对时间t做线性回归,结果如图5所示。
由图5可知,线性方程为-ln(Ct/C0)=0.4469t-0.3845,相关系数R2=0.991 5,反应速率常数为0.4469 min-1。由此可见,在单因素最佳控制条件下,Fenton法对COD的降解速率很快。
3 结 论
(1)正交实验结果表明:决定COD去除率高低的影响因素优先顺序为H2O2投加量、初始pH值、Fe2+/H2O2摩尔比、反应时间;决定挥发酚去除率高低的影响因素优先顺序为初始pH值、H2O2投加量、Fe2+/H2O2摩尔比、反应时间。同时降解COD和挥发酚的最佳控制条件是pH值为3、H2O2投加量为170 mL/L、Fe2+/H2O2摩尔比为1:80、反应时间为20 min。
(2)在各单因素最佳控制条件下稳定运行的实验表明:COD去除率在78%~82%之间,挥发酚的去除率均在95%以上。
(3)COD的降解反应符合一级动力学方程,线性方程为-ln(Ct/C0)=0.4469t-0.384 5,相关系数R2=0.991 5,反应速率常数为0.446 9 min-1。
参考文献:
[1] Zhao Jianliang,Chen Xiaowen,Yan Bo,et al. Estrogenic Activity and Identification of Potential Xenoestrogens in a Coking Wastewater Treatment Plant[J]. Ecotoxicol Environ Saf,2015,112:238 - 246.
[2] 李建军,马超.混凝剂Hf-168系列在焦化废水处理中的试验研究[J]. 冶金动力,2014(6):65-67.
[3] 金文学,朱筱滢,吕树光. 焦化废水除氰工艺的优化研究[J]. 环境污染与防治,2015,37(6):79-82.
[4] D.S. Guo, Q.T. Shi, B.B. He, X.Y. Yuan. Different solvents for the regeneration of the exhausted activated carbon used in the treatment of coking wastewater[J]. Journal of Hazardous Materials, 2011, 186(2-3): 1788-1793.
[5] A.D. Bokare, W.Y. Choi. Review of iron-free Fenton-like systems for activating H2O2 in advanced oxidation processes[J]. Journal of Hazardous Materials, 2014, 275: 121-135.
[6] Lai Peng, Zhao Huazhang, Wang Chao, et al. Advanced treatment of coking wastewater by coagulation and zero-valent iron processes[J]. Journal of Hazardous Materials,2007,147 (1/2):232-239.
[7] 韩剑宏,刘派, 王维大,等. 硅酸钙吸附处理焦化废水的试验研究[J]. 无机盐工业,2011,43(7):45-47.
[8] 曾丹林,刘胜兰,张崎,等. Fenton及其联合法处理有机废水的研究进展[J]. 工业水处理,2015,35(4):14-17.
[9] 魏健, 范冬琪, 宋永会,等. Fenton氧化/混凝沉淀协同处理腈纶聚合废水[J]. 环境工程学报,2015,9(1):14-18.
[10]李再兴, 左剑恶, 剧盼盼,等. Fenton氧化法深度处理抗生素废水二级出水[J]. 环境工程学报,2013,7(1):132-136.
[11]雷庆铎, 刘依林, 谷启源,等. 电催化氧化预处理焦化废水的实验研究[J]. 工业水处理,2014,34(4):51-54.

