下肢深静脉血栓合并肺栓塞的危险因素分析*
冯玉倩, 张少韶, 余 淼, 杨慧敏, 龙 琦, 丁培武, 王 敏
华中科技大学同济医学院附属协和医院心内科基础研究室,武汉 430022
下肢深静脉血栓合并肺栓塞的危险因素分析*
冯玉倩#,张少韶#,余淼,杨慧敏,龙琦,丁培武,王敏△
华中科技大学同济医学院附属协和医院心内科基础研究室,武汉430022
摘要:目的探讨下肢深静脉血栓患者发生肺栓塞的危险因素。方法采用病例-对照研究的方法,收集华中科技大学同济医学院附属协和医院2013年1月到2014年12月确诊的下肢深静脉血栓患者共421例,根据肺动脉计算机断层摄影血管造影术(CTPA)的结果,将合并肺栓塞的患者纳入病例组,不合并肺栓塞的患者纳入对照组,并筛选各危险因素,用多因素Logistic回归分析其与肺栓塞的相关性。结果421例下肢深静脉血栓患者中,219例发生肺栓塞,通过多因素Logistic回归分析显示:合并存在心脑血管疾病(OR=1.795,95%CI 1.146~2.811,P=0.011)、慢性炎症性疾病(OR=2.333,95%CI 1.386~3.927,P=0.001)与下肢深静脉血栓患者发生肺栓塞密切相关。其中心脑血管疾病包括脑梗死、高血压、冠心病、房颤、心脏瓣膜病、心源性肺动脉高压、扩张型心肌病。Logistic回归分析显示冠心病(OR=2.792,95%CI 1.177~6.623,P=0.020)、心源性肺动脉高压(OR=11.472,95%CI 1.402~93.899,P=0.023)、心脏瓣膜病(OR=12.625,95%CI 1.560~102.177,P=0.017)、扩张型心肌病(OR=2.626,95%CI 1.028~6.711,P=0.044)是下肢深静脉血栓患者发生肺栓塞的危险因素。慢性炎症性疾病包括呼吸系统慢性炎症性疾病、消化系统慢性炎症性疾病、慢性肾炎、结缔组织病,单因素分析显示呼吸系统慢性炎症性疾病(P<0.01)是下肢深静脉血栓患者发生肺栓塞的危险因素,其中慢性支气管炎(OR=10.152,95%CI 2.379~46.456,P=0.002)、慢性肺炎(OR=5.902,95%CI 1.254~27.787,P=0.025)的作用尤为显著。结论下肢深静脉血栓形成的患者合并心脑血管疾病和慢性炎症性疾病,尤其是合并冠心病、心脏瓣膜病、心源性肺动脉高压以及慢性肺炎和慢性支气管炎,发生肺栓塞的危险性增加。
关键词:深静脉血栓形成;肺栓塞;危险因素;Logistic回归分析
静脉血栓栓塞症包括肺栓塞和深静脉血栓形成。肺栓塞发病率及致死率均较高,美国每年有60万人发生肺栓塞[1],中国发病率为0.1%,虽低于西方国家,但也呈逐年上升趋势[2]。肺栓塞作为下肢深静脉血栓形成的一个严重并发症,主要是由深静脉血栓脱落导致[3]。然而,影响血栓稳定性和导致静脉血栓脱落的危险因素目前尚不清楚。因此,本研究拟回顾性分析2013年1月到2014年12月在我院治疗的下肢深静脉血栓患者的病例资料,初步筛选血栓脱落发生肺栓塞的危险因素。
1资料与方法
1.1研究对象
采用病例-对照研究方法,回顾性收集2013年1月~2014年12月在华中科技大学同济医学院附属协和医院住院治疗的下肢深静脉血栓形成的患者共421例,入院后给予下肢静脉超声及肺动脉计算机断层摄影血管造影术(CTPA)检查,根据CTPA造影有无肺动脉内的充盈缺损及血管截断,将观察对象分为病例组和对照组,发生肺栓塞的患者纳入病例组,不发生肺栓塞的患者纳入对照组。
1.2研究方法
分别采集两组患者的人口学特征及病史资料,包括:性别、年龄、吸烟史、饮酒史、2个月内手术史、是否制动,以及高脂血症、高尿酸血症、恶性肿瘤、剖宫产和分娩、2型糖尿病、慢性炎症性疾病(包括呼吸系统慢性炎性疾病、消化系统慢性炎性疾病、慢性结缔组织病、慢性肾炎)、心脑血管疾病(包括脑梗死、冠心病、高血压、房颤、心源性肺动脉高压、心脏瓣膜病、扩张型心肌病、外周动脉疾病)等病史。
1.3统计学处理

2结果
2.1一般资料分析
纳入研究的下肢深静脉血栓患者共421例,其中男性226例,女性195例,年龄范围为(54.0±15.4)岁。有吸烟史129例,有饮酒史97例,2个月内有手术史83例,制动者159例,剖宫产和分娩者18例,患恶性肿瘤22例,患高脂血症17例,患高尿酸血症10例,患2型糖尿病37例,患慢性炎症性疾病105例,患心脑血管疾病166例。见表1。
2.2各危险因素Logistic回归分析
在421例下肢深静脉血栓形成的病例中,以是否发生肺栓塞为因变量,以性别、吸烟史、饮酒史、2型糖尿病、高脂血症、高尿酸血症、制动、2个月内手术史、剖宫产和分娩、恶性肿瘤、心脑血管疾病、慢性炎症性疾病为自变量,进行Logistic回归分析筛选出有统计学意义的指标。其中,心脑血管疾病(OR=1.795,95%CI1.146~2.811,P=0.011),慢性炎症性疾病(OR=2.333,95%CI1.386~3.927,P=0.001)病史与下肢深静脉血栓患者发生肺栓塞密切相关。见表2。

表1 观察对象的人口学特征及病史[例(%)]

表2 肺栓塞发生危险因素Logistic回归分析结果
2.3心脑血管疾病分类Logistic回归分析
将心脑血管疾病细分为脑梗死、冠心病、高血压、房颤、肺动脉高压、心脏瓣膜病、扩张型心肌病、外周动脉疾病,并以之为自变量,以是否发生肺栓塞为因变量,采用Logistic回归模型进行分析。其中,合并冠心病(OR=2.792,95%CI1.177~6.623,P=0.020)、心源性肺动脉高压(OR=11.472,95%CI1.402~93.899,P=0.023)、心脏瓣膜病(OR=12.625,95%CI1.560~102.177,P=0.017)、扩张型心肌病(OR=2.626,95%CI1.028~6.711,P=0.044)是下肢深静脉血栓患者发生肺栓塞的危险因素。见表3。

表3 发生肺栓塞的心脑血管疾病分类Logistic回归分析结果
2.4不同慢性炎症性疾病与肺栓塞发生的关联性分析
将慢性炎症性疾病细分为呼吸系统慢性炎症性疾病、消化系统慢性炎症性疾病、慢性结缔组织病、慢性肾炎,通过卡方检验显示:呼吸系统慢性炎症性疾病(P<0.001)是下肢深静脉血栓患者发生肺栓塞的危险因素。见表4。
2.5呼吸系统慢性炎症性疾病分类Logistic回归分析
将呼吸系统慢性炎症性疾病分为慢性支气管炎、慢性肺炎、哮喘和陈旧性肺结核,通过Logistic回归分析显示:慢性支气管炎(OR=10.152,95%CI2.379~46.456,P=0.002)、慢性肺炎(OR=5.902,95%CI
1.254~27.787,P=0.025)是下肢深静脉血栓患者合并肺栓塞的危险因素。见表5。
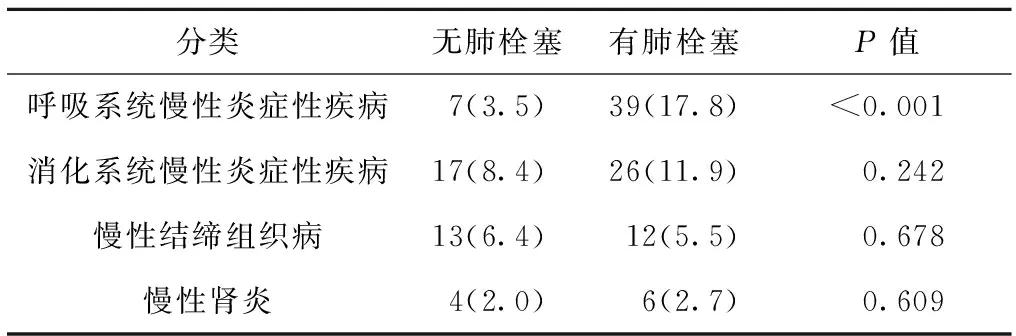
表4 是否发生肺栓塞与慢性炎症性疾病关联的卡方检验结果
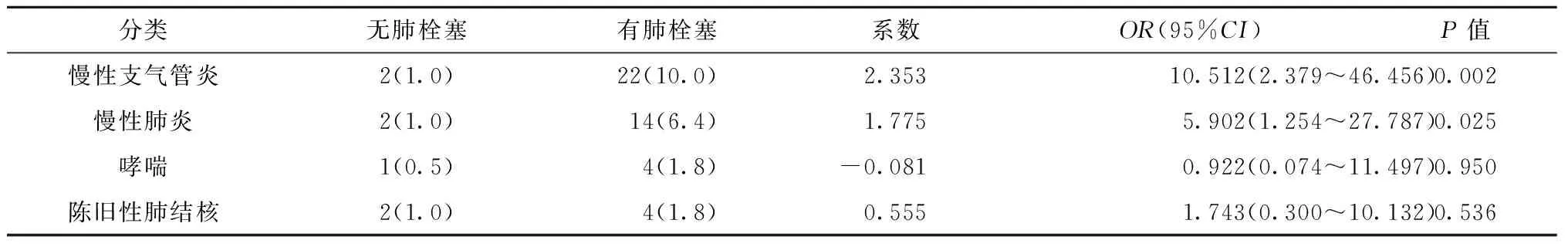
表5 呼吸系统慢性炎症性疾病与肺栓塞关联性分析结果
3讨论
依据2014年欧洲心脏病学会有关急性肺栓塞的指南,临床肺栓塞的诊断主要依靠肺动脉血管造影[4],然而前瞻性诊断研究发现其敏感性也只能达到83%[4],由此可见肺栓塞缺乏有效的预测方法。研究表明,临床确诊为肺栓塞的患者中有72%~82%合并有下肢深静脉血栓,而确诊为下肢深静脉血栓的患者中合并肺栓塞者达34%~58%[5],肺栓塞常常作为深静脉血栓的一种并发症而发生[6],血栓性栓子主要来自下肢静脉系统[7]。因此,我们认为从下肢深静脉血栓入手,筛选下肢深静脉血栓患者发生肺栓塞的危险因素显得尤为重要。
本研究将肺动脉血管造影新近确诊的肺栓塞患者均纳入病例组(包括有症状的和无症状的),肺动脉血管造影检测肺栓塞的敏感性比肺扫描高,因此以此为依据的组间划分更为准确,研究结果可能更加可信。本研究的终点为是否发展为肺栓塞,未进行随访,避免了长期随访过程中其他因素对研究结果的影响。本研究对各危险因素采取多因素Logistic回归,初步证实合并心脑血管疾病和慢性炎症性疾病是下肢深静脉血栓形成患者发生肺栓塞的危险因素。
本研究显示,在心脑血管疾病方面,合并冠心病、肺动脉高压、扩张型心肌病和心脏瓣膜病使下肢深静脉血栓形成患者发生肺栓塞的风险增大。已有研究证实心血管疾病是肺栓塞的危险因素[8-12]。但是心脑血管疾病导致下肢深静脉血栓患者发生肺栓塞的机制仍然未完全阐明,可以从以下几个方面来分析:①合并冠心病的患者由于心肌缺血甚至坏死,心脏收缩舒张功能不全,导致体循环和肺循环障碍,静脉血流淤滞,有利于静脉血栓形成;此外冠心病的患者血小板和凝血系统的活化以及纤维蛋白的更新加快,凝血因子增加,抗凝物质减少[13],血液处于高凝状态,因此易导致血栓形成。②心脏瓣膜病和扩张型心肌病最终均可导致心力衰竭,心衰时患者静脉回流受阻造成血流淤滞[13],左心房压力升高,通过压力诱导的损伤作用使血管内皮细胞功能紊乱[14]。有研究指出内皮功能紊乱和损伤是通过内皮祖细胞修复的,而心血管疾病可使内皮祖细胞数量减少和功能抑制[15],因此可以促进血栓形成。③合并心源性肺动脉高压的患者,由于右心室后负荷加大,右心射血分数降低,右心淤血,继而导致体循环瘀血,长期肺动脉高压时肺微血管结构重塑及呼吸屏障增厚,从而导致换气功能减弱[14],组织缺氧引起继发性红细胞增多,使血液流动性减弱。
本研究还显示慢性炎症性疾病是下肢深静脉血栓合并肺栓塞的危险因素,以呼吸系统的慢性炎症性疾病作用尤为突出。炎症反应和凝血系统通过许多交叉的细胞和分子不断地相互影响[16-17]。炎症主要是通过增加血液的凝固性来影响血栓形成的:①许多研究均报道TNF-α、CD40L、C-反应蛋白(CRP)可以增加白细胞表面组织因子的表达,从而增强内源性凝血途径的反应;②系统性炎症可以使血液中CRP浓度增高,研究证实,CRP可以促进单核细胞和内皮细胞的相互作用,并且促进纤溶酶原激活物抑制剂-1(PAI-1)和组织因子的产生[16,18];③炎性介质如IL-6和TNF-α不仅可以促进血小板的生成,使血小板数量增加,也可以增强血小板的反应性[16,18];④炎性细胞因子TNF-α,IL-1β等可以下调天然抗凝通路,尤其是蛋白C通路[16];⑤炎症反应导致的补体激活、凋亡和坏死可以通过提供凝血反应中关键的细胞膜表面而使血液处于高凝状态[18]。除此之外,炎症可能还与静脉血管的损伤有关[18-19]。因此,慢性肺炎和慢性支气管炎等呼吸系统的慢性炎症性疾病是导致肺栓塞形成的重要危险因素。
本研究显示性别、吸烟史、饮酒史、2型糖尿病、高脂血症、高尿酸血症、制动、2个月内手术史、剖宫产和分娩、恶性肿瘤等不是下肢深静脉血栓患者发生肺栓塞的危险因素,这与之前的相关研究结论相悖:Heit等[20]研究发现手术、创伤、恶性肿瘤、化疗等是静脉血栓性疾病的独立危险因素。分析原因可能是:①研究目的不同。以往研究的目的主要是研究肺栓塞发生的独立危险因素,而本研究的目的是研究深静脉血栓形成的患者血栓脱落导致肺栓塞的危险因素,重点在于影响血栓稳定性的危险因素。②研究方法不同。以往研究主要采取的是单因素分析,强调单个危险因素对肺栓塞形成的影响,而本研究采用多因素Logistic回归模型,同时研究多个危险因素对血栓稳定性的影响,考虑到了各危险因素之间的相互作用。③研究误差的影响。本研究为回顾性分析,资料的采集没有前瞻性研究可信度高,另外样本及参考资料选择的不同对研究结果也会有一定影响。此外,本项研究存在一定的局限性:本研究患者肺栓塞的确诊依靠肺动脉血管造影检查,由于患者经济问题或患者个人意愿等方面的影响,并不是所有下肢深静脉血栓形成的患者都进行了肺动脉血管造影检查,这就导致了一部分无症状肺栓塞的患者漏诊,从而使相关危险因素的作用扩大了。
总结以上,此次研究发现合并心脑血管疾病和慢性炎症性疾病的下肢深静脉血栓形成患者合并肺栓塞的危险性增大,特别是冠心病、心脏瓣膜病、肺动脉高压以及慢性肺炎和慢性支气管炎是下肢深静脉血栓患者合并肺栓塞的危险因素。
参考文献
[1]Gong D Y,Liu X F,Huang F J.Clinical feature analysis of fatal pulmonary thromboembolism:experiences from 41 autopsy-confirmed cases[J].Eur Rev Med Pharmacol Sci,2013,17(5):701-706.
[2]Liu M,Cui A,Zhai Z G,et al.Incidence of pleural effusion in patients with pulmonary embolism[J].Chin Med J(Engl),2015,128(8):1032-1036.
[3]Sevuk U,Bahadir M V,Altindag R,et al.Value of serial platelet indices measurements for the prediction of pulmonary embolism in patients with deep venous thrombosis[J].Ther Clin Risk Manag,2015,11:1243-1249.
[4]Konstantinides S V,Torbicki A,Agnelli G,et al.2014 ESC Guidelines on the diagnosis and anagement of acute pulmonary embolism[J].Eur Heart J,2014,35(43):3033-3069.
[5]Ghaye B,Willems V,Nchimi A,et al.Relationship between the extent of deep venous thrombosis and the extent of acute pulmonary embolism as assessed by CT angiography[J].Br J Radiol,2009,82(975):198-203.
[6]Sørensen H T,Horvath-Puho E,Lash T L,et al.Heart disease may be a risk factor for pulmonary embolism without peripheral deep venous thrombosis[J].Circulation,2011,124(13):1435-1441.
[7]杜捷夫,雷永红,杨光,等.单中心医疗机构20年肺栓塞发病的回顾性分析[J].中国危重病急救医学,2011,23(5):309-312.
[8]Sørensen H T,Horvath-Puho E,Lash T L,et al.Heart disease may be a risk factor for pulmonary embolism without peripheral deep venous thrombosis[J].Circulation,2011,124(13):1435-1441.
[9]Prandoni P,Pesavento R,Sørensen H T,et al.Prevalence of heart diseases in patients with pulmonary embolism with and without peripheral venous thrombosis:findings from a cross-sectional survey[J].Eur J Intern Med,2009,20(5):470-473.
[10]Sørensen H T,Horvath-Puho E,Pedersen L,et al.Venous thromboembolism and subsequent hospitalisation due to acute arterial cardiovascular events:a 20-year cohort study[J].Lancet,2007,370(9601):1773-1779.
[11]Piazza G,Seddighzadeh A,Goldhaber S Z.Heart failure in patients with deep vein thrombosis[J].Am J Cardiol,2008,101(7):1056-1059.
[12]Beemath A,Stein P D,Skaf E,et al.Risk of venous thromboembolism in patients hospitalized with heart failure[J].Am J Cardiol,2006,98(6):793-795.
[13]孙葵葵,王辰,古力夏提,等.深静脉血栓形成的危险因素及临床分析[J].中华结核和呼吸杂志,2004,27(11):727-730.
[14]Guazzi M,Phillips S A,Arena R et al.Endothelial dysfunction and lung capillary injury in cardiovascular diseases[J].Prog Cardiovasc Dis,2015,57(5):454-462.
[15]Lin C P,Lin F Y,Huang P H,et al.Endothelial progenitor cell dysfunction in cardiovascular diseases:role of reactive oxygen species and inflammation[J].Biomed Res Int,2013,2013:845037.
[16]Giannotta M,Tapete G,Emmi G,et al.Thrombosis in inflammatory bowel diseases:what's the link?[J].Thromb J,2015,13:14.
[17]Zöller B,Li X,Sundquist J,et al.Autoimmune diseases and v-enous thromboembolism:a review of the literature[J].Am J Cardiovasc Dis,2012,2(3):171-183.
[18]Esmon C T.The interactions between inflammation and coagulation[J].Br J Haematol,2005,131(4):417-430.
[19]Cermak J,Key N S,Bach R R,et al.C-reactive protein induces human peripheral blood monocytes to synthesize tissue factor[J].Blood,1993,82(2):513-520.
[20]Heit J A,Silverstein M D,Mohr D N,et al.Risk factors for deep vein thrombosis and pulmonary embolism:a population-based case-control study[J].Arch Intern Med,2000,160(6):809-815.
(2016-01-05收稿)
Analysis of Risk Factors of Pulmonary Embolism in Patients with Deep Venous Thrombosis
Feng Yuqian#,Zhang Shaoshao#,Yu Miaoetal
InstituteofCardiology,UnionHospital,TongjiMedicalCollege,HuazhongUniversityofScienceandTechnology,Wuhan430022,China
AbstractObjectiveTo analyze the risk factors of pulmonary embolism(PE)in patients with deep venous thrombosis(DVT).MethodsA total of 421 patients with DVT who were admitted and treated in Wuhan Union Hospital from January 2013 to December 2014 were enrolled in this case-control study.Patients were divided into case group(positive results of PE on CTPA)and control group(negative results of PE on CTPA).Data including sex,smoking,drinking,surgery,immobilization,cancer,parturition,diabetes,hyperlipemia,hyperuricemia,cardiovascular and cerebrovascular diseases,chronic inflammatory diseases,were compared between patients with and without PE.The risk factors of PE in patients with DVT were assessed using multivariate logistic regression.ResultsIn the 421 DVT patients,219(52%)developed PE.The multivariate logistic regression showed that concomitant cardiovascular and cerebrovascular diseases(OR=1.795,95%CI 1.146-2.811,P=0.011)and chronic inflammatory diseases(OR=2.333,95%CI 1.386-3.927,P=0.001)were significantly associated with the development of PE in DVT patients.Further statistical results indicated that coronary heart disease(OR=2.792,95%CI 1.177-6.623,P=0.020),cardiac pulmonary hypertension(OR=11.472,95%CI 1.402-93.899,P=0.023),heart valve disease(OR=12.625,95%CI 1.560-102.177,P=0.017),dilated cardiomyopathy(OR=2.626,95%CI 1.028-6.711,P=0.044),chronic pneumonia(OR=5.902,95%CI 1.254-27.787,P=0.025),and chronic bronchitis(OR=10.152,95%CI 2.379-46.456,P=0.002)were risk factors for PE.ConclusionCoronary heart disease,cardiac pulmonary hypertension,heart valve disease,dilated cardiomyopathy,chronic pneumonia and chronic bronchitis are risk factors of PE in DVT patients.
Key wordsdeep venous thrombosis;pulmonary embolism;risk factors;logistic regression analysis
中图分类号:R543.3
DOI:10.3870/j.issn.1672-0741.2016.03.017
*国家自然科学基金资助项目(No.81370425)
#同为第一作者
冯玉倩,女,1991年生,硕士研究生,E-mail:398294950@qq.com;
张少韶,男,1987年生,硕士研究生,E-mail:395920216@qq.com
△通讯作者,Corresponding author,E-mail:wm-xmy@163.com

