专题分析: 化学工业流程题(上)
◇ 北京 商晓芹(特级教师)
专题分析: 化学工业流程题(上)
◇北京商晓芹(特级教师)
化学工业流程题是高中化学中一类重要的试题.试题将理论和实际相结合,体现了化学知识在生产中的应用;试题引导学生从化学视角认识和分析工业生产过程中的实际问题,体现了学以致用;试题取材丰富,能很好地考查考生掌握的化学知识、技能、方法、学科素养以及运用所学知识解决实际问题的能力.因此,工业流程题是当前各省高考Ⅱ卷试题中的重要题型之一.
工业流程题涉及的学科知识厚重,考查内容宽泛,是教学中的难点.笔者结合多年的教学经验,对这部分内容进行了梳理,力求对大家“了解工业流程题的特点,掌握工业流程题的解题规律”有所帮助.
1工业流程题考查的内容
工业流程题以“元素化合物知识和化学反应原理”的核心内容为依托,围绕一个主题多点设问,将物质的性质、电解原理、化学平衡移动原理、氧化还原反应、离子反应、物质分离提纯以及化学计算等知识综合在一起,考查学生观察能力、获取信息的能力、应用获取信息结合已有知识分析和解决问题的能力、将分析解决问题的过程和结果用正确的化学用语和必要的文字进行表达并做出解释的能力.
2工业流程题的情景素材
工业流程题的情景素材来源于工业实际,如以各种矿石为原料制备物质(铬铁矿为原料制备重铬酸钾、以卤块儿为原料制备轻质氧化镁等)、以海水为原料制备物质、污水处理及废品中有用物质的提取等.
3工业流程题的结构特点
不管以什么任务为载体,工业流程题一般都由以下几部分构成:
1) 题干:提出任务或提出要解决的问题.
如碳酸锂广泛应用于陶瓷和医药等领域.以β-锂辉石(主要成分为Li2O·Al2O3·4SiO2)为原材料制备Li2CO3.
2) 流程图或生产工艺中操作步骤:给出解决问题的过程或措施.
如以β-锂辉石(主要成分为Li2O·Al2O3·4SiO2)为原材料制备Li2CO3的工艺流程如图1.

图1
3) 信息:以前学生没有学过,但解决问题所需要的相关资料.信息常以“已知”形式给出,常见的有化学用语、文字、图、表等.
如:已知Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2、12.7和1.3g. 又如:氯碱工业中电解饱和食盐水的原理如图2所示.
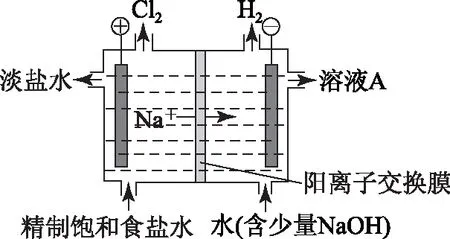
图2
4) 回答问题:常考的问题有加入的试剂及作用、采取的措施、操作名称、用到的仪器,化学方程式、离子方程式、电极反应式、陌生方程式等书写(多为氧化还原陌生方程式也有复分解反应),应用理论解释、相关的计算等.如:
(1) 步骤Ⅰ前,β-锂辉石要粉碎成细颗粒的目的是________.
(3) 步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有________.
(4) 步骤Ⅲ中,生成沉淀的离子方程式为________.
(5) 从母液中可回收的主要物质是________.
4工业流程题中的关键环节
解答工业流程题,必须理解工业流程题中的关键环节.
1) 原料.常见的原料有矿样(明矾石、蛇纹石、孔雀石、蓝铜矿、黄铜矿、锰矿、卤块儿、烧渣),废合金(含废铁、废铜),海水、工业废水、污水等.
2) 原料预处理.如矿石粉碎或煅烧、海带中提取碘时的灼烧,酸浸、碱浸、水浸,使有用的物质转化,易与杂质分离.
3) 物质的分离.常考过滤、洗涤、干燥、结晶,萃取、分液、蒸馏的操作.
过滤有趁热过滤和常温过滤.趁热过滤目的是避免过滤过程中析出晶体造成损失,适合溶解度受温度影响变化大的物质,如苯甲酸、硝酸钾、硫酸亚铁溶液.
结晶有蒸发结晶,降温结晶,蒸发、浓缩、冷却结晶.
4) 转化.常加入的物质及作用有:
a)酸:溶解矿样、去氧化物(膜),作沉淀剂、调pH促进反应发生.
b)碱:溶解矿样(溶解铝、氧化铝、二氧化硅等),去油污、去铝片氧化物(膜)、调pH促进水解形成沉淀.
c)氧化剂(还原剂):氧化(还原)某物质,使其转化为易于除去的离子.
d)氧化物和一些盐:调pH促进水解形成沉淀.如除去硫酸铜酸性溶液中的Fe3+,可向溶液中加入氧化铜或氢氧化铜、碳酸铜、碱式碳酸铜,调pH使Fe3+沉淀.
5) 其他措施.
a)加热煮沸:促进水解,聚沉后利于过滤分离;除去溶解在溶液中的气体,如氧气.
b)控制pH:促进某离子水解使其转化为沉淀,不让其他离子沉淀,通过过滤与其他离子分离,富集、电解等.
5工艺流程题的解题规律
1)要读懂这道题要解决什么问题,弄清给什么干什么,一般在试题的前2句话给出.
2)看看所给物质(原料)与要得到的物质(产品)之间有什么关系,即留哪些、去哪些、转化哪些.
3)运用所学的知识结合题给信息将问题解决.
解题过程中多运用“观察、比较、分析、综合”,注意“定性与定量”相结合.
(未完待续)
(作者单位:北京一零一中)

