纤维素类可吸收止血产品体外降解终点判断的研究
【作者】梅昕,马凤森,喻炎,陈海波,江滔 浙江工业大学药学院,杭州市,3004 浙江省医疗器械检验院,杭州市,3008
纤维素类可吸收止血产品体外降解终点判断的研究
【作者】梅昕1,马凤森1,喻炎1,陈海波2,江滔1
1 浙江工业大学药学院,杭州市,310014
2 浙江省医疗器械检验院,杭州市,310018
【摘要】为了准确、快速、有效地判断可溶性止血产品的体外完全降解时间,对GB/T 16886标准中现行的失重法进行了优化,采用透析袋结合还原糖测试法,于3%过氧化氢溶液、37 ℃、150 rpm条件下进行降解,第3 d、6 d、8 d、10 d、14 d取出透析袋,真空干燥测失重百分率,并测定了降解过程中透析袋外的还原糖累积含量,利用SPSS 22.0软件以Pearson Correlation Coeffi cient法对二者进行相关性分析。结果表明失重百分率与还原糖累积含量之间的相关系数为0.957,说明二者高度相关,验证了透析袋结合还原糖测试法评价体外降解终点的可行性。该方法也为其他类可溶性材料体外降解终点的判断提供思路。
【关 键 词】可吸收止血产品;相关性;完全降解时间;体外降解
0 引言
可吸收止血产品广泛应用于临床及日常生活中,主要包括胶原和微纤维胶原、医用止血明胶、氰基丙烯酸类组织胶、纤维蛋白类以及多糖类止血材料等[1]。其中微纤维胶原以及胶原纤维网、医用止血明胶与纤维蛋白胶类止血产品具有动物源性,患者可能发生过敏反应[2],潜在使用风险较高;氰基丙烯酸类组织胶在降解过程中释放氰和甲醛等有毒物质,容易引起炎症反应或不利伤口愈合[3]。而多糖类止血产品如纤维素类可吸收止血产品[4]具有来源丰富、价格低廉、生物相容性好、不良反应少等诸多优势,成为当前止血材料产品的研究热点[5]。
纤维素类可吸收止血产品目前存在的主要问题是不能在合适的时间内完全降解并吸收[6]。通过检索美国FDA MAUDE数据库,对52例速即纱(纤维素类止血产品)不良反应报告进行统计分析,发现由于感染和不完全吸收的原因约占不良反应事件总数的60%[7]。可吸收止血产品降解速度过快容易引发局部的高渗压和炎症等不良反应;降解速度过慢会引发排异、包裹等一系列免疫反应[7]。因此,理想的可吸收止血产品应满足合适的完全降解吸收时间。
当前,可吸收止血产品的完全降解吸收时间主要通过动物实验获得,但体内研究应考虑动物保护[8],此外动物实验存在个体差异、成本较高、操作困难等诸多缺陷。体外试验方法中,GB/T 16886标准[9]中用来初步评价材料降解性能的失重法,无法直接适用于像可吸收止血产品这类可溶性降解材料。因此,建立快速有效地判断可吸收止血产品的完全降解吸收时间的方法很有必要[10]。
1 材料和方法
1.1主要材料、试剂及仪器
材料 速即纱可吸收止血纱布(15.2 cm×22.9 cm,美国强生公司),透析袋(美国VISKASE公司,MD34 22MM,Mw:2000)
试剂 30%过氧化氢,氢氧化钠,酒石酸钾钠,3, 5-二硝基水杨酸,亚硫酸钠,纯化水
仪器 漩涡混合器(XW-80A,上海精科实业有限公司);电子微量天平(FA1604S,上海天平仪器厂);多功能酶标仪(Spectramax M2,美国分子仪器有限公司);调温电热器(TC-15,上海联营通州市申通电热器厂);真空干燥机(DZG-6020,上海森信实验仪器有限公司);震荡培养箱(BS-S,常州国华电器有限公司);冷冻干燥机(FreeZone 6,美国LABCONCO公司)
1.2材料的称量与降解
剪取相同面积的速即纱15片和透析袋20片,分为A、B、C、D、E五组,并称重。
透析袋经纯水煮沸10 min后取出,前15只透析袋中放入对应编号的止血纱布,并加7 mL新配3%过氧化氢浸没,排除气泡后,夹紧透析袋[11]。后5只透析袋加7 mL新配3%过氧化氢,作为空白对照。以上材料按编号分别置于20个250 mL烧杯中,再加120 mL新配3%过氧化氢,将烧杯口密封并置于震荡培养箱,设置温度37 ℃、转速150 rpm,保持14 d。同时每隔24 h透析袋外更换100 mL新配3%过氧化氢。
1.3失重百分率的计算
在第3 d、6 d、8 d、10 d、14 d分别取出A、B、C、D、E组,真空干燥至恒重,计算失重百分率[12],公式如下:

式中:
W-失重百分率,%;
Wo-纱布原始重量,g;
Wt-指定时间点纱布干燥后的重量,g。
1.4还原糖含量的测定
1.4.1DNS试剂的配制
称取96.028 0 g酒石酸钾钠,溶于250 mL纯化水,加热至45oC,再加3.160 7 g 3,5-二硝基水杨酸、131 mL氢氧化钠(2 mol/L)溶液,溶解后加2.511 0 g苯酚和2.500 3 g亚硫酸钠,搅拌溶解,冷却后加纯化水定容至500 mL,置棕色瓶中暗处保存7 d,备用[13]。
1.4.2标准曲线的绘制
称取0.100 g葡萄糖,纯化水定容至100 mL,分别取0、20、30、50、60、70 µL于1.5 mL离心管,再加纯化水至100 µL稀释成浓度为0、0.2、0.3、0.5、0.6、0.7 mg/mL的葡萄糖标准溶液,再各加100 µL DNS试剂,混匀后沸水浴5 min,流水浴冷却后分别向各离心管中加入800 µL纯化水,混匀后各移取200 µL溶液于96孔板中,用酶标仪测A540值。以葡萄糖质量浓度为横坐标、吸光度值(A)为纵坐标绘制标准曲线。
1.4.3还原糖含量的计算
收集E组烧杯透析袋外1~14 d的降解液,冷冻干燥48 h后加10 mL纯化水溶解,取100 µL于1.5 mL离心管中,再加100 µL DNS试剂,同“1.4.2”法操作,测吸光度值。计算还原糖浓度[14]及累积含量。
1.5统计分析
使用SPSS 20.0软件,采用Pearson Correlation Coeffi cient法对第3 d、6 d、8 d、10 d、14 d的失重百分率和还原糖累积含量两组数据进行相关性分析[15]。
2 结果
2.1失重百分率的计算
通过称量纱布降解前后重量,采用公式(1)计算失重百分率,第3 d、6 d、8 d、10 d、14 d的失重百分率分别为62.02±2.23%、85.94±0.33%、89.35±1.62%、93.87±0.90%、98.64±0.83%。
失重百分率随时间变化的曲线如图1所示。
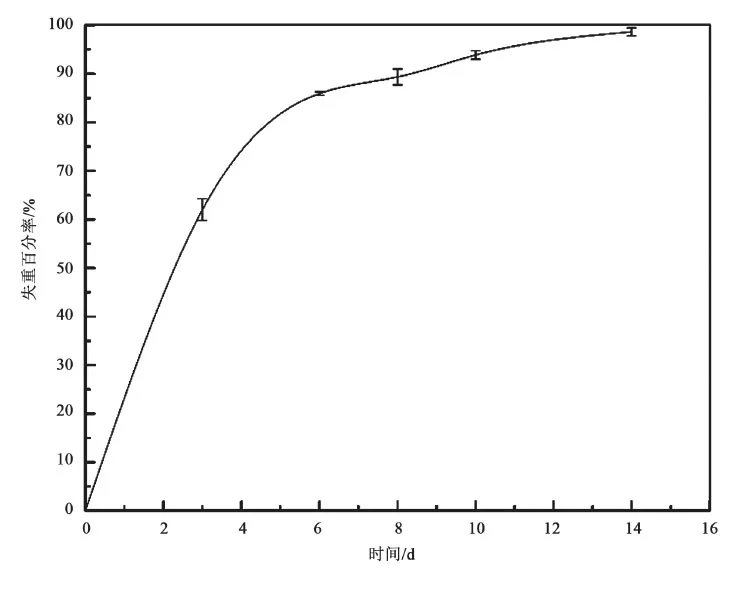
图1 失重百分率随时间的变化(n=3)Fig.1 The relationship between the percentage of weight loss and the time(n=3)
2.2标准曲线
如方法“1.4.2”所述,绘制标准曲线,得到线性回归方程:
Y=0.841 82x-0.004 36, r=0.998 4 (2)
2.3还原糖累积含量
如方法“1.4.2”所述,测得E组每天降解液中还原糖的含量,从而计算出降解液中还原糖累积含量,第3 d、6 d、8 d、10 d、14 d结果分别为16.12±1.69 mg、29.87±2.20 mg、34.92±2.40 mg、38.54±2.98 mg、45.23±0.16 mg。
还原糖累积含量随时间变化的曲线如图2所示。

图2 还原糖累积含量(n=3)Fig.2 Cumulative content of reducing sugar(n=3)
2.4失重百分率与还原糖累积含量的相关性分析结果
对失重百分率和还原糖累积含量进行Pearson Correlation Coefficient分析,结果发现两者之间的相关系数为0.957,在α=0.01水平(双侧)显著相关。
3 讨论
(1) 本研究对标准中的失重法进行了优化,首次采用透析袋与失重法结合的方法,失重百分率的RSD值均<5%,表明该方法的精密度良好。本课题组前期对另一生物技术有限公司出品的手术止血纱(纤维素类止血产品)采用同样的实验方法进行了体外降解研究,其失重百分率的RSD值均<5%,说明该方法可以适用于纤维素类可吸收止血产品体外降解终点的判断。该方法从理论上具备了用于其他类可溶性材料(如:壳聚糖类可吸收止血产品[16])体外降解终点判断的可行性,尚需对该方法进行验证和优化。
(2) 通过对还原糖累积含量的数据进行分析,可以看出还原糖的累积增加量明显小于纱布失去的质量,说明在纱布发生降解过程中,从透析袋中扩散出去的小分子物质可能部分是还原糖。降解产物复杂多样,其种类和含量还需进一步研究。
(3) 本研究通过对失重百分率与还原糖累积含量进行相关性分析,相关系数为0.957,结果表明两组数据具有高度相关性。透析袋内高分子材料在双氧水的氧化作用以及水解作用下,分子链断裂形成小分子物质而从透析袋中渗透出去,使透析袋内的纱布质量减少。从图1可以看出在第10 d透析袋内纱布的失重百分率已经趋于稳定,同样从图2也可以看出透析袋外还原糖累积含量在第10 d时也趋于稳定,说明第10 d纱布基本降解结束,第14 d达到降解终点。对于体外实验与体内实验数据之间的相关性,还需进一步研究来进行验证。
4 结论
本研究优化了失重法,较原有方法相比,该方法精密度良好,准确度高,应用范围更加广泛,可以用来准确地判断纤维素类可吸收止血产品体外降解终点。该方法对其他可溶性材料体外降解研究也有借鉴意义。
参考文献
[1] Emilia M, Luca S, Francesca B, et al. Topical hemostatic agents in surgical practice[J]. Transfus Apher Sci, 2011, 45(3): 305-311.
[2] Kim IY, Eichel L, Edwards R, et al. Effects of commonly used hemostatic agents on the porcine collecting system[J]. J Endourol, 2007, 21(6): 652-654.
[3] 张少锋, 洪加源. 医用生物可吸收止血材料的研究现状与临床应用[J]. 中国组织工程研究, 2012, 16(21): 3941-3944.
[4] 强生日前推出BIO和PT新品[J]. 中国医疗器械信息, 2014, (6): 74.
[5] 武岳, 王冰, 姚天明. 新型创伤急救止血材料的研究进展[J]. 中国临床实用医学, 2014, 5(4): 78-80.
[6] 张世庆, 赵雄, 鲁景艳, 等. 可吸收止血材料研究现状与相关技术要求[J]. 军事医学, 2012, 36(11): 862-866.
[7] 李玉基, 史玉清. MAUDE数据库中速即纱不良事件报告分析[J].中国药物警戒, 2013, 10(5):312-314.
[8] 中华人民共和国质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T 16886.2-2011, 医疗器械生物学评价. 第2部分: 动物福利要求[S].
[9] 中华人民共和国质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T 16886.13-2001, 医疗器械生物学评价 第13部分:聚合物医疗器械的降解产物的定性与定量[S].
[10] 熊绪琼, 梅昕, 马凤森. 多糖类可吸收止血材料的研究进展[J]. 中华创伤杂志, 2015, 31(6): 571-574.
[11] Zhu W, Wang B, Zhang Y, et al. Preparation of a thermosensitive and biodegradable microgel via polymerization of macromonomers based on diacrylated Pluronic/oligoester copolymers[J]. Europ Polymer J, 2005, 41(5): 2161-2170.
[12] Malwela T, Ray SS. Enzymatic degradation behavior of nanoclay reinforced biodegradable PLA/PBSA blend composites[J].Int J Biol Macromol, 2015, 77: 131-142.
[13] 张波. 生物化学与分子生物学实验教程[M]. 北京: 人民军医出版社, 2009.
[14] 邵锦挺, 应国清, 王琦, 等. 微型化DNS法测定多糖水解液中还原糖的质量浓度[J]. 浙江工业大学学报, 2012, 40(3): 250-252.
[15] 汪俊英, David Burns, 胡文立, 等. 血清25羟基维生素D水平与老年人卒中后抑郁的相关性[J]. 中华老年医学杂志, 2015, 34(6): 616-618.
[16] 外伤急救止血用新型急救止血敷片[J]. 中国医疗器械杂志, 2009, 33(4): 291.
Research of Determining Complete Degradation Time in Vitro Based on Cellulose Absorbable Hemostatic Products
【Writers】MEI Xin1, MA Fengsen1, YU Yan1, CHEN Haibo2, JIANG Tao1
1 College of Pharmaceutical Science, Zhejiang University of Technology, Hangzhou, 310014
2 Zhejiang Institute for the Control of Medical Device, Hangzhou, 310000
【Abstract】To develop a method for determining complete degradation time of soluble hemostatic products in vitro with accuracy, high speed and effectiveness, the current weight loss method originated from GB/T 16886 serial standards was optimized by using dialysis bag combined with assay of reducing sugar. The degradation was carried out with 3% hydrogen peroxide solution, at 37 ℃, 150 rpm. The dialysis bags were taken out in the 3rd, 6th, 8th, 10th and 14th day, vacuum drying followed by percentage of weight loss testing. Cumulative content of reducing sugar in degradation solution out of dialysis bag was determined simultaneously. The correlation analysis was performed by SPSS 22.0 equipped with Pearson Correlation Coeffi cient. The correlation coeffi cient between percentage of weight loss and cumulative content of reducing sugar was 0.957, which illustrated high correlation with each other. Hence dialysis bag combined with assay of reducing sugar is capable of evaluating the degradation endpoint of soluble hemostatic products in vitro. The method also provides a way for the evaluation of degradation of other degradable biomaterials in vitro.
【Key words】absorbable hemostatic products, correlation, complete degradation time, degradation in vitro
【中图分类号】R318.08
【文献标志码】A
doi:10.3969/j.issn.1671-7104.2016.02.015
文章编号:1671-7104(2016)02-0125-03
收稿日期:2015-12-08
作者简介:梅昕,E-mail: messi_power@126.com
通信作者:马凤森,教授,E-mail: merrigen@126.com

