低温电解条件下铝电解用NiFe2O4-10NiO基金属陶瓷阳极Fe元素腐蚀行为研究
郑 鑫,秦庆伟,杨建红,,杨文杰,刘 英,郭 洁
(1. 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2. 中国铝业郑州有色金属研究院有限公司绿色冶金与材料研究所,河南 郑州,450041)
低温电解条件下铝电解用NiFe2O4-10NiO基金属陶瓷阳极Fe元素腐蚀行为研究
郑鑫1,秦庆伟1,杨建红1,2,杨文杰2,刘英2,郭洁2
(1. 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2. 中国铝业郑州有色金属研究院有限公司绿色冶金与材料研究所,河南 郑州,450041)
摘要:采用粉末冶金技术制备出铝电解用NiFe2O4-10NiO陶瓷基体和30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷阳极,并在低温电解条件下,对NiFe2O4陶瓷相中Fe元素的腐蚀行为进行研究。结果表明,在烧结过程中,NiFe2O4尖晶石陶瓷基体会在氮气中发生离解,在动态化学腐蚀试验和电解试验中,陶瓷相中的Fe元素更容易进入电解质;电解24 h后,铝液中Fe、Ni、Cu的含量分别为0.45%、0.13%和0.03%。
关键词:NiFe2O4-10NiO;惰性阳极;铝电解;低温电解;铁元素;腐蚀
熔盐电解是轻金属和部分稀有金属的主要提取方法,其中铝电解规模最大,在熔盐电解中具有典型意义。我国铝电解技术目前还存在单位设备产率低、能耗高、能量利用低和单位投资大等缺陷,因此,加强工业节能降耗意义重大。目前,相关研究主要包括新型铝电解质体系、惰性阳极及阴极材料的改进及优化,大型电解槽的磁场、热场、流场模拟与研究等。其中,惰性阳极的研究是铝业界和材料界的关注重点和研究热点[1-3]。多年来,关于铝电解用惰性阳极的研究尽管取得了较大进展,但仍未达到工业应用水平。究其原因,从技术角度看,目前存在的主要问题是其耐腐蚀性不够强,所生产的原铝成本较高[4]。
前期的研究工作发现,NiFe2O4陶瓷具有尖晶石结构,对冰晶石熔体的侵蚀具有较强的抵抗能力,可用作惰性阳极基体材料[5]。Chin[6]在电解试验中发现NiFe2O4中的Fe、Ni并非以化学计量比溶解进入电解质,且Fe/Ni原子比总是大于NiFe2O4中的Fe、Ni化学计量比。考虑到NiFe2O4离解时Fe2O3与NiO在冰晶石熔体中溶解度的逆相关性[7],本文拟选择NiFe2O4-10NiO陶瓷基体,烧结制备出30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷阳极,通过低温化学腐蚀试验和电解实验,对Fe元素优先腐蚀行为进行研究,以期为制备性能良好的金属陶瓷阳极材料提供理论依据。
1实验
1.1试样制备
实验原料主要包括Cu、Ni、NiO、Fe2O3粉末,均为分析纯。首先,按质量分数为61.32%和38.68%分别称取Fe2O3、NiO粉末,球磨混合均匀并干燥后,在1000 ℃空气气氛下煅烧6 h,得NiFe2O4-10NiO陶瓷粉体。然后,以制得粉体为陶瓷相基料,配入质量分数为30%的Cu、Ni混合金属粉末(m(Cu)∶m(Ni)=2∶3),加入1.5% PVA作为黏结剂、乙醇作为分散剂,在聚四氟乙烯球磨罐中球磨180 min,得30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷粉体。将制得的两种粉体经干燥处理后,在150 MPa压力下压制成柱状(外径为30 mm、内径为10 mm、高约为7 mm)和块状(70 mm×45 mm×10 mm)两种规格的生坯,并分别于空气和氮气保护氛围下,按图1所示的升温制度进行烧结,最终得NiFe2O4-10NiO陶瓷基体和30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷烧结试样。

图1 烧结过程的升温制度
1.2实验方法
1.2.1电解质组成
动态化学腐蚀实验和电解实验所用电解质均
为钾冰晶石体系电解质,其化学组成及相关参数如表1所示。
1.2.2动态化学腐蚀实验
采用柱状NiFe2O4-10NiO和30(40Cu-Ni)/(NiFe2O4-10NiO)烧结试样进行动态化学腐蚀实验,其装置示意图如图2所示。实验过程中,先将电解质与连接完成的待测试样放入石墨坩埚中,并将试样悬于电解质上方,然后将石墨坩埚置于高温井式炉中,在Ar气保护氛围下进行加热,当电解质温度达到800 ℃时,将试样完全浸入电解质中开始旋转,转速控制为100 r/min,每隔一段时间用干净的钨丝取出一定量的电解质,用于测定其中Cu、Ni、Fe的含量。

表1 实验用电解质组成及参数
注:CR 表示电解质中NaF+KF与AlF3的摩尔比。

图2 动态化学腐蚀实验装置示意图
Fig.2 Schematic diagram of dynamic chemical corrision equipment
1.2.3电解实验
采用块状30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷试样作为阳极,TiB2可润湿性复合材料作为阴极进行电解实验,其装置示意图如图3所示。实验开始前,先将固化好的电极悬挂于电解质上方,随电解质一起加热至800 ℃,保温2 h,以确保电解质充分熔化,然后将电极完全浸入电解质中并开始通电,电流强度为20 A,电流密度为0.5 A/cm2,电解24 h。根据电解消耗速度,每隔一段时间补充一定量的Al2O3。待实验结束后,将阳极试样提升至电解液面以上,待电解槽冷却后取出电极和电解所得的铝块,清除其表面附着的电解质,并对电解后的阳极试样进行剖切、镶样、磨抛处理。
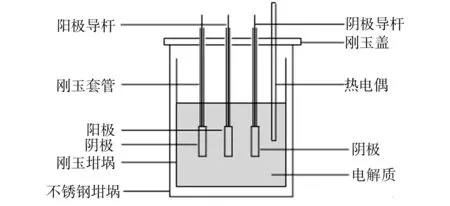
图3 电解实验槽装置示意图
1.3性能检测与表征
采用Archimedes排水法测定烧结样品的体积密度;采用Nova400Nano型场发射扫描电子显微镜(SEM)和能谱仪(EDS)表征和分析样品的组织形貌及微区成分;采用DGS-III型电感耦合等离子原子发射光谱仪(ICP)测定电解质和铝液中的杂质含量。
2结果与讨论
2.1烧结试样的物相分析
表2为NiFe2O4-10NiO陶瓷和30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷烧结试样的密度参数。由表2可见,两种试样烧结后致密度较高,且NiFe2O4-10NiO陶瓷试样的致密度略高于金属陶瓷试样。原因可能是在烧结金属陶瓷试样的过程中,由于金属粉末与陶瓷基体的浸润性较差,引起金属相溢出,产生少量气孔,导致所得金属陶瓷试样的致密度下降。
图4和图5分别为两种烧结试样的SEM照片和典型区域的EDS分析结果。由图4可见,NiFe2O4-10NiO陶瓷试样烧结后致密度高,孔洞少且很小,浅灰色的NiO相均匀分布在灰色NiFe2O4基底上;而30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷试样在烧结过程中,产生了少量气孔,致密度有所下降,白色的金属相呈不规则状均匀弥散分布在陶瓷相上。这与两种烧结试样体积密度的测定结果相一致。

表2 烧结试样的密度参数

(a)NiFe2O4-10NiO(b)30(40Cu-Ni)/(NiFe2O4-10NiO)
图4烧结试样的SEM照片
Fig.4 SEM images of as-sintered samples

(a) 点Ⅰ处(b) 点Ⅱ处
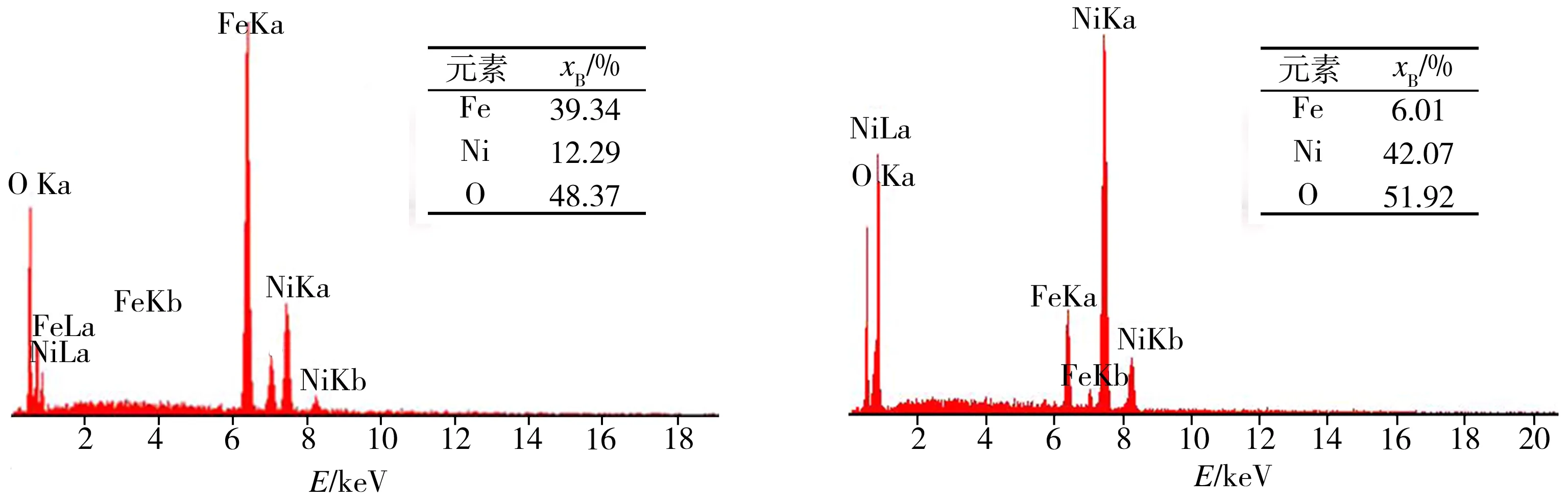
(c) 点Ⅲ处(d) 点Ⅳ处
图5图4中典型区域的EDS图谱
Fig.5 EDS spectra of typical areas in Fig.4
结合图5可知,NiFe2O4-10NiO陶瓷试样在空气中烧结后,NiFe2O4相中Fe/Ni原子比为1.90,接近NiFe2O4中Fe、Ni原子的化学计量比,表明NiFe2O4在烧结过程中并没有发生分解。30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷试样在氮气气氛下烧结后,金属相中被检测出含有少量Fe元素,且Ni/Cu原子比为2.95,大于初始时金属相中的Ni/Cu原子比(1.62),可能是陶瓷相中的Fe、Ni经烧结后被还原进入金属相所致;NiFe2O4相中Fe/Ni原子比为3.20,大于NiFe2O4中Fe、Ni的化学计量比,同时在NiO相中也发现少量Fe元素,表明NiFe2O4相中一部分Fe3+被还原成Fe2+,且部分Fe2+仍存在于NiFe2O4相中,而另一部分被还原的Fe2+则通过扩散进入NiO,形成(FexNiy)Oz相。
2.2烧结试样的低温化学腐蚀行为
为考察两种烧结试样在低温电解体系下的化学腐蚀行为,每隔一段时间测定电解质中溶解杂质元素的含量,其结果如图6所示。从图6可以看出,两组实验电解质中杂质含量的变化趋势基本相同:当实验时间少于4 h时,电解质中杂质含量显著增加,其中Fe元素含量增加最快;当实验进行8 h时,电解质中杂质元素的含量趋于稳定,此时Fe元素的溶解量远高于Cu、Ni。其中,对于NiFe2O4-10NiO烧结试样,其Fe元素在电解质中的溶出量比Ni元素高,这表明NiFe2O4尖晶石结构中的Fe比Ni更容易在该电解体系中溶出;而对于30(40Cu-Ni)/(NiFe2O4-10NiO)烧结试样,其Fe元素的溶解量则高于相同实验时间下的NiFe2O4-10NiO试样,可能是由于在氮气气氛下烧结的金属陶瓷试样中,部分NiFe2O4相已发生离解,使得部分不稳定相更易与电解质发生化学反应,导致Fe、Ni元素的溶出。
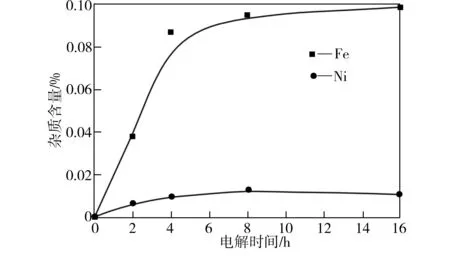
(a) NiFe2O4-10NiO

(b)30(40Cu-Ni)/(NiFe2O4-10NiO)
Fig.6 Variation of impurity content in electrolyte with the electrolysis time
2.3金属陶瓷阳极的低温电解腐蚀行为
30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷在低温电解过程中,电压稳定,平均值为3.44 V,电流效率达92%。图7为金属陶瓷阳极试样电解前后的外观形貌。由图7可见,阳极试样电解后形貌完整,表面附着有少量的电解质,但未出现肿胀和开裂现象。由ICP测定结果可知,电解后铝液中Fe、Ni、Cu的含量分别为0.45%、0.13%和0.03%。

(a) 电解前

(b) 电解后
图730(40Cu-Ni)/(NiFe2O4-10NiO) 金属陶瓷阳极电解前后的照片
Fig.7 Photos of as-sintered and electrolyzed 30(40Cu-Ni)/(NiFe2O4-10NiO) cermet anode
图8和图9分别为金属陶瓷试样电解24 h后膜层的SEM照片及不同区域的EDS图谱。由图8可见,金属陶瓷腐蚀边界较为平滑,在阳极外表面形成了厚约40 μm的电解膜,该层较为致密,孔洞较少,金属相明显消失,且NiO相也相对较少。这可能是由于电解过程中,阳极表层的金属相电化学活性较强,与电解质直接接触时易发生快速的电化学腐蚀,随着电解质不断地通过晶界向阳极内渗透,表层的金属相逐渐溶解消失;另一方面,阳极表面产生的氧也可通过扩散进入电解膜层,氧化其中的金属相,由于陶瓷相密度较低,被氧化的金属相体积膨胀,填充膜层中的部分孔洞,使得电解膜层更为致密。

图830(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷阳极电解24 h后的SEM照片
Fig.8 SEM image of electrolyzed 30(40Cu-Ni)/(NiFe2O4-10NiO) cermet anode
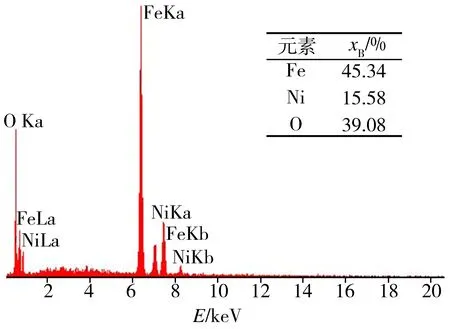
(a) 点Ⅰ处

(b) 点Ⅱ处
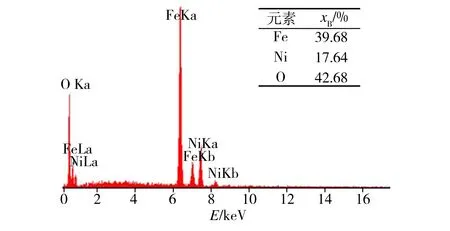
(c) 点Ⅲ处
结合图9可知,距离阳极表面200 μm(点I处)陶瓷相中Fe/Ni原子比为2.91,距阳极表面约40 μm(点II处)陶瓷相中Fe/Ni原子比为2.49,表面膜层区域(点Ⅲ处)陶瓷相中Fe/Ni原子比为2.25,从阳极内部到表面陶瓷相中Fe/Ni比呈递减趋势,这一结果与前期研究结论相一致[8]。
2.4Fe元素腐蚀分析
动态化学腐蚀实验和电解实验结果均表明,30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷在NaF-KF-AlF3低温电解体系下,存在陶瓷相中Fe元素优先腐蚀问题,且这是化学腐蚀和电化学腐蚀共同作用的结果。

在电解过程中阳极表面组分与电解质中的AlF3发生反应而溶解,阳极表面溶解的Fe2+会被新生态氧迅速氧化成Fe3+,Fe、Ni、Cu元素以Fe3+、Ni2+、Cu2+等离子形态进入电解质,并向阴极扩散,溶解的离子扩散到阴极附近被还原进入铝液。
3结论
(1)空气气氛下烧结后,NiFe2O4尖晶石相中Fe/Ni原子比为1.90,接近其化学计量比;在氮气气氛下烧结后,NiFe2O4陶瓷基体中Fe/Ni原子比增大为3.20,表明NiFe2O4相发生离解。
(2)动态化学腐蚀实验结果表明,NiFe2O4相中Fe元素溶出量高于Ni元素。
(3)30(40Cu-Ni)/(NiFe2O4-10NiO)金属陶瓷阳极电解24 h后,铝样中Fe、Ni、Cu含量分别为0.45%、0.13%和0.03%,且阳极表面膜层中Fe/Ni原子比明显下降,电解过程中Fe元素发生优先腐蚀。
参考文献
[1]Margolis N, Eisenhauer J. Inert anode roadmap: a framework for technology development[R]. Washington, D. C.: The Aluminum Association in Conjunction with the U.S. Department of Energy, 1998: 1-29.
[2]Hanneman R E, Hayden H W, Goodnow W, et al. Report of the American Society of Mechanical Engineers Technical Working Group on Inert Anode Technologies[R]. Washington, D. C.: The U.S. Department of Energy, 1999: 1-45.
[3]Pawlek R P. Inert anode: an update[C]//Proceedings of the Symposia Sponsored by the TMS Aluminum Committee at the 143rdAnnual Meeting and Exhibition. San Diego, California: The Minerals, Metals & Materials Society, 2014: 1309-1313.
[4]田忠良.铝电解NiFe2O4基金属陶瓷惰性阳极及其相关工程技术研究[D].长沙:中南大学,2006.
[5]秦庆伟.铝电解惰性阳极及腐蚀率预测研究[D].长沙:中南大学,2004.
[6]Chin P, Sides P J, Keller R. The transfer of nickel, iron, and copper from hall cell melts to molten aluminum[J]. Canadian Metallurgical Quarterly, 1996, 35(1): 61-68.
[7]DeYoung D H. Solubilities of oxides for inert anodes in cryolite-based melts[C]//Proceedings of the Technical Sessions Sponsored by the TMS Light Metal Committee at the 115thAnnual Meeting. New Orleans, Louisiana: The Metallurgical Society, 1986: 299-307.
[8]He H B, Wang Y, Long J J, et al. Corrosion of NiFe2O4-10NiO-based cermet inert anodes for aluminum electrolysis[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(12): 3816-3821.
[责任编辑董贞]
Corrosion behaviors of Fe element in NiFe2O4-10NiO-based cermet anodes for aluminum electrolysis in low temperature electrolyte
ZhengXin1,QinQingwei1,YangJianhong1,2,YangWenjie2,LiuYing2,GuoJie2
(1. Key Laboratory for Ferrous Metallurgy and Resources Utilization of Ministry of Education,Wuhan University of Science and Technology, Wuhan 430081, China; 2. Green Metallurgy Division,Zhengzhou Non-ferrous Metals Research Institute Co., Ltd. of CHALCO, Zhengzhou 450041, China)
Abstract:The NiFe2O4-10NiO ceramic substrate and 30(40Cu-Ni)/(NiFe2O4-10NiO) cermet anode for aluminum electrolysis in NiFe2O4 phase were prepared by using powder metallurgy technology. The corrosion behaviors of Fe element were studied under the condition of low temperature electrolyte. The results show that NiFe2O4 ceramic substrate can be dissociated under N2 atmosphere dur-ing the sintering process. As a result, the Fe element in NiFe2O4 phase is more easily dissolved in electrolyte in dynamic chemical corrosion and electrolysis tests. After 24 hours of electrolysis, the impurity contents of Fe,Ni and Cu in liquid aluminum are 0.45%,0.13% and 0.03%,respectively.
Key words:NiFe2O4-10NiO; inert anode; aluminum electrolysis; low temperature electrolysis; Fe element; corrosion
收稿日期:2015-11-13
基金项目:中国博士后科学基金资助项目(20100480885);湖北省新世纪高层次人才工程专项经费资助项目(鄂人社函[2011]763号);2014年湖北省重点产业创新团队项目(鄂组通[2014]36号);武汉科技大学钢铁冶金及资源利用教育部重点实验室开放基金资助项目(FMRU201206).
作者简介:郑鑫(1991-),男,武汉科技大学硕士生.E-mail: zhengxin199104@126.com通讯作者:秦庆伟(1974-),男,武汉科技大学副教授,博士.E-mail: qingweiqin@126.com
中图分类号:TF821
文献标志码:A
文章编号:1674-3644(2016)02-0092-06

