甲苯甲醇烷基化制对二甲苯动力学模型
谭远婷,祝 然,张新平,唐 勇,曾作祥
1.上海华谊集团技术研究院,上海 200241;2.华东理工大学化工学院,上海 200237;3.上海计算化学与化工工程技术研究中心,上海 200241
甲苯甲醇烷基化制对二甲苯动力学模型
谭远婷1,2,祝 然1,3,张新平1,3,唐 勇1,3,曾作祥2
1.上海华谊集团技术研究院,上海 200241;
2.华东理工大学化工学院,上海 200237;
3.上海计算化学与化工工程技术研究中心,上海 200241
摘要:采用固定床反应器,在消除内外扩散影响的基础上,在反应温度480~560 ℃、甲苯甲醇总质量进料空速2 h-1、甲苯甲醇物质的量之比为1~6、水与甲苯物质的量之比为2~6和氢气与甲苯物质的量之比为2~8的条件下,研究了在自制沸石分子筛催化剂上甲苯甲醇烷基化反应的本征动力学,建立了包括甲苯甲醇烷基化制对二甲苯、二甲苯间异构化、二甲苯深度烷基化生成三甲苯和甲醇生成烯烃等7个反应的完整反应网络。采用非线性优化方法进行参数估算,并对模型的适用性进行了误差分析和统计检验。结果表明,甲醇生成烯烃反应的加入使模型能较好地反映出甲苯甲醇物质的量比对反应结果的影响,甲苯甲醇烷基化制对二甲苯的表观活化能为76.66 kJ/mol,通过误差分析和统计检验表明,动力学模型是适用的。
关键词:甲苯 甲醇 对二甲苯 烷基化 动力学
对二甲苯(PX)是工业生产中基本的有机化工原料之一,是合成聚酯的主要原料[1]。目前,由于PX的需求量日益增加,已经工业化生产PX的工艺,如甲苯歧化法和烷基转移等[2,3]生产的产品已经远远不能满足工业需求。而甲苯甲醇烷基化反应是增产PX的重要新工艺,具有良好的市场前景。与已工业化的甲苯歧化工艺相比,甲苯甲醇烷基化工艺具有显著的优势[4-6],如:PX收率较歧化工艺高一倍,甲苯的利用率高;副反应联产烯烃,附加值高;PX选择性高[7],可减少后续PX分离的成本;甲醇作为烷基化的原料,成本低。因此,甲苯甲醇烷基化制对二甲苯这一新工艺的研究,对未来芳烃的发展有很重要的意义。Wei[8]于1982年开始研究甲苯甲醇烷基化的动力学模型,认为甲苯甲醇烷基化主反应与二甲苯异构反应均发生在催化剂孔道内,忽略了在催化剂外表面可能进行的反应。而Bhat 等[9]假设速率控制步骤为表面反应,采用Langmuir-Hinshelwood双原子吸附机理以双曲线形的方程来描述动力学方程,所建立的动力学模型的计算值与实验值吻合较好,但该模型忽略了甲醇生成烯烃这一重要的副反应,这可能会导致动力学模型的适用性不强。本工作采用上海华谊技术研究院自主开发的沸石分子筛催化剂[10,11],开展了甲苯甲醇烷基化制对二甲苯的动力学研究,以期为后续反应器模拟及甲醇多段进料工艺的模拟优化提供研究基础。
1 实验部分
1.1 实验流程
实验装置如图1所示。采用Ø10 mm×2 mm,管长600 mm,且内装有热电偶套管的管式反应器。取一定量(1~6 g)的催化剂,装在反应管的恒温区内,其他部分用石英砂装填。实验前,进行了气密性检测,用调制好的肥皂水在装置的各个接口和阀门处进行检漏,若无明显气泡产生,说明装置没有明显的漏气,再定期观察压力的变化,24 h后若压力基本没有改变,说明装置的气密性良好。经气密性检查后开始实验:先通入载气(N2)对装置进行吹扫,去除装置中的杂质以及残余空气;然后关闭N2,打开氢气(H2)并程序升温至一定温度;关闭H2,再通入水经气化炉至反应器,水蒸气处理催化剂2 h后,停止进水,开通H2吹扫;再程序升温至反应温度,甲苯(T)、甲醇(M)、水(H2O)和氢气(H2)按一定的物质的量比进样反应。产物采用低温冷却液循环泵冷凝,定时收集液相产物,并用气相色谱对有机相进行分析。
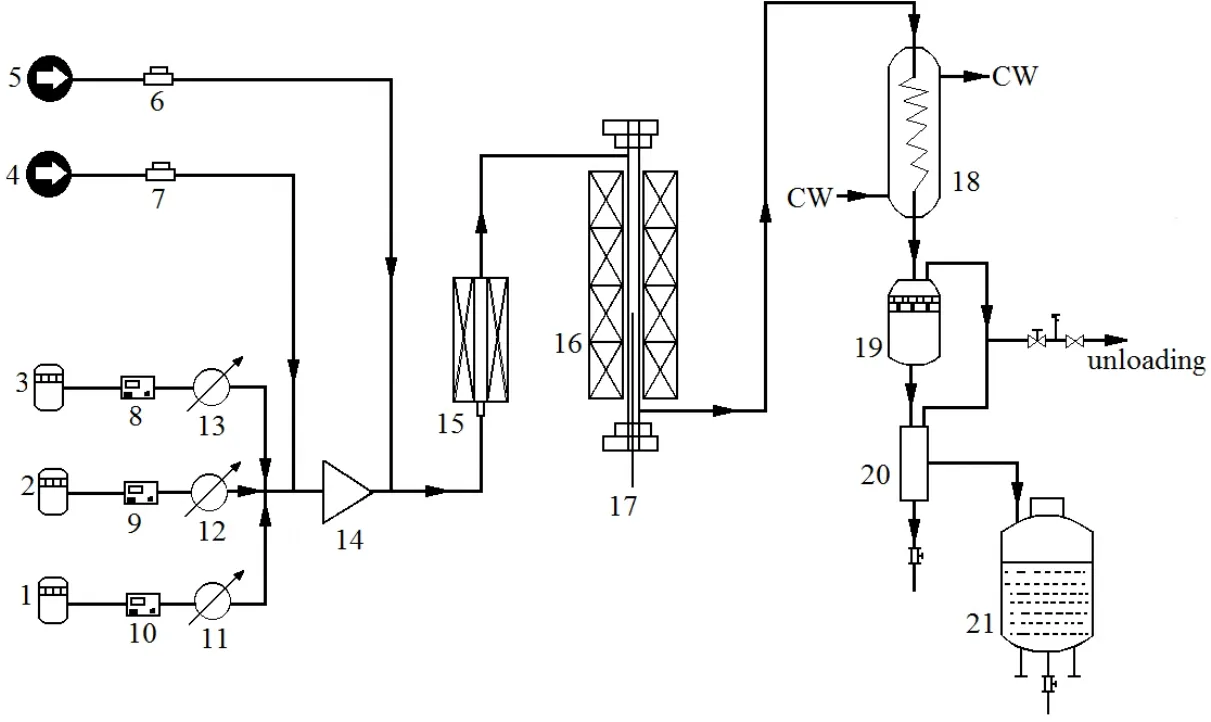
图1 甲苯甲醇择形烷基化实验装置Fig.1 Experimental device of toluene alkylation with methanol 1-methanol tank; 2-toluene tank; 3-water tank; 4-hydrogen; 5-nitrogen; 6,7-valve; 8,9,10-pump; 11,12,13-heater; 14-mixer;15-gasifier; 16-fixed-bed reactor; 17-thermocouple; 18-condenser; 19-gas-liquid separator; 20-liquid sampler; 21-product tank
1.2 实验条件
动力学实验的条件如下:反应压力为0.1~0.3 MPa;反应温度为480~560 ℃;催化剂质量3 g;甲苯甲醇进料的总质量空速为2 h-1;甲苯和甲醇物质的量之比为1~6;水和甲苯物质的量之比为2~6;氢气和甲苯物质的量之比为2~8。
1.3 计算方法的确立
甲苯的转化率(xT)可根据式(1)中甲苯的进出料的摩尔数进行计算,其中摩尔数可根据式(2)和(3)中甲苯进料的质量流率(min T)和液态产物的出料质量速率(mout)以及通过气相色谱面积归一法测定的产物中甲苯的质量分率(wout T)进行计算(其他产物摩尔数计算方法相同)。



对二甲苯的选择性(SPX)可根据液态产物的出料质量速率和产物中PX、邻二甲苯(OX)和间二甲苯(MX)的质量分率(wout i)进行计算,如式(4)和(5):


式中,i 为PX,OX和MX。
液态产物中各组分的收率(yi)可通过甲苯的进料质量流率和液态产物的出料质量速率以及产物中各组分的质量分率进行计算,如式(6)和(7):


式中,i为PX,MX,OX和TMB(三甲苯)。
2 实验结果与处理
2.1 内外扩散排除
实验用催化剂粉末粒径大小为0.55~0.83 mm (10~30目),催化剂装填量分别为1.5,2.5和3.0 g,在反应温度520 ℃,氢气、水、甲苯和甲醇的物质的量之比为12:4:2:1,甲苯甲醇总质量空速(WHSV)为0.5~4 h-1的条件下,考察外扩散对甲苯甲醇烷基化反应的影响,甲苯转化率及对二甲苯选择性如图2所示。由图可看出,随着WHSV的增加,甲苯的转化率均逐渐下降,对二甲苯的选择性均略有增加。当WHSV大于等于1 h-1时,反应器中3种催化剂装填量的甲苯转化率和对二甲苯选择性基本接近,表明此时甲苯转化率与床层线速率大小无关,可认为外扩散阻力的影响基本消除。
在排除外扩散的基础上,控制反应温度和进料的质量空速不变,通过改变催化剂颗粒的粒径来考察内扩散对烷基化反应的影响。当催化剂颗粒的粒径在一定范围内时,甲苯转化率基本不发生变化,则认为该反应过程的内扩散基本已经消除。在反应温度520 ℃,氢气、水、甲苯和甲醇的物质的量之比为12:4:2:1,WHSV为2 h-1,催化剂装填量3.0 g的条件下,考察不同催化剂粒径对烷基化反应的影响,结果如表1所示。当催化剂的粒径在0.55~1.65 mm变化时,甲苯转化率变化不大,表明内扩散已基本消除。本实验中,内扩散实际上并不能完全消除。内扩散主要包括催化剂颗粒内的微孔扩散和催化剂颗粒之间的大孔扩散两部分。而实验中排除的内扩散是催化剂颗粒间的大孔扩散,而微孔扩散是分子筛催化剂的特性,对本反应体系来说,微孔扩散体现的是甲苯甲醇烷基化反应的择形性,是由催化剂的孔道和反应物分子的大小来确定的,表现为反应物择形、约束过渡态择形和产物择形,因此在甲苯甲醇烷基化反应中对二甲苯有很高的选择性。
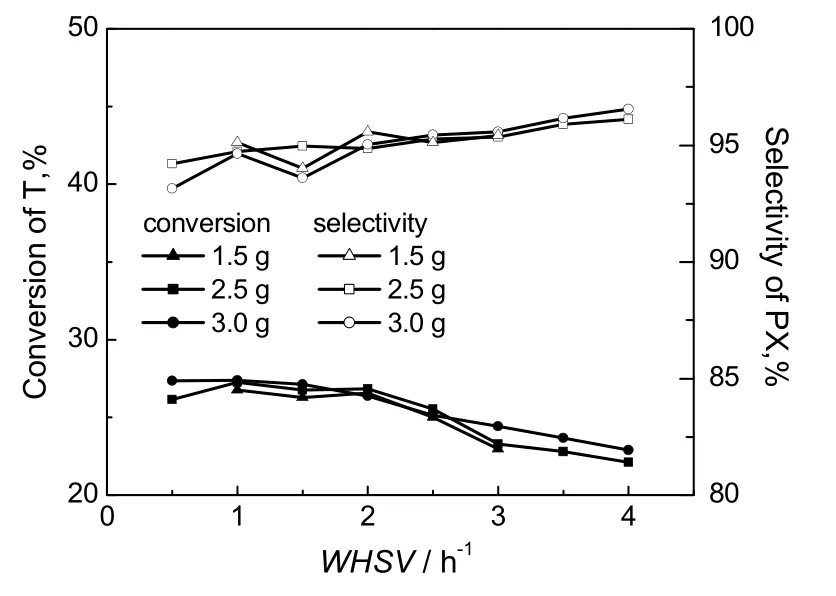
图2 外扩散的影响Fig.2 Influence of external diffusion

表1 内扩散的影响Table 1 Influence of internal diffusion
2.2 动力学数据采集
通过分析烷基化实验的产物分布,可计算不同温度、甲苯甲醇物质的量之比和原料空时下的xT以及PX,MX,OX和TMB的收率,分别为yPX,yMX,yOX和yTMB,结果如表2所示。

表2 甲苯甲醇烷基化反应产物分布Table 2 Product distribution of toluene alkylation with methanol
2.3 动力学模型及参数估值
2.3.1 反应网络的建立
经气相色谱分析,甲苯甲醇烷基化反应的液相产物主要包含甲苯、乙苯、对二甲苯、间二甲苯、邻二甲苯和三甲苯等。因为分子筛催化剂对产物中的对二甲苯具有一定择形性[12],所以产物以对二甲苯为主,结合Bhat等[9]的研究成果,作如下假设:
(1)甲苯甲醇烷基化反应首先生成对二甲苯;
(2)对二甲苯异构化生成邻二甲苯和间二甲苯;
(3)对、间和邻3种二甲苯深度烷基化生成三甲苯,且反应速率常数均相同;
(4)与芳烃反应后剩余的甲醇完全脱水生成烯烃,并以乙烯作为集总;
(5)反应体系中各反应的平衡常数极大,忽略逆反应。
所建反应网络如图3所示。反应网络包含甲苯甲醇烷基化制对二甲苯、二甲苯间异构化、二甲苯深度烷基化生成三甲苯和甲醇生成烯烃等7个反应。2.3.2 动力学模型的建立
本工作的动力学模型是在H2,H2O,T和M物质的量之比为6n:2n:n:1(其中n为甲苯甲醇物质的量之比)的条件下建立的。从图3的反应网络可知,除甲醇生成乙烯外,其他反应均为等摩尔反应,因此整个烷基化反应体系是一个总摩尔数增加的体系。Sotelo等[12]的研究表明,反应网络中主反应对甲醇甲苯均为1级时,有较好的拟合效果。本工作对烷基化反应网络中主反应的反应级数进行了一定筛选,发现当主反应对甲苯甲醇的级数均为1级,副反应甲醇生成烯烃对甲醇的级数为2级,其余副反应对各反应物均为1级反应时,拟合效果较好。各反应速率方程如式(8)~(13):
甲苯消耗速率

图3 甲苯甲醇烷基化反应网络Fig.3 Reaction network of toluene alkylation with methanol
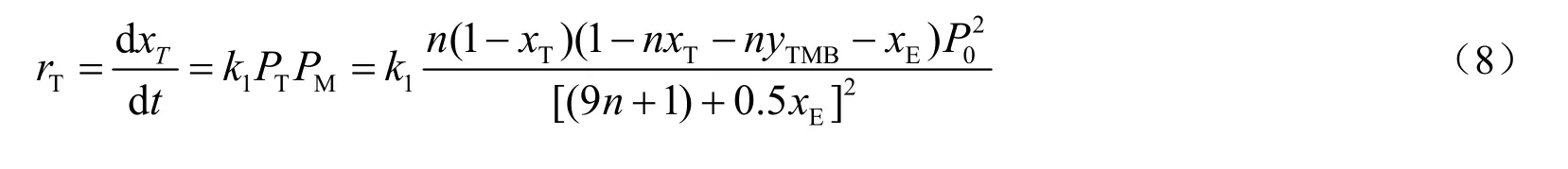
对二甲苯生成速率

间二甲苯生成速率

邻二甲苯生成速率

三甲苯生成速率

烯烃(乙烯)生成速率

其中:t = W/FT 0。
2.3.3 动力学参数拟合
以上常微分方程组中含有k1~k55个未知参数,从烷基化实验的产物分布得到如表2所示的不同温度、不同甲苯甲醇配比和不同的原料空时下的甲苯转化率,对二甲苯、邻二甲苯、间二甲苯和三甲苯的收率。采用非线性回归的方法将各温度下的速率常数分别估算出来。采用非线性最小二乘法进行参数的估值优化,参数估值采用的目标函数表达式为:

采用Runge-Kutta法进行数值积分,求得各温度下动力学参数的值,如表3所示。

表3 不同温度下动力学常数拟合值Table 3 Fitted kinetic constants at different temperatures
从表3中可看出,在甲苯甲醇烷基化这个反应体系中,随着反应温度的升高,各反应动力学常数随之增加,即主副反应的动力学常数都随温度升高而增大,还可以看出,在不同温度下拟合的动力学常数的误差小于5%。该规律与阿伦尼乌斯方程相符合,再通过两端取对数,经线性回归可得到各反应的指前因子(k0)和活化能(Ea),如表4所示。

表4 线性回归的指前因子和活化能Table 4 Linear regression of pre-exponential factors and activation energies
从表4可以看出,甲苯烷基化生成对二甲苯的活化能最大为76.66 kJ/mol,比对二甲苯异构化生成间二甲苯(19.24 kJ/mol)和邻二甲苯(16.80 kJ/mol)的活化能大得多。这与Sotelo等[13]的研究结果一致。二甲苯生成三甲苯的活化能(57.47 kJ/mol)较高,可能是因为三甲苯的空间位阻较大,从而影响反应的进行,使得该反应的活化能较高;甲醇脱水生成烯烃的反应活化能(44.94 kJ/mol)也较高,这与胡浩[14]的甲醇制烯烃催化反应的研究规律基本相符。
2.4 模型实用性检验
2.4.1 误差分析
甲苯甲醇烷基化反应得到不同温度下甲苯转化率和对二甲苯收率的模型计算值与实验值的对比见图4,甲苯转化率和对二甲苯收率的计算值与实验值的相对误差分布图见图5。从图4可看出,模型计算值与实验值之间有较好的相关性。从图5可看出,模型计算值与实验值的相对误差基本在10%以内,表明本工作建立的反应网络和动力学模型与实验结果吻合较好。
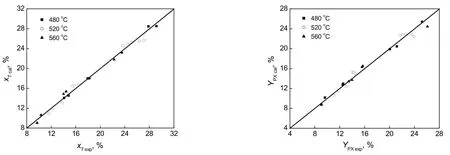
图4 模型计算值和实验值的比较Fig.4 Comparison of experimental data and calculated data

图5 模型计算值和实验值的相对误差分布Fig.5 Residual distributions of experimental data and calculated data
2.4.2 统计检验
为检验建立的动力学模型实用性,需对该动力学模型进行F统计和复相关指数ρ2的检验,结果如表5所示。

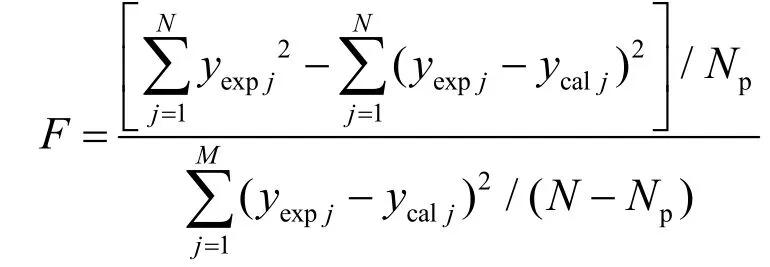

表5动力学模型的统计检验Table 5 Statistical test of kinetic model
根据决定性指标ρ2的式子,显然ρ2值越大越好,而F值,可判断是否存在对回归均值的偏差,显然,F值越大越好。为简便起见,一般认为当ρ2大于0.9,F大于10FT(NP,N-NP)时,且残差分析均匀地分布在对角线两侧,或均匀分布在零线的上下侧时,则可以认为所选模型及参数估值是可靠的。由表5可看出,动力学模型的ρ2为0.998 1,大于0.9;通过查表得FT(10,13)为2.67,F为701.13,大于10FT(10,13)。综上所述,本工作所选用的动力学模型是适用的。
3 结 论
a)采用固定床反应器,反应温度为480~560 ℃,催化剂质量1~6 g,甲苯甲醇进料的总质量空速为2 h-1的条件下测定了不同甲苯甲醇配比下的烷基化反应动力学数据,采用非线性最小二乘法进行参数估算,并选用幂函数型动力学模型,获得了7个反应的动力学方程,其中主反应的动力学方程如下:

b)误差分析和统计检验的结果与判断模型合理性标准的比较表明,所建立的动力学模型能够准确地描述甲苯甲醇烷基化反应的行为,所以该动力学模型是适用的。
符号说明

F —— 回归均方和与模型误差均方和之比 N —— 甲苯甲醇的物质的量之比FT —— 显著水平为5%下的F表值 N —— 实验次数FT 0 —— 进料甲苯的摩尔流率,mol/h Np —— 参数个数k1 —— 甲苯消耗反应速率常数,mol/(g·Pa2·h) Pi —— 组分i在整个体系中的分压,Pa k2 —— 间二甲苯生成反应速率常数,mol/(g·Pa·h) P0 —— 一个标准大气压,1.013×105Pa k3 —— 邻二甲苯生成反应速率常数,mol/(g·Pa·h) S —— 模型计算值与实验值之差的平方和k4 —— 三甲苯生成反应速率常数,mol/(g·Pa2·h) W —— 催化剂质量,g k5 —— 乙烯生成反应速率常数,mol/(g·Pa2·h) wout i —— 出料组分i的质量分率mout —— 液态产物的出料质量速率,g/h xE —— 甲醇转化为烯烃的转化率,% min T —— 甲苯的进料质量流率,g/h ycal —— 模型计算值Mi —— 组分i的摩尔质量,g/mol yexp —— 实验值nin T —— 进料甲苯的摩尔数,mol β —— 选择性,% nout i —— 出料组分i的摩尔数,mol ρ2 —— 决定性指标
参考文献:
[1] 多 米, 王 晔. 2004年世界对二甲苯市场综述[J]. 化工科技市场, 2005, 8: 37-40. Duo Mi, Wang Ye. Overview of world paraxylene market[J]. Chemical Technology Market, 2005, 8: 37-40.
[2] 徐兆瑜. 增产PX的工艺技术新进展与展望[J]. 精细化工原料及中间体, 2007, (1): 24-29.Xu Zhaoyu. Resent progress and foresight in p-xylene production increasing technology[J]. Fine Chemical Industrial Raw Materials & Intermediates, 2007, (1): 24-29.
[3] 丁春华. 甲苯/甲醇选择烷基化催化剂的研制和催化性能研究[D]. 大连理工大学, 2007.
[4] 邵 平. 甲苯甲醇合成对二甲苯的新技术及市场分析[J]. 炼油与化工, 2012, 23: 6-8. Shao Ping. New technology and market analysis of producing para-xylene by toluene and methanol[J]. Refining and Chemical Industry,2012, 23: 6-8.
[5] 曹德安. 甲苯甲醇制对二甲苯技术研究进展[J]. 化学反应工程与工艺, 2007, 23(4): 359-362. Cao Dean. Technology advances on selective methylation of toluene with methanol to para-xylene[J]. Chemical Reaction Engineering and Technology, 2007, 23(4): 359-362.
[6] 曹劲松, 徐 磊. 甲苯甲醇烷基化制PX技术的开发优势[J]. 石油化工技术与经济, 2010, 26(1): 8-10. Cao Jingsong, Xu Lei. Superiorities for developing PX production process through alkylation of toluene alcohol[J]. Techno-Economics in Petrochemicals, 2010, 26(1): 8-10.
[7] 王天宝. 甲苯甲醇烷基化反应动力学研究及反应器的模拟[D]. 大连理工大学, 2011.
[8] Wei J. A mathematical theory of enhanced para-xylene selectivity in molecular sieve catalysts[J]. Journal of Catalysis, 1982, 76(2): 433-439.
[9] Bhat Y S, Halgeri A B, Rao T S R P. Kinetics of toluene alkylation with methanol on HZSM-8 zeolite catalyst[J]. Industrial & Engineering Chemistry Research, 1989, 28(7): 890-894.
[10] 娄报华. 甲苯甲醇烷基化合成对二甲苯[M]. 华东理工大学, 2013.
[11] 唐建远, 娄报华, 宁春利. 改性的高硅铝比的HZSM-5催化剂上甲苯与甲醇的择形烷基化制对二甲苯[J]. 复旦学报(自然科学版),2013, 52(1): 23-29. Tang Jianyuan, Lou Baohua, Ning Chunli. Shape-selective alkylation of toluene and methanol to p-xylene over modified HZSM-5 catalyst with high Si/Al molar ratios[J]. Journal of Fudan University(Natural Science), 2013, 52(1): 23-29.
[12] Bhat Y S, Das J, Rao K V, et al. Inactivation of external surface of ZSM-5: zeolite morphology, crystal size, and catalytic activity[J]. Journal of Catalysis, 1996, 159(2): 368-374.
[13] Sotelo J L, Uguina M A, Valverde J L, et al. Kinetics of toluene alkylation with methanol over magnesium-modified ZSM-5[J]. Industrial & Engineering Chemistry Research, 1993, 32(11): 2548-2554.
[14] 胡 浩. 甲醇制烯烃(MTO)催化反应工程的研究[D]. 华东理工大学, 2010.
Kinetic Model of Toluene Alkylation with Methanol to para-Xylene
Tan Yuanting1,2, Zhu Ran1,3, Zhang Xinping1,3, Tang Yong1,3, Zeng Zuoxiang2
1. Technology Research Institute of Shanghai Huayi Group, Shanghai 200241, China;
2. Chemical Engineering Institute, East China University of Science and Technology, Shanghai 200237, China;
3. Computational Chemistry and Chemical Engineering Technology Research Center of Shanghai, Shanghai 200241, China
Abstract:The intrinsic kinetics of toluene alkylation with methanol over homemade zeolite catalyst was studied in a fixed bed reactor. Excluding internal and external diffusion, kinetic data was obtained under the conditions of 480-560 ℃, the total mass space velocity of toluene and methanol 2 h-1, the molar ratio of toluene to methanol 1-6, the molar ratio of water to toluene 2-6, the molar ratio of hydrogen to toluene 2-8. A complete reaction network was established including seven reactions of toluene alkylation with methanol to para-xylene, xylene isomerization, xylene depth alkylation with methanol to trimethylbenzene and methanol to olefins. The kinetic model parameters were estimated using the nonlinear optimization method, and the applicability of the model was verified by residual analysis and statistical test. The results showed that the addition of methanol to olefins reaction made the kinetic model have a better reflection of the effect of the molar ratio of toluene to methanol on reaction results. And the activation energy of toluene alkylation with methanol to para-xylene was 76.66 kJ/mol. The residual analysis and statistical tests showed that the proposed kinetic model was reliable and adequate.
Key words:toluene; methanol; para-xylene; alkylation; kinetic
作者简介:谭远婷(1990—),女,硕士;张新平(1974—),男,高级工程师,通讯联系人。E-mail: zhangxinping@shhuayi.com。
收稿日期:2015-07-28;
修订日期:2015-11-24。
文章编号:1001—7631 ( 2016 ) 02—0120—09
中图分类号:TQ013.2
文献标识码:A

