解脲支原体DNA检测室内质控物的制备及质控方案的设计
葛燕梅,张 娣,樊苏逸,袁 杭,毛 源
(南京金域医学检验所,江苏南京 210042)
·论著·
解脲支原体DNA检测室内质控物的制备及质控方案的设计
葛燕梅,张娣,樊苏逸,袁杭,毛源△
(南京金域医学检验所,江苏南京 210042)
摘要:目的制备解脲支原体(UU)DNA荧光定量PCR室内质控物,建立室内质量控制体系,对其临床应用进行初步评价。方法分别留取Ct值为24~25(阳性)和32~33(弱阳性)标本和检测结果为阴性的标本,待留取到15 mL时充分混匀,按每管150 μL分装作为室内质控物。前20次检测采用“即刻法”判断检测结果是否在质控范围内,20次以后绘制Levey-Jennings图,确定靶值、标准差(s)和变异系数(CV),采用Westdard多规则质控方法对自制室内质控物检测结果进行判断。在Unity Real Time(URT)系统中使用质控规则配置操作导出UU-DNA的功效函数图(OPSPecs图),根据OPSPecs图设置质控规则。结果131次实验中,前20次采用“即刻法”判断室内质控物;20次以后采用Levey-Jennings图判断,质控品稳定,质控规则合理。结论用临床分泌物混合液制备UU-DNA检测项目的室内质控物品,制备方法简单,测定结果稳定,可作为实验室检测UU-DNA项目的质控品;依据OPSPecs图设置分子生物学检测项目的室内质控规则简便、实用。
关键词:解脲支原体;室内质控;质控图;功效函数图;质控规则
与常规PCR技术相比,实时荧光定量PCR具有高度的敏感性与特异性,这项检测技术的出现使临床对抗病毒治疗疗效判断达到了核酸定量水平。尽管实时荧光定量PCR技术具有特异性强,能有效解决PCR产物污染和自动化程度高等特点,但严格的室内质量控制体系仍是临床PCR实验室不可忽视的问题[1-3]。由于目前尚无统一有效的室内质控品,因此临床PCR实验室需要建立符合本单位的室内质量控制体系。在总结多年PCR实验室工作经验的基础上,笔者结合PCR实验室工作的实际情况,自制了解脲支原体(UU)DNA室内质控物,绘制Levey-Jennings图,采用Westdard多规则质控方法评价UU-DNA的室内质控动态[4-6]。而且在Unity Real Time(URT)系统中利用功效函数图(OPSPecs图)工具软件进行质控规则的设计,选择使用更加符合的分子项目的质控规则。
1材料与方法
1.1质控品来源收集实验室标本中UU-DNA Ct值为24~25(阳性)和32~33(弱阳性)的阳性标本和检测结果为阴性的标本。
1.2仪器与试剂试剂使用上海科华生物公司UU-DNA检测试剂盒,仪器使用ABI公司的7300实时荧光定量仪。
1.3方法
1.3.1质控品的制备收集每天Ct值为24~25和32~33的阳性标本分别作为高值标本和低值标本,收集每天检测结果为阴性的标本作为阴性质控标本,待留到15 mL时充分混匀,然后将标本进行每管150 μL分装-20 ℃保存,每次实验前将冷冻保存的标本各自取一管室温复融20 min并充分混匀后与正常标本同样进行检测,记录Ct值。
1.3.2PCR扩增按照试剂盒上的操作说明对标本进行DNA模板提取,反应体系为28 μL的扩增反应液和2 μL提取的DNA模板上清液。扩增结束后,按照仪器操作获得质控结果和标准曲线,分别记录高值质控品和低值质控品的Ct值。
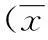
1.3.4质控规则采用的是Westdard多规则质控方法:如果阴性质控标本的检测结果为阳性,判断为失控,所有阳性标本均进行重新检测,并增加一定数量的阴性质控标本。如阴性质控标本检测结果为阴性,阳性质控检测结果为阳性,并且测得的高值质控品和低值质控品的要满足笔者利用OPSPecs图工具软件设计的质控规则。
2结果
2.1采用“即刻法”判断质控结果用PCR连续对自制的阳性和弱阳性质控标本检测20次,采用“即刻法”判断质控结果,结果在控,见表1、2(见《国际检验医学杂志》网站主页“论文附件”)。
2.2根据OPSPecs图得出建议质控规则连续检测100次后,在URT系统中使用质控规则配置操作导出UU-DNA的OPSPecs图,见图1、2,根据OPSPecs图可得出建议的质控规则。得出的质控规则与项目的总允许误差(TEa)、偏倚(%)和变异系数(CV)等有关。UU-DNA阳性质控的TEa为12.8,偏倚(%)为0,CV为4.26%。UU-DNA弱阳性质控的TEa为8.96,偏倚(%)为0,CV为2.96。建议规则均为:1-3s|2-2s|R-4s|4-1s|10-X。
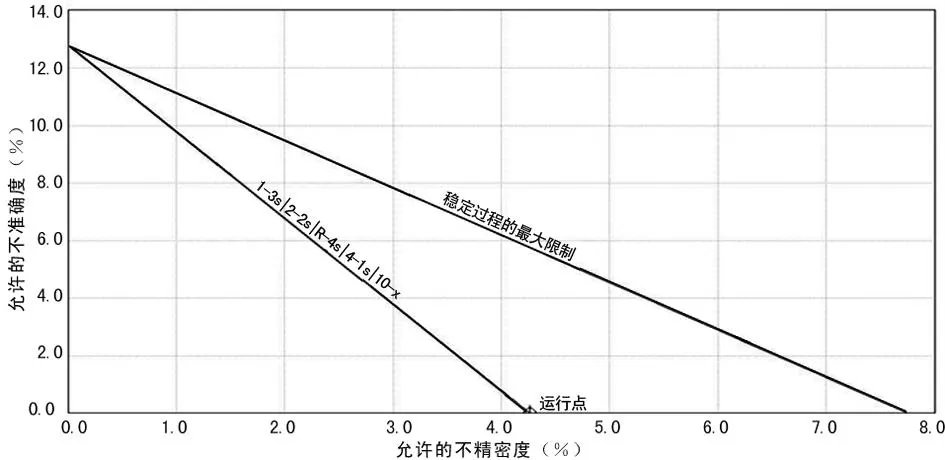
图1 UU-DNA阳性质控OPSPecs图
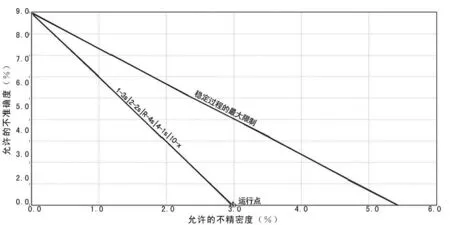
图2 UU-DNA弱阳性质控OPSPecs图
2.3质控品的Levey-Jennings图本批自制的阳性和弱阳性质控品,总共进行131次室内质控检测,根据质控规则,结果都在控。131次室内质控阳性和弱阳性质控品Levey-Jennings图,见图3、4(见《国际检验医学杂志》网站主页“论文附件”)。
2.4阴性质控品的检测自制的阴性质控品,总共进行131次室内质控检测,Ct值均显示为“未检出”,根据质控规则,阴性质控品结果都在控。
3讨论
近年来,临床实验室的管理越来越规范,尤其是临床基因扩增实验室的质量管理日益受到关注。而实验室要获得可靠的检测结果,必须要建立有效的质量管理体系,其中实验室室内质量控制是保证检验质量的一个重要环节[5]。在对临床标本进行检测的同时,需要进行室内质量控制来确保检测结果的准确性。
用于临床基因扩增实验室室内质控的理想质控品应具备以下几个条件:(1)基质与待测标本一致;(2)所含待测物浓度应接近试验的决定性水平;(3)有很好的稳定性;(4)靶值或预期结果已定;(5)无已知的生物传染危险性;(6)单批可大量获得[7]。由于现在商品化的质控品尚不齐全,各实验室须根据自己实验室的实际情况自行制备质控品。
UU支原体感染是近年来国内外最常见的性传播疾病之一[8],临床多用荧光定量PCR方法检测UU-DNA。本实验室在检测过程中发现UU-DNA阳性检出率较高,阳性标本易于收集,而且UU-DNA送检标本多为用无菌拭子取的临床分泌物混合液,易于采集。基于此种情况,建议将日常收集的UU-DNA阳性标本(Ct值为24~25)作为室内质控阳性标本,UU-DNA阴性标本作为室内质控阴性标本,而且考虑到检测的临界值,笔者也收集了UU-DNA弱阳性标本(Ct值为32~33)作为室内质控弱阳性标本。
笔者将收集的UU-DNA不同结果的标本分别充分混匀后,按每管150 μL用离心管分装好,-20 ℃保存。连续检测20次,用“即刻法”判断结果是否在控,第21次开始采用“Levey-Jennings图质控法”,用前20次检测结果计算得出的 和s绘制Levey-Jennings图,判断结果是否在控,采用的是Westdard多规则质控方法进行评价。 在设计质控方法时,首先要确定质量目标。质量目标可以用TEa的形式表示,目前中国尚未确立各项目的TEa[9]。本实验室设置的TEa来源为3 s。在检测次数达到100次以后,笔者使用URT系统中,质控规则配置操作导出UU-DNA的OPSPecs图,根据OPSPecs图评价误差检出概率和假失控概率,确定新的质控方法。本研究中根据OPSPecs图得出建议的质控规则1-3s|2-2s|R-4s|4-1s|10-X;n=2,然后将此规则应用到UU-DNA质控品的结果判断,切合实际且能达到临床工作发现误差的要求,同时假失控率也控制在合适的水平。
本研究对收集到的阳性、弱阳性和阴性3个不同浓度的标本共进行了131次检测,每周进行3次检测,连续进行了10个月的时间,检测结果仍然比较稳定,因此可以考虑将自制的UU-DNA标本混合液作为PCR实验室UU-DNA检测的室内质控物。
参考文献
[1]Jardi R,Rodriguez F,Buti M,et al.Quantitative detection of hepatitis B virus DNA in serum by a new rapid real-time fluorescence PCR assay[J].J Viral Hepat,2001,8(6):465-471.
[2]Heermann KH,Gerlich WH,Chudy M,et al.Quantiative detection of hepatitis B virus DNA in two international reference plasma preparations[J].J Clin Microbiol,1999,37(1):68-73.
[3]申子瑜,李金明.临床基因扩增检测技术[M].北京:人民卫生出版社,2002:147-148.
[4]冯仁丰.临床检验质量管理技术基础[M].上海:上海科学技术文献出版社,2003:245-258.
[5]秦晓光.室内质控的主要工具——质量控制图[J].中华检验医学杂志,2003,26(11):710-713.
[6]张正.分子生物学中PCR临床检测的室内质控(IQC)[C]//中华医学会,全国检验医学感染控制和病原检测学术研讨会论文集.北京:中华医学会,2004:6.
[7]李金明.实时荧光PCR技术[M].北京:人民军医出版社,2014:148.
[8]梁汉锦.比较两种检测支原体(UU)的方法[J].中国医药指南,2012,10(20):420-421.
[9]中华人民共和国国家质量监督检验检疫总局.临床实验室定量测定室内质量控制指南(GB/T 20468-2006)[M].北京:中国标准出版社,2006:3-7.

Preparation of internal quality control substance of real-time PCR to analyze UU-DNA and the design quality control programs
GeYanmei,ZhangDi,FanSuyi,YuanHang,MaoYuan△
(MedicalLaboratoryofNanjingKingmed,Nanjing,Jiangsu210042,China)
Abstract:ObjectiveDeveloping an internal quality control substance of Ureaplasma urealyticum(UU)-DNA for real-time PCR to establish an internal quality control system and preliminary evaluation its clinical value.MethodsInternal quality control substance was prepared by mixing samples which Ct value were 24-25(positive sample) and 32-33(weak positive sample),respectively.At the same time,selecting samples that test results were negative as negative control.The target value,standard deviation(s) and coefficient of variation(CV) of internal quality control substance were defined by “instant method” for the first 20 runs and Levey-Jennings quality control(QC) chart after the first 20 runs.Using the “Westdard” multi-rule quality control methods to analyze the detection results.Exporting OPSPecs chart by quality control rules in Unity Real Time (URT) system and setting up new quality control rules according with OPSPecs chart.Results131 times of the detection of quality control substance were performed totally.The first 20 runs were defined by “instant method” and later 111 runs were defined by Levey-Jennings QC chart,the results were stable of quality control substance and reasonable quality control rules.ConclusionPreparing of internal quality control substance of UU-DNA used in real-time PCR might be easy and stable.So,the internal quality control substance of UU-DNA could be worthy for practical application in this PCR laboratory.Design internal quality control rules based OPSPecs chart in molecular detection is very simple and practical.
Key words:Ureaplasma urealyticum;internal quality control;quality-control chart;OPSPecs chart;quality-control rules
(收稿日期:2015-12-08)
DOI:10.3969/j.issn.1673-4130.2016.08.022
文献标识码:A
文章编号:1673-4130(2016)08-1070-03
作者简介:葛燕梅,女,硕士,主要从事分子诊断学的研究。△通讯作者,E-mail:LABMY@kingmed.com.cn。

