吲哚衍生物的3D-QSAR研究和分子设计
仝建波, 占 培, 李凌霄, 吴英纪, 李康南
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
吲哚衍生物的3D-QSAR研究和分子设计
仝建波, 占 培, 李凌霄, 吴英纪, 李康南
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
采用Topomer CoMFA方法对52个吲哚衍生物进行了三维定量构效关系研究,建立3D-QSAR模型,所得优化模型的非交叉验证相关系数、交叉验证相关系数以及外部验证的复相关系数分别为0.996、0.651和0.764,结果表明该模型具有良好的稳定性和预测能力.Topomer CoMFA模型等势面图提供的立体场和静电场可视化图像,直观地揭示了这一系列化合物中不同的取代基结构对其生物活性的影响,运用这些信息进行分子设计,在理论上获得了一些具有较高活性新的吲哚衍生物抗艾滋病药物,该QSAR的研究结果可为实验工作者合成新药提供理论参考.
三维定量构效关系; 易位体比较分子场; 分子设计; 吲哚衍生物
0 引言
获得性免疫缺陷综合症(Acquired Immune Deficiency Syndrome,AIDS),即艾滋病病毒,是造成人类免疫缺陷病毒(Human Immunodeficiency Virus HIV)的一种致命疾病,HIV(分为HIV-1和HIV-2型)属逆转录病毒的一种,通过破坏人体的T淋巴细胞(CD4)、感染单核细胞和巨噬细胞,然后经过吸附、融合过程进入宿主细胞, 进而阻断细胞免疫和体液免疫过程,可导致机体免疫功能部分或全部丧失,继而发生机会性感染肿瘤等[1].
HIV的药物目前有逆转录酶抑制剂、蛋白酶抑制剂、整合酶抑制剂和进入抑制剂4种[2].前3种不仅仅容易诱导HIV耐药性突变,而且对人体有较大的毒副作用,导致艾滋病患者无法持续性的接受抗HIV的药物治疗[3].HIV进入抑制剂对前三种药物缺陷有进一步改善,目前有两种药物Enfuvitide和Maraviroc已经上市,此外,Veazey等人发现HIV进入抑制剂还可以作为杀微生物剂(Microbicides),为艾滋病的预防提供一项疫苗以外的选择[4].吲哚衍生物作为一种进入抑制剂,是一种典型的抗艾滋病药物.进入抑制剂是作用在HIV感染的早期阶段,能够阻止HIV与靶细胞的融合,被认为在艾滋病的防治上具有更好的应用前景[5].因此,开发新的阻止病毒进入的抗HIV药物已经成为目前抗艾滋病药物研究的热点.
定量构效关系(Quantitative Structure Activity Relationship,QSAR)是基于配体的计算机辅助药物设计的主要方法之一,具有代表性的方法有CoMFA[6]与CoMSIA[7].本实验采用的是第二代CoMFA 方法——Topomer CoMFA[8,9]对52种吲哚衍生物进行了3D-QSAR研究.通过分析系列化合物Topomer CoMFA模型静电场和立体场的分布特征,可获得受体生物活性的结构调控因素,从而进行分子设计, 提出一些可能具有较高抗艾滋病活性的新的吲哚衍生物, 为实验工作者合成该系列新药物提供理论参考.
1 研究方法与步骤
1.1 易位体比较分子场
Topomer CoMFA是CoMFA与Topomer的联合技术,能够在短时间内准确、快速构建3D-QSAR模型.采用Topomer技术将整个配体分子切割成两个或两个以上的小片段,所切割形成的小片段会自动生成三维构象的碎片,碎片根据一定的经验规则进行调整,生成Topomer模型[10].计算每个分子片段周围的立体场和静电场参数,作为自变量,以EC50的负对数(pEC50)[11]为建模响应值,用偏最小二乘回归分析方法[12]寻找这些三维结构的特征信息与化合物活性的联系,实现模型拟合.
1.2 数据来源和分子结构构建
本文所选择具有确定活性的52个吲哚衍生物样本来源于文献[13](如表1所示)作为研究对象,其化学结构如图1和表1所示,活性标度为pEC50(-logEC50).
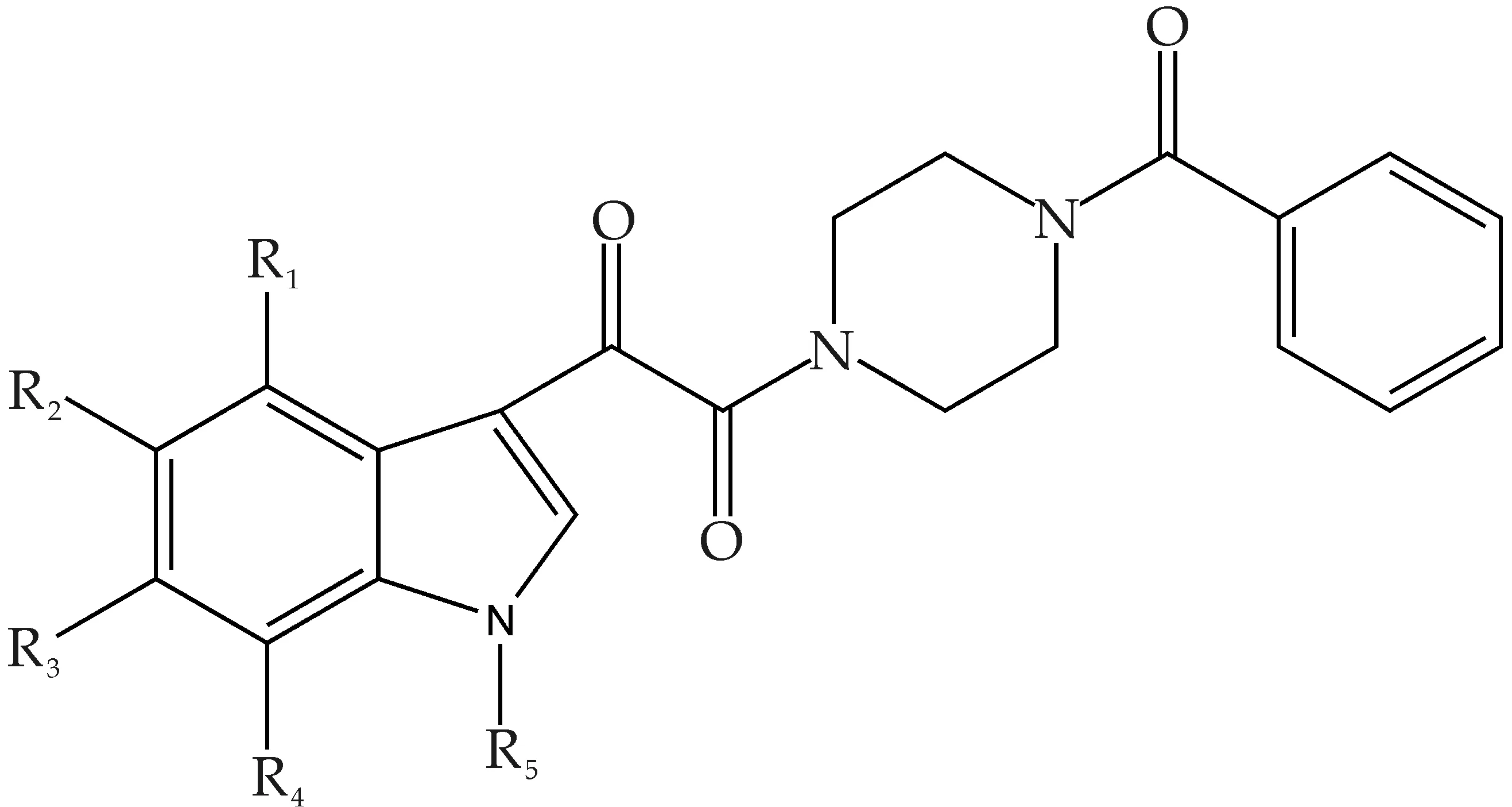
图1 52个吲哚衍生物的分子结构示意图
从文献中随机选取41个化合物作为训练集(training set)用来建立模型, 其余11个分子作为测试集(test set)用来验证模型的外部预测能力.利用SYBYL 2.0-X软件包中的Sketch Molecule模块绘制出化合物的结构,52个吲哚衍生物采用最陡梯度下降法对所有的化合物进行能量优化,得到其最低能量构象.优化过程中采用Tripos力场[14]、powell 能量梯度和加载Gasteiger-Huckel电荷,迭代系数设置为2 000 次,能量收敛限定设为0.5 kcal/mol,并将RMS(均方根)设为0.005,其余参数采用SYBYL2.0-X的默认值.
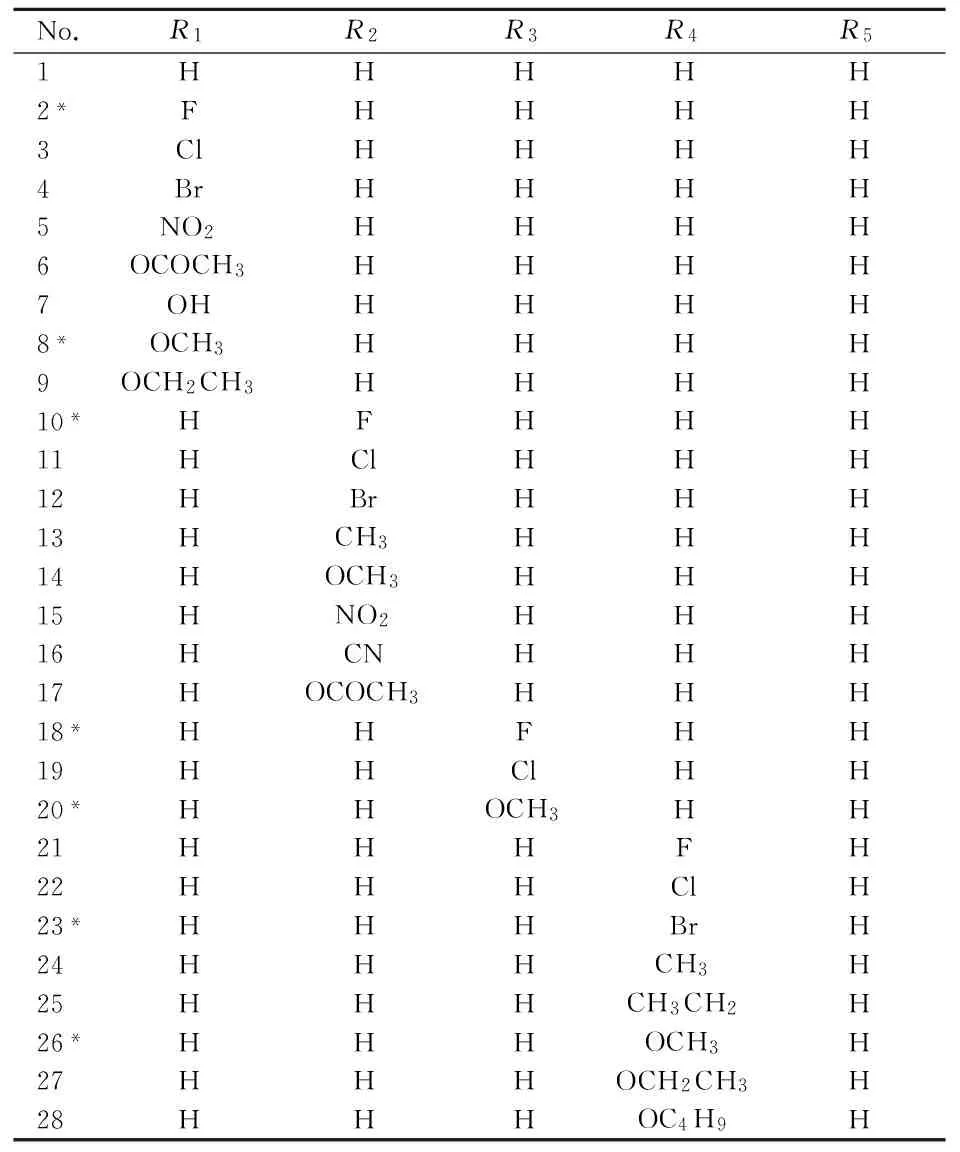
表1 化合物的结构
续表1

29HHHCNH30FBrFHH31HClClHH32HOCH3OCH3HH33HFHBrH34FHHFH35OCH3HHOCH3H36OCH3HHClH37*OCH3HHBrH38OCF3HHBrH39FHHBrH40*FHHCH3H41FHHOCH3H42FHHOCH2CF3H43FHHCNH44BrHHFH45FHFHH46FFFFH47HHHHCH348*HHHHCH2CH349HHHH(CH2)3CH350*HHHHCH2-CH=CH251HHHHCH2Ph52OCH3HHCNH
*为测试集
2 结果与讨论
2.1 Topmer CoMFA模型的统计结果及预测能力
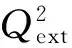

图2 吲哚衍生物实验值与预测值 的线性回归图表2 化合物实验活性值及预测活性值
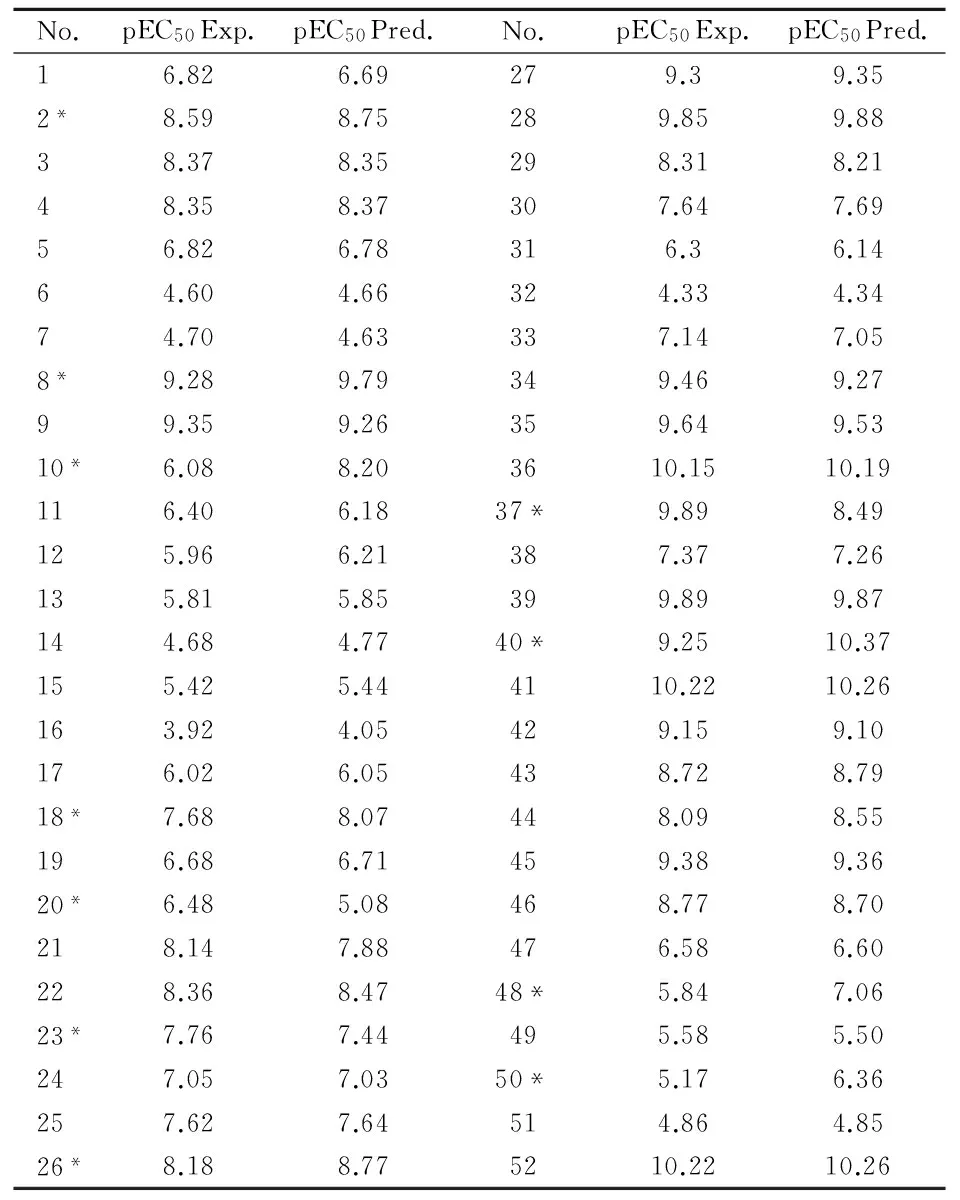
No.pEC50Exp.pEC50Pred.No.pEC50Exp.pEC50Pred.16.826.69279.39.352*8.598.75289.859.8838.378.35298.318.2148.358.37307.647.6956.826.78316.36.1464.604.66324.334.3474.704.63337.147.058*9.289.79349.469.2799.359.26359.649.5310*6.088.203610.1510.19116.406.1837*9.898.49125.966.21387.377.26135.815.85399.899.87144.684.7740*9.2510.37155.425.444110.2210.26163.924.05429.159.10176.026.05438.728.7918*7.688.07448.098.55196.686.71459.389.3620*6.485.08468.778.70218.147.88476.586.60228.368.4748*5.847.0623*7.767.44495.585.50247.057.0350*5.176.36257.627.64514.864.8526*8.188.775210.2210.26
*为测试集
2.2 3D-QSAR分析
图3显示了以52号分子为模板的立体场和静电场的三维等势图,其中52号分子是生物活性最高化合物.图3(a)、(c)分别为Ra,Rb的立体场三维等势图,图3(b)、(d)分别为Ra,Rb的静电场三维等势图,图3(a)、(c)中绿色区域表示引入大体积的基团有利于分子抑制活性,而黄色的区域代表引进小体积的基团有利于化合物抑制活性增加;图3(b)、(d)中蓝色区域表示引入带正电荷的基团有利于分子抑制活性,而红色的区域代表引进带负电荷的基团有利于化合物抑制活性增加.
由图3(a)立体场等势图可以看到在R4取代基上有小片绿色区域.图3(c)立体场等势图可以看出在临近切割处环绕着一块绿色等势域,这表明在这2个区域中,将大分子基团引于此可以增加分子的活性.例如化合物28(R4=OC4H9,pEC50=9.85)> 27(R4=OC2H5,pEC50=9.30)>26(R4=OCH3,pEC50=8.18)>25(R4=C2H5,pEC50=7.62)>24(R4=CH3,pEC50=7.05)>1(R4=H,pEC50=6.82),24~28号分子生物活性依次增大并且都大于1号化合物,是因为R4取代基的体积依次增大并且都大于1号R4取代基-H.由图3(a)立体场等势图可以看到在R1、R2、R3、R5等取代基上都有大片的黄色区域.
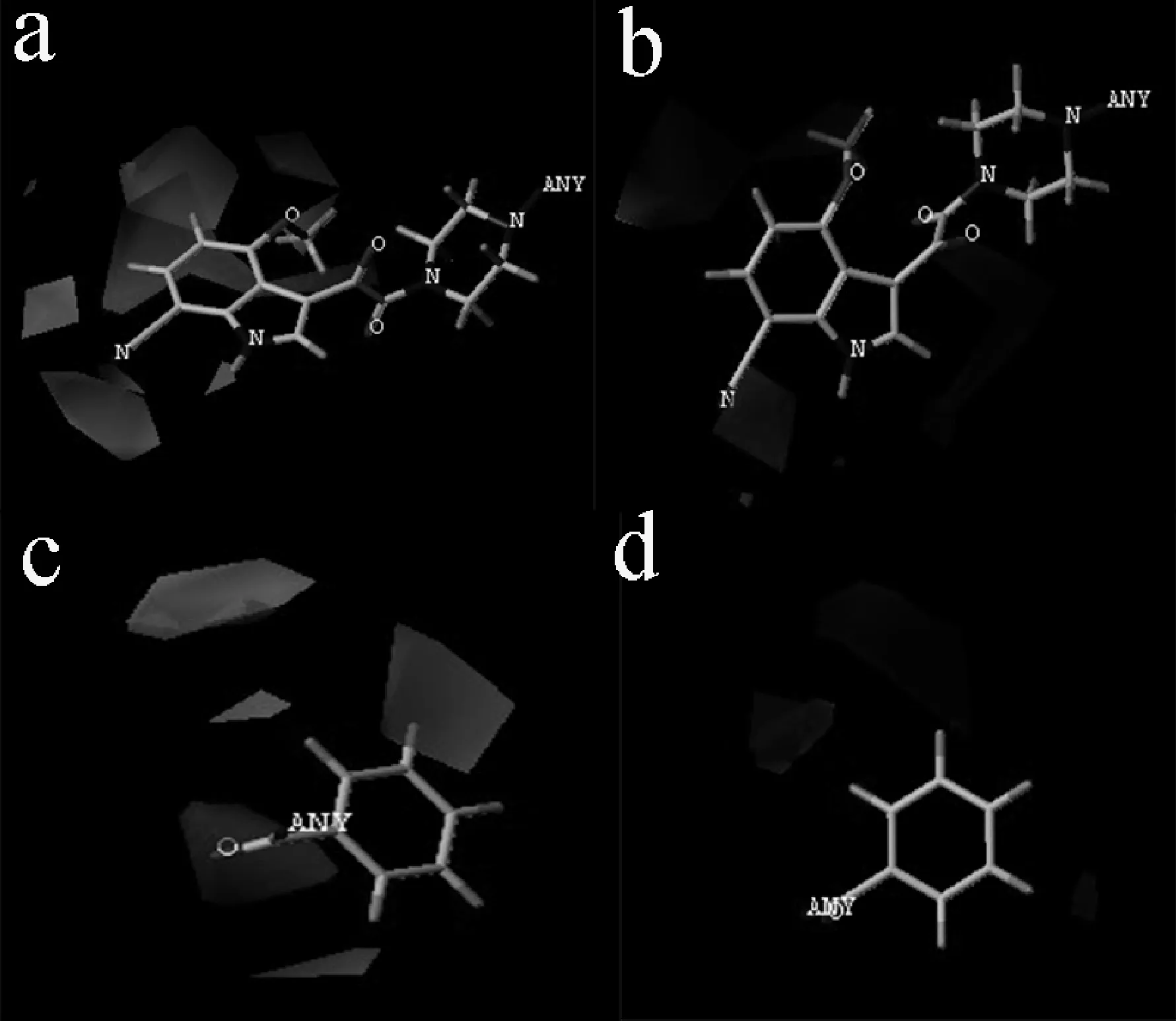
(a)Ra 立体等势图 (b)Ra静电等势图 (c)Rb立体等势图 (d)Rb静电等势图图3 分子的立体场与静电场等势图
图3(c)立体场等势图可以看出在苯基上有大片黄色区域,这表明在这些区域中,将小分子基团引于此可以增加分子的活性.在以下化合物中,9号分子由较大的基团-OCH2CH3取代了8号分子R1基团上较小的取代基-OCH3,其活性明显降低.1(R3=H,pEC50=6.69)>20(R3=OCH3,pEC50=6.48),20号分子由较大的基团-OCH3取代了1号分子R3基团上较小的取代基-H,其活性降低.1(R2=H,pEC50=6.69)> 13(R2=CH3,pEC50=5.85)>14(R2=OCH3,pEC50=4.77),在R2取代基上1、13、14号分子体积依次增大,所以活性依次降低.1、47、48、49、50、51号分子的R5基团体积依次增大,其活性值依次减小.
图3(b)静电场等势图可知,R2取代基、R5、吲哚环平面上聚有蓝色等势域,由图3(d)可以看到,在苯基上环绕着一块蓝色等势域表明在此区域若引入带正电的取代基可促使化合物活性增加, 例如13(R2=CH3,pEC50=5.85)>16(R2=CN,pEC50=4.05),13号分子的R2基团以-CH3取代了16号分子的取代基-CN,其活性相对的提高.由图3(b)静电场等势图可知,在R4取代基上可以看到有红色区域,表明在此区域引入带负电的取代基可促使化合物活性增加, 比如21(R4=F,pEC50=7.88)>23(R4=Br,pEC50=7.44)>24(R4=CH3,pEC50=7.05),再观察26号、25号,29号、1号,52号、8号都可以看出在R4上有带负电的取代基使得化合物的活性提高.
从以上分析可得出,若要使化合物活性增加,可在绿色区域引入大基团或在黄色区域引进小分子基团,在红色区域引入负电荷基团或在蓝色区域引入正电荷基团.
3 基于研究结果的分子设计
研究结果表明,取代基R4被大体积基团取代,R1、R2、R3、R5被小体积基团取代,在R2、R5上引入正电荷取代基,在R4上引入负电荷取代基都有利于提高化合物的活性,以活性最高的化合物52为母体进行了结构修饰,将改变化合物52中R5部位上取代基,以期能够提高化合物的生物活性.根据极性叠加原理[15-17],设计了三个使R5取代基第一个原子具有大的净正电荷的基团及相应的化合物.设计基团其原子间的极性示意图如图4所示,设计相应的具有较好活性化合物的分子结构及预测活性值如表3所示.
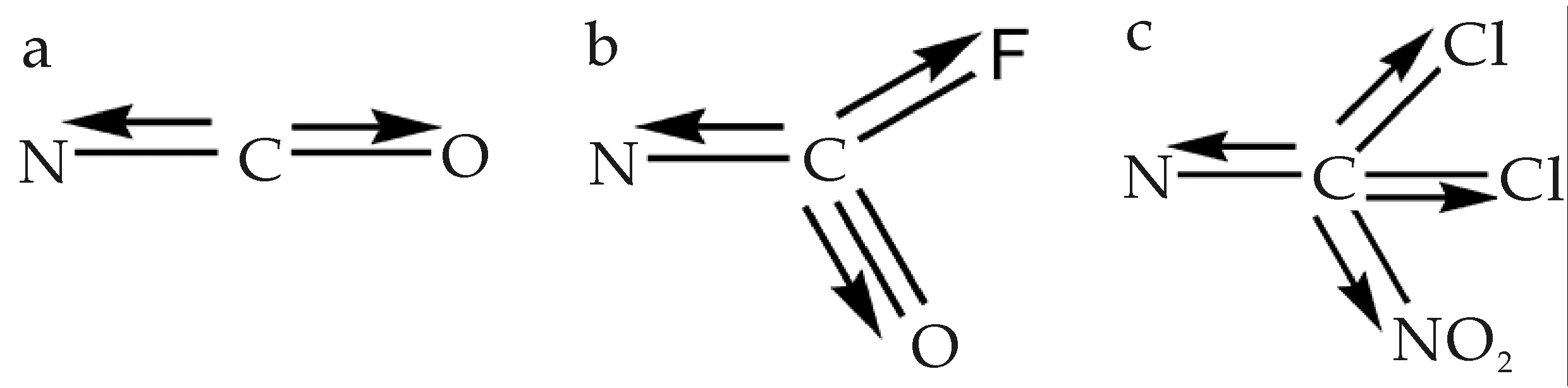
(a)R5基团为-CH2OH (b)R5基团为基团-COF (c)R5基团为-CCl2NO2图4 设计三个R5基团的极性叠加示意图表3设计相应分子的结构及预测活性值
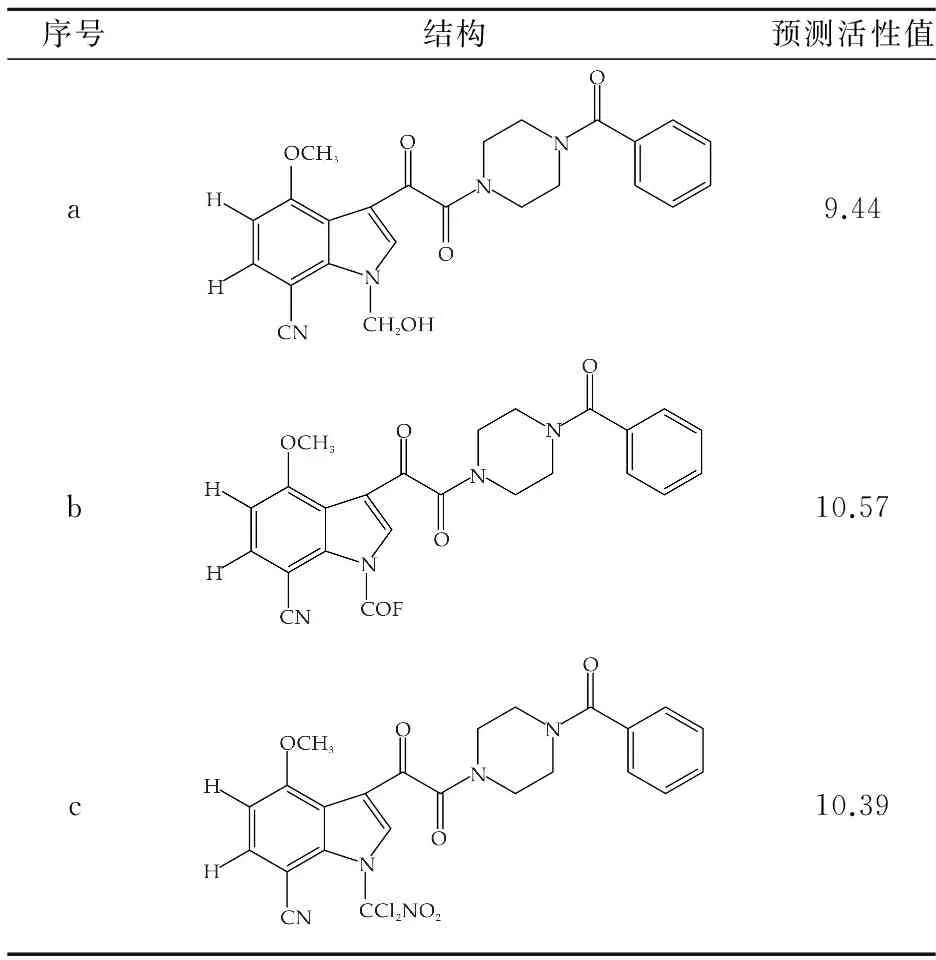
序号结构预测活性值a9.44b10.57c10.39
由图4可知,和基团相连接的C原子的箭头都是离开C原子的,由此可见C的静正电荷必定很大,这与计算得到的结果相符.表3列出了由本模型计算得到的相应化合物的活性, pEC50值在9.44~10.57之间,由此可见所设计的化合物具有高活性.
4 结论
本文利用Topomer CoMFA方法对52个吲哚衍生物进行了研究,建立了3D-QSAR模型,模型等势面图提供了立体场和静电场的可视化图像,直观地揭示了这一系列化合物中不同的取代基结构对其生物活性的影响,应用这些信息进行分子设计,在理论上提出了一些具有较高活性的吲哚衍生物,为实验工作者合成新药提供理论参考.
[1] Fauci A S.Human T cell line chronically infected with HIV[J].J.Science,1998,39(4 840):617-622.
[2] 仝建波,王 平,李云飞,等.咪唑衍生物类抗艾滋病药物3D-QSAR研究[J].原子与分子物理学报,2011,28(1):41-46.
[3] 刘叔文,吴曙光,姜世勃.新型抗艾滋病药物-HIV进入抑制剂的研究进展[J].中国药力学通报,2005,21(9):1 034-1 040.
[4] Veazey R S,Klasse P J,Schader S M. Protection of macaques from vaginal SHIV challenge by vaginally delivered inhibitors of virus cell fusion[J].Nature,2005,438(7 064):99-102.
[5] Kaushik Bausu N,Basu A,Harris D.Peptide inhibition of HIV-1:Current status and future potential[J].Clinical Trials of Drugs and Biopharmaceuticals,2008,22(3):161-175.
[6] Cramer R D,Punce J D,Patterson D E,et al.Comparative molecular field analysis (CoMFA).1.effect of shape on binding of steroids to carrier proteins[J].Journal of the American Chemical Society,1988,110(18):5 959-5 967.
[7] Klebe G.Comparative molecular similarity indices analysis:CoMSIA[J].Perspectives in Drug Discovery and Design,1998,3(12):87-104.
[8] Cramer R D,Patterson D E,Bunce J D.Topomer COMFA:A design methodology for rapid lead optimization[J].Medicinal Chemistry,200,46(3):374-388.
[9] Richard D C ,Phillip C,Gunther S.Virtual screening for R-groups, including predicted pIC50contributions,within large structural databases,using topomer CoMFA[J].Journal of Chemical Information and Modeling,2008,48 (11):2 180-2 195.
[10] 李月婷,刘永澜,史博智,等.分子对接技术用于马来酰亚胺类GSK-3α抑制剂的作用特征分析[J].分子科学学报,2013,29(4):265-275.
[11] 张青青,姚其正,张生平,等.靛玉红类CDK1抑制剂的同源模建、分子对接及3D-QSAR研究[J].物理化学学报,2014,30(2):371-381.
[12] Wold S,Sjostrom M,Eriksson L.PLS-regression: A basic tool of chemometrics[J].Chemometr Intell Lab Syst,2001,58:109-130.
[13] Peng L,Xia W,Ruisheng Z.CoMFA and CoMSIA studies on HIV-1 attachment inhibitors[J].European Journal of Medicinal Chemistry,2010,45:1 792-1 798.
[14] Clark M,Cramer R D,Opdenbosch N O.Validation of the general purpose Tripos 5.2 force field[J].Journal of Computational Chemistry,1989,10(8):982-1 012.
[15] Pople J A,Gordon M.Substituent effects and dipole moments[J].American Chemical Society,1967,89(3):4 253-4 265.
[16] 郑康成,何 峰,云逢存,等.抗癌性吲哚喹唑啉衍生物3D-QSAR研究及其分子设计[J].物理化学学报,1999,15(8):698-703.
[17] Zheng K C,Wang J P,Peng W L,et al.Studies on 6,6-disubstitution effects of the dpq in [Ru (bpy) (2) (dpq)] (2+) with DFT method[J].Journal Physical Chemistry A,2001,105:10 899-10 901.
【责任编辑:陈 佳】
3D-QSAR and molecular design of indole derivatives
TONG Jian-bo, ZHAN Pei, LI Ling-xiao, WU Ying-ji, LI Kang-nan
(College of Chemistry and Chemical Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China)
Topomer CoMFA was used to build the 3D-QSAR model of 52 indole derivatives in this paper.Three-dimensional quantitative structure-activity relationship model were built by Topomer CoMFA.The coefficient of cross validation,the coefficient of non-cross validation and external validation were 0.651,0.996 and 0.764.The result showed that this model had good stability and predictive ability.Contour maps of Topomer CoMFA model provide visual field of electrostatic and steric field,it reveal that structure of compounds of different substituent have effected on its biological activity.Based on the above informations, three new molecules of indole derivatives with higher activity have been theoretically designed,the QSAR results can offer atheoretical reference for the pharmaceutical synthesis.
three-quantitative structure-activity relationship; Topomer CoMFA; molecular design; indole derivatives
2016-04-01
国家自然科学基金项目(21475081); 陕西省科技厅自然科学基础研究计划项目(2015JM2057); 陕西科技大学研究生创新基金项目
仝建波(1975-),男,山西怀仁人,副教授,博士,研究方向:计算机辅助药物设计
1000-5811(2016)05-0137-05
O6-04
A

