HPLC-MS-MS测定犬血浆中间尼索地平含量
李敏 李少燕 张爱国 张玉梅 苑霖 贾佩佩
·药物研究·
HPLC-MS-MS测定犬血浆中间尼索地平含量
李敏 李少燕 张爱国 张玉梅 苑霖 贾佩佩
目的 利用HPLC-MS-MS测定Beagle犬血浆中间尼索地平的含量,并计算药动学参数。方法 利用Symmetry C18柱,20℃下,以乙腈-水(70∶30, v/v)为流动相,流速为0.8 ml/min,检测波长237 nm。采用负离子多离子反应监测,用于定量分析的离子反应为m/z 387.0→ m/z 122.0。血浆样品采用乙腈沉淀蛋白,进样质谱分析。结果 方法的最低定量下限为0.25 ng/ml;间尼索地平检测浓度在0.25~20 ng/ml的范围内线性关系良好(r=0.9943)。药代动力学参数:Cmax为(13.86±3.12)ng/ml,Tmax为(2.6±2.25)h,t1/2为(9.37±2.74)h,ke为(1.24±0.52)×10-3,AUC0-t为(88.46±4.79)ng·h-1·ml-1,AUC0-∞为(98.35±1.89)ng·h-1·ml-1。结论 本法灵敏度高,操作方便,适合于Beagle犬血浆中间尼索地平的药动学研究。
间尼索地平;HPLC-MS-MS;药动学
高血压是持续血压过高的疾病,可伴有心脏、血管、脑和肾脏等器官功能性或器质性改变的全身性疾病,稍有不慎会引起中风、心脏病、血管瘤、肾衰竭等疾病,因此已引起人们的高度重视。间尼索地平(m-Nisoldipine)是新型的1,4-二氢吡啶类血管扩张性钙通道受体拮抗剂[1,2],具有良好的降压效果[3-5]。本文旨在通过优化色谱质谱条件,采用液-质联用(LC-MS-MS)技术测定Beagle犬血浆中间尼索地平的含量[6-9],进行药代动力学研究[10-15]。
1 仪器与试药
1.1 试验仪器 Agilent 1100LC/MSD色谱系统API 4000型液相色谱-三重四级杆质谱联用仪,配有ESI源(美国ABI公司);Shimadzu 20A 系统输液泵:二元梯度泵、在线脱气机、柱温箱(日本Shimadzu公司);MDS Sciex Analyst software (version1.4.1,美国ABI公司);TG16-WS型离心机(湖南湘仪离心机仪器有限公司)。
1.2 药品及方法 间-尼索地平对照品(河北医科大学药学院提供);乙腈(色谱纯,Fisher化学公司);醋酸铵(色谱纯,Tedia化学公司)。6只Beagle犬(购自上海新冈实验动物场)体重7~11 kg,雌雄各半,试验前12 h禁食,将药物夹在馒头中喂食。
2 结果
2.1 溶液的配制 精密称取间-尼索地平对照品25 mg,置25 ml量瓶中,用乙腈溶解并定容配成浓度为1.0 mg/ml的储备液。
2.2 血浆样本的制备 按体重以2.5 mg/kg剂量,使6只Beagle犬吞服夹有药物的馒头,分别于0.25、0.5、1、1.5、2、3、4、8、12、24、48 h时间点,从皮下隐静脉取血置于肝素化离心塑料管中,分离血浆,同法取空白血浆, -20℃保存备用。
2.3 血浆样品预处理 精密吸取Beagle犬血浆100 μl,依次加入300 μl乙腈(或200 μl乙腈,100 μl乙腈标准系列溶液),涡旋30 s,离心(10 000 r/min)5 min,取上清液100 μl,加200 μl水溶液,涡旋30 s,取200 μl上述溶液于进样器小瓶,进样50 μl进行 LC-MS分析。
2.4 色谱质谱条件的选择 色谱柱:C18柱(150 mm×4.6 mm;4.6 μm),预柱同分析柱配套;20℃下,以乙腈-水(70∶30, v/v)为流动相,进样量:50 μl;流速:0.8 ml/min,检测波长237 nm。
MSD检测条件:离子源为ESI源;喷雾电压-4 000 V;雾化温度500℃;雾化气NEB 40 L/min;碰撞气CAD为8 L/min;帘气CUR为20 L/min;辅助气AUX40 L/min;检测方式为负离子多离子反应监测(MRM),碰撞诱导解离(CID)电压为27 V;驻留时间(dwell time)为100 ms,用于定量分析的离子反应为m/z 387.0→m/z 122.0。
2.5 方法学考察
2.5.1 专属性:间尼索地平的主要碎片离子m/z 122为定量分析时监测的产物离子。测得Beagle犬空白血浆、空白血浆加药及给药后血浆样品的典型色谱图,间尼索地平的保留时间5.97 min。且Beagle犬空白血浆中的内源性物质不影响间尼索地平的测定。见图1。
2.5.2 标准曲线与最低定量下限:精密称取“2.1”储备液,用乙腈稀释成一系列浓度0.25、0.5、1.0、2.0、5.0、15.0、20.0 ng/ml的标准溶液。分别精密吸取上述溶液100 μl,精密加入Beagle犬空白血浆100 μl,按“2.3”项下同法操作,以间尼索地平的峰面积(A)对其浓度C(ng/ml)进行线性回归,得回归方程为:A=5590C+254(r=0.9943)。结果表明,间尼索地平血浆浓度在0.25~20.0 ng/ml范围内,线性关系良好。血浆中间尼索地平的定量下限为0.25 ng/ml。
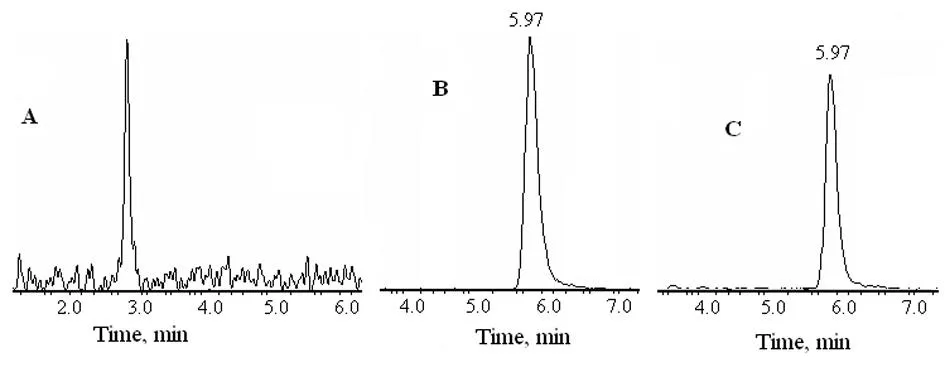
图1 间尼索地平在Beagle犬血浆中的色谱图
注:A:空白Beagle犬血浆;B:空白Beagle犬血浆加间尼索地平;C:Beagle犬口服间尼索地平30 min后血浆样品
2.5.3 精密度与准确度:分别精密吸取0.5、2.0、15.0 ng/ml 3种浓度间尼索地平标准溶液100 μl各3份,精密加入Beagle犬空白血浆100 μl,按“2.3”项下同法操作,依上述质谱条件测定,计算结果表明,3种浓度间尼索地平的准确度RE、日内及日间RSD均小于15%,符合目前生物样品分析方法指导原则的有关规定。
2.5.4 回收率与基质效应:分别精密吸取0.5、2.0、15.0 ng/ml 3种浓度间尼索地平标准溶液100 μl各3份,按“2.3”项下同法操作,计算间尼索地平的回收率为:(101.6±1.11)%,(98.7±0.53)%,(99.7±7.21)%。血浆中3种浓度的回收率均大于80%,其相对偏差均小于10%,说明该方法的回收率符合要求。
取间尼索地平0.5,2.0,15.0 ng/ml 3种浓度的标准液,用流动相代替血浆,按“2.3”项下同法操作,记录间尼索地平的峰面积为A1。另取Beagle犬空白血浆按“2.3”项下方法萃取并“N2流下吹干”后,加入3种浓度的标准品溶液进行检测,记录间尼索地平的峰面积为A2。计算基质效应ME=A2/A1×100%,ME分别为:(95.4±5.1)%,(97.5±3.1)%,(101.5±6.7)%,3种浓度间尼索地平的ME均大于80%,符合规定。
2.5.5 样品稳定性考察:按“2.3”项下方法制备0.5、2.0、15.0 ng/ml 3种浓度间尼索地平样本各3份,考察其室温放置24 h及在-20℃冷冻15 d,经3次冷冻-解冻循环后间尼索地平的稳定性。结果表明,间尼索地平在上述3种条件下均稳定,相对误差RE均在±10%之间,RSD<15%。
2.6 药代动力学参数 6只Beagle犬均口服2.5 mg/kg的间尼索地平,于给药后不同时间从后肢皮下隐静脉取血,采用LC-MS-MS测得各样品中间尼索地平的浓度,根据药-时曲线,采用梯形法计算药代动力学参数。见表1、见图2。
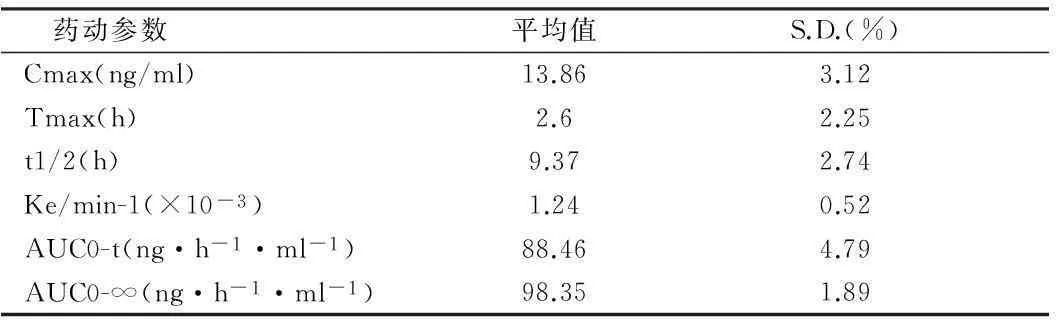
表1 Beagle犬按2.5 mg/kg剂量口服间-尼索地平药动学参数 n=6
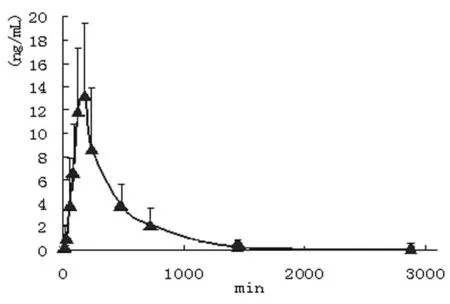
图2 Beagle犬服用间-尼索地平后药-时曲线
3 讨论
3.1 目前,我国高血压患者达1亿人之多,并有继续上升的趋势,已成为临床常见病和引发心脑血管并发症最严重的疾病之一,而有效抗高血压药物治疗可以预防由高血压引起的脑血管意外、心功能衰竭和肾功能不全,并明显降低其病死率。钙拮抗剂(Calcium antagonists)是目前治疗高血压和心绞痛的主要药物。其中二氢吡啶类钙拮抗剂(DHP-CaA)特异性高、作用强,发展迅速,现已上市的药物已达十几种,临床效果良好,大都成为心血管系统疾病的一线用药,同时与其他类型的降压药可联合应用以增强疗效,具有广阔的市场前景。
因此,间尼索地平作为新型的二氢吡啶类钙拮抗剂[3-5],对其进行全面的药动学研究刻不容缓,以便为该药的申报及上市后生产及使用提供全面的保障。
3.2 间尼索地平为新型的二氢吡啶类钙拮抗剂,迄今尚未见到利用液质联用技术测定间尼索地平在Beagle犬体内的药代动力学研究的报道。本实验通过优化色谱条件,首次建立了用LC-MS-MS法测定Beagle犬血浆中间尼索地平血药浓度的方法。并进一步研究了Beagle犬口服给药后间尼索地平在其体内的药代动力学特征,获得了可靠的动力学参数。新药的全方位研究可加强新药研发过程中对化合物的生理活性和生物利用度的确认,给药途径、剂型选择及相应工艺的优化,从而全面提高药物质量和稳定性,为新药的研制与开发提供试验根据。
3.3 本文通过LC-MS-MS对间尼索地平在Beagle犬体内药动学进行研究,由于该药在生物样品中的血药浓度相对较低[16,17],故采用简单的沉淀蛋白法处理样品,避免了二氢吡啶类生物样品经常采用的液-液萃取的冗繁操作,减少样品处理过程带来的不必要的损失。
3.4 本研究对内标物质的选择进行多项实验考察过多项物质,主要涉及到氯硝西泮、地西泮、尼莫地平、芍药苷、曲克芦丁、栀子苷和吲达帕胺等。由于色谱质谱条件、内源性物质干扰以及质谱负离子检测等多方面的局限性,未能找到合适的内标物质;经过对试验方法进行研究,采用乙腈沉淀蛋白进行样品前处理,操作简便,误差因素较少,且间尼索地平的质谱响应变异较小,经过考证分析方法的可行性,最终本法专属性、线性范围和线性关系、精密度和准确度均能够满足生物样品测定的要求,故犬血浆中间尼索地平的含量测定采用外标法进行。
3.5 生物样品进行质谱分析的前提条件是选择合适的离子化检测模式。本研究通过优化MSD参数以获得足够丰度的准分子离子峰[M-H]-进行二级质谱分析,质谱实验发现在正离子检测模式下,采用ESI或APCI离子化源,间尼索地平的测定方法均不能获得较高的灵敏度,而在负离子模式下采用ESI源,实验方法不仅有较高的灵敏度而且重现性也很好。同时,对液相色谱条件也进行了优化,在20℃下,色谱柱采用C18柱(150 mm×4.6 mm;4.6 μm),流动相为乙腈-水(70 ∶30, v/v),流速为0.8 ml/min,进样量50 μl,检测波长237 nm。
3.6 本研究采用液质联用技术测定Beagle犬血浆中间尼索地平的含量,方法精密度和准确度高、简单快速、专属性好,为该类药物研究方法的建立以及药代动力学研究奠定了基础,为间尼索地平消旋体的研制与开发提供理论和实验依据,为高血压患者的治疗提供新的药物,使高血压病人能够用到安全有效的药物。
1 武引文,颜廷仁,聂辉,等. 间尼索地平的合成. 中国医药工业杂志,1989,20:104-106.
2 袁凤燕,张振华,刘伟娜,等. 间尼索地平的HPLC测定. 中国医药工业杂志,1995,26:316-318.
3 张永健,张国红,张雅兰,等. 间尼索地平和尼索地平对自发性高血压大鼠的降压作用. 河北医学院学报,1994,15:135-137.
4 孟静,张永健,张喜仁,等. 间尼索地平对KC l及ET-1所致离体家兔冠状动脉分支收缩的拮抗作用. 华西药学杂志,2007,22:38-40.
5 陈雪彦,刘焕龙,潘振华,等. 间尼索地平对5-羟色胺诱导的大鼠肺动脉平滑肌细胞增殖中Ca2+/CaM/CaN 通路的影响. 药学学报,2010,45:49-54.
6 吴华,袁志芳,张兰桐,等. 间尼索地平含量测定方法的研究. 中国新药杂志,2006,15:367-371.
7 景秀娟,韩学静,宫立红,等. 气相色谱一质谱联用法测定间尼索地平含量. 药物分析杂志,2008,28:2048-2050.
8 景秀娟, 韩学静, 张兰桐,等. 间尼索地平的毛细管GC-电子捕获检测器法测定. 中国医药工业杂志,2008,39:125-127.
9 孔德志,张兰桐,段坤峰,等. 间尼索地平的胶束电动毛细管电泳法测定. 中国医药工业杂志,2009,40:450-456.
10 Chong HL,Sicen W.Studies on differences of pharmacokinetic behavior and tissue distribution of nimodipine and its two enantiomers in rats using achiral and chiral liquid chromatography.Brain Research,2003,38:603-608.
11 Rong WH,Qiao W,Tong ZL,et al. Validated LC-MS-MS method for determination of m-nisoldipine polymorphs in rat plasma and its application to pharmacokinetic studies. J Chromatogr B,2006,835:71-76.
12 张志清,王永利,李晓娜,等. 反相高效液相色谱法测定恒河猴血浆中间尼索地平的浓度. 中国药房,2006,17:101-103.
13 王树华,储金秀,尚清,等. RP-HPLC法测定Beagle犬血浆中间尼索地平浓度及其药代动力学.中国药科大学学报,2007,38:140-143.
14 齐晓丹,张晶,王伟. 间尼索地平控释微丸Beagle犬体内药动学研究. 中国现代应用药学,2012,29:242-245.
15 Jian Z,Yuan T,Li N,et al.High-performance liquid chromatography-electrospray ionization mass spectrometric determination of nisoldipine in human plasma. J Chromatogr Sci,2004,42:501-505.
16 Baranda R,Ana B,Mueller E,et al.Quantitative determination of the calcium channel antagonists amlodipine, lercanidipine, nitrendipine, felodipine, and lacidipine in human plasma using Liquid Chromatography-Tandem Mass Spectrometry. Therapeutic Drug Monitoring,2005,27:44-52.
17 Baranda AB,Etxebarria N,Jimenez RM,et al. Development of a liquid-liquid extraction procedure for five 1, 4-dihydropyridines calcium channel antagonists from human plasma using experimental design.Talanta,2005,67:933-941.
10.3969/j.issn.1002-7386.2016.08.046
项目来源:河北省医学科学研究重点课题(编号:20130069)
063000 河北省唐山市,华北理工大学附属医院药学部(李敏、李少燕、张爱国、张玉梅);河北医科大学药学院(苑霖、贾佩佩)
R 927.2
A
1002-7386(2016)08-1259-03
2015-11-01)

