声化学辅助溶剂热合成高光催化性能的BiOCl光催化剂
何洪波薛霜霜余长林*,,2樊启哲
(1江西理工大学冶金与化学工程学院,赣州 341000)(2福州大学能源与环境光催化国家重点实验室,福州 350002)
声化学辅助溶剂热合成高光催化性能的BiOCl光催化剂
何洪波1薛霜霜1余长林*,1,2樊启哲1
(1江西理工大学冶金与化学工程学院,赣州341000)
(2福州大学能源与环境光催化国家重点实验室,福州350002)
摘要:以五水硝酸铋和氯化钠为原料,乙二醇(EG)和水作溶剂,通过声化学辅助溶剂热法合成了系列BiOCl纳米晶光催化剂。应用氮气物理吸附、X射线粉末衍射(XRD)、扫描电镜(SEM)、傅里叶变换红外光谱(FTIR)、紫外-可见(UV-Vis)漫反射(DRS)和光电流等测试手段对所制备的光催化剂进行了表征。在汞灯和氙灯照射下,以苯酚和甲基橙为水体模型污染物,系统考察了超声辐射时间和醇水比(V(EG)/V(H2O))对BiOCl光催化剂性能的影响。结果表明,当超声辐射时间为60 min,V(EG)/V(H2O)=1/4时,合成的BiOCl表现出最佳的光催化活性,为常规沉淀法制备的BiOCl的3.3倍。活性提高的主要原因是,适当时间的超声波辐射和醇水比有利于催化剂比表面积的提高,同时可以丰富催化剂表面羟基(-OH)的数量和提高光生电子和空穴的分离效率。
关键词:超声辐射;醇水比;BiOCl;溶剂热;污染物;光催化
国家自然科学基金资助项目(No.21567008,21263005)、江西省自然科学基金青年科学基金计划(No.20133BAB21003)、江西省教育厅高等学校科技落地计划项目(No.KJLD14046);江西省青年科学家培养项目(No.20122BCB23015)、2015年江西省研究生创新专项资金项目(No. YC2015-S293)和2015江西理工大学研究生创新资金项目(No.XS201540)资助。
*通信联系人。E-mail:yuchanglinjx@163.com
在众多环境治理技术中,半导体光催化技术因其具有反应条件温和、反应设备简单、二次污染小、易于操控和可利用太阳光为能源等优点,近年来受到了人们的广泛关注[1-4]。BiOX(X=Cl, Br, I)是一类层状结构的半导体,这种高度各向异性的层状结构有利于光生电子与空穴的分离,同时这类半导体的光吸收还可以通过卤素的调控实现紫外到可见光的调控。其中,BiOCl的带隙较宽(3.5 eV),激发波长主要为紫外光[5],但BiOCl因其安全无毒、光腐蚀少、使用寿命长等优点,获得了不少研究者的青睐[6-8]。
BiOCl的光催化性能与其晶体结构和微观结构等密切相关,而微观结构主要取决于制备方法。例如,Liu等[9]报道了具有花状微球(FMs)的BiOCl,这种BiOCl (FMs)具有较大的比表面积和合适的带隙能,能有效地增强BiOCl对光的吸收,因此在紫外光照下对甲基橙表现出优异的降解性能。Zhang等[10]采用聚乙烯吡咯烷酮(PVP)和柠檬酸做形貌控制剂,合成了一系列中空结构的BiOCl光催化剂,这种中空结构有助于催化活性的提高。Hu等[11]报道了采用水热法合成了正方形BiOCl纳米片,这种纳米片在紫外光下表现出优异的光催化活性和良好的稳定性。此外,采用合适的方法对BiOCl改性,也能有效拓展其可见光光响应范围或增强其可见光光催化效果。例如,利用g-C3N4[12]、Fe3O4[13]和Bi2S3[14]复合, Fe[15]、S[16]掺杂及Ag[17]、Pt[18]等贵金属负载。
声化学是一种特殊的纳米材料的合成方法。它主要是利用超声空化产生特殊的物理化学环境,如瞬间高压(约100 MPa)、高温(约5 000 K)、高强度的温度变化速率(109K·s-1)和很强的冲击波来强化化学键的断裂、自由基的生成,实现半导体从无定型态到固定晶型的转变。这种独特的环境有利于合成特殊结构的纳米光催化剂[19-21]。本论文采用超声辅助溶剂热法制备系列BiOCl光催化剂。考察了超声辐射时间和反应介质(醇水比)对BiOCl的结构和光催化性能的影响。研究表明,当超声时间为60 min,VEG/ VH2O=1/4时,合成的BiOCl对苯酚和甲基橙具有极高的光催化降解能力。
1 实验部分
1.1催化剂的制备
本实验所采用的药品均为分析纯试剂,由上海国药集团提供。采用声化学辅助溶剂热法合成BiOCl,具体方法如下:5 mmol Bi(NO3)3·5H2O溶解在一定比例的EG和去离子水溶液中制成A溶液;5 mmol NaCl溶解在20 mL去离子水得到B溶液。在磁力搅拌器强烈搅拌下,把B溶液滴加至A溶液中,然后利用VOSHIN-501D超声波信号发生器连接Φ10变幅杆(选择超声功率为10%,超声2 s,间隔5 s)超声反应相应的时间。超声辐射完成后,将反应后的悬浮液体转入高压釜中,于140℃处理14 h,自然冷却后用无水乙醇与去离子水交替洗涤3次,在80℃下烘干5 h,得到BiOCl样品。为了考察超声辐射时间和反应介质对BiOCl的结构和性能的影响,首先固定VEG/VH2O(β)为2/3,溶剂的总体积为50 mL,改变超声时间α(min),制备不同时间的超声辐射下的BiOCl样品;然后固定超声时间α,改变β,制备不同醇水比下的BiOCl样品。根据参数α和β,所得的样品记为α(β)-BiOCl。
1.2催化剂的表征
样品的比表面积在ASAP2020进行N2-物理吸附上测定,测试前在110℃下脱气1 h,然后在液氮温度下进行吸附-脱附,结合BET方程计算样品的比表面积。样品的晶相和结晶度采用Bruker-D8-Advance X射线衍射仪对样品进行分析(Cu Kα,λ= 0.154 18 nm)进行测试,测试电压为40 kV,电流为40 mA。利用UV-2550型(日本岛津)紫外-可见漫反射分光光度计测定样品的吸收光谱,用BaSO4作为参比,扫描范围为200~800 nm。样品的傅里叶变换红外光谱在德国布鲁克公司ALPHA型红外光谱仪上进行测试,分辨率为4 cm-1。样品的整体形貌采用MLA650F型扫描电子显微镜(SEM,美国FEL公司)进行观察。光电流测试采用CHI660D电化学工作站进行分析,以石墨电极、标准甘汞电极和样品作为对电极、参考电极和工作电极,以0.5 mol·L-1硫酸钠溶液作为电解液。工作电极的制备是将0.01 g催化剂分散到0.1 mL无水乙醇中,超声分散30 min,然后取20 μL悬浮液滴在FTO玻璃上。采用500 W氙灯作为可见光光源测试样品光电流。
1.3催化剂的评价
BiOCl的光催化性能通过紫外光降解苯酚溶液和模拟太阳光降解甲基橙溶液来评价。紫外光源选用300 W汞灯,光催化反应器为南京胥江机电厂生产的XPA系列光催化反应器。将0.03 g催化剂分散在50 mL浓度为20 mg·L-1的苯酚溶液中,于暗处磁力搅拌40 min以达催化剂与苯酚溶液的吸附-脱附平衡。然后打开光源进行照射,每间隔15 min取一次样(2~3 mL),样液经高速离心分离后,上层清液用UV-6300型紫外-可见分光光度测试苯酚溶液的吸光度,其最大吸收波长λ=268 nm。模拟太阳光光源催化降解时,将0.05 g催化剂分散于80 mL甲基橙(20 mg·L-1)中,暗处磁力搅拌40 min以达到甲基橙溶液与催化剂的吸附-脱附平衡。通入循环水冷却,打开500 W氙灯光源后开始计时,每间隔15 min取一次样(2~3 mL),样液经高速离心分离后,上层清液采用同型号的紫外-可见分光光度计测试其吸光度,甲基橙最大吸收波长λ=460 nm。通过测定吸光度的变化来计算苯酚溶液和甲基橙溶液的降解率。即降解率D=(C0-Ct)/C0×100%=(A0-At)/A0× 100 %,式中C0为初始溶液中目标物的浓度,Ct为反应时间为t时目标物的浓度, A0为初始溶液的吸光度,At为反应时间为t时溶液的吸光度。
2结果与讨论
2.1 XRD和BET比表面积分析
图1为不同超声辐射时间和不同VEG/VH2O时合成的BiOCl样品的XRD图。从图中可以看出,不同条件下制备的BiOCl具有大致相同的衍射峰。在衍射角2θ=24.42°,26.1°,32.5°,33.6°,41.0°,46.8°,49.9°,54.3°,58.9°处出现了强的特征衍射峰,分别对应于六方晶系的BiOCl (002),(011),(110),(012),(112),(020),(113),(121),(122)晶面(JCPDS No. 73-2060),空间群为P4/nmm。从图1(a)可知,在维持VEG/VH2O=2/3,改变超声辐射时间(0~75 min),样品表现出相似的衍射峰,表明超声辐射时间对BiOCl的晶相结构影响不大。图1(b)为选取超声辐射时间为60 min,改变反应溶剂VEG/VH2O(0~3/2)合成的BiOCl样品衍射图。比较图1(b)的衍射曲线可知,当溶剂中不加入EG时,BiOCl在衍射角2θ=33.6°处出现最强特征衍射峰,说明其具有较好的(012)晶面;随着溶剂中EG的含量增大,衍射角2θ=33.6°处的特征衍射峰减弱,而衍射角2θ=32.5°处的特征衍射峰增强。说明在水溶液的环境下,有益于(012)晶面的生长,而在EG溶液的环境下,有益于(110)晶面的生长。

图1 不同超声辐射时间(a)和不同VEG/VH2O(b)合成的BiOCl样品的XRD图Fig.1 XRD patterns of the BiOCl samples prepared in different ultrason irradiation time(a) and with various ratios of EG and H2O(b)
根据Scherrer公式L=0.89λ/(Bcosθ)选取XRD图中(012)晶面的衍射峰的半峰宽,计算各样品的晶粒尺寸,式中L为平均晶粒尺寸,λ为X射线波长,B为半峰宽,θ为入射角。所得结果列于表1。从表1中可见,超声辐射时间对BiOCl平均晶粒尺寸影响不是很大。但是EG的影响却很大,其中60 (0∶5)-BiOCl的平均晶粒尺寸最大(67.85 nm),而60(1∶4)-BiOCl的平均晶粒尺寸仅为37.49 nm,说明加入少量的EG有利于抑制BiOCl晶粒的长大。
对所制备的样品进行N2-物理吸附测试,利用BET方程式计算各样品的比表面积,结果列于表1。可以看出,EG的浓度对样品的比表面积起决定性作用,少量EG的存在(VEG/VH2O=1/4)明显增大BiOCl的比表面积,且随着EG的浓度的增大,样品的比表面积单调递增;超声时间对比表面积的影响总体不是很大,随着超声时间的增加,比表面积表现出先增大后减少的趋势,在超声时间为45 min时,比表面积最大。

表1 样品的比表面积和晶粒尺寸Table1 Specific surface area and crystals size of the samples
2.2样品的扫描电镜(SEM)分析
图2为不同条件下制备的典型BiOCl样品的扫描电镜照片。(a)、(b)、(c)和(d)分别是0(2∶3)-BiOCl、60 (2∶3)-BiOCl、60(0∶5)-BiOCl、60(1∶4)-BiOCl的SEM照片。从图2(a)和图2(b)可以看出以,当溶剂VEG/VH2O= 2/3时,所合成的BiOCl样品是由厚度为25~30 nm的片状粒子所组成,样品分散性较好,且超声辐射后样品的整体形貌并未发现明显变化。从图2(c)中可以看出,当溶剂中未添加EG时,制备的BiOCl为边角光滑谷粒状颗粒,颗粒直径明显大于其它添加了EG制备的样品,这是其比表面积极小的原因所在,也和前面的XRD和BET测试结果相吻合。因此EG的存在可以抑制BiOCl晶体的长大,并提高其比表面积。图2(d)表明,当VEG/VH2O=1/4,超声辐射时间为60 min,制备的60(1∶4)-BiOCl的整体形貌更规整,由大量分散均匀的纳米四方或长方体所组成。

图2 不同超声辐射时间和不同VEG/VH2O合成的BiOCl样品的SEM照片Fig.2 SEM images of BiOCl samples prepared in different ultrasonic irradiation time and with various ratios of EG and H2O
2.3红外光谱(FTIR)分析
利用红外光谱分析样品表面性质。图3为各样品的FTIR谱图。对比该图中所有样品的红外光谱图,可见当溶剂中未添加EG时,超声合成的60(0∶5) -BiOCl在3 500 cm-1附近仅出现一微弱吸收峰,而其它样品在此处对应的吸收峰更强。这个吸收峰为BiOCl表面羟基(-OH)的特征伸缩振动峰。可见当反应溶剂中存在EG时有利于丰富BiOCl的表面羟基数量。所有样品在1 640 cm-1附近的吸收峰为吸附游离水的H-O-H弯曲振动峰;所有样品在500 cm-1附近出现Bi-O特征吸收峰,且峰型较为尖锐。经比对可以发现,当固定VEG/VH2O=2/3,改变超声辐射时间时,超声时间延长,羟基(-OH)的特征吸收峰强度略有增强;而固定超声辐射时间为60 min,VEG/VH2O越大,羟基(-OH)的特征吸收峰增强越明显。在光催化反应中,催化剂的表面羟基是羟基自由基(·OH)的重要来源,而羟基自由基是氧化降解有机分子的重要活性物质,由此可见,超声和添加乙二醇做溶剂是有利于提高BiOCl光催化活性的。比较在500 cm-1附近出现的Bi-O特征吸收峰(图3(a)),还可以看出,在相同溶剂的条件下,超声时间为60min制备的BiOCl的Bi-O特征吸收峰最强;图3(b)则显示相同超声时间的条件下,溶剂VEG/VH2O=1/4所制备的BiOCl的Bi-O特征吸收峰最强,说明在此条件下,生成的Bi-O键最强,这可能来自于BiOCl结晶度的提高。

图3 不同超声辐射时间(a)和不同VEG/VH2O(b)合成的BiOCl样品的FTIR谱图Fig.3 FTIR infrared spectra of the BiOCl samples prepared in different ultrasonic irradiation time(a) and various ratios of EG and H2O(b)
2.4紫外可见漫反射光谱(UV-Vis DRS)分析
利用紫外-可见漫反射吸收光谱测试所制备样品对不同波长的光吸收情况。图4 (a)为固定VEG/ VH2O=2/3的条件下,不同超声时间下制备的样品的吸收光谱。由该图可见,BiOCl的吸收边在365 nm左右,超声辐射后,BiOCl的整体吸收略有不同程度的加强,且60(2∶3)-BiOCl在紫外区和可见光区的吸收最强,这可能得益于其特殊的形貌和晶面结构。
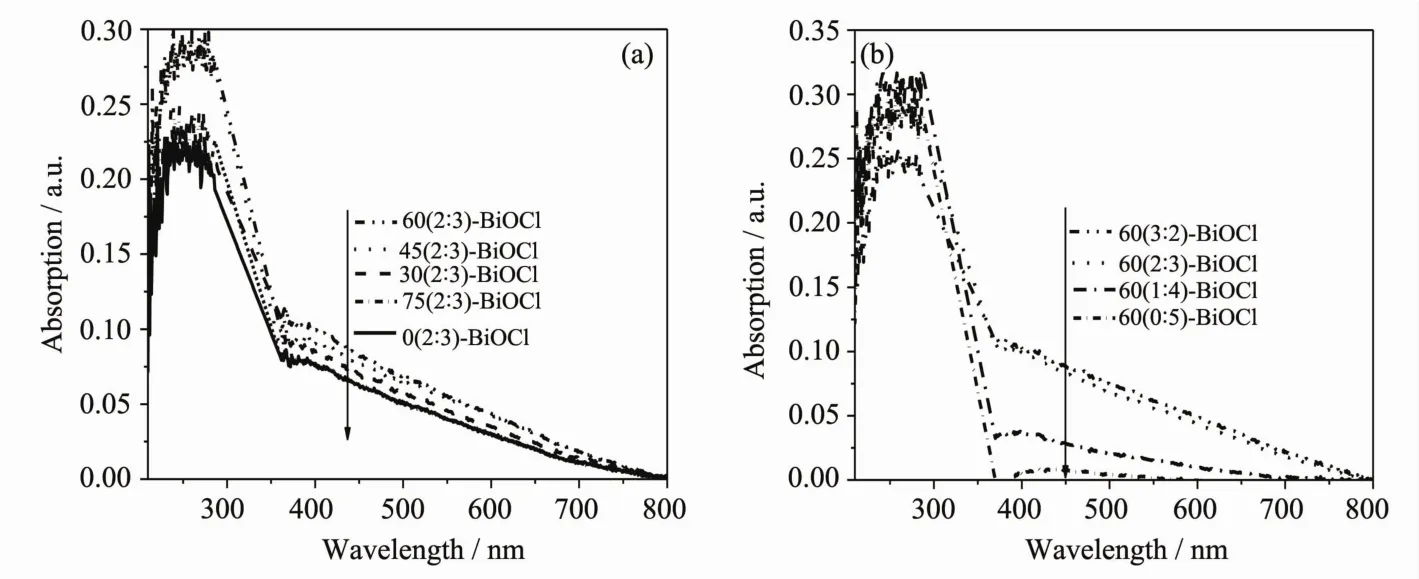
图4 不同超声辐照时间(a)和不同VEG/VH2O比(b)合成的BiOCl样品的UV-Vis DRS谱图Fig.4 UV-Vis spectra of the BiOCl samples prepared in different ultrason irradiation time(a) and with various ratios of EG and H2O(b)
图4(b)为固定超声辐射时间为60 min,不同VEG/VH2O下制备的样品的吸收光谱。以水为溶剂制备的BiOCl在可见光区几乎没什么吸收。在固定超声辐射时间为60 min的条件下,随着溶剂中EG浓度的增大,合成的BiOCl在可见光区的吸收逐渐增强。
2.5光电流分析
光电流可以间接的反映半导体材料在光照条件下,光生电子和空穴的复合情况,图5为典型样品的光电流测试Ipht曲线。光照开始后光电流密度由Iph(max)快速衰减为Iph(ss),其主要原因是由于光生电子-空穴对在催化剂界面发生的表面复合。因此,可用表观表面复合几率(SPR)表示光生电子和空穴在催化剂表面复合的情况[22]:
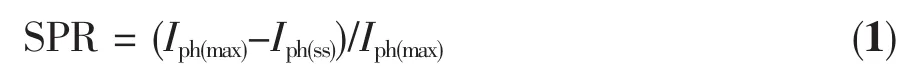
根据式(1)和Iph-t曲线得出的Iph(ss)及Iph(max)数据可以确定催化剂的表观复合几率,具体列于表2。可以看出,在超声时间同为60 min的条件下,水热法制备的BiOCl的表观SPR是25.9%,而VEG/VH2O=1/4时溶剂热法制备的BiOCl的表观SPR仅为9.27%。因此,可以推测,与60(0∶5)-BiOCl相比,60(1∶4)-BiOCl对迁移至催化剂表层的光生电子和空穴的有效利用率提高了约65%。同理,60(1∶4)-BiOCl对表层光生电子和空穴的有效利用率也高于60(2∶3)-BiOCl。

图5 典型BiOCl光催化剂的暂态光电流密度响应Fig.5 Transient photocurrent density responses of 60(0∶5) -BiOCl, 60(1∶4)-BiOCl and 60(2∶3)-BiOCl

表2 典型BiOCl的峰值光电流密度(Iph(max)),暂态光电流密度(Iph(ss))及载流子表面复合几率Table2 Values of peak photocurrent densities (Iph(max)) and transient photocurrent densities (Iph(ss)), and apparent surface-recombination probability of BiOCl
2.6光催化性能测试
不同条件下制备的BiOCl的光催化性能首先通过降解苯酚来评价。图6(a)为固定VEG/VH2O=2/3的条件下,不同超声辐射时间所制备的BiOCl在紫外光照射下苯酚的浓度C/C0对光照时间的关系曲线。从图6(c)苯酚降解率的柱状图可以看出,紫外光照射75 min时,60 (2∶3)-BiOCl对苯酚的降解率达到85.8 %。可见在固定VEG/VH2O=2/3的条件下,超声辐射60 min下合成的BiOCl光催化性能最好。图6(b)为固定超声辐射时间为60 min,不同VEG/VH2O下制备的样品在紫外光照射下苯酚的浓度C/C0对光照时间的关系曲线。图6(c)表明,紫外光照射75 min时,60(0∶5)-BiOCl对苯酚的降解率为51.4%,而60(1∶4)-BiOCl基本上可以实现苯酚的完全降解,降解率接近100%。溶剂VEG/VH2O的逐渐增大,BiOCl对苯酚的降解率逐渐降低,可见醇水比对BiOCl的活性影响非常大。图6(d)为60(1∶4)-BiOCl对苯酚降解过程中,苯酚的紫外可见吸收光谱变化图。
为了进一步比较声化学辅助溶剂热合成BiOCl的光催化性能,我们同时采用常规沉淀法制备了BiOCl,并比较了两者在模拟太阳光(氙灯)下降解染料甲基橙的光催化性能。图7(a)为60(1∶4)-BiOCl和沉淀法制备的BiOCl在氙灯光照下,甲基橙的浓度C/C0对光照时间的关系曲线。
该图表明,氙灯照射90 min时,沉淀法制备BiOCl对甲基橙的降解率约为60%,而60 (1∶4)-BiOCl对甲基橙的降解率高达95%。图7(b)为60(1∶4)-BiOCl和沉淀法制备的BiOCl对甲基橙光催化降解的反应动力学模拟曲线,由图可求得60 (1∶4)-BiOCl的反应速率常数(0.031 7 min-1)为常规沉淀法制备BiOCl的速率常数(0.009 5 min-1)的3.3倍。可见采用超声辅助溶剂热法合成的BiOCl能有效提高太阳光照下的光催化活性。
结合前面的表征,我们分析了60(1∶4)-BiOCl表现出优异光催化性能的主要原因有以下几点:首先,XRD和比表面积测试表明,维持适当的VEG/VH2O和超声辐射时间有利于增大催化剂的比表面积和缩小BiOCl平均晶粒粒径,这样光生电子迁移到催化剂表面所需的时间更短,也能够有效地抑制光生电子和空穴的复合;其次,FTIR谱图表明,60(1∶4)-BiOCl具有丰富的表面羟基(-OH)以及较高的结晶度,有利于生成更多的活性物质,提高光催化效率;同时紫外可见吸收光谱测试表明,60(1∶4)-BiOCl在紫外可见光谱区具有较强的吸收;最后,光电流测试的SPR间接表明,60(1∶4)-BiOCl光生电子空穴对重组的几率小,电子和空穴的寿命长,光生电子和空穴的有效利用率高。
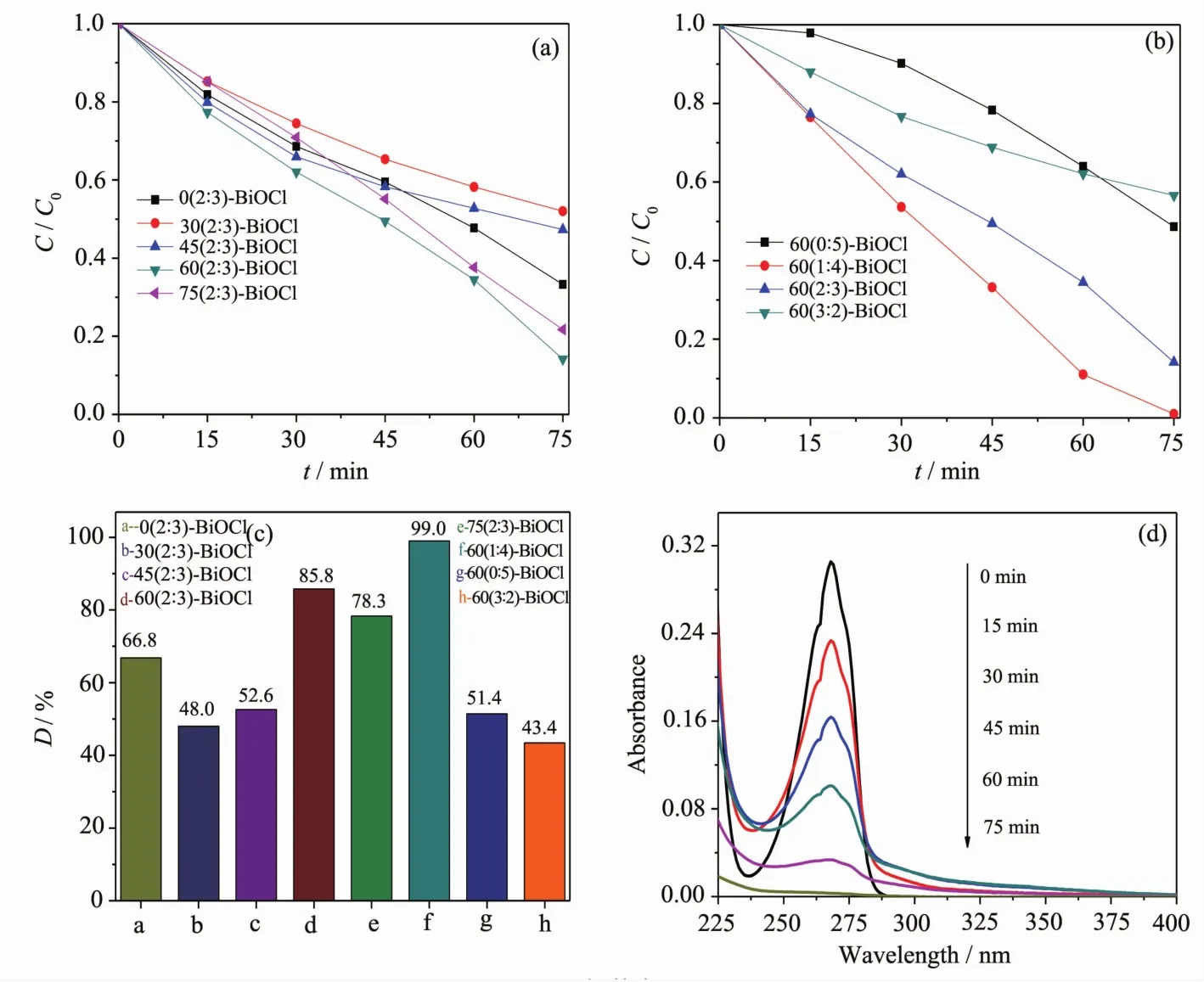
图6 不同条件制备的BiOCl在紫外光照射下降解苯酚光催化性能Fig.6 UV-photocatalytic performance of BiOCl prepared under different condition in degradation of phenol: (a) BiOCl prepared in different ultrasound irradiation time (VEG/VH2O=2/3); (b) BiOCl prepared with different ratios of EG and H2O under ultrasound irradiation for 75 min; (c) Degradation rates of phenol over different BiOCl samples; (d) UV-Vis absorption spectra of phenol in different reaction time in the presence of 60(1∶4)-BiOCl

图7 氙灯照射下60(1∶4)-BiOCl和BiOCl(沉淀法)降解甲基橙光催化活性比较Fig.7 Photocatalytic performance comparison of 60(1∶4)-BiOCl and BiOCl (prepared by traditional precipitation method) in degradation of methyl orange (MO) under xenon lamp irradiation: (a) Degradation profiles of MO over the 60(1∶4)-BiOCl and BiOCl (prepared by traditional precipitation method); (b) Reaction kinetics of degradation of the MO over the 60(1∶4) -BiOCl and BiOCl(prepared by traditional precipitation method)
3结 论
通过声化学辅助溶剂热法合成了系列BiOCl光催化剂,系统考察了超声辐射时间和醇水比(VEG/ VH2O)对BiOCl结构和光催化性能的影响。结果表明,当超声辐射时间为60 min,VEG/VH2O=1/4时合成的60(1∶4)-BiOCl对苯酚和甲基橙表现出最佳的光催化活性。紫外光照射75 min时,对苯酚的降解率接近100%;氙灯照射90 min时,对甲基橙的降解率达到95%,为常规沉淀法制备的BiOCl活性的3.3倍。光催化活性的提高得益于声化学辅助溶剂热法合成的BiOCl具有丰富的表面羟基(-OH)、较小的晶粒尺寸、较大的比表面积以及较高的光生电子和空穴的分离效率。
参考文献:
[1] Yu J G, Low J X, Xiao W, et al. J. Am. Chem. Soc., 2014,136:8839-8842
[2] ZHANG Qin(张琴), WANG Xiao-Feng(汪晓凤), DUAN Fang(段芳), et al. Chinese J. Inorg. Chem.(无机化学学报), 2015, 31:2151-2158
[3] LI Ai-Chang(李爱昌), ZHU Ning-Ning(朱柠柠), LI Jing -Hong(李京红), et al. Chinese J. Inorg. Chem. (无机化学学报), 2015,31:681-688
[4] YU Chang-Lin(余长林), ZHOU Wan-Qin(周晚琴), Yu J C. Chinese J. Inorg. Chem. (无机化学学报), 2011,27:2033 -2038
[5] Peng H L, Chan C K, Meister S, et al. Chem. Mater., 2008, 21:247-252
[6] Shen K, Gondal M A, Al-Saadi A A, et al. Res. Chem. Intermed., 2015,41:2753-2766
[7] Ye L Q, Zan L, Tian L H, et al. Chem. Commun., 2011,47: 6951-6953
[8] Jiang J, Zhao K, Xiao X Y, et al. J. Am. Chem. Soc., 2012, 134:4473-4476
[9] Liu J Q, Hu J J, Ruan L, et al. Chin. Sci. Bull., 2014,59: 802-809
[10]Zhang K, Liang J, Wang S, et al. Cryst. Growth Des., 2012,12:793-803
[11]Hu J J, Liu J Q, Ruan L L, et al. Optoelectron. Lett., 2015,11:5-9
[12]Yang Y F, Zhou F, Zhan S, et al. J. Inorg. Organomet. Polym., 2015:1-9
[13]Tan C W, Zhu G Q, Hojamberdiev M, et al. J. Cluster Sci., 2013,24:1115-1126
[14]Cheng H F, Huang B B, Qin X Y, et al. Chem. Commun., 2012,48:97-99
[15]Nussbaum M, Shaham-Waldmann N, Paz Y. J. Photochem. Photobiol. A, 2014,290:11-21
[16]Weng S X, Hu J, Lu M L, et al. Appl. Catal. B, 2015,163: 205-213
[17]Jiang J, Zhang L Z, Li H, et al. Nanoscale, 2013,5:10573-10581
[18]YU Chang-Lin(余长林), CHEN Jian-Chai(陈建钗), CAO Fang-Fang(操芳芳), et al. Chin. J. Catal.(催化学报), 2013,34:385-390
[19]Yu C L, Yu J C, Chan M. J. Solid State Chem., 2009,182: 1061-1069
[20]Yu C L, Yu J C. Mater. Sci. Eng. B, 2009,164:16-22
[21]Zhou W Q, Yu C L, Fan Q Z, et al. Chin. J. Catal. (催化学报), 2013,34:1250-1255
[22]Kong D S, Wei Y J, Li X X, et al. J. Electrochem. Soc., 2014,161:H144-H153
Sonochemistry Assisted Solvothermal Preparation of BiOCl Photocatalyst with High Photocatalytic Performance
HE Hong-Bo1XUE Shuang-Shuang1YU Chang-Lin*,1,2FAN Qi-Zhe1
(1School of Metallurgy and Chemical Engineering, Jiangxi University of Science and Technology, Ganzhou, Jiangxi 341000, China) (2State Key Laboratory of Photocatalysis on Energy and Environment, Fuzhou University, Fuzhou 350002, China)
Abstract:Using Bi(NO3)3·5H2O and NaCl as precursors, ethylene glycol and water as solvent, BiOCl photocatalysts were synthesized by sonochemistry assisted hydrothermal or solvothermal method. The as-synthesized products were characterized by N2physical adsorption,X-ray diffraction, scanning electron microscopy, Fourier translation infrared spectroscopy (FTIR),UV-Vis diffuse reflectance spectroscopy (DRS) and photoelectrochemical measurements. With phenol and methyl orange as the model degradation pollutants and mercury lamp and xenon lamp as light source, the effects of ultrason irradiation time and the V(EG)/V(H2O)on photocatalyst performance of the BiOCl were studied. Results indicated that BiOCl synthesized under ultrason irradiation time for 60 min and with V(EG)/V(H2O)of 1/4 showed the excellent photocatalytic activity. With respect to BiOCl synthesized by traditional precipitation, 3.3 times increase over the ultrason fabricated BiOCl were obtained. The main reasons for the enhanced activity could be that the ultrason irradiation with appropriate time and suitable V(EG)/V(H2O)might benefit the increase in surface area and surface -OH groups, and the decrease in crystal size. Moreover, a high separation efficiency of photogenerated electrons (e-) and hole (h+) was observed over the ultrason fabricated BiOCl.
Keywords:ultrason irradiation; ratio of ethylene glycol and water; BiOCl; solvothermal; pollutants; photocatalysis
收稿日期:2015-12-02。收修改稿日期:2016-03-03。
DOI:10.11862/CJIC.2016.091
中图分类号:TQ426.6
文献标识码:A
文章编号:1001-4861(2016)04-0625-08

