IFCC促甲状腺激素国际溯源和检测一致性系列研究(二)
于 翔,陈文霏,余小六,江 明,李 可,余枝广
(深圳迈瑞生物医疗电子股份有限公司免疫试剂开发部,广东深圳 518057)
IFCC促甲状腺激素国际溯源和检测一致性系列研究(二)
于翔,陈文霏#,余小六,江明,李可,余枝广△
(深圳迈瑞生物医疗电子股份有限公司免疫试剂开发部,广东深圳 518057)
摘要:目的通过参与国际临床化学联合会(IFCC)甲状腺功能检测标准化委员会(C-STFT)一致性研究方案,初步实现迈瑞检测系统促甲状腺激素(TSH)检测结果的一致性。方法使用不同批次试剂和校准品搭配构成的3种组合,分别检测发放的20例健康者标本,评估检测结果的批内不精密度和批间差异。与C-STFT提供的所有测量程序修剪均值(APTM)比对,评估一致性,并修正校准曲线进行重校准。结果检测结果的批内不精密度为1.95%,批间差异范围为0.47%~1.15%;与APTM存在正偏差,修正校准曲线重校准后,检测结果Passing & Bablok回归线斜率为1.0,相关系数大于0.975。结论通过检测IFCC统一发放的血清盘和参考提供的APTM值,修正校准曲线重校准,实现了该检测系统与其他厂家检测系统TSH检测结果的一致性。
关键词:促甲状腺激素;化学发光免疫分析法;国际临床化学联合会甲状腺功能检测标准化委员会;测量程序修剪均值
促甲状腺激素(TSH)检测具有世界卫生组织国际标准品(NIBSC 81/565),但由于存在基质效应、分析物差异性等问题,不能保证可溯源至标准品的所有检测系统对实际标本检测结果的一致性[1]。自2010年开始,国际临床化学联合会(IFCC)甲状腺功能检测标准化委员会(C-STFT)尝试推出特定的血清盘及所有测量程序修剪均值(APTM)的概念,在全球范围征集了具有代表性的十余个厂家检测系统,包括罗氏、雅培、贝克曼、西门子、迈瑞等,分阶段进行TSH检测结果一致性的可行性研究[2-3]。迈瑞公司采用CL2000i免疫检测系统和配套TSH试剂盒,检测了C-STFT提供的首期20份血清标本。C-STFT结合所有参与厂家的检测结果,对CL2000i系统TSH检测结果的可靠性和一致性进行了客观评估。迈瑞公司则结合C-STFT反馈结果,根据20份标本的APTM数值修正校准曲线,并对检测系统进行了重校准,初步实现了与国际主流厂家TSH检测结果的一致性。
1材料与方法
1.1标本来源IFCC第1期20例标本来自Solomon Park Research Laboratories收集的自愿献血者,均为表观健康者,涵盖有代表性的年龄段。严格按照美国临床和实验室标准化协会(CLSI)C37-A程序文件的要求采集血液标本,未进行抗甲状腺球蛋白抗体(Anti-Tg)和抗甲状腺过氧化物酶抗体(Anti-TPO)检测。标本长期冻存,运送过程中温度控制在-20 ℃以下。血清标本TSH浓度根据已完成一致性研究的数个国际性生产厂家分析系统的检测结果确定[4]。C-STFT通过因子分析(FA)模型对厂家检测结果进行统计处理,剔除明显离群值,以模拟数值代替,最终获得各标本的APTM,见表1[5-6]。
1.2方法采用迈瑞公司CL2000i全自动化学发光免疫检测系统及配套TSH试剂盒、校准品和甲状腺功能复合质控品进行C-STFT标本检测。
1.2.1仪器维护与基础性能测试按维护规程对CL2000i检测系统进行维护,并作基础性能测试,确保所有基础性能满足要求。
1.2.2校准与质控仪器装载试剂盒,使用匹配的校准品校准后,检测甲状腺功能复合定值质控品,确定质控品检测结果在(靶值±2s)范围内后检测C-STFT标本。根据实验室内长期质控结果,质控靶值与范围见表2。

表1 C-STFT标本APTM(mIU/L)

表2 TSH质控品靶值和允许偏差(mIU/L)
1.2.3试剂性能评估为满足一致性研究的要求,对CL2000i检测系统TSH试剂盒进行全面的基本性能研究,包括最低检测限、功能灵敏度、线性范围、分析特异性、抗内源性干扰、不精密度及校准一致性等,要求各性能指标符合文献[7]的要求。
1.2.4C-STFT标本检测采用2批试剂和2批校准品随机搭配成3种组合(见表3)进行第1批IFCC标本检测。每批标本检测开始前和结束后检测质控品。每批检测将C-STFT标本按编号顺序检测1次,再逆序检测1次。
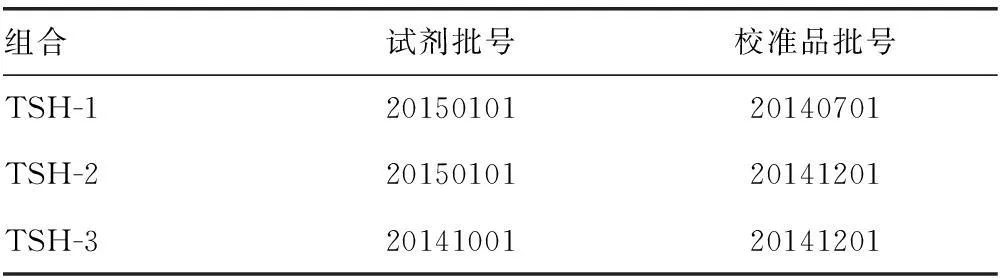
表3 TSH检测试剂和校准品批号组合

表4 标本检测前、后质控品检测结果(mIU/L)
2结果
3种组合在C-STFT标本检测前、后的质控品检测结果均在(靶值±2s)范围内,系统均在控(见表4)。试剂各性能指标均符合要求。方差成分分析结果显示,20个C-STFT标本检测结果批内不精密度为1.95%。采用Passing & Bablok回归分析进行方法学比对,结果显示,采用3种试剂与校准品组合进行C-STFT标本检测,结果间的总偏差范围为0.47%~1.15%,见图1。试剂与校准品3种组合的正向和反向检测结果的偏差分析见图2,偏差在±10%范围内,测试结果稳定,无明显的漂移。3批检测结果均值与APTM存在一定的正偏差。根据APTM反向拟合,修正校准曲线,重新校准检测系统,可使检测结果与APTM具有一致性。重校准后的均值偏差分布见图3。对重校准后的检测结果进行残差分析,仅有1份标本超出+1.96s上限。残差分布分析见图4。重校准后的检测结果相对APTM的平均偏差为2.09%,相关系数大于0.975,Passing & Bablok回归线斜率约为1.0,见图5。

图1 3种试剂与校准品组合检测结果比较

图2 稳定性与漂移分析

图3 重校准后标本检测结果均值与APTM的偏差
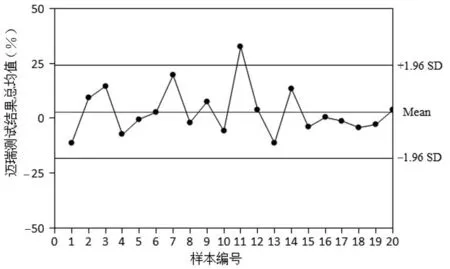
图4 残差分布

图5 Passing & Bablok回归线
3讨论
IFCC下属机构C-STFT希望通过颁布统一的血清盘,采用APTM作为血清盘标定值,同时执行分阶段递进的实验方案,实现TSH检测结果的一致性。迈瑞公司参与C-STFT一致性研究计划的流程包括3个阶段。第一阶段:测试C-STFT第一部分血清盘(健康者标本),上报检测结果后,C-STFT结合参与研究的各厂家系统检测结果,对检测结果可靠性和一致性进行评估。第二阶段:结合第一部分血清盘检测结果,修正主校准曲线,检测C-STFT第二部分血清盘(全范围标本),上报检测结果后,C-STFT结合参与研究的各厂家系统检测结果,对系统修正后的检测结果一致性进行再评估。第三阶段:在第一阶段和第二阶段检测结果通过的情况下,检测第三部分血清盘(患者标本),C-STFT结合参与研究的各厂家系统检测结果,评估TSH测试结果一致性程度,证实概念的可行性。第四阶段,检测C-STFT在北美收集的120例表观正常者标本,对参考范围进行研究。C-STFT如果对各厂家参考范围比对结果满意,有望在2018年实现全球范围TSH检测系统一致性。大分子蛋白质结构的复杂性使检测结果很难实现标准化,而由于生产厂家普遍采用的国际标准品或企业内部标准品往往存在基质效应、分析物差异等问题,使得检测结果的一致性很难达到预期水平。C-STFT推出包含健康者标本和病理标本的全范围真实临床血清盘[8],作为溯源链中的一个等级,解决了标准品的“人造性”;同时采用APTM作为血清盘的定值,既建立了统一的溯源标准,又直接保证了各生产厂家检测系统对临床标本检测结果的可比性。分阶段递进实验方案(Step-Up approach)的贯彻,进一步加强了一致性结果的可靠性[2]。当然,检测结果标准化/一致性实验计划的成功执行,离不开权威机构,如IFCC的支持和推进,也离不开各主要生产厂家的支持与合作。这些都是可供国内相关机构和体外诊断系统生产厂家借鉴的宝贵经验。
目前,迈瑞公司检测系统已顺利通过IFCC首期标本检测结果一致性要求,为进入下一步C-STFT全范围临床标本检测奠定了基础。
参考文献
[1]Thienpont LM,van Houcke SK.Traceability to a common standard for protein measurements by immunoassay for in-vitro diagnostic purposes[J].Clinica Chimica Acta,2010,411(23):2058-2061.
[2]van Uytfanghe K,Linde A,Thienpont LM.A “Step-Up” approach for harmonization[J].Clinica Chimica Acta,2014,432(1):62-67.
[3]Thienpont LM,van Uytfanghe K,van Houcke S.Standardization activities in the field of thyroid function tests:a status report[J].Clin Chem Lab Med,2010,48(11):1577-1583.
[4]Thienpont LM.A progress report of the IFCC committee for standardization of thyroid function tests[J].Eur Thyroid J,2014,16(3):109-116.
[5]Stockl D,van Uytfanghe K,van Aelst S,et al.A statistical basis for harmonization of thyroid stimulating hormone immunoassays using a robust factor analysis model[J].Clin Chem Lab Med,2014,52(8):965-972.
[6]van Houcke SK,Van Aelst S,Van Uytfanghe K,et al.Harmonization of immunoassays to the all-procedure trimmed mean-proof of concept by use of data from the insulin standardization project[J].Clin Chem Lab Med,2013,51(5):103-105.
[7]闫玉峰,张娟,李可,等.IFCC促甲状腺激素(TSH)国际溯源和检测一致性系列研究(一)[J].国际检验医学杂志,2016,37(4):496-497.
[8]Van Houcke SK,Thienpont LM.“Good samples make good assays”-the problem of sourcing clinical samples for a standardization project[J].Clin Chem Lab Med,2013,51(5):967-972.
Serial research of traceability and harmonization of thyroid-stimulating hormone detection approved by IFCC
YuXiang,ChenWenfei#,YuXiaoliu,JiangMing,LiKe,YuZhiguang△
(ShenzhenMindrayBio-MedicalElectronicsCO.,LTD,Shenzhen,Guangdong518057,China)
Abstract:ObjectiveTo implement the harmonization of thyroid-stimulating hormone(TSH) of Mindray assay system by participating in harmonization research program of International Federation of Clinical Chemistry(IFCC)-Standardization of Thyroid Function Tests(C-STFT).MethodsA total of three combinations of TSH reagents and calibrators were used to measure 20 serum samples of healthy human.Within-run precision and batch-to-batch variation were assessed.The concept of harmonization was demonstrated by comparing our test results with All Procedure Trimmed Mean(APTM) provided by IFCC and recalibrating with Mater Calibrators.ResultsThe within-run precision was 1.96%,batch-to-batch variation was 0.47%-1.15%,depending on the level of TSH analyte.There existed a positive bias compared to APTM values.After recalibration with Mater Calibrators and Passing & Bablok regression,the slope of method comparison was 1.0,and correlation coefficient was more than 0.975.ConclusionBy using a panel of real human specimen and recalibration based on APTM,the test results of Mindray assay system could be harmonized with mainstream manufacturers globally.
Key words:thyroid-stimulating hormone;chemiluminescent immunoassay;international federation of clinical chemistry-committee of standardization of thyroid functional tests;all procedure trimed mean
(收稿日期:2015-12-16)
DOI:10.3969/j.issn.1673-4130.2016.06.013
文献标识码:A
文章编号:1673-4130(2016)06-0751-03
#共同第一作者。
·论著·

