沉淀法和NHSG法制备钛酸钡纳米粉体的对比研究
邵志鹏,江伟辉,,冯 果,刘健敏,苗立峰,张 权,吴 倩
(1.景德镇陶瓷学院材料科学与工程学院,江西 景德镇 333403;2.国家日用及建筑陶瓷工程技术研究中心,江西 景德镇 333001)
沉淀法和NHSG法制备钛酸钡纳米粉体的对比研究
邵志鹏1,江伟辉1,2,冯 果2,刘健敏2,苗立峰2,张 权2,吴 倩2
(1.景德镇陶瓷学院材料科学与工程学院,江西 景德镇 333403;2.国家日用及建筑陶瓷工程技术研究中心,江西 景德镇 333001)
摘要:以乙酸钡和钛酸丁酯为原料,分别采用沉淀法和非水解溶胶-凝胶 (NHSG) 法制备钛酸钡纳米粉体,利用DTA-TG,XRD、FT-IR以及TEM等测试手段研究了钛酸钡的物相转变过程,探讨了两种方法不同的微观反应机制。研究结果表明:采用沉淀法,以去离子水和乙醇为复合溶剂,乙酰丙酮为螯合剂,尿素为沉淀剂,能够在750 ℃下制备出钛酸钡纳米粉体,并且红外测试表明沉淀物中有Ti-OH的振动峰位和CO32-的特征峰位;采用NHSG法,以丙三醇为单一溶剂,能够在650 ℃下合成钛酸钡纳米粉体;与沉淀法合成钛酸钡的反应过程不同,NHSG法合成钛酸钡是由于先发生脱酯反应,形成Ba-O-Ti异质键合,然后直接晶化成钛酸钡,这是NHSG法能够低温合成钛酸钡纳米粉体的原因。
关键词:钛酸钡;纳米粉体;沉淀法;非水解溶胶-凝胶法; Ba-O-Ti异质键合
E-mail:jiangweihui@jci.edu.cn
0 引 言
钛酸钡是一种重要的钙钛矿型铁电材料,因具有优良的介电性、压电性、热释电性等电学性能被广泛用于多层陶瓷电容器、热敏电阻、存储器、传感器等各个方面,被称为“电子陶瓷工业的支柱”[1-3]。随着电子元件向微、薄、轻方向的发展,要求多层陶瓷电容器介质层的层数不断增加并且介质层的厚度持续减小,因此对于制备晶粒尺寸小、粒径分布范围窄、分散性好、组份均匀的钛酸钡纳米粉体的需求日益增长。
目前制备钛酸钡粉体的常用方法主要有固相法,水热法,沉淀法,水解溶胶-凝胶法等。固相法制备钛酸钡粉体合成温度高,晶粒大且粒径分布宽,容易引入杂质。水热法需要在高压下进行,对设备要求较高,使得该方法难以推广。水解溶胶-凝胶法工艺复杂,周期长,难以控制其水解速率。而采用沉淀法制备钛酸钡粉体,具有操作简单,制备周期短,设备投资少等优点[4,5],但该法对工艺控制要求高,并且很难获得组分均匀、粒径分布窄的钛酸钡粉体。因此探索钛酸钡粉体新的制备方法具有非常重要的意义。
非水解溶胶-凝胶法不经过水解过程,直接由反应前驱体缩聚为凝胶,简化了工艺过程,避免了以水为溶剂而引发的团聚,更重要的是在溶胶-凝胶过程中易于实现原子级均匀混合,可大大降低氧化物的合成温度,在钛酸钡及掺杂钛酸钡纳米粉体的制备方面有广阔的应用前景。目前国内外采用NHSG法制备钛酸钡粉体的报道极少。
本文分别采用沉淀法和非水解溶胶-凝胶法制备钛酸钡纳米粉体,对比研究了两种方法不同的物相转变过程,探讨了沉淀法和非水解溶胶-凝胶法制备钛酸钡纳米粉体的微观反应机制。
1 实 验
1.1试样制备
1.1.1 沉淀法制备钛酸钡纳米粉体
将0.025 mol乙酸钡(A.R.)和0.1 mol尿素(A.R.)加入到装有12.5 ml去离子水的锥形瓶中,放置在磁力搅拌器上搅拌;用移液管量取0.025 mol的钛酸丁酯(C.P.),将其迅速移入锥形瓶中并加入50 ml乙醇(A.R.)和0.025 mol乙酰丙酮(A.R.),放置在恒温磁力搅拌器上搅拌;将乙酸钡溶液缓慢地加入到钛酸丁酯的乙醇溶液中,继续在恒温磁力搅拌器上搅拌15 min,得到混合液;将装有混合液的锥形瓶放置在110 ℃数显恒温油浴槽中回流8 h,得到乳白色沉淀,经过滤、洗涤、干燥,以及不同热处理温度下煅烧5 h,最后研磨得到钛酸钡纳米粉体。
1.1.2 非水解溶胶-凝胶法制备钛酸钡纳米粉体
将0.025 mol乙酸钡加入到装有100 ml丙三醇(A.R.)的锥形瓶中,放置在磁力搅拌器上190 ℃加热搅拌;用移液管量取0.025 mol的钛酸丁酯,将其迅速移入锥形瓶中并加入25 ml丙三醇,放置在恒温磁力搅拌器上搅拌10 min;将适量的钛酸丁酯溶液加入到钡源溶液中,继续在恒温磁力搅拌器上搅拌15 min,得到前驱体混合液;将装有前驱体混合液的锥形瓶放置110 ℃数显恒温油浴槽中回流24 h,并将得到的前驱体放置在加热套中蒸馏得到干凝胶粉。将干凝胶粉在不同温度下煅烧5 h,最后研磨得到钛酸钡纳米粉体。
1.2样品表征
利用德国NETZSCH公司生产STA 499C型综合热分析仪对干凝胶进行热分析(TG/DTA);采用德国Bruker AXS公司生产D8 Advance X-ray衍射分析仪(Cu-Kα辐射,λ= 0.154 nm)对各工艺条件下制备的样品进行物相分析测试,以确定所制备产物的晶相组成;采用日本电子生产JEM-2010型透射电子显微镜观察产物的尺寸及微观形貌;采用Nicolet5700型傅立叶变换红外光谱仪研究钛酸钡粉体制备过程中样品的键合变化,测量的波数范围为4000-400 cm-1。
2 分析与讨论
图1给出了沉淀法制备钛酸钡沉淀物的DTATG曲线和经不同温度煅烧得到粉体的XRD图谱。
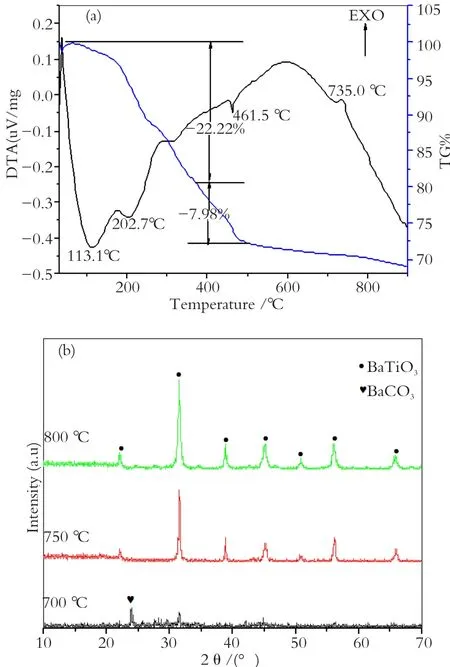
图1 沉淀法制备钛酸钡沉淀物的TG-DTA曲线(a)和经不同煅烧温度所得粉体的XRD图谱(b)Fig.1 DTA-TG curves of BT precipitates prepared via precipitation method (a) and XRD patterns of their nanopowders calcined at different temperatures (b)
从图1(a)可以看出:DTA曲线分别在113.1 ℃、202.7 ℃和461.5 ℃附近出现三个明显的吸热峰,这是由去离子水或部分有机溶剂蒸发、有机物的挥发或有机配位体的分解所引起[6]。此外在735.0 ℃附近有一个明显的放热峰,为探明该放热峰形成的原因,将沉淀物经700 ℃、750 ℃和800 ℃热处理,然后进行XRD分析,结果见图1(b)。
由图1(b)可知:700 ℃所得样品的主晶相是BaCO3,同时还包含1个极其微弱的BaTiO3晶相衍射峰。而在750 ℃时,样品全部由BaTiO3晶相组成,未见BaCO3以及其它晶相衍射峰。继续提高煅烧温度,BaTiO3的衍射峰有所增强,表明BaTiO3的晶体发育程度进一步提高。由此可以推断,DTA曲线中735.0 ℃处的放热峰是由于钛酸钡晶相的形成所致。
图2给出了750 ℃和800 ℃热处理所得样品的TEM照片。从图2可以看出:当煅烧温度为750 ℃时,钛酸钡粉体呈无规则形状,粒径分布宽,颗粒大小在20-80 nm之间,粉体间团聚比较明显;煅烧温度为800 ℃时,钛酸钡粉体仍然呈现无规则形状,颗粒尺寸明显增大,并且团聚程度有所加强。图3给出了NHSG法制备钛酸钡干凝胶粉的DTATG曲线和经不同温度煅烧得到粉体的XRD图谱。
从图3(a)可以看出:钛酸钡干凝胶的DTA曲线从室温至200 ℃范围分别在113.4 ℃和176.9 ℃处出现两个吸热峰,TG曲线上相应温度范围内的失重率为15.17%,这是有机溶剂的蒸发所引起[6]。同时样品在378.4 ℃以及629.3 ℃处出现两个放热峰,其中378.4 ℃处较强的放热峰是有机配位体的分解所致[7]。为探明629.3 ℃处放热峰形成的原因,将干凝胶经过600 ℃、650 ℃和700 ℃热处理,然后进行XRD分析,结果见图3(b)。
由图3(b)可知,煅烧温度为600 ℃时,未检测出晶相衍射峰,说明样品为无定形相组成。当温度提高到650 ℃时,样品由单一的钛酸钡晶相组成。继续提高煅烧温度到700 ℃,钛酸钡的晶相衍射峰有所增强,说明钛酸钡的晶相发育更好。由此可以推断,DTA曲线629.3 ℃处的放热峰是由于钛酸钡晶相的形成所致。

图2 沉淀法制得钛酸钡粉体的TEM照片Fig.2 TEM photographs of BT powders prepared via precipitation method

图3 NHSG法制备钛酸钡干凝胶粉的TG-DTA曲线(a)和经不同煅烧温度所得粉体的XRD图谱(b)Fig.3 DTA-TG curves of BT xerogels prepared via NHSG method (a) and XRD patterns of their nanopowders calcined at different temperatures (b)
图4给出了650 ℃和700 ℃热处理所得样品的TEM照片。从图4可以看出:650 ℃热处理所得钛酸钡粉体粒径分布较窄,颗粒大小在15-25 nm之间,粉体存在轻微的团聚现象;热处理温度上升到700 ℃时,钛酸钡粉体轮廓较清晰,大部分为近球形结构,颗粒大小在25-50 nm之间,虽然粒径有所增大,但粉体的团聚程度没有明显变化。
通过以上的分析结果可以看出:采用沉淀法制备钛酸钡粉体的最低合成温度为750 ℃;而采用NHSG法制备钛酸钡粉体的最低合成温度为650 ℃。
为探究NHSG法能够低温合成钛酸钡粉体的原因,图5分别给出沉淀法和NHSG法制备钛酸钡沉淀物与干凝胶粉的红外图谱。


采用非水解溶胶-凝胶法制备钛酸钡粉体时,峰位1338.7 cm-1对应于-CH3变形振动或反对称形变,而峰位1050.3 cm-1和1018.8 cm-1对应于Ti-O键合[11]。值得注意的是:红外图谱在1414.9 cm-1处的特征峰对应于Ba-O-Ti异质键合[12],说明前驱体之间发生了异质缩聚反应。

图4 NHSG法制得钛酸钡粉体的TEM照片Fig.4 TEM photographs of BT powders prepared via NHSG method

图6 蒸馏产物的红外图谱Fig.6 Infrared spectrum of distilled liquid
为了进一步探明NHSG法制备钛酸钡的反应机理,图6给出了在该工艺条件下蒸馏产物的红外图谱。由红外图谱可以看出,1717.8 cm-1处振动峰对应于C=O双键[11],1250.0 cm-1峰位对应于C-O-C键合[13],说明产物中有酯的存在。结合图5测出NHSG法所得干凝胶包含Ba-O-Ti异质键合的结果,可以证明乙酸钡和钛酸丁酯之间发生了非水解脱酯反应。
非水解溶胶-凝胶法低温合成钛酸钡的关键是通过脱酯反应形成了Ba-O-Ti异质键合,其反应方程式如下:
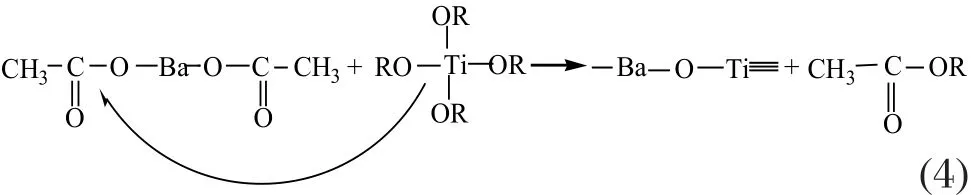
由于钛酸丁酯中的钛是六配位的,但它的价键是4,所以乙酸钡中的乙酸根离子很容易和钛配位,而钛酸丁酯中的-OR基团攻击Ba(C1H3C2OO)2中的C2,导致脱酯反应的进行,从而形成Ba-O-Ti键合(见公式4)。
3 结 论
(1)沉淀法制备钛酸钡纳米粉体的最低合成温度为750 ℃,钛酸钡粉体呈无规则形状,粒径分布宽,颗粒大小在20-80 nm之间,粉体间团聚比较明显。煅烧温度为800 ℃时,钛酸钡粉体仍然呈现无规则形状,颗粒尺寸明显增大,并且团聚程度有所加强。
(2)NHSG法制备钛酸钡纳米粉体的最低合成温度为650 ℃,所得钛酸钡粉体粒径分布较窄,颗粒大小在15-25 nm之间;热处理温度上升到700 ℃时,钛酸钡粉体大部分为近球形结构,颗粒大小在25-50 nm之间,粒径有所增大,但粉体的团聚程度没有明显变化。
(3)沉淀法合成钛酸钡首先形成中间产物碳酸钡和氢氧化钛,再经热处理转变而成;NHSG法合成钛酸钡是由于溶胶-凝胶转变阶段首先通过脱酯反应形成了Ba-O-Ti异质键合,然后直接晶化形成钛酸钡晶相;NHSG法有助于Ba和Ti原子级的均匀混合,是低温合成钛酸钡纳米粉体的原因。
参考文献:
[1]陈杰,闫峰,罗昆鹏.微波水热合成钛酸钡纳米粉体[J].人工晶体学报,2013,42(11):2359-2363.CHENG Jie,et al.Journal of Synthetic Crystals,2013,42 (11):2359-2363.
[2]翟学良.水热法制备四方相钛酸钡及其晶相转化机理[J].硅酸盐学报,2000,28(4):357-360.ZHAI Xueliang,et al.Journal of the Chinese Ceramic Society,2000,28(4):357-360.
[3]张效华,辛凤,胡跃辉.几种电子陶瓷材料的研究进展与应用前景[J].陶瓷学报,2013,34(2):219-223.ZHANG Xiaohua,et al.Journal of Ceramics,2013,34(2):219-223.
[4 LEE B W,CHOI G S.Hydrothermal synthesis of barium titanate powders from a co-precipitated precursor[J].Journal of Ceramic Processing Research,2003,3(4):151-154.
[5]白改玲,芶立,冉均国.均相法和共沉淀法制备Nd:YAG透明陶瓷的对比研究[J].陶瓷学报,2015,36(1):14-18.BAI Gailing,et al.Journal of Ceramics,2015,36(1):14-18.
[6]苏毅,杨亚玲,胡亮.溶胶-凝胶法制备钛酸钡超细粉体的研究[J].化学研究与应用,2002,14(2):201-204.SU Yi,et al.Chemical Research and Application,2002,14(2):201-204.
[7]FU C L,LIAO H,CAI W.Effect of calcination temperature on the microstructures of barium titanate hafnate nanopowders prepared by the sol-gel process[J].Intergrated Ferroelectrics,2012,139(1):20-25.
[8]刘黎明,林志东 张万荣.RuO2包覆的TiO2纳米复合粒子的表面与界面分析[J].表面技术,2006,35(2):27-29.LU Liming,et al.Surface Technology,2006,35(2):27-29.
[9]SHAO L M,ZHANG L N,CHEN M H.Reactions of titanium oxides with water molecules.A matrix isolation FT-IR and density functional study[J].Chemical Physics Letters,2001,343(1):178-184.
[10]吴东辉,施新宇,张海军.草酸盐共沉淀法制备钛酸钡粉体研究[J].压电与声光,2009,34(4):42-46.WU Donghui,et al.Piezoelectrics and Acoustooptics,2009,34(4):42-46.
[11]陈志雄,周方桥,潘祥生.BaTiO3凝胶合成的红外吸收光谱研究[J].无机材料学报,1992,7(2):168-174.CHENG Zhixiong,et al.Journal of Inorganic Materials,1992,7(2):168-174.
[12]KAMALASANAN M N,KUMAR N D,CHANDRA S.Structural and microstructural evolution of BaTiO3thin films deposited by the sol-gel process[J].Journal of Applied Physics,1994,76(8):4603-4609.
[13]BRUN N,GARCIA-GONZALEZ C A,SMIRNOVA I.Hydrothermal synthesis of highly porous carbon monoliths from carbohydrates and phloroglucinol[J].RSC Advances,2013,3(38):17088-17096.
Comparative Study on the Preparation of BatiO3Nano Powder via Precipitation Method and NHSG Method
SHAO Zhipeng1,JIANG Weihui1,2,FENG Guo2,LIU Jianmin2,MIAO Lifeng2,ZHANG Quan2,WU Qian2
(1.School of Material Science and Engineering,Jingdezhen Ceramic Institute,Jingdezhen 333403,Jiangxi,China; 2.National Engineering Research Center for Domestic and Building Ceramics,Jingdezhen 333001,Jiangxi,China)
Abstract:BaTiO3(BT) nano powders were prepared via precipitation method and non-hydrolytic sol-gel (NHSG) method by using barium acetate and titanium tetrabutoxide as precursors,respectively.The process of BT phase transformation and the reaction mechanism of these two methods were researched by DTA-TG,XRD,FTIR,TEM,etc.The results show that BT nanopowder can be synthesized at 750 ℃ via precipitation method using deionized water and ethonal as complex solvent,acetylacetone as chelating agent,and urea as precipitant; it can also be synthesized at 650 ℃ via NHSG method using glycerol as solvent; FT-IR indicates that the synthesis mechanism of NHSG method for BT nanopowders is different from that of precipitation method,the Ti-OH and CO32-characteristic peaks were presented via precipitation method,while the Ba-O-Ti heterogeneous bond was formed in the de-esterification of polycondensates via NHSG method,and then the xerogel was turned into the BT nanocrystalline directly after calcination.Therefore,the BT nanopowders were obtained at low temperature.Key words:barium titanate; nano powder; precipitation method; non-hydrolytic sol-gel method; Ba-O-Ti heterogeneous bond
基金项目:国家自然科学基金项目(51162013,51362014)。
收稿日期:2015-05-22。
修订日期:2015-09-20。
DOI:10.13957/j.cnki.tcxb.2016.01.009
中图分类号:TQ174.75
文献标志码:A
文章编号:1000-2278(2016)01-0044-05
通信联系人:江伟辉(1965-),男,博士,教授。
Received date:2015-05-22.Revised date:2015-09-20.
Correspondent author:JIANG Weihui(1965-),male,Doc.,Professor.

