SCR脱硝过程中硫酸氢铵形成特性实验研究
马双忱, 邓 悦, 吴文龙, 张立男, 马京香, 张小霓
(1.华北电力大学 环境科学与工程学院,河北保定 071003;
2.国网河南省电力公司电力科学研究院,郑州 450052)
SCR脱硝过程中硫酸氢铵形成特性实验研究
马双忱1,邓悦1,吴文龙2,张立男1,马京香1,张小霓2
(1.华北电力大学 环境科学与工程学院,河北保定 071003;
2.国网河南省电力公司电力科学研究院,郑州 450052)
摘要:在自主设计的实验台上开展硫酸氢铵(ABS)形成特性实验,研究了温度和反应物体积分数对ABS形成机理的影响,通过热重分析实验得到ABS的挥发温度,并计算ABS分解反应的吉布斯自由能,从而得到ABS的热力学分解温度.结果表明:ABS的形成是温度和反应物体积分数的函数,其形成温度在220~261 ℃;φ(NH3)与φ(H2SO4)乘积越大,ABS的形成温度越高;H2SO4过量且体积分数一定的情况下,φ(NH3)越大,ABS沉积量越大;相反,若φ(NH3)一定,φ(H2SO4)对ABS沉积量的影响不大;热重分析实验显示,ABS的挥发温度为173.7 ℃,热力学分解温度为447.18 ℃.
关键词:ABS; 形成机理; 热力学; 温度; 实验研究
NOx是燃煤电厂的主要烟气污染物之一.1959年,美国Eegelhard公司最早申请了选择性催化还原法(SCR)烟气脱硝发明专利.1972年,日本正式研发出SCR技术,并于1978年实现工业化应用.20世纪80年代和90年代以后,SCR技术在欧洲和美国相继投入工业应用[1-3].经过多年的发展和完善,脱硝催化剂的活性、选择性、抗毒性和耐硫性有了很大提升,SCR工艺也得到了优化和改进,脱硝性能更加高效.商业SCR催化剂中V2O5质量分数通常在0.5%~4%.由于在烟气脱硝过程中,V2O5催化剂在催化还原NOx的同时,也使烟气中部分SO2氧化成SO3,进而在一定的反应条件下与SCR脱硝过程中未完全反应的氨生成硫酸氢铵(ABS),ABS在催化剂表面及SCR反应器的下游设备和管道上沉积,从而引起堵塞、腐蚀和阻力上升等问题[4-6].
在SCR脱硝过程中,ABS的产生是不可避免的,空气预热器常规设计中冷段及中温段下方区域温度范围大致为120~230 ℃.而ABS的沸点为350 ℃,熔点为147 ℃.所以在此温度范围内,ABS正好处于凝固的过程.处于液相区的ABS黏性极强,会迅速黏附于换热元件表面,吸附大量烟气中的飞灰,最终导致大量的飞灰沉积于金属壁面或卡在层间,使得空气预热器烟气侧流通截面积减少,导致其堵塞,进而造成空气预热器运行阻力增加[7-8].
ABS的形成会造成严重危害,电力企业不得不寻求解决办法来应对.目前电厂采用的主要方法是采取一系列的清洗方式,更换已经腐蚀、堵塞的设备.这不仅花费大、效率低,也带来了一系列的环境问题.排放到大气中的ABS是一种有害的酸性物质,也是雾霾的前体物.马双忱等[9-10]曾发表了2篇关于ABS形成的论文,引起有关学者和技术人员的关注.但由于ABS形成研究方面的困难,目前尚缺乏关于ABS形成机理的探讨,对影响ABS形成的因素也缺乏详细认识.特别是当前对NOx控制更加严厉,SCR经常在低负荷条件下运行,而SCR的最低运行温度取决于ABS的露点.因此,了解ABS的形成规律及其露点就变得非常重要.笔者通过在自主设计的实验台上开展ABS形成实验,研究温度和反应物体积分数对ABS形成机理的影响.
1ABS的形成机理
ABS在常温下为无色结晶,易潮解,易溶于水,几乎不溶于乙醇、丙酮和吡啶,其水溶液呈强酸性,密度为1.79 g/mL.这种很少见的铵盐却在SCR脱硝过程中产生了诸多问题.
1978年,Saleem等[11]的研究表明铵盐的形成取决于温度和反应物体积分数,此研究成果经常被引用.1980年,Radian公司通过理论热力学分析提出了硫酸铵(AS)和ABS同时在空气预热器中形成[12].这个结论通过Burke等[13]的研究得以验证,其用实验的方法测试了二者的比热容、生成热、反应熵和焓.从Radian公司的报告中可以看出,实际上AS是热力学优先产物[12].然而,动力学分析却表明ABS会优先形成,这是因为其反应速率更快.
1.1ABS形成热力学
理论上讲,当n(NH3)/n(SO3)大于2时,只生成AS;当n(NH3)/n(SO3)小于1时,只生成ABS;当n(NH3)/n(SO3)介于1和2之间时,会生成ABS和AS的混合物,反应方程式如下:
(1)
(2)
目前,国内SCR脱硝工艺中氨逃逸量不超过2×10-6~3×10-6,电厂烟气中SO3体积分数一般在10×10-6左右,n(NH3)/n(SO3)小于1,因此不利于生成AS.到目前为止,有关ABS形成的2种反应机理仍存在争议[14].
第一种理论认为:ABS形成的第一步是在高温(315 ℃)热空气中SO3与H2O的反应(式(3)),其中反应的焓变ΔHθ=-105 kJ/mol,吉布斯自由能ΔGθ=-10 kJ/mol;第二步是基于硫酸气溶胶的反应(式(4)),其中ΔHθ=-222 kJ/mol,ΔGθ=-50 kJ/mol,ΔGθ所取温度为近似烟道温度(260 ℃).
(3)
(4)
式(3)的化学反应平衡常数K可表示为:
K=φ(H2SO4)/[φ(SO3)·φ(H2O)]
(5)
在温度分别为350 ℃、300 ℃和250 ℃时,K分别为3.57、18.6和138.取烟气中的水蒸气体积分数为12%,计算可得H2SO4与SO3的体积分数之比分别为0.43、2.2和16.6.即在250 ℃时H2SO4蒸气的体积分数是SO3体积分数的16.6倍.此外,式(3)和式(4)的吉布斯自由能均为负,反应可自发进行.因此,从热力学角度可认为式(4)是生成ABS的主要途径.
第二种理论认为:逃逸的氨与SO3和H2O(300 ℃)直接反应生成液态ABS.
(6)
其中,ΔHθ=-311 kJ/mol,ΔGθ=-61.4 kJ/mol.
对于ABS形成的形态也存在2种理论[15]:一种认为ABS以气溶胶的形式在烟气中形成,然后沉积在设备表面;另一种认为ABS直接在管壁表面形成并沉积,沉积现象与晶体颗粒形成、长大的动力学机理有关[16].文献[15]的实验结果与前者一致,认为ABS以一种气溶胶的形式形成并沉积在管道表面,且出现在一个大温度梯度区域.ABS最初形成的区域和最大程度形成区域不同,在形成方式上前者是薄雾,后者是浓密的云.ABS雾在低温度梯度区域更浓密,其在管壁冷凝区密度随温度梯度的变化如图1所示.

图1 管壁处ABS密度随温度梯度冷凝区的分布[12]
Fig.1Variation of ABS concentration distribution with temperature gradient in condensation area of tube wall
1.2ABS形成动力学
近些年,许多学者对ABS的形成动力学进行了研究[17-19].从动力学角度来讲,ABS形成的速率要比AS形成的速率快得多[20].1982年,Radian公司建立了空气预热器ABS生成的动力学方程[12],用Radian数来表示空气预热器中ABS生成反应速率.Radian数越大,表示ABS生成反应速率越快.
(7)
(8)
式中:TIFT为ABS形成的初始温度,℃,对于中低硫煤电厂,TIFT为200~220 ℃,高硫煤电厂TIFT要高一些;Tcold为空气预热器冷端综合温度,℃;Texit为烟气离开空气预热器时的温度,℃;Trep为出口烟气平均温度,℃;高硫煤(w(S)约为3.0%) 、中硫煤(w(S)约为1.7%)、低硫煤电厂中烟气的φ(SO3)分别约为50×10-6、28×10-6和12×10-6.
式(7)定性地说明了ABS的形成与温度和反应物体积分数呈正相关,利用这些易于测量的参数提供机组可预见的空气预热器堵塞情况.对SCR和选择性非催化还原法(SNCR)来说,沉积物形成量不足以造成空气预热器堵塞时所对应的Radian数在5 000~7 000[12],这样利用Radian数可大致估计允许的氨逃逸量.
在实际运行中也发现,ABS的形成取决于反应物体积分数、反应物比例以及温度.ABS的确切形成区域取决于初始形成温度和空气预热器冷端综合温度,并在空气预热器轴向上下波动.大约有30%的ABS会在空气预热器中沉积,其余部分会以气溶胶形态随烟气离开,ABS的沉积受空气预热器冷端限制,很少会在其中间层沉积.
2实验系统与方法
2.1ABS形成实验
在如图2所示的自主设计的实验装置上开展ABS形成实验.模拟烟气包含北方特种气体有限公司配制的NH3、N2和雾化的H2SO4酸雾.其中NH3体积分数为500×10-6和30×10-6,N2作为载气.H2SO4酸雾是先将浓硫酸稀释至所需浓度再采用广州浩奇电器有限公司生产的浩奇HQ-2008A6工业静音喷雾器进行超声波雾化,雾化原理类似加湿器.
采用杭州卓驰仪器有限公司生产的SK3-2-10-4节能程控管式炉对石英管反应器的前部进行加热.石英管尾部(距入口60 cm处之后)为ABS的冷凝区,不进行加热.将模拟烟气喷入石英管反应器,石英管中放置10个热电偶,每个热电偶间距为10 cm,透过石英管可观察模拟烟气的密度变化及分布,确定ABS形成的反应温度.

2.2ABS分解反应的热重分析实验
取A-R级试剂NH4HSO4,100 ℃下恒温干燥3 h后研碎,过筛(80 μm).取NH4HSO4试样10 mg左右,放入直径为 5 mm、高为25 mm的铝坩埚,采用Pyris Diamond TG热重分析仪对ABS进行热重分析实验,以5 K/min的升温速率进行测定,N2体积流量为20 mL/min,用计算机进行分析得出ABS分解的热重分析(TG)曲线和TG的一次微分(DTG)曲线.
3结果与分析
3.1ABS的形成温度与NH3和H2SO4体积分数之间的关系由于ABS的形成取决于反应物的体积分数和温度,因此,研究ABS的形成温度与NH3和H2SO4的体积分数之间的关系有利于进一步了解ABS的形成过程.
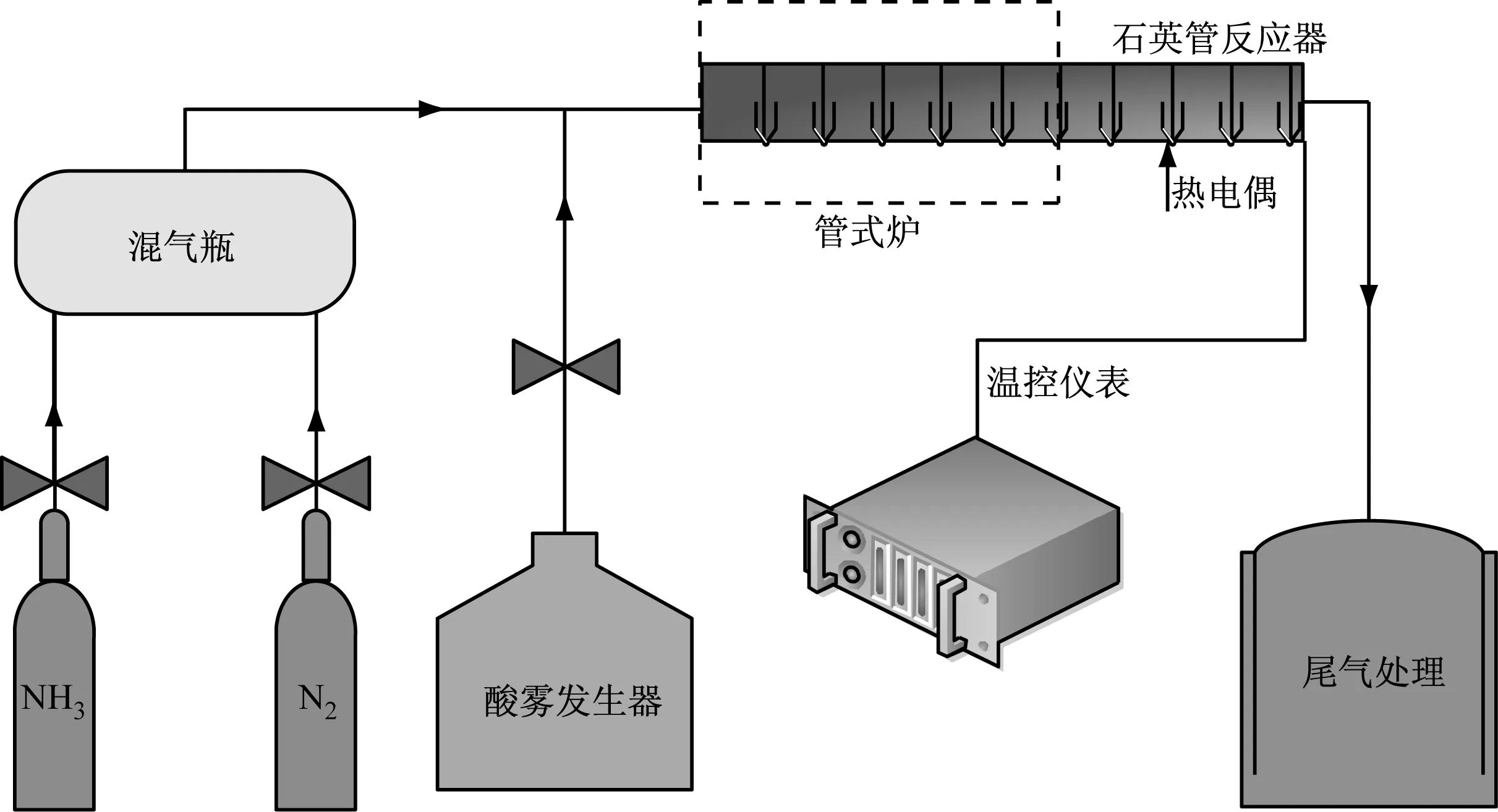
图2 ABS生成实验图
图3和图4分别为φ(NH3)=2×10-6、φ(H2SO4)=15×10-6和φ(NH3)=15×10-6、φ(H2SO4)=50×10-6时ABS的形成温度曲线,其中横坐标表示各热电偶与反应区入口的距离.由于管式炉只加热石英管的前半部分,后半部分作为ABS冷凝区不进行加热,因此,随着距离的增加形成温度逐渐下降.
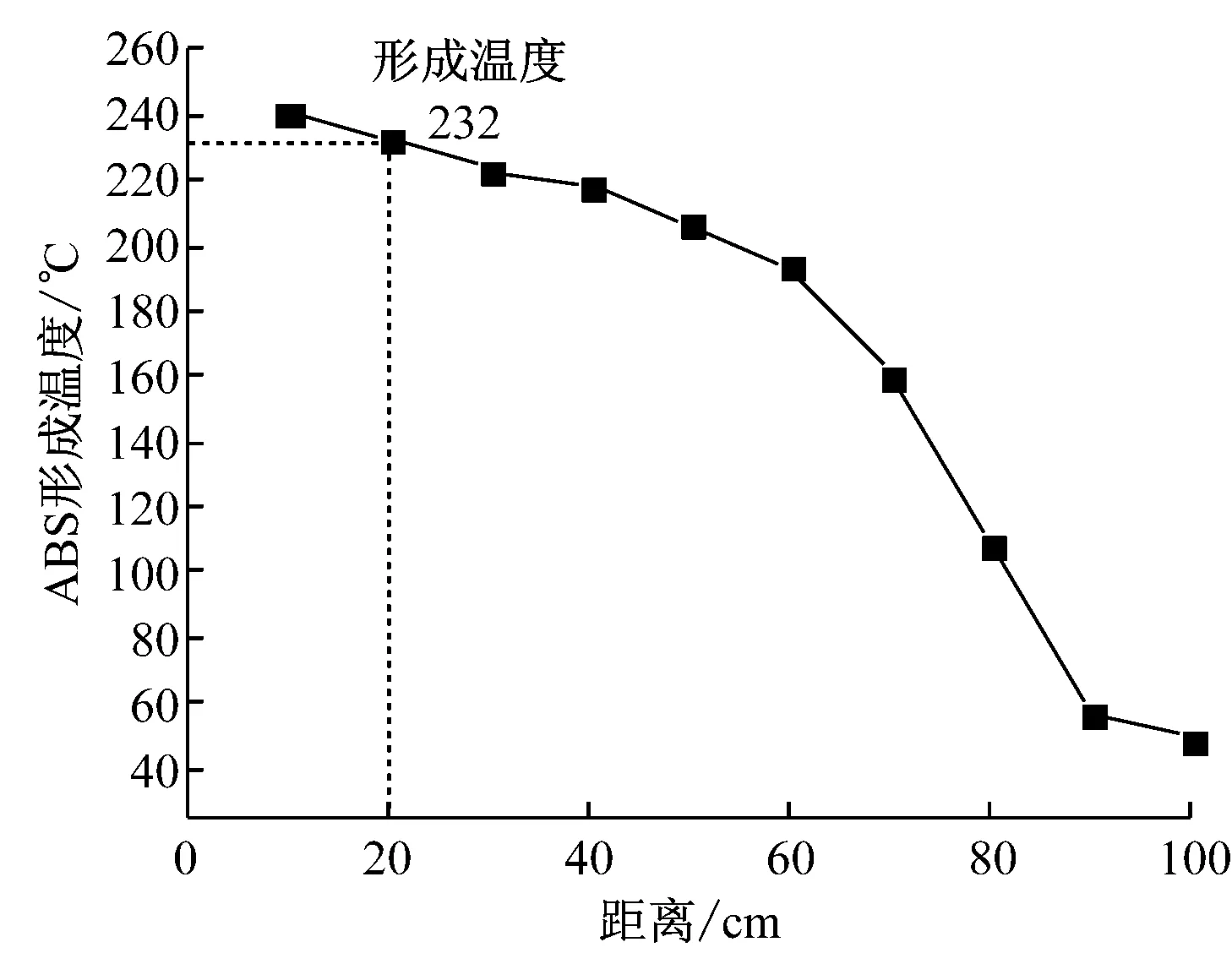
图3 φ(NH3)=2×10-6,φ(H2SO4)=15×10-6时
Fig.3ABS formation temperature forφ(NH3)=2×10-6and
φ(H2SO4)=15×10-6

图4φ(NH3)=15×10-6,φ(H2SO4)=50×10-6时ABS的形成温度
Fig.4ABS formation temperature forφ(NH3)=15×10-6and
φ(H2SO4)=50×10-6
由图3可知,在φ(NH3)=2×10-6,φ(H2SO4)=15×10-6,且反应区入口温度为240 ℃时,在距离反应区入口20 cm处可观察到ABS的形成,此位置ABS的形成温度为232 ℃.同样地,由图4可知,在φ(NH3)=15×10-6,φ(H2SO4)=50×10-6时,ABS的形成温度为261 ℃.
图5为NH3和H2SO4体积分数对ABS形成温度的影响.其中所选的NH3和H2SO4体积分数为尽可能贴近燃煤电厂的实际工况,且保证二者的物质的量之比小于1,从而保证生成物为ABS而非AS.由此得到的ABS形成温度可能存在微小误差,这是由于随着时间的增加,高温下密封胶会融化,进而导致有微量气体泄漏而影响实验结果.由图5可知,ABS形成温度在220~261 ℃内,且ABS形成温度随着反应物体积分数的增大而升高.

图5 NH3和H2SO4体积分数对ABS形成温度的影响
Fig.5Effects of NH3and H2SO4concentration on ABS formation temperature
图6给出了ABS形成温度与反应物体积分数乘积的关系.由图6可知,ABS的形成是温度和反应物体积分数的函数,具体形成温度与NH3和H2SO4的体积分数有关,且二者体积分数乘积越大,ABS的形成温度越高.

图6 ABS形成温度与反应物体积分数乘积的关系
通过实验得到的ABS照片如图7所示,其中从左图可以明显看出,沉积在石英管壁上的黏稠状液体,这是在φ(NH3)=15×10-6,φ(H2SO4)=50×10-6时所生成的ABS,右图是为了能清晰地分辨出产物,在石英管内部塞入耐高温石英棉的实验图示.
3.2NH3体积分数对ABS沉积量的影响
在SCR反应过程中,为提高脱硝效率通常会向反应器中喷入过量的NH3,n(NH3)/n(NOx)的增大有助于脱硝效率的提升.此外,NH3在催化剂层分布不均以及实际运行过程中诸多因素导致催化剂性能下降时,都会造成反应器内的NH3过剩,这部分未与NOx反应的NH3会随烟气进入反应器后部烟道和空气预热器,形成NH3逃逸.逃逸的NH3可与SO3和水蒸气反应形成ABS,进而腐蚀空气预热器冷端换热元件和下游设备.NH3作为ABS产生的主要反应物,其体积分数也成为ABS生成量的关键控制因素.


图7 ABS实验生成形态

为了降低NH3体积分数对ABS沉积量的影响,在电厂生产实际中,可优化SCR反应器设计,保证NH3分布的均匀性.另外,合理布置烟道导流板、保证喷氨格栅每个喷嘴流速的均匀性,能在一定程度上降低氨逃逸率.

图8 NH3体积分数对ABS沉积量的影响
3.3H2SO4体积分数对ABS沉积量的影响


图9 H2SO4体积分数对ABS沉积量的影响
3.4ABS挥发温度
温度是影响ABS形态的最主要因素,如果采用高温烟气干预空气预热器,使沉积的ABS挥发,ABS的相态发生变化,可物质本性并未发生改变,ABS沿着热力流程会进入后续静电除尘器、脱硫风机及脱硫塔中.因此,研究ABS的挥发温度有助于揭示ABS挥发后对后续设备的影响.
图10为ABS分解的热重分析曲线.由图10可知,随着温度的升高,ABS逐渐失重,从A点开始质量分数逐渐降低,挥发为气体,此时所对应的温度为173.7 ℃.从A点到B点质量分数从99.982%缓慢下降到90.711%,失重并不明显,而从B点开始失重加快,此时对应温度为323.59 ℃,到C点(DTG曲线所对应的C′点为峰值,说明此时达到最大分解温度)达到最低,此时温度为412.49 ℃,而后几乎稳定不变.因此,认为ABS的挥发温度为173.7 ℃,但此时挥发得相当缓慢,再加上电厂实际工况的复杂多变性,实际ABS的挥发温度高于173.7 ℃,ABS也不一定会立即变为气态,只有当温度高于323.59 ℃时,ABS才会大量挥发.

图10 ABS分解的热重分析曲线
3.5ABS热力学分解温度

(9)

736.098T-1-0.203T+318.888
(10)


图11 ABS分解反应的吉布斯自由能与温度T的关系
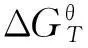

(11)
根据热力学第二定律,一个化学反应的吉布斯自由能变化可表示为:
(12)
对比式(11)可得,该分解反应中ΔHθ=311.066 7,ΔSθ=0.431 84,则
(13)
由式(13)可知,ΔGθ=0时,T=720.33 K,如图11中B点,即当T>720.33 K时,ΔGθ<0.也就是说温度超过720.33 K后,ΔGθ从0变为负值,分解反应可以自发进行.由此可得ABS的热力学分解温度为447.18 ℃.但ABS的真实分解温度仍然受反应动力学的限制,与反应物的体积分数和温度等因素有关.
4结论
(1) ABS的形成是温度和反应物体积分数的函数.ABS的形成温度在220~261 ℃内,且ABS形成温度随着反应物体积分数的增大而升高.具体形成温度与NH3和H2SO4的体积分数有关,且二者体积分数乘积越大,ABS的形成温度越高.
(2) H2SO4过量且体积分数一定的情况下,NH3体积分数越大,ABS沉积量越大.相反如果NH3体积分数一定,H2SO4体积分数对ABS沉积量的影响不大.为了降低NH3体积分数从而减少ABS沉积量,在电厂生产实际中,可优化SCR反应器设计,保证NH3分布均匀性,合理布置烟道导流板、保证喷氨格栅每个喷嘴流速的均匀性.
(3) 热重分析实验得出,ABS的挥发温度为173.7 ℃.通过计算NH4HSO4分解反应的吉布斯自由能,得到ABS的热力学分解温度为447.18 ℃.
参考文献:
[1]李德波,廖永进,徐齐胜,等.我国SCR脱硝催化剂服役过程中运行规律的研究[J].动力工程学报,2014,34(10): 808-813.
LI Debo, LIAO Yongjin, XU Qisheng,etal. Experimental study on running condition of the catalyst in a domestic SCR denitrication system[J].Journal of Chinese Society of Power Engineering,2014,34(10):808-813.
[2]陈晓露,赵钦新,鲍颖群,等.SO3脱除技术实验研究[J].动力工程学报,2014,34(12): 966-971.
CHEN Xiaolu, ZHAO Qinxin, BAO Yingqun,etal. Experimental research on SO3removal[J].Journal of Chinese Society of Power Engineering,2014,34(12): 966-971.
[3]YANG Yang. NOxemissions reduction technology and the flue gas denitration engineering[M].Beijing: Metallurgical Industry Press, 2007.
[4]钟礼金,宋玉宝.锅炉SCR烟气脱硝空气预热器堵塞原因及其解决措施[J].热力发电,2012,41(8): 45-47.
ZHONG Lijin, SONG Yubao. Air preheater blocking in boiler with SCR denitrification device: reason analysis and solutions[J].Thermal Power Generation,2012,41(8):45-47.
[5]LIU Kewei,CHEN Tianlang. Studies on the thermal decomposition of ammonium sulfate[J].Chemical Research and Application,2002,14(6):737-738.
[6]范芸珠,曹发海.硫酸铵热分解反应动力学研究[J].高校化学工程学报,2011,25(2):341-346.
FAN Yunzhu,CAO Fahai. Thermal decomposition kinetics of ammonium sulfate[J].Journal of Chemical Engineering of Chinese Universities,2011,25(2):341-346.
[7]梁登科.脱硝过程伴生硫酸氢铵对于烟气灰颗粒性质影响的实验研究[D].济南:山东大学,2014.
[8]王鑫,陈城,李富宝,等.SCR脱硝工艺空气预热器堵塞对策分析[J].吉林电力,2012,40(6):43-45.
WANG Xin, CHEN Cheng, LI Fubao,etal. Counter-measurement analysis on SCR denitration process caused air pre-heater blocking[J].Jilin Electric Power,2012,40(6):43-45.
[9]马双忱,金鑫,孙云雪,等.SCR烟气脱硝过程硫酸氢铵的生成机理与控制[J].热力发电,2010,39(8):12-17.
MA Shuangchen, JIN Xin, SUN Yunxue,etal. The formation mechanism of ammonium bisulfate in SCR flue gas denitrification process and control[J].Thermal Power Generation,2010, 39(8):12-17.
[10]马双忱,郭蒙,宋卉卉,等.选择性催化还原工艺中硫酸氢铵形成机理及影响因素[J].热力发电,2014,43(2):75-78.
MA Shuangchen, GUO Meng, SONG Huihui,etal. Formation mechanism and influencing factors of ammonium bisulfate during the selective catalytic reduction process[J].Thermal Power Generation,2014,43(2):75-78.
[11]SALEEM A, GALGANO M, INABA S.Hitachi-zosen deNOxprocess for fossil fuel-fired boilers[C]//Proceedings of the Second NOxControl Technology Seminar. Denver,USA:EPRI,1978.
[12]WILBURN R T, WRIGHT T L. SCR ammonia slip distribution in coal plant effluents and dependence upon SO3[J].Power Plant Chemistry,2004,6(5):295-304.
[13]BURKE J M, JOHNSON K L. An investigation of ammonium sulfate/bisulfate formation and deposition in air preheaters[R]. Nashville,Tennessee, USA: Radian Corporation,1980.
[14]MATSUDA S, KAMO T, KATO A,etal. Deposition of ammonium bisulfate in the selective catalytic reduction of nitrogen oxides with ammonia[J].Industrial and Engineering Chemistry Product Research and Development,1982,21(1):48-52.
[15]MENASHA J, DUNN-RANKIN D, MUZIO L,etal. Ammonium bisulfate formation temperature in a bench-scale single-channel air preheater[J].Fuel,2011,90(7):2445-2453.
[16]WIX A, BRACHERT L, SINANIS S,etal. A simulation tool for aerosol formation during sulphuric acid absorption in a gas cleaning process[J]. Journal of Aerosol Science,2010,41(12):1066-1079.
[17]SHIKADE T, OBA T, FUJIMOTO K,etal. Chemical product research and development[J]. Industrial Engineering,1984,23:417.
[18]BURKE J M, JOHNSON K L. Ammonium sulfate and bisulfate formation in air preheaters[R]. Washington,USA:United States Environment Protection Agency,1982.
[19]HANS J H, LINDENHOFF P, SAFRONOV S. SCR design issues in reduction of NOxemissions from thermal power plants[R]. Frederikssund, Danmark: Haldor Topsoe Inc,2007:1-21.
[20]MORETTI A L, TRISCORI R J,RITZENTHALER D P. A system approach to SO3mitigation[R].Ohio,USA:The Babcock & Wilcox Company,2006:1-6.
[21]李靖华,张桂恩.硫酸氢铵分解动力学及其分解机理的研究[J].物理化学学报,1992,8(1):123-127.
LI Jinghua, ZHANG Guien. Investigation of the kinetics and mechanism of decomposition of ammonium hydrogen sulfate[J].Acta Physico-chimica Sinica,1992,8(1):123-127.
Experimental Research on ABS Formation Characteristics in SCR Denitrification Process
MAShuangchen1,DENGYue1,WUWenlong2,ZHANGLinan1,MAJingxiang1,ZHANGXiaoni2
(1.College of Environmental Science and Engineering, North China Electric Power University,Baoding 071003, Hebei Province, China;2. Henan Electric Power Research Institute, State Grid, Zhengzhou 450052, China)
Abstract:To study the effects of temperature and reactant concentrations on the formation mechanism of ammonium bisulfate (ABS), characteristic experiments were conducted on a self-developed test setup, during which the vaporating point of ABS was obtained through thermogravimetric analysis, and subsequently its decomposition temperture was acquired by calculating the Gibbs free energy for decomposition of ABS. Results show that the formation of ABS is a function of temperature and reactant concentrations, and its formation temperature lies in 220-261 ℃; the larger the concentration product of NH3 and H2SO4, the higher the formation temperature of ABS; for a constant excessive concentration of H2SO4, the higher the concentration of NH3, the larger the ABS precipitation amount; whereas for a constant concentration of NH3, the effect of H2SO4 concentration on ABS precipitation is not obvious. Thermogravimetric analysis indicates that the volatization and decomposition temperature of ABS are respectively 173.7 ℃ and 447.18 ℃.
Key words:ABS; formation mechanism; thermodynamics; temperature; experimental research
文章编号:1674-7607(2016)02-0143-08
中图分类号:X701
文献标志码:A学科分类号:610.30
作者简介:马双忱(1968-),男,满族,辽宁大连人,教授,博士,主要从事燃煤电厂烟气脱硫、脱硝技术方面的工作.电话(Tel.): 0312-7525521;E-mail:msc1225@163.com.
基金项目:国网河南省电力公司电力科学研究院资助项目(SGTYHT/13-JS-178)
收稿日期:2015-06-25
修订日期:2015-07-10

