美多巴单用及联合普拉克索治疗帕金森病的疗效和安全性比较
姜立刚 李海平 李 威 (北华大学附属医院神经内科,吉林 吉林 132000)
美多巴单用及联合普拉克索治疗帕金森病的疗效和安全性比较
姜立刚李海平李威(北华大学附属医院神经内科,吉林吉林132000)
〔摘要〕目的探讨美多巴单用及联合普拉克索治疗帕金森病( PD)的疗效和安全性。方法选取100例该院帕金森病专病门诊及住院PD患者,随机分为观察组和对照组各50例。对照组给予美多巴,观察组给予多巴联合普拉克索,连续治疗8 w。比较两组汉密顿抑郁量表( HAMD)评分、Hoehn-Yahr分期、临床疗效及副作用量表( TESS)评分。结果治疗后1~8 w,观察组HAMD评分显著高于对照组( P<0.05)。治疗8 w后,观察组Hoehn-Yahr分期显著低于对照组( P<0.05)。观察组治疗有效率显著高于对照组( P<0.05)。观察组TESS评分显著低于对照组( P<0.05)。结论
美多巴联合普拉克索治疗PD可有效提高临床疗效,减少不良反应,其效果优于单纯美多巴治疗。
〔关键词〕帕金森病;美多巴;普拉克索
第一作者:姜立刚( 1978-),男,博士,博士后,副主任医师,副教授,硕士生导师,主要从事帕金森病基础与临床研究。
帕金森病( PD)主要表现为肌肉强直、静止性震颤、动作迟缓及情感障碍等〔1,2〕。左旋多巴是PD治疗的首选药物,但长期服用易导致开关现象、剂末现象、异动症及晨僵少动等不良反应〔3〕。为避免长期、大剂量使用左旋多巴引起的不良反应,部分学者提出采用左旋多巴与多巴胺( DA)受体激动剂早期联合治疗PD,但其疗效及安全性尚未明确〔4〕。本研究探讨PD患者给予单纯美多巴或美多巴联合普拉克索治疗的疗效。
1资料与方法
1. 1一般资料选取2012年9月至2015年2月我院收治的PD患者100例。纳入标准: ( 1)原发性PD患者; ( 2)知情同意并签署知情同意书者。排除标准: ( 1)合并严重心、肝、肾等脏器功能障碍者; ( 2)精神分裂症史者; ( 3)脑部立体定向手术史者。按入组顺序进行编号,奇数者纳入对照组,偶数者纳入观察组,每组50例。对照组中男29例,女21例;年龄43~73岁,平均( 62.5±5.7)岁;病程1~9年,平均( 6.1±2.7)年。观察组中男28例,女22例;年龄45~80岁,平均( 63.8±4.9)岁;病程1~10年,平均( 6.8±3.0)年。两组患者性别、年龄、病程等一般资料比较无统计学意义( P>0.05),具有可比性。
1. 2方法对照组:给予美多巴(生产厂家:上海罗氏药业,批号: I10930198,规格: 250 mg/片),初次使用为每日早晚各口服1次,62.5 mg/次,后根据治疗需要逐步调整为每日早中晚各口服1次,250 mg/次,连续治疗8 w。观察组:给予美多巴单及联合普拉克索治疗,美多巴使用方法同对照组。普拉克索(生产厂家:德国勃林格殷格翰药业,批号: 404949,规格: 0.25 mg),初次使用为每日早中晚各口服1次,0.062 5 mg/次,后根据治疗需要逐步调整剂量为0.5 mg/次,连续治疗8 w。
1. 3观察指标
1. 3. 1汉密顿抑郁量表( HAMD)评分〔5〕采用HAMD评价患者治疗前及治疗后1、2、4、8 w时的抑郁状态,量表共包括17个条目,≤17分为轻度抑郁,>17分且≤24分为中度抑郁,>24分为重度抑郁。
1. 3. 2 Hoehn-Yahr分期〔6〕Ⅰ期:单侧受累;Ⅱ期:双侧受累,但无姿势平衡障碍;Ⅲ期:存在姿势平衡障碍,易跌倒;Ⅳ期:日常生活无法自理,独立行走较为困难;Ⅴ期:几乎全天须依赖轮椅或者无法起身。
1. 3. 3临床疗效〔7〕根据Webster量表评分计算进步率,进步率=〔(治疗前积分-治疗后积分) /治疗前积分〕×100%。痊愈:进步率为100%,显效:进步率为50%~99%,有效:进步率为10%~49%,无效:进步率为0~10%。治疗有效率=〔(痊愈+显效+有效) /总例数〕×100%。
1. 3. 4副作用量表( TESS)评分〔8〕采用TESS评价治疗后1、2、4、8 w的副作用。总评分越高为副作用越大。
1. 4统计学方法采用SPSS19.0进行软件秩和检验、χ2检验和t检验。
2结果
2. 1 HAMD评分治疗前,两组患者HAMD评分比较无统计学差异( P>0.05) ;治疗后1~8 w,两组患者HAMD评分均显著降低,观察组显著高于对照组( P<0.05)。见表1。
表1两组患者HAMD评分(±s,分,n=50)

表1两组患者HAMD评分(±s,分,n=50)
组别 治疗前 治疗后1 w治疗后2 w治疗后4 w治疗后8 w观察组 28.3±4.3 24.7±3.2 21.5±2.9 18.4±3.1 13.5±2.1对照组 28.1±4.0 18.7±3.0 14.8±2.3 13.7±2.2 7.3±1.9 t值 0.152 2.899 3.002 2.961 2.953 P值 0.889 0.049 0.043 0.045 0.046
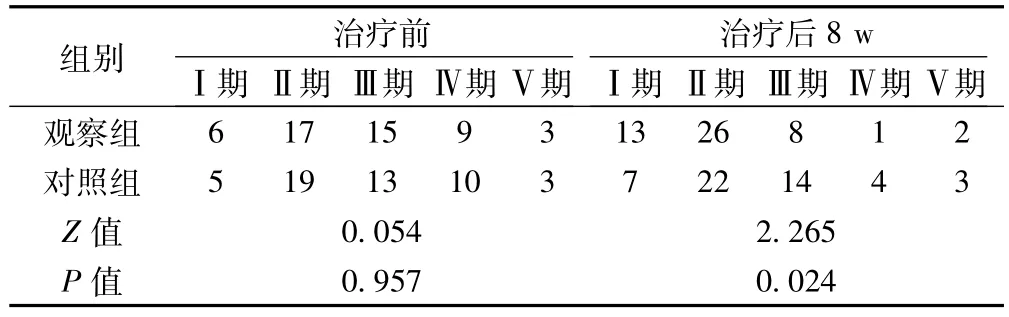
表2两组患者Hoehn-Yahr分期( n,n=50)
2. 2 Hoehn-Yahr分期见表2。治疗前,两组患者Hoehn-Yahr分期比较无统计学差异( P>0.05) ;治疗后8 w,观察组Hoehn-YahrⅢ、Ⅳ、Ⅴ分期显著低于对照组( P<0.05)。
2. 3临床疗效观察组治疗有效率显著高于对照组(χ2= 5.263,P=0.022)。见表3。
2. 4 TESS评分观察组TESS评分显著低于对照组( P<0.05)。见表4。
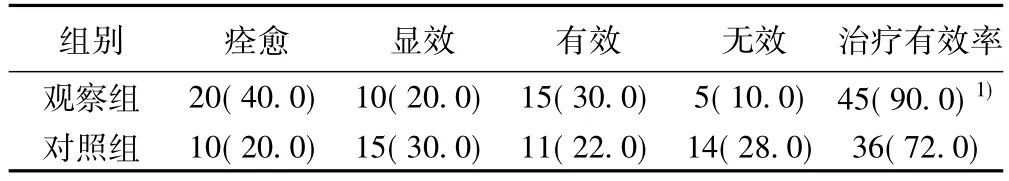
表3两组患者临床疗效〔n( %),n=50〕
表4两组患者TESS评分(±s,分,n=50)

表4两组患者TESS评分(±s,分,n=50)
组别 治疗后1 w 治疗后2 w 治疗后4 w 治疗后8 w观察组 2.2±1.0 2.3±0.9 2.4±1.1 2.5±0.9对照组 3.1±0.8 3.4±1.0 3.6±0.9 4.0±1.1 t值 3.012 2.951 2.967 3.131 P值 0.042 0.048 0.048 0.043
3讨论
中枢神经递质DA合成减少是诱发PD的主要作用机制。因此,补充脑内DA水平仍是目前治疗PD的首要原则〔9〕。美多巴是目前国内治疗PD最常用的药物。但长期、大剂量服用美多巴,不仅无法有效阻止黑质DA神经元的变性坏死,相反还会进一步加速其程序化死亡,导致诸如开关现象、剂末现象、异动症及晨僵少动等不良反应。研究证实,在长期服用美多巴的PD患者中,约有60%患者会在服药4~6年后出现症状波动、异动症等运动并发症,这也是导致患者致残的主要因
素〔10〕。
普拉克索可在不依赖内源性DA作用的前提下,对DA受体直接产生刺激,降低或延迟PD运动并发症的发生〔11〕。美多巴在治疗PD时,随着病情进展,黑质纹状体内多巴脱羧酶活性逐渐降低甚至消失,导致外源性左旋多巴也无法经过脱羧反应转化为DA,因此即使大剂量使用美多巴也无法起到明显疗效,但普拉克索则不受上述因素影响〔12〕。故采用美多巴联合DA受体激动剂进行治疗,不仅可有效减少美多巴的服用剂量,还可显著降低美多巴所致不良反应的发生。与其他DA受体激动剂类似,普拉克索可通过抑制氧化应激反应,减少活性氧自由基的生成,阻断兴奋谷氨酸毒性作用,减少DA能神经元变性、坏死,发挥神经保护作用,进而达到延缓PD进程的作用〔13〕。
本研究结果与赵杰〔14〕的研究一致。抑郁症是PD患者常见的临床表现之一,主要体现为情绪低落、思维迟缓及信心欠缺等,而美多巴联合普拉克索治疗可有效改善PD患者精神症状,分析其原因可能与普拉克索激动D3受体进而改善患者抑郁情绪有关。本研究与国内〔15〕研究报道相符,分析其原因可能与普拉克索联合使用降低美多巴使用剂量有关。本研究结果也与陈军〔16〕的研究一致。美多巴联合普拉克索治疗,可有效减少美多巴的使用剂量,通过激动DA受体,调整脑内DA分泌,纠正机体平衡障碍,改善临床症状;同时,普拉克索的使用还可对美多巴长期服用所致的不良反应起到有效的缓冲作用。
4参考文献
1 Litvan I,Goldman JG,Tröster AI,et al.Diagnostic criteria for mild cognitive impairment in Parkinson's disease: Movement Disorder Society Task Force guidelines〔J〕.Movement Disorders,2012; 27( 3) : 349-56.
2 Lill CM,Roehr JT,McQueen MB,et al.Comprehensive research synopsis and systematic meta-analyses in Parkinson's disease genetics: The PDGene database〔J〕.PLoS Genetics,2012; 8( 3) : e1002548.
3 Muller T,Hellwig R,Muhlack S.Levodopa induces synthesis of nerve growth factor and growth hormone in patients with Parkinson disease〔J〕.Clin Neuropharmacol,2011; 34( 3) : 101-3.
4 Schapira AH,McDermott MP,Barone P,et al.Pramipexole in patients with early Parkinson's disease( PROUD) : a randomised delayed-start trial〔J〕.Lancet Neurol,2013; 12( 8) : 747-55.
5 Broen MP,Moonen AJ,Kuijf ML,et al.Factor analysis of the Hamilton Depression Rating Scale in Parkinson's disease〔J〕.Parkinsonism Relat Dis,2015; 21( 2) : 142-6.
6 Kataoka H,Tanaka N,Saeki K,et al.Low frontal assessment battery score as a risk factor for falling in patients with Hoehn-Yahr StageⅢParkinson's disease: a 2-year prospective study〔J〕.European Neurol,2013; 71( 3-4) : 187-92.
7吕荣祥.美多巴联合普拉克索治疗帕金森病的有效性及安全性研究〔J〕.中国生化药物杂志,2014; 3( 34) : 53-4.
8沈国柱.多巴胺受体激动剂普拉克索治疗帕金森氏病的临床疗效分析与安全性评价〔J〕.海峡药学,2012; 24( 1) : 162-3.
9 Hauser RA,Schapira AH,Barone P,et al.Long-term safety and sustained efficacy of extended-release pramipexole in early and advanced Parkinson 's disease〔J〕.European J Neurol,2014; 21( 5) : 736-43.
10刘国敏.单用美多巴及与多巴胺受体激动剂合用治疗帕金森病的疗效和安全性研究〔J〕.中国医学工程,2013; 13( 8) : 56-7.
11 Mizuno Y,Yamamoto M,Kuno S,et al.Efficacy and Safety of Extended-Versus Immediate-Release Pramipexole in Japanese Patients With Advanced and L-dopa-Undertreated Parkinson Disease: A Double-Blind,Randomized Trial〔J〕.Clin Neuropharmacol,2012; 35( 4) : 174-81.
12龙武,杨期明,蒋柏菊,等.普拉克索治疗帕金森病运动并发症的临床疗效观察〔J〕.国际神经病学神经外科学杂志,2013; 40( 2) : 118-22.
13 Eggert K,Öhlwein C,Kassubek J,et al.Influence of the nonergot dopamine agonist piribedil on vigilance in patients with parkinson disease and excessive daytime sleepiness( PiViCog-PD) : an 11-week randomized comparison trial against pramipexole and ropinirole〔J〕.Clin Neuropharmacol,2014; 37( 4) : 116-22.
14赵杰.分析研究左旋多巴联合普拉克索治疗帕金森病的有效性及安全性〔J〕.中国实用医药,2014; 9( 22) : 136-7.
15姚亚妮,王玉玲,杨新玲.普拉克索添加治疗帕金森病临床随机对照研究〔J〕.中华神经医学杂志,2009; 8( 7) : 685.
16陈军.多巴丝肼联合普拉克索治疗中晚期帕金森病疗效观察〔J〕.药物流行病学杂志,2014; 23( 3) : 148-50.
〔2015-06-20修回〕
(编辑滕欣航)
通讯作者:李威( 1959-),女,主任医师,教授,硕士生导师,主要从事帕金森病基础与临床研究。
基金项目:吉林省科技厅青年基金项目( 20130522026JH)
〔中图分类号〕R742. 5
〔文献标识码〕A
〔文章编号〕1005-9202( 2016) 02-0424-02;
doi:10. 3969/j. issn. 1005-9202. 2016. 02. 081

