研究经典题型 探析创新方式
——以无机推断试题为例
江苏 印志林
研究经典题型 探析创新方式
——以无机推断试题为例
江苏 印志林
无机推断题是高考最经典的题型之一。研究发现,近年高考中的无机推断题在传统的直线型、三角型、归中型等基本形式的基础上有了很大改变,下面就其创新形式略加分析。
一、综合型
高考需要在有限的几道试题中,考查高中全部知识内容,这就形成了一题多个知识点的命题趋势。而无机推断题经常与物质结构、化学实验、化学计算、化学反应原理、定量分析等内容相融合,体现出较强的综合性。
例1 (2016江苏)在给定的条件下,下列选项所示的物质间转化均能实现的是 ( )
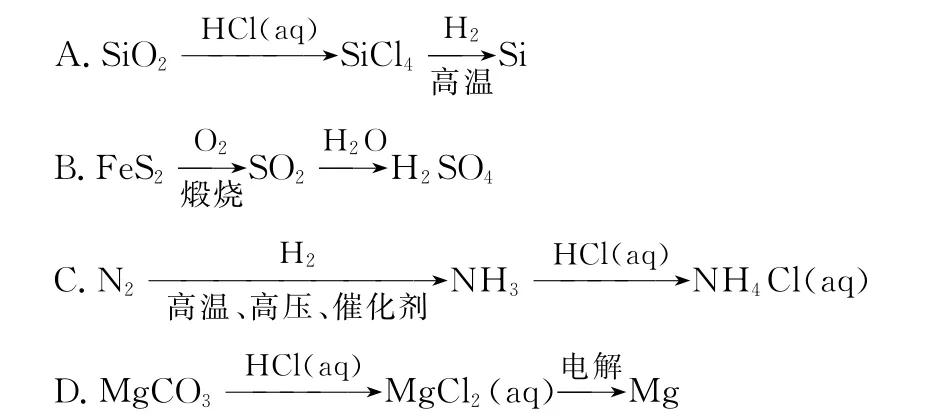
解析:SiO2是酸性氧化物,与盐酸不反应,A项错误;SO2和H2O反应生成的是H2SO3,B项错误;N2与H2在一定条件下可化合生成NH3,NH3与HCl可化合生成NH4Cl,C项正确;工业上用电解熔融的MgCl2的方法制镁,D项错误。
答案:C
例2 (2016全国Ⅰ)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
解析:n是元素Z的单质,通常为黄绿色气体,则n是Cl2,Z是Cl元素;0.01mol·L-1r溶液的pH为2,说明r是一元强酸;Cl2和二元化合物m生成一元强酸r和有漂白性的q,则m是水,r是HCl,q是HClO;Cl2和二元化合物p在光照条件下反应生成HCl和难溶于水的混合物s,则p是CH4,s是CH4的氯代产物;短周期元素W、X、Y、Z的原子序数依次增加,则四种元素依次是H、C、O、Cl。推出有关元素后,根据元素的位、构、性关系即可确定答案。
答案:C
二、开放型
无机推断题中的一框多解现象很常见,这类试题体现出较强的开放性,注重考查学生的发散思维能力。只有基础知识掌握牢固、视野开阔才能顺利解答这类试题。
例3 (2015福建)纯净物X、Y、Z转化关系如下图所示,下列判断正确的是 ( )

A.X可能是金属铜
B.Y不可能是氢气
C.Z可能是氯化钠
D.Z可能是三氧化硫
解析:若X是Cu,则Y是Cl2,Cu在Cl2燃烧产生CuCl2,电解CuCl2溶液产生Cu和Cl2,符合上述转化关系,A正确;若X是Cl2,则Y是H2,H2在Cl2中燃烧产生HCl,电解HCl的水溶液(盐酸)产生H2和Cl2,符合上述转化关系,B错误;若Z是NaCl,则X、Y分别是Na和Cl2中的一种,电解NaCl溶液产生H2、Cl2和NaOH,不符合上述转化关系,C错误;若Z是SO3,而X、Y可能是O2和SO2中的一种,SO3溶于水产生H2SO4,电解硫酸溶液实质是电解水,产生H2和O2,不符合上述转化关系,D错误。
答案:A
三、流程型
在传统的推断题中,物质间的转化关系人为设计的成分较多,缺乏真实的应用背景,学生解题时经常是一步不通,全题皆错。在最近几年的高考中,无机推断题有了一些明显改变,经常给出一些工业生产或实验流程图,试题的背景更有实际意义和应用价值。
例4 (2016浙江)为落实“五水共治”,某工厂拟综合处理含废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
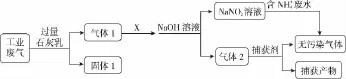
下列说法不正确的是 ( )
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
解析:工业废气通过过量石灰乳时,其中的CO2和SO2被吸收生成CaCO3和CaSO3,A项正确;气体1为N2、NO和CO的混合物,气体1与X反应的产物与NaOH溶液反应生成了NaNO2,则产物中应有NO和NO2,有关反应为NO+NO2+2NaOH2NaNO2+H2O,故X为空气,且不能过量,B项错误;CO与NaOH溶液不反应,捕获剂所捕获的气体主要是CO,C项正确;和发生归中反应生成N2,D项正确。
答案:B
例5 (2016浙江)磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
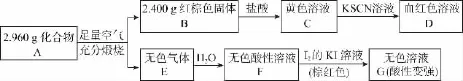
请回答:
(1)A的组成元素为________(用元素符号表示),化学式为_________________。
(2)溶液C可溶解铜片,例举该反应的一个实际应用:_____________________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g·L-1),该气体分子的电子式为_____________。写出该反应的离子方程式:_____________________。
(4)写出F→G反应的化学方程式:________________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-):_________________________________________。
解析:(1)红棕色固体B为Fe2O3,Fe2O3与盐酸反应后生成黄色的FeCl3(C)溶液,FeCl3与KSCN溶液反应生成血红色溶液D。无色气体E溶于水后得到酸性溶液F,F溶液与I2反应后生成无色溶液G,G溶液酸性变强,说明原来的酸为弱酸,且具有还原性,则F为H2SO3,E为SO2。
原化合物A中含有铁元素和硫元素,根据质量关系进行换算可求其化学式:

所以,A的化学式为Fe3S4。
(2)C为FeCl3,FeCl3溶液可以溶解铜,用来制印刷电路板。
(3)A与硫酸反应生成硫,另一气体的摩尔质量为1.518g·L-1×22.4L·mol-1=34.00,则该气体为H2S。该反应生成FeSO4、S和H2S,离子方程式为:Fe3S4+ 6H+3H2S↑+3Fe2++S。
(4)H2SO3和I2反应生成H2SO4和HI,不考虑H2O、H+、K+、I-时,溶液G中主要含有SO2-4,可能还有未反应完的H2SO3分子。可用钡盐检验,H2SO3可以用氧化剂氧化成后再检验,实验时应先检验,后检验H2SO3。
答案:(1)S、Fe Fe3S4(2)制印刷电路板

(4)H2SO3+I2+H2OH2SO4+2HI 取溶液G,加入过量BaCl2溶液,若产生白色沉淀,则有SO2-4;过滤后取滤液,滴加H2O2溶液,若再产生白色沉淀,则有H2SO3
无机推断题的呈现形式很多,无论是哪种类型的推断题,均应遵循这样的推断思路:迅速浏览、整体扫描、产生印象、寻找“突破口”,突破点由点到面,随时检验,注意联系,大胆假设,全面分析(正推或逆推),验证确认。解题的关键是仔细审题,依物质的特性或特征转化来确定“突破口”,顺藤摸瓜,进而完成全部未知物的推断。推断题的解题方法及推理过程可简单表示如下:

(作者单位:江苏省常州市横山桥高级中学)

