赖氨酸在Maillard 反应中形成有害产物AGEs的研究
李 普 夏秋琴 刘贵梅 卢永翎 吕丽爽
(南京师范大学金陵女子学院,江苏 南京 210097)
赖氨酸在Maillard 反应中形成有害产物AGEs的研究
李 普 夏秋琴 刘贵梅 卢永翎 吕丽爽
(南京师范大学金陵女子学院,江苏 南京 210097)
模拟食品加工条件,构建赖氨酸—还原糖和精氨酸—赖氨酸—还原糖体系,分析各影响因素在体系发生Maillard反应中产生有害AGEs(晚期糖基化终末产物)的作用,比较两个体系添加和不添加黄酮条件下对AGEs形成量的影响。用荧光光谱法(λex /λem =370 / 440 nm)测定AGEs的含量,考察不同因素如还原糖种类、浓度、金属离子、温度、pH和染料木素对有害AGEs形成的影响,以及赖氨酸/精氨酸并存对AGEs形成量的影响。结果表明:在赖氨酸发生Maillard反应过程中,温度越高、还原糖中核糖,糖浓度越大、pH 9.2,形成的AGEs越多;不同的金属离子对AGEs的作用各异,Mg2+和Fe2+能促进AGEs的形成,Ca2+抑制AGEs的形成;抑制剂染料木素浓度越大(9 mmol/L),AGEs抑制效果越好;赖氨酸/精氨酸混合体系中AGEs形成量主要由赖氨酸来决定。各影响因素对赖氨酸Maillard反应过程中产生AGEs均有一定作用,时间是最主要因素,其次是pH和温度;而赖氨酸/精氨酸混合体系中AGEs的形成量取决于赖氨酸的含量。
荧光性晚期糖基化终末产物;赖氨酸;美拉德反应;荧光光谱法
加工和贮藏过程中所发生的一些化学变化不仅改变了食品的结构和功能,同时也会产生一些有害物质。美拉德反应(又称非酶糖基化)对于食品风味、色泽的形成皆具重要作用[1];但是非酶糖基化反应也会产生不可逆转的晚期糖基化终末产物[2],AGEs是一类物质的总称,目前已发现20多种AGEs,在体内以多种不同的形式存在,包括羧甲基赖氨酸(CML)、吡咯素、戊糖素、羧乙基赖氨酸(CEL)等[3-4]。AGEs通过在体内蓄积[5-6]可以导致一些疾病的发生,如阿兹海默症、动脉粥样硬化、糖尿病病症、慢性心脏衰竭等[7-9]。人体试验[10]研究发现,高AGEs膳食与低AGEs膳食相比,能更为严重地损伤II型糖尿病患者的血管功能。
Goldberg等[11]研究表明,肉类以及肉类替代品中AGEs的含量平均可以达到43 kU/g;脂肪类食品中AGEs可达到100 kU/g(1 U≈1.660×10-27kg),平均含量最高,碳水化合物类食品中AGEs仅为3.4 kU/g,平均含量最低。房红娟等[12]研究发现油炸类食品(如麻花、油条等)的AGEs含量均在100 AU之上,麻花、油条分别达到(186.365±1.337),(100.553±1.981) AU。Koschinsky等[13]研究认为,大约10%的食源性AGEs与体内循环系统和组织中的AGEs有着密切联系。其中赖氨酸含有两个氨基(伯),因此由赖氨酸及蛋白质赖氨酸残基引发的糖基化反应最为普及,广泛引起食品界关注,所以,构建赖氨酸还原糖体系并研究不同因素对该体系中荧光性AGEs形成的影响,具有一定的现实意义。
部分AGEs具有一定的荧光吸收,其荧光强度随着体系中AGEs浓度的增大而增大[14]。荧光光谱法(λex = 340~370 nm和λem = 420~440 nm)可以较为直观地表征Maillard反应中荧光性AGEs的总含量。本试验针对还原糖浓度、金属离子、温度、pH和染料木素等各影响因素,分析各因素对赖氨酸—还原糖体系中AGEs形成的影响,并确定主要因素。进而结合实验室前期精氨酸—还原糖试验结果[15],分析赖氨酸—精氨酸—还原糖体系中决定AGEs形成关键因素。
1 材料与方法
1.1 试验试剂与仪器
1.1.1 试剂
精氨酸、赖氨酸:分析纯,上海生物生工有限公司;
果糖、半乳糖、葡萄糖、核糖:分析纯,上海国药化学试剂有限公司;
染料木素:分析纯,南京广润生物制品有限公司
1.1.2 仪器
数字式pH计:PHS-3C型,上海三信仪表厂;
TECAN多孔酶标仪:Infinite 200Pro型,瑞士帝肯贸易有限公司;
微型漩涡混合仪:XW-80A型,上海沪西分析仪器厂有限公司。
1.2 试验方法
1.2.1 糖的种类和浓度对赖氨酸引发的Maillard反应中有害产物AGEs的影响 参照文献[15]建立赖氨酸—还原糖体系,测定不同还原糖种类和浓度条件下,λex/λem=370 nm/440 nm处荧光值。
1.2.2 温度对赖氨酸引发的Maillard反应中有害产物AGEs的影响 参照文献[15]的方法模拟食品加工条件构建赖氨酸—还原糖反应,测定不同温度条件下λex/λem=370 nm/440 nm处荧光值,即AGEs的量。
1.2.3 金属离子对赖氨酸引发的Maillard反应中有害产物AGEs的影响 参照文献[15]的方法模拟食品加工条件构建赖氨酸—还原糖反应,测定5种金属离子各自存在时体系中AGEs量。
1.2.4 pH对赖氨酸引发Maillard反应中有害产物AGEs的影响 参照文献[15]的方法模拟食品加工条件构建赖氨酸—还原糖反应,测定不同pH条件下,体系中AGEs量。
1.2.5 染料木素含量对赖氨酸引发Maillard反应中有害产物AGEs的影响 参照文献[15]的方法模拟食品加工条件构建赖氨酸—还原糖体系,测定添加不同浓度(1.5~9.0 mmol/L)染料木素时,体系中AGEs的量。
1.2.6 赖氨酸/精氨酸—葡萄糖体系中有害产物AGEs的测定 用0.2 mol/L pH 7.4的磷酸盐缓冲液分别配置浓度为1,2,3 mmol/L的赖氨酸和精氨酸溶液各25 mL,配置浓度为4 mmol/L的葡萄糖溶液50 mL。在不同的10 mL试管中分别加入最终摩尔浓度比为1∶1∶4,1∶2∶4,1∶3∶4,2∶1∶4,3∶1∶4的赖氨酸、精氨酸和葡萄糖溶液各2 mL,再加2 mL PBS。以磷酸盐缓冲液代替氨基酸溶液做空白对照,参照文献[15]的方法测定体系中AGEs量。
1.2.7 染料木素抑制赖氨酸/精氨酸—葡萄糖体系中有害产物AGEs的测定 根据1.2.6的试验结果,选取其中荧光值最高的一组浓度(赖氨酸∶精氨酸∶葡萄糖=3∶1∶4)进行本组实验。分别将赖氨酸、精氨酸和葡萄糖溶解于0.2 mol/L pH 7.4的磷酸盐缓冲液中,分别取2 mL赖氨酸,2 mL精氨酸,2 mL葡萄糖于10 mL样品管中,使赖氨酸、精氨酸和葡萄糖的最终浓度分别为3,1,4 mmol/L,加入2 mL染料木黄酮溶液,使其浓度为1.5,3,6,9 mmol/L。参照文献[15]的方法测定体系中AGEs量。
1.3 数据分析方法
采用Excel2010、Minitab16分析数据。
2 结果与讨论
2.1 赖氨酸—糖体系发生Maillard反应产生有害产物AGEs的研究
2.1.1 糖的种类和浓度对赖氨酸-还原糖体系中有害产物AGEs的作用 图1结果表明,反应240 min时,在4种赖氨酸—还原糖体系中,还原糖的浓度越大,体系中荧光性AGEs的形成量就越多。其中在赖氨酸—核糖模型中形成的荧光性AGEs的量最高,而果糖、半乳糖、葡萄糖诱导产生AGEs的量相差不大;核糖在糖浓度为3 mmol/L时体系中,产生的AGEs量大约是另外3种糖分别与赖氨酸反应形成AGEs量的2倍。原因推测核糖为五碳糖,果糖、半乳糖、葡萄糖为六碳糖,而五碳糖的反应活性和速率远大于六碳糖[16]。Bunn等[17]研究表明,葡萄糖99%以上的六元环结构是高度稳定的,相对于其它糖类不容易受到来自其他分子的亲和攻击;与此同时,葡萄糖以其环状结构高度稳定性,限制蛋白质发生潜在有害的非酶糖基化反应。Jalbout等[18]也证实开环的核糖更易形成Amadori产物,因而比环状的六碳糖反应要快。

图1 糖的种类和浓度对赖氨酸—还原糖体系中有害产物AGEs的作用
将该试验结果与本课题组[15]前期报道的Arg还原糖体系的结果相对比,尽管AGEs的总量偏高,但还原糖浓度和种类的变化对两种氨基酸体系荧光性AGEs的量带来的影响,差异性不显著。
2.1.2 温度对赖氨酸—还原糖体系中有害产物AGEs的作用 图2是反应时间为240 min时,温度对赖氨酸—还原糖模拟体系产生荧光性AGEs的影响。由图2可知,温度对赖氨酸—还原糖模型中荧光性AGEs的形成有很大的影响;且温度越高,产生的荧光性AGEs越多。在较低温度(37,60 ℃)下,荧光性AGEs形成量无明显变化;当温度≥85 ℃时,随着温度的升高,体系中荧光性AGEs的形成量显著增加,并在121 ℃时达到最高值。很显然是因为高温促进了美拉德反应的进程。对比4种不同的还原糖可知,核糖体系产生的荧光性AGEs最多,其他3种还原糖产生的AGEs量差别不大。相比前期发表的Arg还原糖模型[15],Lys还原糖模型相同条件下产生的荧光性AGEs含量均高于Arg模型,最高差别约1倍以上;且不同还原糖之间差异较大。
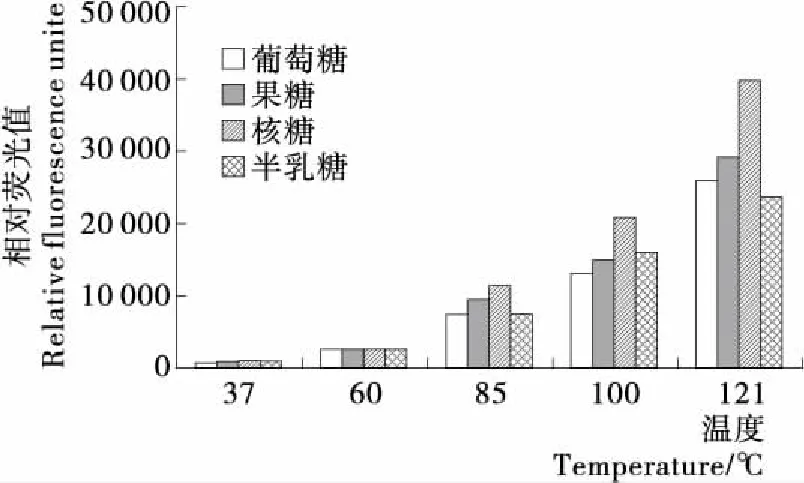
图2 温度对赖氨酸—还原糖体系中有害产物AGEs的作用
2.1.3 金属离子对赖氨酸—还原糖体系中有害产物AGEs的作用 图3为赖氨酸—还原糖模拟体系中,金属离子对荧光性AGEs形成的影响。由图3可知,不同金属离子对体系中荧光性AGEs的形成影响不同。其中,Ca2+会抑制体系荧光性AGEs的产生,Mg2+和Fe2+会促进荧光性AGEs的形成,而其他金属离子的作用效果则不明显。这是因为金属离子可以促进氢过氧化物的降解,从而促进自由基生成,而自由基在AGEs的生成中起着重要的作用[19]。Ramonaityte等[20]的研究表明过渡金属离子如Fe3+、Fe2+等会通过催化作用形成自由基而促进AGEs的产生。
但在本课题组[15]前期研究的Arg—还原糖模型中,5种金属离子均会增加体系中荧光性AGEs产生的量,而且不同金属离子在不同还原糖模型体系中的作用效果不同。在核糖和果糖体系中,金属离子诱导产生的荧光性AGEs量比较大,其次是半乳糖,葡萄糖体系影响最低。金属离子对两种氨基酸糖基化反应的差异性原因有待进一步研究。
2.1.4 pH对赖氨酸—还原糖体系中有害产物AGEs的作用 图4为反应240 min时,pH对赖氨酸—还原糖模拟体系荧光性AGEs的影响。由图4可知,在本研究设定的4种pH(4.0,6.5,7.4,9.2)条件下,pH越偏碱性,体系的荧光性AGEs的形成量就越高,pH 9.2时产生的荧光性AGEs含量最高,而pH 4.0时产生量较少。这是由于在偏酸性条件下,Maillard的前体物质N-葡萄糖胺容易被水解,从而导致反应速率降低[21];碱性条件能显著促进美拉德反应尤其是其后期反应的进行[22]。在4种还原糖模型中,形成荧光性AGEs量最大的体系为赖氨酸—核糖,反应强度最大,其他糖反应活性依次排序为果糖、半乳糖和葡萄糖。该反应趋势与前期精氨酸试验[15]结果相一致。

图3 金属离子对赖氨酸—还原糖体系中有害产物AGEs的影响

图4 pH对赖氨酸—还原糖体系中有害产物AGEs的影响
2.1.5 染料木素对赖氨酸—核糖体系中有害产物AGEs的影响 图5为赖氨酸—还原糖模拟体系中,染料木素对荧光性AGEs形成的影响。由图5可知,染料木黄酮的浓度越大、反应的时间越长,其抑制效果越好。当时间为240 min、染料木素浓度为9 mmol/L时,荧光性AGEs的抑制率达到96%,效果良好。该试验结果与前期研究[15]精氨酸—糖体系的抑制率95%相一致。表明黄酮对不同的糖基化体系均能达到显著的抑制效果。Jung D. H等[23]研究发现染料木素能阻断AGEs与多种不同的细胞表面受体RAGE的结合,AGE—RAGE交联导致病变。染料木素含量越高,阻断效果越好。2.1.6 各影响因素对体系中有害产物AGEs的贡献值分析 如表1所示,在赖氨酸—还原糖模拟体系中,影响荧光性AGEs产生的因素,第一位是时间,其次是pH,第三是温度。而其他因素对体系荧光性AGEs的形成所占比例较低且相差不大。对照前期研究[15]精氨酸—还原糖体系,前3个主要影响因素依次为时间、还原糖种类和pH。由此,不同氨基酸发生糖基化反应过程中,对比各影响因素的贡献值发现,时间是关键因素,其次是对pH的敏感性,而温度和还原糖种类相差较大。
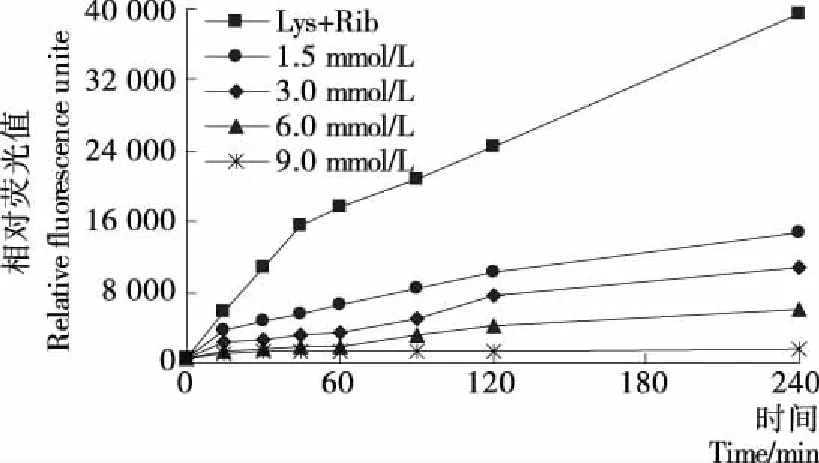
图5 染料木素对赖氨酸—核糖体系中有害产物AGEs的影响

因素贡献值因素贡献值时间41.04温度×时间2.62温度9.86还原糖×时间0.82还原糖0.95还原糖浓度×时间2.95还原糖浓度6.30pH×时间8.44pH13.84金属离子×时间0.68金属离子2.04染料木黄酮×时间0.01染料木黄酮0.19误差5.27
2.2 赖氨酸/精氨酸—葡萄糖体系产生荧光性AGEs的研究
2.2.1 赖氨酸/精氨酸—葡萄糖体系荧光性AGEs的产生情况 鉴于不同氨基酸发生糖基化反应的差异性,以及在食品体系中多种氨基酸的共存,选取两种易于与还原糖发生美拉德反应的氨基酸,赖氨酸(两个伯氨基)、精氨酸(多氨基),建立赖氨酸/精氨酸—葡萄糖体系。由图6可知,赖氨酸/精氨酸—葡萄糖体系中,相对荧光值RFU随着赖氨酸比例的增大而提高,但精氨酸比例提高则几乎没变化。本课题的前期研究[15]表明在精氨酸—葡萄糖体系中,随着时间的延长,相对荧光值RFU在240 min即可达到20 000。而当两种氨基酸共存发生Maillard反应时,体系中AGEs的产生主要由赖氨酸的含量来决定,推测其原因可能是,两分子赖氨酸可以发生交联作用(赖氨酸—赖氨酸—糖)[24],另外赖氨酸与精氨酸也进行交联反应(赖氨酸—精氨酸—糖)[24]。
2.2.2 染料木素对赖氨酸/精氨酸—葡萄糖体系AGEs形成的影响 图7是染料木素对赖氨酸/精氨酸—葡萄糖体系产生荧光性AGEs的影响。由图7可知,在添加染料木素后,赖氨酸/精氨酸—葡萄糖体系中相对荧光值RFU明显下降,3组试验的RFU在反应前2 h均下降到了半值以下。且其抑制率与染料木素的添加量呈量效关系,染料木素的浓度越大,抑制率越高,说明染料木素对赖氨酸/精氨酸共存体系中荧光性 AGEs的产生有明显的抑制作用。
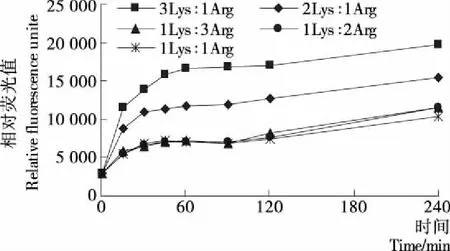
图6 赖氨酸/精氨酸—葡萄糖体系AGEs的产生

图7 染料木素对赖氨酸/精氨酸—葡萄糖体系AGEs形成的影响
3 结论
各种影响因素对于赖氨酸—还原糖体系中荧光性AGEs的产生皆有明显的影响。当反应时间为定值时,温度、还原糖浓度和pH越高,产生荧光性AGEs的量就越高;染料木素的浓度越大对荧光性AGEs的抑制效果越好,且有显著抑制作用。通过分析各个影响因素的贡献值,反应时间是赖氨酸—还原糖体系产生荧光性AGEs的决定性因素,其次为pH;第三为温度,其他因素对荧光性AGEs产生的影响较小且差别不大。当赖氨酸和精氨酸共存时,赖氨酸含量决定混合体系精氨酸/赖氨酸—葡萄糖反应中产生AGEs的量,精氨酸含量的高低影响不大。
[1] WALLER G R, FEATHER M S, MILTON S. The Maillard reaction in foods and nutrition [M]. Washington D C, USA: ACS, 1983: 1-15.
[2] LUEVANO-CONTRERES C, CHAPMAN-NOVAKOFSKI K. Dietary advanced glycation end products and aging[J]. Nutrients, 2010, 2(12): 1 247-1 265.
[3] AHMED M U, THORPE S R, BAYNES J W. Identification of Nε-(carboxymethyl)lysine as a degradation product of fructoselysine in glycated protein[J]. The Journal of Biological Chemistry, 1986, 261: 4 889-4 894.
[4] HENLE T. Protein-bound advanced glycation endproducts (AGEs) and bioactive amino acid derivatives in foods[J]. Amino Acids, 2005, 29(4): 313-322.
[5] URIBARRI J, WOODRUFF S, GOODMAN S. Advanced glycation end products in foods and a practical guide to their reduction in the diet[J]. Journal of the American Dietetic Association, 2010, 110(6): 911-916.
[6] KRAJCOVICOVA-KUDLACKOVA M, SEBEKOVA K, SCHINZEL R, et al. Advanced glycation end products and nutrition[J]. Physiological Research, 2002, 51(3): 313-316.
[7] SMIT A J, HARTOG J W, VOORS A A, et al. Advanced glycation endproducts in chronic heart failure[J]. Annals of the New York Academy of Sciences, 2008, 1 126(1): 225-230.
[8] MEERWALDT R, LINKS T, ZEEBREGTS C, et al. The clinical relevance of assessing advanced glycation endproducts accumulation in diabetes[J]. Cardiovasc Diabetol, 2008, 7(1): 29-29.
[9] BAYNES J W, THORPE S R. Role of oxidative stress in diabetic complications: a new perspective on an old paradigm[J]. Diabetes, 1999, 48(1): 1-9.
[10] NEGREAN M, STIRBAN A, STRATMANN B, et al. Effects of low- and high-advanced glycation endproduct meals on macro- and microvascular endothelial function and oxidative stress in patients with type 2 diabetes mellitus[J]. The American journal of clinical nutrition, 2007, 85(5): 1 236-1 243.
[11] Goldberg T, CAI Wei-jing, PEPPA M, et al. Advanced glycoxidation end products in commonly consumed foods[J]. Journal of the American Dietetic Association, 2004, 104(8): 1 287-1 291.
[12] 房红娟. 食品加工过程中晚期糖基化末端产物形成及控制研究[D]. 西安: 西北农林科技大学, 2013: 1-46.
[13] KOSCHINSKY T, HE Ci-jiang, MITSUHASHI T, et al. Orally absorbed reactive glycation products (glycotoxins): an environmental risk factor in diabetic nephropathy[J]. Proceedings of the National Academy of Sciences of the United States of America, 1997, 94(12): 6 474-6 479.
[14] BOSCH L, ALEGRIA A, FARRE R, et al. Fluorescence and color as markers for the Maillard reaction in milk-cereal based infant foods during storage[J]. Food chemistry, 2007, 105(3): 1 135-1 143.
[15] 夏秋琴, 吕丽爽. 影响精氨酸-还原糖模拟体系荧光性晚期糖基化终末产物形成的因素[J]. 食品科学, 2015, 36(15): 50-55.
[16] DELPHINE L, CLAUDE I, CELINE B, et al. Kinetic study on the Maillard reaction. Consideration of sugar reactivity[J]. Food Chemistry, 2008, 111(4): 1 032-1 042.
[17] BUNN H F, HIGGINS P J. Reaction of monosaccharides with proteins: possible evolutionary significance[J]. Science, 1981, 213(4 504): 222-224.
[18] JALBOUT A F, MAH S, NAVARRO J L. Density functional computational studies on ribose and glycine Maillard reaction: Formation of the Amadori rearrangement products in aqueous solution[J]. Food Chemistry, 2007, 103(3): 919-926.
[19] 房红娟, 李红姣, 张双凤, 等. 加工条件对 BSA-Glucose 模拟体系中晚期糖基化末端产物形成的影响[J]. 食品科学, 2012, 33(21): 6-10.
[20] RAMONAITYTE D, KERIENE M, ADAMS A, et al. Theinteraction of metal ions with Maillard reaction products in a lactose-glycine model system[J]. Food Research International, 2009, 42(3): 331-336.
[21] 肖怀秋, 李玉珍, 林亲录. 美拉德反应及其在食品风味中的应用研究[J]. 中国食品添加剂, 2005, 69(2): 27-30.
[22] NAGAI R, IKEDA K, KAWASAKI Y, et al. Conversion of Amadori product of Maillard reaction toN-(carboxymethyl)lysine in alkaline condition[J]. FEBS Letters, 1998, 425(2): 355-360.
[23] JUNG D H, KIM Y S, KIM J S. Screening system of blocking agents of the receptor for advanced glycation endproducts in cells using fluorescence[J]. Biological and Pharmaceutical Bulletin, 2012, 35(10): 1 826-1 830.
[24] TESSIER F, MONNIER V M, KORNFIELD J A. Characterization of novel chromophores, fluorophores and cross-links from glyceraldehyde, lysine and arginine[J]. International Congress, 2002, 1 245(6): 303-311.
Studies on formation of AGEs by lysine in maillard reaction
LI PuXIAQiu-qinLIUGui-meiLUYong-lingLULi-shuang
(GinlingCollege,NanjingNormalUniversity,Nanjing,Jiangsu210097,China)
[Purpose] The different influencing factors are investigated on producing AGEs by Lysine in Maillard reaction, and the different between single amino acid (Lysine, or Argine) -reducing and mixed Lys- Arg -reducing sugar system are compared. [Method] Fluorescence spectrometry (λex /λem =370 / 440 nm) is used to detect the amount of AGEs, the factors of sort and concentration of sugar, metal ion, temperature, pH and genistein concentration in Maillard reaction and proportion of lysine and arginine in Lys/Arg-reducing sugar system was discussed. [Result] The increasing of sugar concentration, pH, or temperature, the more amounts of AGEs was produced. Fe2+and Mg2+could promote the formation of AGEs. But metal ion (Ca2+) could inhibit the formation of AGEs; at the present of 9 mmol/L genistein, the inhibitory ratio is the best. The lysine played an important role on the Lys-Arg cross-linking with glucose in Lys/Arg-reducing sugar system. [Conclusion] All the factors have a little bit impact on the formation of AGEs, and genistein can significantly suppress the formation of AGEs. The reaction time is the main point on the formation of AGEs, the second is pH and temperature. Additionally, the lysine played an important role on the formation of fluorescent AGEs in Lys-Arg-glucose system.
advanced glycation end products; lysine; maillard reaction; fluorescence spectrometry
10.13652/j.issn.1003-5788.2016.12.006
国家自然科学基金项目资助(编号:31571783)
李普,男,南京师范大学在读硕士研究生。
吕丽爽(1969—),南京师范大学副教授,博士。 E-mail: lishuanglv@126.com
2016-09-26

