47例臭氧治疗仪不良事件分析
赵 瑛,黄 璞,黄 晖,赵 丽,郑思维,史 琛
1 华中科技大学同济医学院附属协和医院药剂科,武汉市,430022
2 湖北省药品(医疗器械)不良反应监测中心,武汉市,430071
47例臭氧治疗仪不良事件分析
【作 者】赵 瑛1,黄 璞1,黄 晖2,赵 丽2,郑思维1,史 琛1
1 华中科技大学同济医学院附属协和医院药剂科,武汉市,430022
2 湖北省药品(医疗器械)不良反应监测中心,武汉市,430071
采用回顾性研究法,对47份臭氧治疗仪不良事件报告进行分类、汇总与评价。结果表明25例不良事件明确与臭氧治疗仪的使用有关;上报单位以使用单位为主体,因器械故障延误治疗是最常见的不良事件表现;不良事件的发生与产品质量、患者体质、技术人员操作、器械消毒等风险因素有关。应加强臭氧治疗仪不良事件监测和风险控制,降低其不良事件发生率,维护患者用械安全。
臭氧;腰椎间盘突出症;医疗器械;不良事件
腰椎间盘突出症是一种常见疾病,严重影响患者的生活质量,而且其发病年龄呈现年轻化。该病症的传统治疗方法包括保守药物治疗和开放手术[1]。近年来,椎间盘的微创介入治疗被广泛应用于临床,与传统方法相比,具有创伤小、恢复快、有效率高、并发症少等诸多优点,受到医生和患者的关注[2-4]。臭氧治疗是一种微创介入治疗技术,通过氧化脊髓组织、减轻神经根压迫,同时产生抗炎和镇痛作用,可有效缓解疾病症状[5-9]。与传统化学药物治疗相比,臭氧治疗具有一定的优越性,为腰椎间盘突出症引起的腰腿痛的治疗提供了新的途径,但目前还没有其安全性监测的相关报道。
2014年,国家食品药品监督管理总局启动了医疗器械不良事件重点监测工作,并遴选了100个重点监测品种,臭氧治疗仪为监测品种之一。医疗器械不良事件(Medical Device administration events, MDaes)监测是确保上市后医疗器械安全有效的重要手段[10-13]。根据注册分类,医用臭氧治疗仪属于第三类医疗器械。本研究以臭氧治疗仪为重点监测对象,对其不良事件发生率、主要临床表现、处理和转归、主要影响因素进行分析评价,发现和识别上市后器械存在的不合理风险,为提升上市后医疗器械的安全监测预警能力,提升医疗器械质量标准,完善医疗器械推荐使用方案提供依据。
1 资料与方法
资料来源于国家药品不良反应监测中心2010年1月1日至2015年6月30日收集的全国所有与臭氧治疗仪(第三类)相关的不良事件报告,共47例。
采用描述性方法,对收集的臭氧治疗仪(第三类)不良事件报告进行统计分析。对所有收集报告的构成情况、上报单位情况进行统计分析;对与使用相关的不良事件分析其生产企业分布情况、患者人群基本信息、不良事件主要表现、严重程度分级、发生原因以及处理转归,全面系统的找出风险因素并提出相关控制建议。
2 结果
2.1 报告构成情况分析
2010年1月1日至2015年6月30日共收集全国所有与臭氧治疗仪(第三类)相关的医疗器械可疑不良事件报告,共47例,明确与使用臭氧治疗仪相关的不良事件为25例,6例明确与臭氧治疗仪的使用不相关,16例未明确不良事件发生是否与使用臭氧治疗仪相关。
2.2 上报单位构成比
47例臭氧治疗仪不良事件报告中,涉及的上报单位有20家,其中器械生产企业1家,上报6例(占12.00%);经营企业2家,上报6例(占12.00%);使用单位16家,上报33例(占72.00%);aDR中心1家,涉及2例(占4.00%)。
2.3 生产企业分布情况分析
25例相关的不良事件中,均明确记录了生产企业(图1),共涉及8家企业。其中7家企业为国内3个省份的生产厂家,1家为意大利生产厂家。国内3个省份的报告总数为23份,分别是山东省12份,河南省6份,山西省5份。由于没有各个企业臭氧治疗仪产品在国内的销售使用情况具体数据,因此无法判定产品或地域产品的不良事件发生率。

图1 臭氧治疗仪不良事件生产企业构成情况Fig.1 composition of different ozonic therapy instrument manufacturers which have occurred adverse events
2.4 不良事件患者人群基本情况分析
25例相关不良事件中,男性患者12例,女性患者8例,性别不详5例。20人注明患者年龄,年龄不详5人,年龄最小为14岁,最大为72岁,中位年龄为50.00岁。如图2,不良事件人群主要分布在40~80岁年龄段,占64.00%。
2.5 预期治疗疾病
25例相关不良事件中,记录了预期治疗疾病的有22例,主要用于治疗腰椎间盘突出症,具体分布见表1。说明书中的适应证为缓解腰椎间盘突出症引起的腰腿痛,因此中风后遗症、颈椎病、肝腹水均超出说明书使用范围。使用臭氧治疗这些超适应证疾病时,会加大不良反应发生率,临床医生应严格规范使用臭氧治疗。
2.6 不良事件表现

图2 臭氧治疗仪使用者年龄构成情况Fig.2 age composition of ozonic therapy device users

表1 使用臭氧治疗仪预期治疗疾病统计Tab.1 Statistics of using ozonic therapy instrument for expected diseases
全部25例可疑不良事件中,有15例记录了不良事件的表现,其余根据事件陈述判断不良反应事件表现。延误治疗是发生率最高的不良事件,占72.00%。不良反应表现与发生率见表2。
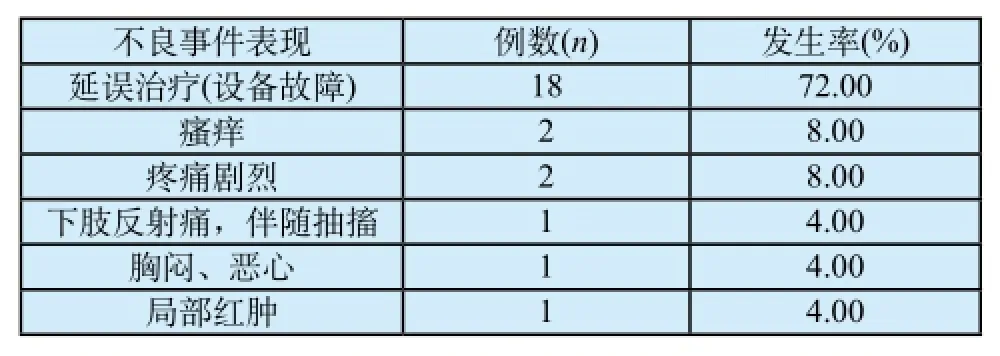
表2 不良事件表现Tab.2 clinical symptoms of adverse events
2.7 不良事件相关原因分析
25例相关不良事件中, 4例与患者因素有关,如臭氧引起过敏反应、心理因素等;3例可能与臭氧输出浓度有关;18例的原因为仪器故障,如机器内臭氧传输管路脱落、臭氧浓度不稳定、臭氧发生器故障、压力开关失效、采集阀漏气等。仪器故障引起的不良事件占比为72.00%,提示应企业应提高产品质量,保证仪器使用安全、有效。
2.8 不良事件的后果及处理措施
在25例可疑不良事件中,均记录了不良事件处理情况。3例不良事件后果为可能导致机体功能结构永久性损伤。2例疼痛加剧,1例是由于心理因素,通过医生和护士及工作人员的细心开导,使患者心情放松,休息之后疼痛缓解;1例行腰椎微创介入术,因局部电流不稳,出现下肢反射痛,伴随抽搐,患者感心慌,下肢乏力,术后行抗炎,脱水对症治疗,减少神经损伤。余22例处理措施为停止治疗或仪器检修。
2.9 未作关联性评价事件
16例未作关联性评价事件报道时间为2010年1月1日至2015年6月30日。其中,男性1例,女性15例。16例均记录了不良事件后果,2例局部皮肤起泡,可能是由于臭氧输出浓度过高引起,判断为可能导致机体功能结构永久性损伤和需要内外科治疗,其余处理措施为停止治疗或仪器检修。
3 讨论
由此次监测分析结果,臭氧治疗仪的不良事件与产品质量、患者体质、器械操作等因素有关,风险基本可控,后续工作中应加强药械监测人员培训、提高产品质量标准、完善说明书信息、注意产品使用风险,从而保障患者用械安全。
3.1 作用机理
臭氧用于治疗椎间盘疾病,其机理主要包括以下几个方面:①氧化作用:氧化髓核基质内的蛋白多糖,使其发生变性、坏死和萎缩,降低髓核内的渗透压,达到机械性减压的目的。②抗炎作用:释放拮抗炎症反应的免疫因子,扩张血管,促进炎症吸收。③镇痛作用:抑制损伤感受器纤维,刺激抑制性中间神经元,释放脑啡肽等镇痛性化学物质。
3.2 加强药械监测人员培训
在收到的全部47例不良事件报告中,6例确定不相关,16例未作关联性判断。相关的25例中,仅6例信息填写完善,其余报告均有一项以上重要项目缺项。在有不良事件经过描述的报告中,大部分信息填写简单,缺乏规范的填写格式,每份表之间填写内容及形式差别较大。药械相关注册信息、不良事件表现、初步原因分析、主要伤害等关键要素缺失或准确具体描述欠缺较多。因此在统计过程中部分项目,如预期治疗结果、不良事件发生原因分析,很难进行量化处理。建议加强监测人员规范化培训,尤其是使用单位药械监测人员培训,这样才能全面真实地反映药械使用的具体情况。
3.3 提高产品质量标准
25例相关不良事件中,器械故障引起的不良事件占比较高,提示企业应提高产品质量,加强工艺验证,保证器械使用安全、稳定。尤其是对臭氧输出浓度稳定性的考察和验证。
3.4 完善说明书信息
不同厂家说明书关键要素表述不一致:部分产品使用年限未在说明书中注明;用于缓解腰椎间盘突出症引起的腰腿痛的治疗时臭氧输出浓度未作限定;部分产品制备的臭氧浓度上限过高;内部管道使用年限未作标注;部分产品对取臭氧的注射器未作要求。建议开展相关研究,制定和提高行业标准。超说明书适应证使用时会加大风险,建议加强对禁忌证的收集与研究工作,以统一修订器械说明书中禁忌证内容。
3.5 注意器械使用风险
臭氧治疗应严格按照规范进行操作:①临床使用时应注意臭氧治疗的最大浓度、剂量,治疗浓度应控制在10 ~ 40 μg/mL,浓度过高会损坏纤维环,过低则氧化不充分,影响治疗效果;②治疗腰椎间盘突出症时,注意穿刺手法和部位,穿刺部位不适当,引起患者肌体无力及肌肉萎缩;③为避免局部组织坏死,同一部位注射次数应不超过3次;④控制制备的臭氧纯氧杂质含量,取气应进行过滤;⑤应及时发现和处理患者过敏反应。此外,还应监测环境臭氧浓度,注意未猝灭臭氧对医护人员呼吸系统,血液系统的影响,加强操作人员防护。
[1] 胡有谷. 腰椎间盘突出症[M]. 北京: 人民卫生出版社, 1995.
[2] 牟明威, 王泽茂, 何鹏宇. 传统手术与微创治疗腰椎间盘突出症的疗效比较[J]. 疑难病杂志, 2013, 12(9): 688-690.
[3] 王翔奕, 黄迅, 谭伦,等.腰椎间盘突出症臭氧治疗与保守治疗的疗效比较[J]. 中国矫形外科杂志, 2009, 17(19): 1514-1515.
[4] 缪洁, 赵金彩, 安永慧,等.微创手术与开放性手术治疗腰椎间盘突出症的疗效比较与并发症护理[J]. 中华现代护理杂志, 2014, 20(13): 159-162.
[5] al-Zain F, eisenschenk a, Killeen T, et al. Minimally invasive spinal surgery using nucleoplasty: a 1-year follow-up study[J]. acta Neurochir, 2008, 150(12): 1257-1262.
[6] Zhu H, cheng MH, Shen YX, et al. The efficacy of coblation nucleoplasty for protrusion of lumbar intervertebral disc at a twoyear follow-up[J]. Int orthopaedics, 2011, 35(11): 1677-1682.
[7] Maximilian eP, Nils a, Volker K, et al. Nucleoplasty, a minimally invasive procedure for disc decompression: a systematic review and meta-analysis of published clinical studies[J]. Pain Phys, 2014, 17(2): e149-173.
[8] 冯硝刚, 李坚. 医用臭氧治疗腰椎间盘突出症的进展[J]. 中国实用医药, 2010, 5(12): 263-265.
[9] 黄绍权, 向年虎, 张海江, 等. cT引导下臭氧治疗椎间盘突出的临床应用[J].中国辐射卫生, 2011, 20(1): 102-103.
[10] 吴斌, 吴建茹, 宋新康, 等. 广东省5地区医务人员医疗器械不良事件监测认知度调查[J]. 药物流行病学杂志, 2015, (2): 93-96.
[11] 张素敏. 我国医疗器械不良事件报告的影响因素探讨[J].中国药物警戒, 2008, 5(4): 205-207.
[12] 曲婷婷, 崔昊. 影响医疗器械不良事件监测在医疗机构中开展的因素探讨[J]. 中国医疗器械信息, 2010, 16(9): 47-66.
[13] 谢琼. 医疗器械风险管理应用的研究[J].中国医疗器械杂志, 2014, 38(6): 451-453.
Analysis of 47 Cases of Adverse Events of Ozonic Therapeutic Instrument
【 Writers 】ZHAO Ying1, HUANG Pu1, HUANG Hui2, ZHAO Li2, ZHENG Siwei1, SHI Chen1
1 Department of Pharmacy, Union Hospital, Tongji Medical College of Huazhong University of Science and Technology, Wuhan, 430022
2 Monitoring Center for Adverse Reaction of Drug and Medical Instrument of Hubei, Wuhan, 430022
ozonic, intervertebral disc protrusion, medical device, adverse events
R681.5
A
10.3969/j.issn.1671-7104.2016.03.016
1671-7104(2016)03-0214-03
2015-12-28
湖北省药品(医疗器械)不良反应监测中心项目(2015B4Q9)
赵瑛,e-mail: 23zhaoying@163.com
史琛,e-mail: 29136909@qq.com
【 Abstract 】With retrospective case study, this paper classified, summerized and evaluated 47 reports induced by ozonic therapeutic instrument. The results showed: 25 cases of adverse events were clearly related to the use of instruments; the cases mainly reported by equipment use enterprises; the delay treatment by instrument failure was the most common adverse event performances; adverse events might be relevant to the risk factors of product quality, technical operation, patient specifcity and instrument disinfection. Monitoring should be strengthened in order to reduce the ozonic therapeutic instrument adverse events and maintenance of public safety.

