壳聚糖对珠江口海域牡蛎酶解液中镉离子的脱除研究*
李衍森, 党爱翠
(1.国家海洋局 珠海海洋环境监测中心站,广东 珠海 519015;2.国家海洋局 南海分局南海环境监测中心,广东 广州 510300)
壳聚糖对珠江口海域牡蛎酶解液中镉离子的脱除研究*
李衍森1, 党爱翠2*
(1.国家海洋局 珠海海洋环境监测中心站,广东 珠海 519015;2.国家海洋局 南海分局南海环境监测中心,广东 广州 510300)
为了探究壳聚糖清除牡蛎中镉离子的最优条件,在单因素试验基础上采用响应面法对壳聚糖脱除酶解液中镉离子的关键参数进行了优化,单因素结果为振荡速率150 r/min、酶解液pH值为7.0、吸附时间50 min、壳聚糖添加量为8 mg/mL.从简化实验和节约能源的角度考虑,将振荡速率设定为150 r/min;对酶解液pH、吸附时间和CTS添加量三因素通过响应面Box-Behnken来进行工艺优化,最佳工艺为时间53.3 min、pH 7.6、添加量为8.4 mg/mL,预测脱镉率为61.8%.经验证在此条件下的脱镉率为(61.5±1.3)%,略小于预测值61.8%,这表明优化后的壳聚糖吸附条件对珠江口海域牡蛎酶解液中隔离子具有着较好的吸附作用.
壳聚糖;牡蛎酶解液;镉离子脱除;条件优化
镉是一种对人体和水生动物危害严重的重金属元素,具有残留时间长,可沿食物链转移蓄积和不可逆性等特点[1-2].它主要由人类活动产生,进入自然界.镉能溶于水体中或富集于沉积物,从而成为各种水生食物链的污染源.镉能够在鱼类、贝类和浮游生物等水生生物体内富集,损害生物体内的蛋白质,抑制酶的活性[3-4].珠海牡蛎销量大减,经海洋农渔和水务局对该区5个地方样品进行镉离子检测,结果显示桂山海域和市场样品低于规定限量,而横琴新区、金湾区、高栏港区样品分别超出规定限量0.69倍、1.36倍和1.00倍,表明当地部分牡蛎受到镉污染.牡蛎中重金属镉的严重超标对其生理活性、经济价值和使用安全带来了严重的影响.壳聚糖(Chitosan,CTS)是天然碱性多糖,化学结构较为独特,结构中具有羟基和氨基,对重金属具有较强的吸附能力[5].目前,壳聚糖及其衍生物在工业净水、食品、医药以及生活用品中取得了良好的进展.魏婉楚[6]研究发现壳聚糖及其衍生物对贝类中的镉离子脱除率达到90%以上,然而脱除剂加入,也带来了成本高、营养成分流失等弊端.因此,清洁、高效地对贝类中的镉离子进行清除具有重要的意义[7-8].本实验分析了壳聚糖对牡蛎匀浆酶解液中隔离子的吸附条件首先利用单因素试验对吸附条件进行了初步分析,并利用响应面试验对壳聚糖脱除隔离子的条件进行了优化,为牡蛎中隔离子的脱除方法提供实验依据.
1 材料与方法
1.1 材料与仪器
1.1.1 试验材料 牡蛎,珠海金湾区海鲜市场;胰蛋白酶、枯草杆菌酶,北京索莱宝科技有限公司;壳聚糖(CTS),脱乙酰度≥90%;NaOH、HCl等,国药集团化学试剂有限公司.
1.1.2 试验仪器 DKS-24型电热恒温水浴锅,嘉兴市中新医疗仪器有限公司;UB-7型pH计,丹佛仪器(北京)有限公司;BS110S型分析天平,赛多利斯(北京)教学仪器公司;Z-5000原子吸收光谱仪,日本日立公司;超纯水机,美国Millipore公司.
1.2 试验方法
1.2.1 牡蛎匀浆酶解液的制备 参考郭妍妍[9]等方法并略加改动,用匀浆机在5 000 r/min条件下匀浆,并先后用胰蛋白酶和枯草杆菌酶酶解牡蛎匀浆液,将酶解液在沸水浴中灭酶活10 min,在3 500 r/min条件下离心10 min,得到上清液即为牡蛎酶解液.
1.2.2 脱镉率的计算 酶解液用磷酸二氢胺(120 g/L)作为基体改进剂,石墨炉原子吸收光谱法测定镉的含量.脱镉率(%)=[(M1-M2)/M1]×100%,其中M1、M2分别为脱镉前后酶解液中镉离子的含量,将酶解液中的镉离子浓度稀释至4 μg/mL.
1.2.3 壳聚糖(CTS)脱除隔离子单因素实验 以脱镉率为指标,对影响吸附率的酶解液pH、振荡时间、CTS的添加量及振荡速度进行单因素实验.
(1) 酶解液pH单因素实验:吸取7份酶解液30 mL,分别向其中加入0.3 g壳聚糖,依次用0.1 mol/L的NaOH和HCl分别将pH值调整为2.5、4、5.5、7、8.5、10和11.5,在常温下振荡吸附30 min,振荡速率为150 r/min,测量隔离子含量,计算脱镉率.
(2) CTS吸附时间单因素实验:pH值为7.0,在常温下振荡吸附,时间分别为5,20,30,50,70,90 min,其他步骤同1.2.1.
(3) CTS的添加量单因素实验:pH值为7.0,吸附时间为50 min,CTS的添加量分别为2、5、8、10、13、16 mg/mL,其他步骤同1.2.1.
(4) 振荡速率单因素实验:pH值为7.0,吸附时间为50 min,CTS的添加量为8.0 mg/mL,振荡速度分别设定为40、80、120、150、190、230、270 r/min,其他步骤同1.2.1.
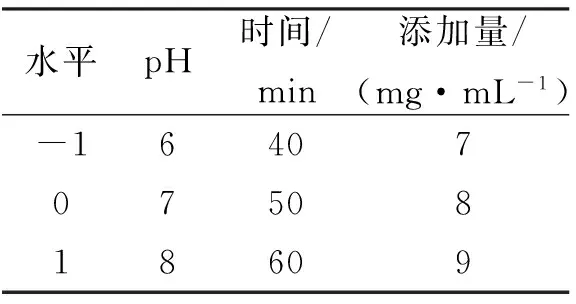
表1 壳聚糖脱除条件优化的响应面实验设计Tab.1 The experimental design for response surface experimental conditions of chitosan to remove
1.2.4 响应面优化吸附条件 当振荡速率为150 r/min与190 r/min时,脱镉率分别为(59.6±1.1)%和(60.4±1.4)%,两组之间不存在着显著性差异(p>0.05),这表明振荡速率对脱镉率的影响不大,从优化实验和节约能源的角度考虑,将振荡速率设定为150 r/min.对酶解液pH、吸附时间和CTS添加量三因素通过响应面Box-Behnken来进行工艺优化,确定最优镉离子吸附条件,实验因素水平见表1.
1.2.5 数据处理 采用Microsoft Excel软件和SAS软件Design-Expert 7.0.0进行响应面数据分析.若p>0.05,则差异不显著;若p<0.05,则差异显著;若p<0.01,则差异极其显著.
2 实验结果
2.1 单因素实验
2.1.1 酶解液的pH值对CTS脱镉率的影响 通过图1(a)可知,CTS对镉离子的吸附率随着pH的增加出现先升后降的趋势,在pH为7.0时,脱镉率最高为(53.2±1.1)%.当酶解液过酸时,会释放出更多的H+,H+会与镉离子产生竞争性的吸附作用,这不利于氢氧根和氨根对镉离子的吸附螯合作用;随着pH值的升高,会形成氢氧化镉沉淀,有助于CTS对镉离子的吸附,但是碱性过强不利于镉离子从酶解液中解离出来,CTS的脱镉率降低.所以,当酶解液的pH值维持在中性范围时,CTS脱镉率最高.
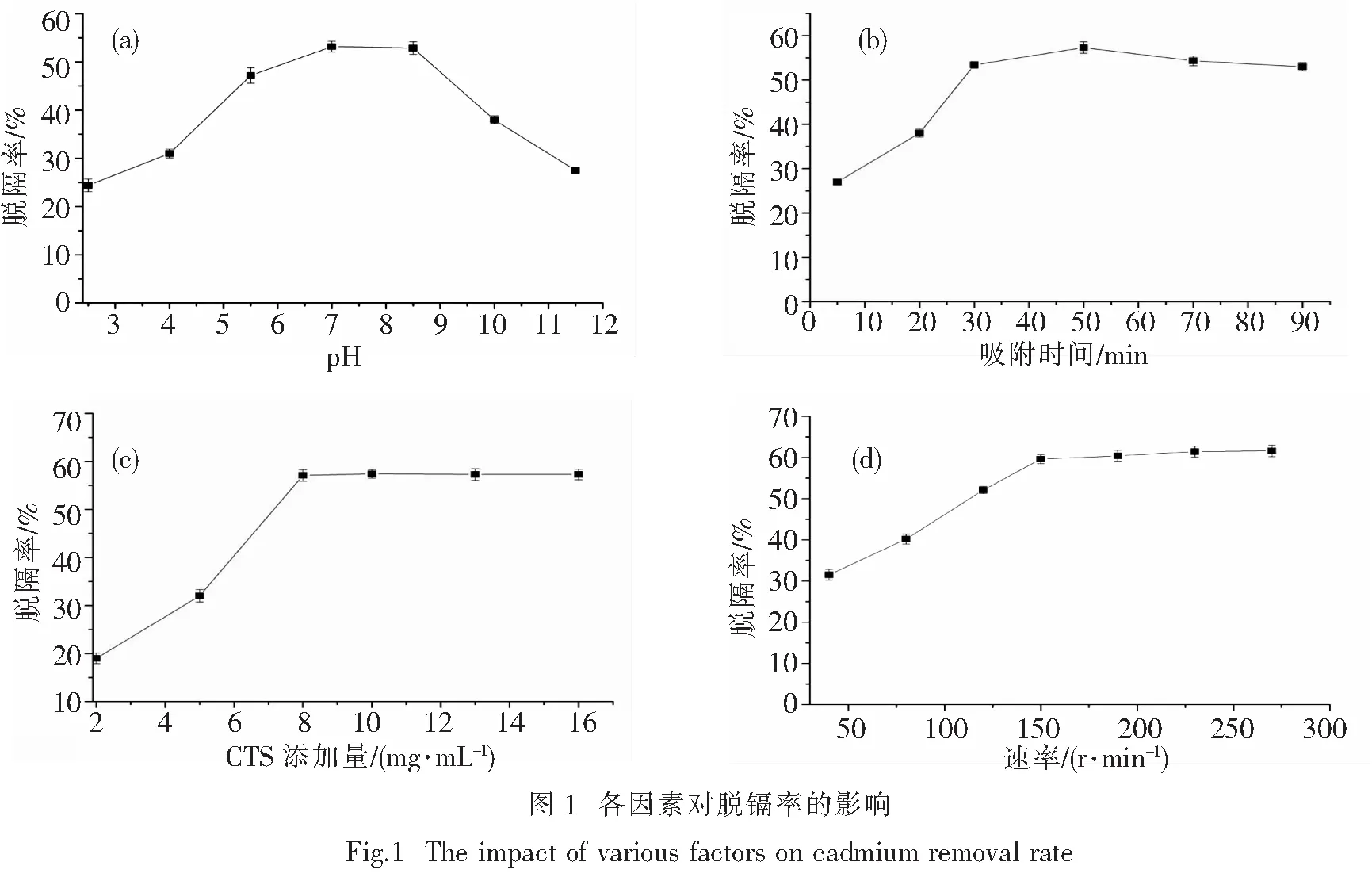
2.1.2 CTS吸附时间对脱镉率的影响 通过分析图1(b)可知,CTS对脱镉离子的吸附率随着时间的延长出现先升后降的趋势,在吸附时间为50 min时,脱镉率最大为(57.3±1.3)%,此时对镉离子的吸附已经达到饱和.当吸附时间为90 min时吸附率为(53.0±0.9)%,下降较为明显.这是由于CTS发生部分降解,吸附率下降.
2.1.3 CTS添加量对脱镉率的影响 通过图1(c)可知,CTS添加量在2~8 mg/mL时,脱镉率迅速提高,但随着剂量逐渐提高,脱镉率基本持平,这表明CTS添加量在8 mg/mL时,对镉离子的吸附已经达到饱和.
2.1.4 振荡速率对脱镉率的影响 通过图1(d)可知,在振荡速率为40~150 r/min时,脱镉率迅速提高至(59.6±1.1)%,这表明随着振荡速度的提升,加快了分子之间的运动速率,有助于镉离子与复合物之间的接触,加快了螯合吸附作用.但是随着振荡速率的增加,镉离子的脱除率已不再显著增加,这表明振荡速率继续增加,不会对脱镉率造成较大影响.
2.2 响应面优化实验结果
2.2.1 壳聚糖对镉离子吸附条件分析和优化 对酶解液pH、吸附时间和CTS添加量三因素通过响应面Box-Behnken来进行工艺优化,确定最优吸附工艺,实验结果如表2和表3所示.
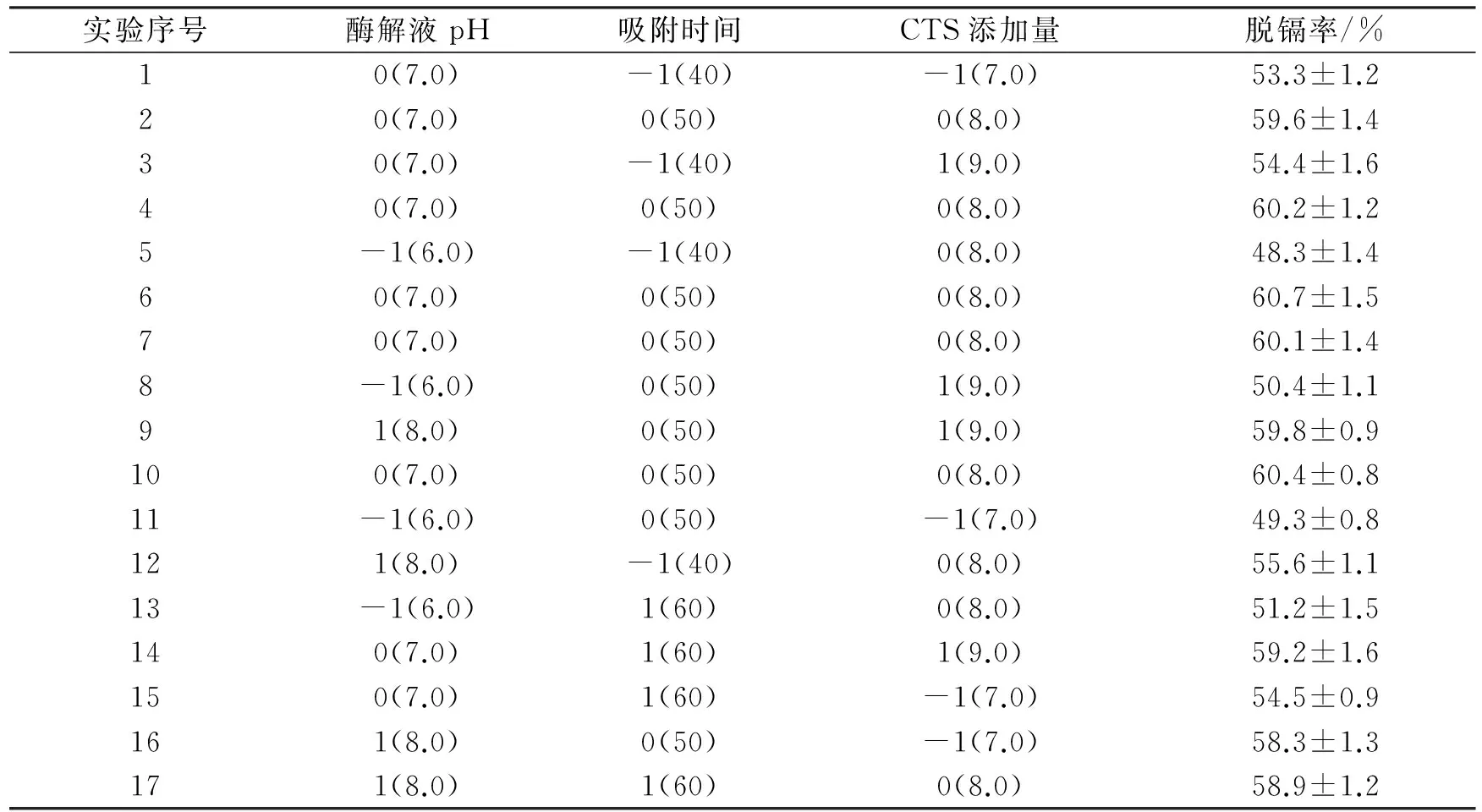
表2 响应面实验表及结果Tab.2 The design and results of Response surface experiments
2.2.2 方差分析 获得壳聚糖吸附工艺的回归方程:
脱镉率(%)= 60.2 + 4.18A+ 1.53B+ 1.05C+ 0.100AB+ 0.100AC+ 0.90BC- 3.80A2- 2.90B2- 1.95C2,其中,A、B、C分别表示pH、吸附时间、添加量.
由表3方差分析得出,该模型Prob>F(a),F(a)小于0.01,表明本模型是极显著的.失拟项(lack of fit)表示模型预测值与实际值不拟合的概率.表3中壳聚糖吸附条件的模型失拟项的Prob>F(a),F(a)为0.066 3,大于0.05,模型失拟项不显著,模型选择合适,可以用此模型对壳聚糖对镉离子吸附条件的工艺优化.
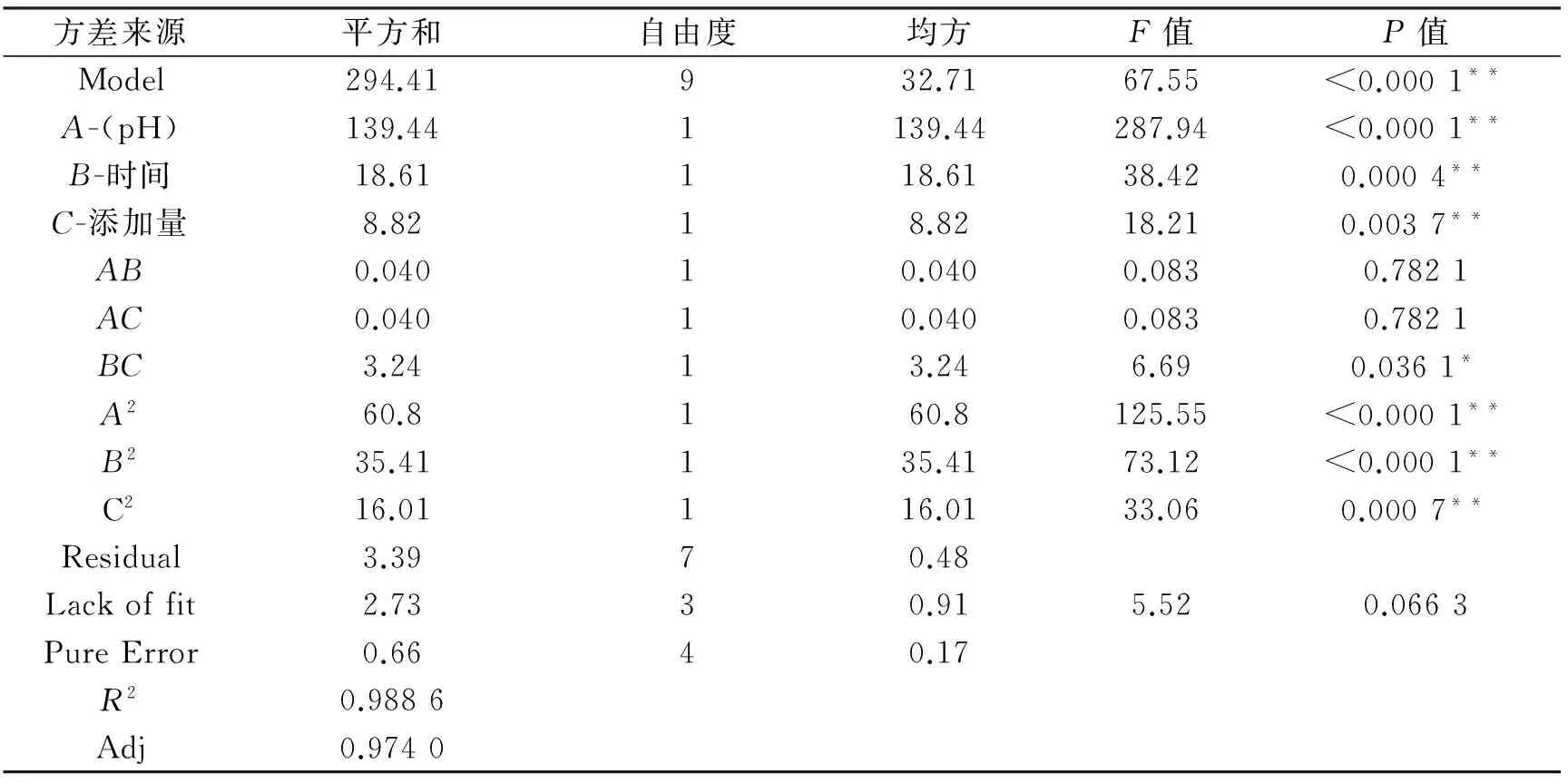
表3 响应面方差分析Tab.3 Analysis the response surface of variance
注:(a)P-value Prob>F,F的大小表示模型及各因素的显著水平;
(b)P-value Prob>F,F大于0.05,表示模型及各因素无显著影响,P-value Prob>F,F小于0.05表示模型及各因素有显著影响,P-value Prob>F,F小于0.01表示模型及因素有极显著影响.
从回归方程及表3和图2~图4来看,AB、AC对壳聚糖吸附影响不显著,A、B、C、A2、B2、C2对壳聚糖吸附有极显著影响,BC对壳聚糖吸附有显著影响.回归方程优化后得:
脱镉率(%)= 60.2 + 4.18A+ 1.53B+ 1.05C+ 0.90BC- 3.80A2- 2.90B2- 1.95C2.其中,A、B、C分别表示pH、吸附时间、添加量.
2.2.3 交互作用分析与优化
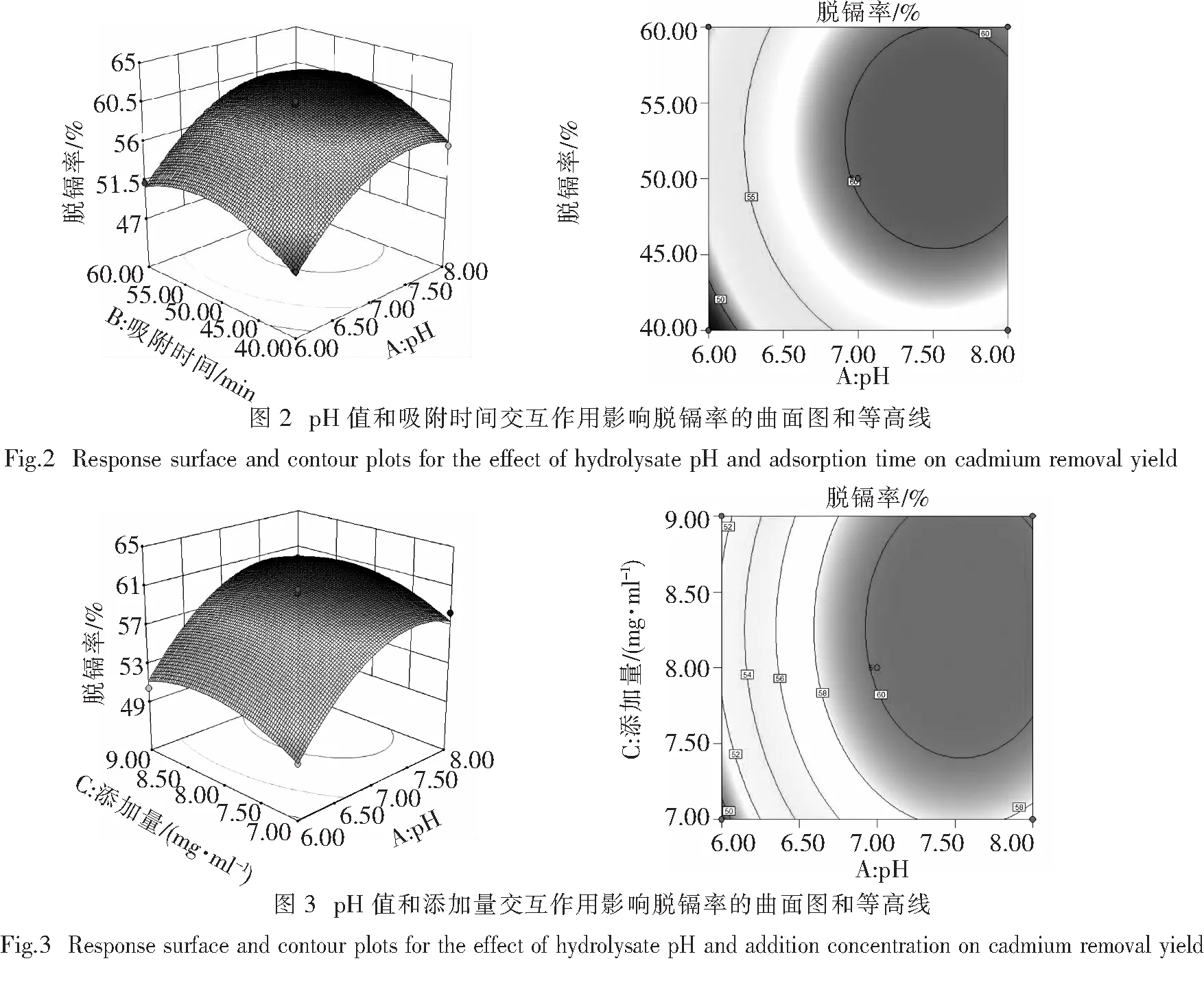
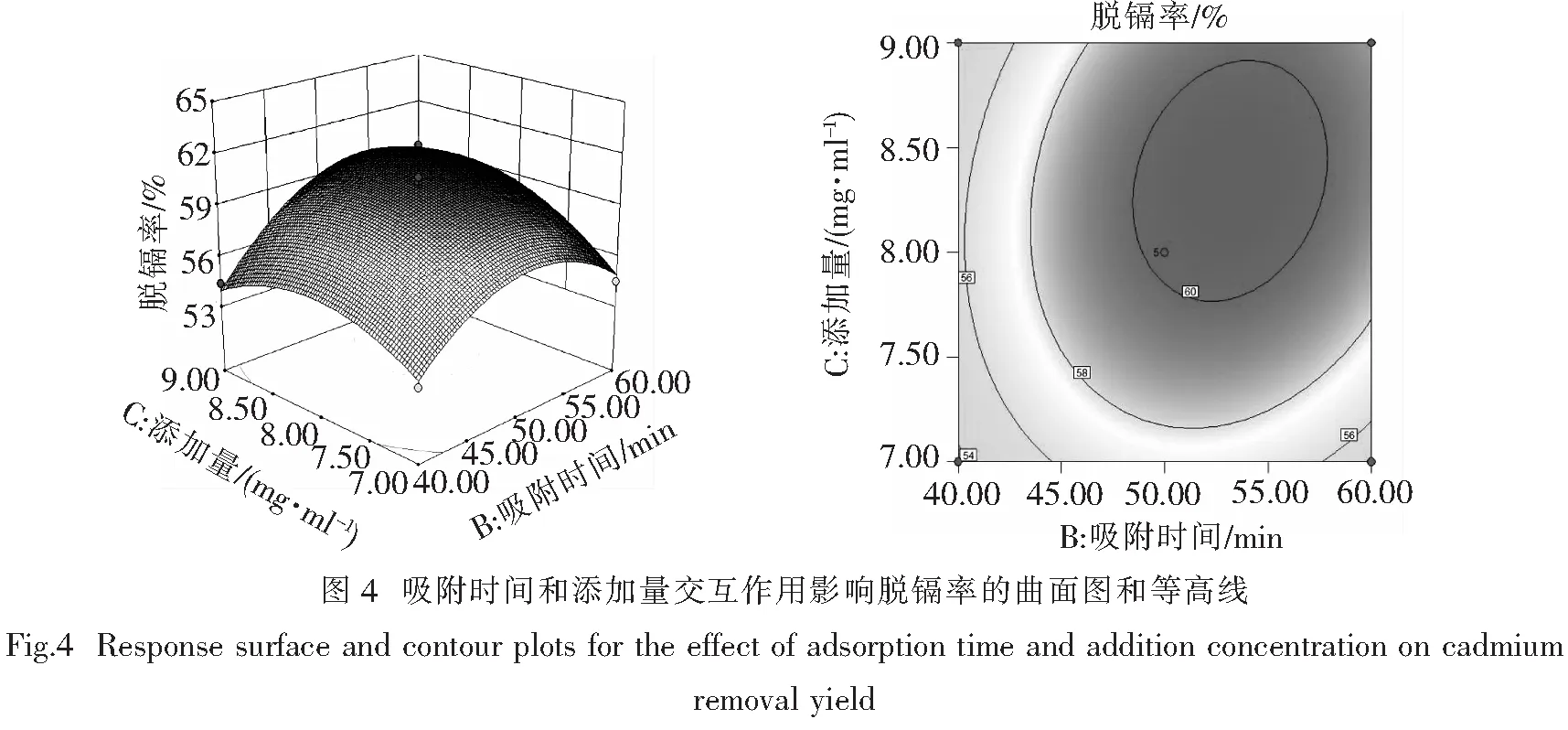
通过Design-Expert软件求解方程,对于壳聚糖吸附镉离子,吸附时间、添加量和pH值都会对镉离子的脱除率产生较大的影响.由实验可知,壳聚糖脱除镉离子的最佳工艺为吸附时间53.28 min、酶解液pH 7.56、CTS添加量8.36 mg/mL,预测脱镉率为61.80%.
2.2.4 验证实验 将壳聚糖脱除镉离子的最佳工艺调整为吸附时间53.3 min、酶解液pH 7.6、CTS添加量8.4 mg/mL,验证壳聚糖的脱镉率.经验证,在此条件下的脱镉率为(61.5±1.3)%,略小于预测值61.8%,其误差范围在1%之内.说明壳聚糖脱除镉离子工艺优化效果较好.
3 讨 论
本文对壳聚糖对珠江口海域牡蛎酶解液中镉离子吸附条件进行优化,在吸附时间53.3 min、酶解液pH 7.6、CTS添加量为8.4 mg/mL时,对酶解液中隔离子的脱镉率为(61.5±1.3)%.经检测,珠江口海域牡蛎中隔离子的含量为2.94 mg/kg,超过了食品安全国家标准《食品中污染物限量》(GB2762—2012)中规定的水产品贝(双壳)类中重金属镉限量2.0 mg/kg.本文通过对壳聚糖吸附条件的优化,脱镉率达到(61.5±1.3)%,而酶解液中隔离子浓度稀释为4 μg/mL,经壳聚糖吸附后,隔离子浓度为1.54 μg/mL,对镉离子的吸附效果较好.
关于壳聚糖及其复合物对镉离子的吸附作用,梁鹏[10]模拟了壳聚糖对含镉水溶液中镉离子的吸附作用,通过条件优化,其对隔离子的吸附率达到了98.0%,壳聚糖对含镉水溶液中镉离子的吸附效果较好.张井[11]研究了OU-2型大孔吸附树脂对北太平洋鱿鱼内脏酶解中重金属镉的吸附情况,吸附后酶解液中镉残留量低于0.1 mg/kg.本文的研究与其他学者之间存在着一定的差异,这可能是因为实验材料、实验方法等原因造成的.通过对壳聚糖脱除牡蛎酶解液中镉离子条件进行优化,镉离子的脱除效果较好,其对水产品重金属污染去除效果较好,应用价值较大.
[1] 吴小胜, 魏帅, 魏益民, 等. 镉肾脏毒性生物标志物的研究进展[J].环境与健康, 2011, 23(9): 739-742.
[2] VILLANUEVA M J, YOKOYAMA W H, HONG Y J, et al. Effect of high-fat dirts supplemented with okara soybean by-product on lipid profiles of plasma, liver and faeces in Syrian hamsters[J]. Food Chemistry, 2011, 124(1): 72-79.
[3] 江天久, 牛涛. 重金属Cu2+, Pb2+和Zn2+胁迫对近江牡蛎(Crassostrea rivularis) SOD活性影响研究[J]. 生态环境, 2006, 15(2): 289-294.
[4] 陈海刚, 林钦, 蔡文贵, 等. 3 种常见海洋贝类对重金属Hg、Pb和Cd的积累与释放特征比较[J]. 农业环境科学学报, 2008, 27(3): 1163-1167.
[5] CRINI G. Recent developments in polysaccharide-basedma-terials used as adsorbents in waste water treatment[J]. Progress Polymer Science, 2005, 30(1): 38-70.
[6] 魏婉楚. 壳聚糖的改性及其应用[J]. 中山大学研究生学刊, 2013,34(1): 1-12.
[7] 梁鹏, 吴晓萍, 徐慧, 等. 壳聚糖脱除牡蛎匀浆液中重金属镉的初步研究[J]. 食品工业科技, 2010, 31(7): 107-109.
[8] 许爱清, 向言词, 李会东. 运用丝状真菌生物吸附镉(Ⅱ)污染物的研究[J].环境科学与技术, 2013, 36(4): 55-61.
[9] 郭妍妍,吴红棉,衣美艳,等. 壳聚糖复合物对近江牡蛎糖胺聚糖中镉的脱除[J]. 食品科学,2014,35(12): 46-53.
[10] 梁鹏, 吴晓萍,徐慧,等. 壳聚糖脱除牡蛎匀浆中重金属镉的初步研究[J]. 食品科技,2010,7(31):107-110.
[11] 张井. 北太平洋鱿鱼内脏酶解液中重金属镐的脱除研究[D]. 青岛:中国海洋大学, 2009.
责任编辑:龙顺潮
Chitosan for Removal of Cadmium from Oyster Hydrolyzate of Pearl River Estuary
LIYan-sen1,DANGAi-cui2*
(1.Zhuhai Central Station of Marine Environmental Monitoring,State Oceanic Administration,Zhuhai 519015;2.South China Sea Branch ,State Oceanic Administration,Guangzhou 510300 China)
In order to explore the optimal conditions of chitosanlear cadmium,on the basis of single-factor experiments, the key parameters of adsorption conditions were optimized by response surface method for hydrolyzate of cadmium ions.The operating conditions were: rate of 150 r/min, pH value of 7.0, adsorption time 50 min and CTS dosage 8 mg/mL. From the experimental simplification and energy conservation point of view, the oscillation rate was set to 150 r/min; the three-factor which were pH of hydrolyzate, adsorption time and CTS added concentration of Box-Behnken response surface to process optimization. The optimum were:oscillation rate of 150 r/min, pH value of 7.6, adsorption time 53.3 min and CTS dosage 8.4 mg / mL, the prediction cadmium removal was 61.80%. Proven under these conditions, the removal rate of cadmium(61.5 ± 1.3)%, slightly less than the predicted value of 61.8%.This suggests that chitosan adsorption conditions optimized for the Pearl River Estuary in hydrolyzate spacer having a good adsorption.
chitosan;oyster hydrolyzate;cadmium removal;optimization
2016-05-24
南海分局海洋科学技术局长基金(1352)
党爱翠(1983-)女,广西 贵港人,博士,工程师.E-mail:liyansen21@sohu.com
TQ91
A
1000-5900(2016)03-0048-06

