MnO2/碳纳米球电化学超级电容器电极材料的制备与性能研究
江 超, 李 君, 陶令令, 黄金萍
(上海师范大学 生命与环境科学学院,上海 200234)
MnO2/碳纳米球电化学超级电容器电极材料的制备与性能研究
江 超, 李 君, 陶令令, 黄金萍
(上海师范大学 生命与环境科学学院,上海 200234)
利用水热法合成了纳米棒状的MnO2/碳纳米球(CNPs)作为电化学超级电容器的电极材料.利用场发射扫描电镜(FESEM)、X射线衍射光谱分析(XRD)对样品的微观形貌、物相进行分析;利用循环伏安法和恒电流充放电测试材料的电化学性能.结果表明:纳米棒状MnO2/CNPs复合材料具有良好的电化学性能.在0.1 A/g的电流密度,1 mol/L Na2SO4电解液中,电极材料的比电容高达305.6 F/g,远高于纯碳球的比电容(49.3 F/g),当电流密度增至5 A/g时,材料的比电容为235 F/g,比电容仍能保持76.9%.
水热合成; MnO2/CNPs; 电化学超级电容器; 电极材料
0 前 言
超级电容器又称为电化学电容器,由于其具有高的功率密度,快速充放电,良好的循环稳定性等特征逐渐成为重要的能量储存装置.电化学电容器根据原理可分为两种不同的类型:双电层电容器和赝电容器.双电层电容器是通过在电极/电解液表面进行静电电荷的吸附分离来储存电荷.赝电容器是在电极材料表面发生高度可逆的氧化还原反应来储存电荷[1-2].电化学电容器的电极材料主要有碳基材料、过渡金属氧化物和导电聚合物.不同的电极材料都有自身的优缺点:碳基材料具有良好的导电性,高的功率密度和循环稳定性.金属氧化物的导电性较差[3],但比碳基材料具有更高的能量密度[3-4].为了改善这些不足,人们用过渡金属氧化物修饰碳基材料形成C@金属氧化物复合材料[1],如:MnO2/CNT[5]、MnO2/GO[6]、rGO@CNTs@MnO2[7]等等,以提高电极材料的电化学性能.
在过渡金属材料中,MnO2对环境无污染,资源丰富,价格低廉[8]且具有高的电化学理论容量(1 370 F/g)[9]等优点而受到广泛关注.MnO2与碳基材料的复合是电化学电容器电极材料的研究热点.利用MnO2高的电容量以及碳基材料良好的导电性和循环稳定性,通过MnO2修饰碳基材料,提高复合材料的电化学性能.MnO2与碳基材料的复合制备已有很多报道,Zhang等[10]利用水热合成法,有效地制备了MnO2/Ketjen Black(KB)复合材料,在1 mol/L Na2SO4电解液,5 mV/s扫描速度下比电容为252 F/g;Rakhi等[11]合成了石墨烯/MnO2/CNTs复合材料,在20 mV/s的扫描速度下比电容高达308 F/g;Chen等[6]利用水热法合成了针状MnO2/GO复合材料,在1 mol/L Na2SO4电解液,0.15 A/g的电流密度下比电容值为216 F/g.
本文作者采用三聚氰胺甲醛树脂球作为碳源,利用水热法合成纳米棒状的MnO2/C复合材料.通过X射线衍射(XRD),场发射扫描电镜(FESEM)研究复合材料的结构特征和微观形貌,采用X射线光电子谱(XPS)分析元素的化学价态以及在1 mol/L Na2SO4电解液中的电容性能.研究发现,在0.1 A/g的电流密度下,纳米棒状MnO2/碳纳米球(CNPs)比电容高达305.6 F/g,当电流密度增大至5 A/g时,比电容为235 F/g,仍保持76.9%.
1 实 验
1.1 三聚氰胺甲树脂碳球的制备
将0.54 g聚乙烯醇(PVA 1750)溶于90 mL去离子水中,升温到150 ℃直至PVA完全溶解,停止加热,待溶液降到室温.取2.8 g三聚氰胺溶于5.5 mL甲醛溶液中,升温到60 ℃并搅拌直至溶液变透明.将聚乙烯醇溶液与三聚氰胺乙二醛溶液混合,并加入1.2 mL的乙酸,60 ℃继续加热搅拌直至出现悬浮液.在10 000 r/min下离心20 min,得到固体样品,并用去离子水和无水乙醇反复洗涤,将所得沉淀物放入60 ℃干燥箱中干燥12 h.将所得产物放入管式炉中,在氮气保护下,5 ℃/min升温到700 ℃煅烧5 h得到黑色固体粉末.
1.2 纳米棒状MnO2/CNPs复合材料的制备
合成MnO2/CNPs是在如下的氧化还原基础上的[12]:
4KMnO4+ 3C + H2O → 4MnO2+ 2KHCO3+ K2CO3.
取0.1 g黑色固体粉末溶于35 mL,0.1 mol/L KMnO4溶液中,超声30 min,将混合液倒入内衬聚四氟乙烯的不锈钢反应釜内,于180 ℃恒温反应35 min.冷却至室温,并用乙醇和去离子水洗涤,将所得固体放入60 ℃干燥箱中干燥12 h.干燥后的固体样品简记为CMNs-180.
按照上述同样的制备条件,改变反应的温度(160、140、120 ℃),所得的固体样品分别记为CMNs-160,CMNs-140,CMNs-120.
1.3 结构表征和电化学性能测试
利用FESEM对样品形貌进行表征.采用X射线衍射仪(CuKα辐射,管电流40 kV,管电流30 mA)对合成的样品进行物相分析,衍射峰扫描范围为10°~80°,扫描速度为5(°)/min.利用XPS检测样品中元素的化学价态.利用比表面积测试测定仪器(NOVA 4000e)对样品的比表面积和孔径分布进行表征.利用电化学工作站(科斯特CS310)进行循环伏安和恒电流充放电测试.以1 mol/L Na2SO4为电解液,辅助电极为铂片,参比电极为饱和甘汞电极进行三电极体系测试.
1.4 工作电极的制备
将合成的活性材料、乙炔黑和聚偏氟乙烯(PVDF)按质量比80∶15∶5混合,充分研磨,取适量的N-甲基-二吡咯烷酮作为溶剂,将混合的样品调制成浆糊,用移液枪将样品涂覆在1 cm×1 cm滚压处理过的泡沫镍片上,然后在真空干燥箱中110 ℃下干燥12 h.
2 结果与讨论
2.1 SEM观察
图1为纯的碳球和不同温度下MnO2/CNPs复合材料.从图1(a)可以看出合成的三聚氰胺甲醛树脂碳化后得到表面光滑,分散均匀的小球,并且纳米碳球的直径为1.3~1.4 μm.图1(b)~(e)表示的是MnO2/CNPs复合材料在不同的温度下随着水热反应的进行,在光滑的碳球表面得到不同形态的MnO2晶体.当水热反应温度为180 ℃时,在碳球表面形成颗粒较小的MnO2纳米粒子,并且MnO2纳米粒子的直径为50~100 nm.当反应温度在160 ℃时,在碳球表面形成分散均匀,粒径为200~ 300 nm的MnO2纳米棒.随着反应温度的降低,140、120 ℃时,在碳球的表面形成无序大块的MnO2纳米粒子.从SEM图中可看出,在水热反应中碳球和MnO2形成核壳结构,不同的反应温度下,在碳球表面得到不同形态的MnO2纳米粒子,随着反应温度的降低,形成的MnO2纳米粒子直径逐渐增大.

图1 (a)碳球;(b)CMNs-180;(c)CMNs-160;(d)CMNs-140;(e)CMNs-120复合材料的SEM图
2.2 X射线衍射光谱分析
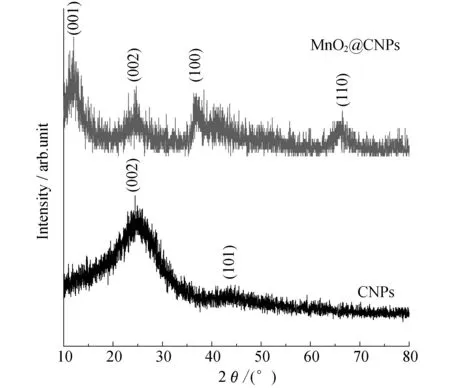
图2 碳材料和MnO2/CNPs的X射线衍射图谱
图2是三聚氰胺乙二醛树脂碳化材料和MnO2/CNPs复合材料的XRD图谱.对于树脂碳化材料,碳材料在23°和43°出现衍射峰,分别对应于碳材料的(002)和(101)晶面[13],说明三聚氰胺乙二醛树脂材料在N2保护,700 ℃煅烧5 h的条件下,已经完全石墨化.对于MnO2/C复合材料,在12.3°,24.7°,36.7°,65.8°可以明显地观察到4个特征衍射峰,分别对应于(001),(002),(100)和(110)晶面.在2θ=12.3°时,利用布拉格方程计算得到复合材料的层间距为0.72 nm和文献中表述的一致[14],也说明了MnO2是由碳和KMnO4之间发生氧化还原反应形成的.
2.3 XPS分析
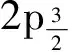
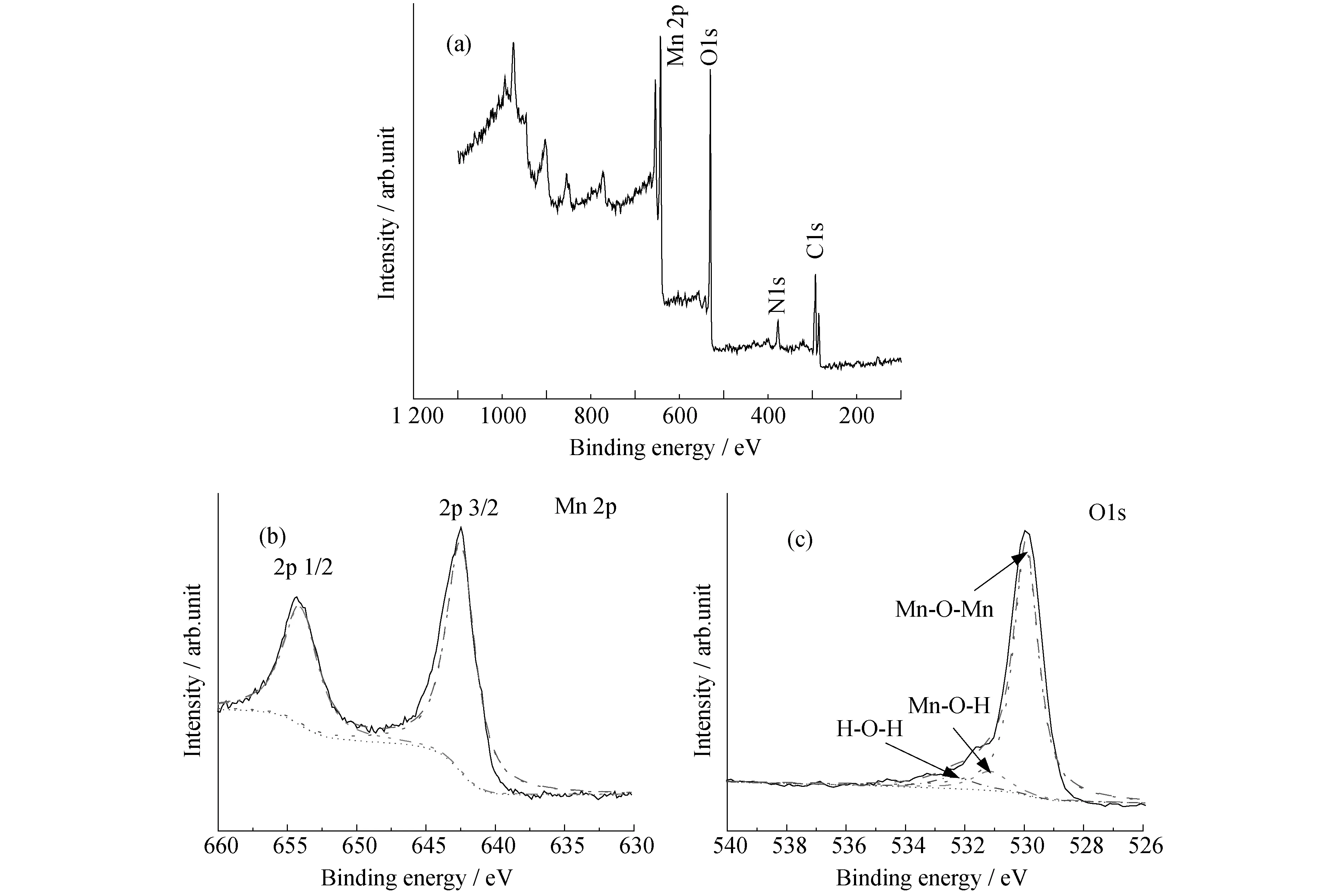
图3 MnO2/CNPs复合材料的XPS图谱.(a)复合材料全峰图谱;(b)Mn 2p;(c)O 1s
2.4 比表面积分析
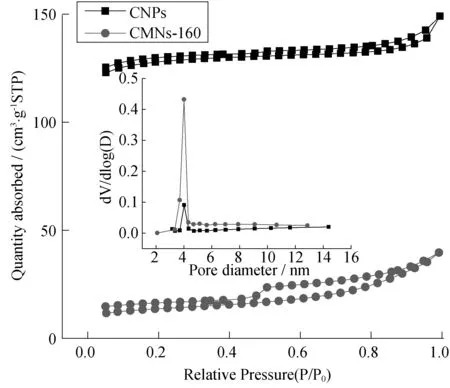
图4 碳球和MnO2/CNPs复合材料的BET分析
图4为碳球和MnO2/CNPs复合材料的比表面积测试分析.从图4中可以看出碳球和MnO2/CNPs复合材料的N2吸附脱附等温线属于Ⅳ型等温线,表明合成的材料存在一定的介孔.在吸附和脱附等温线之间形成的回滞环属于H3类型,表明存在的介孔属于裂缝孔类型[17].利用BET方程和BJH方程可以计算出碳球和CMNs-160(160 ℃水热条件下合成的MnO2/CNPs复合材料)的比表面积和孔径分布,从表1中可以看出碳球的比表面积为389.4 m2/g,CMNs-160的比表面积只有44.8 m2/g,这是因为MnO2附着在碳球的表面掩盖了碳球的裂缝孔,从而导致复合材料的比表面积下降.从平均孔径分布上看,碳球和复合材料的孔径大小相似,表明MnO2是在碳球的表面形成的.

表1 碳球和MnO2/CNPs复合材料比表面积和孔径分布
2.5 循环伏安测试
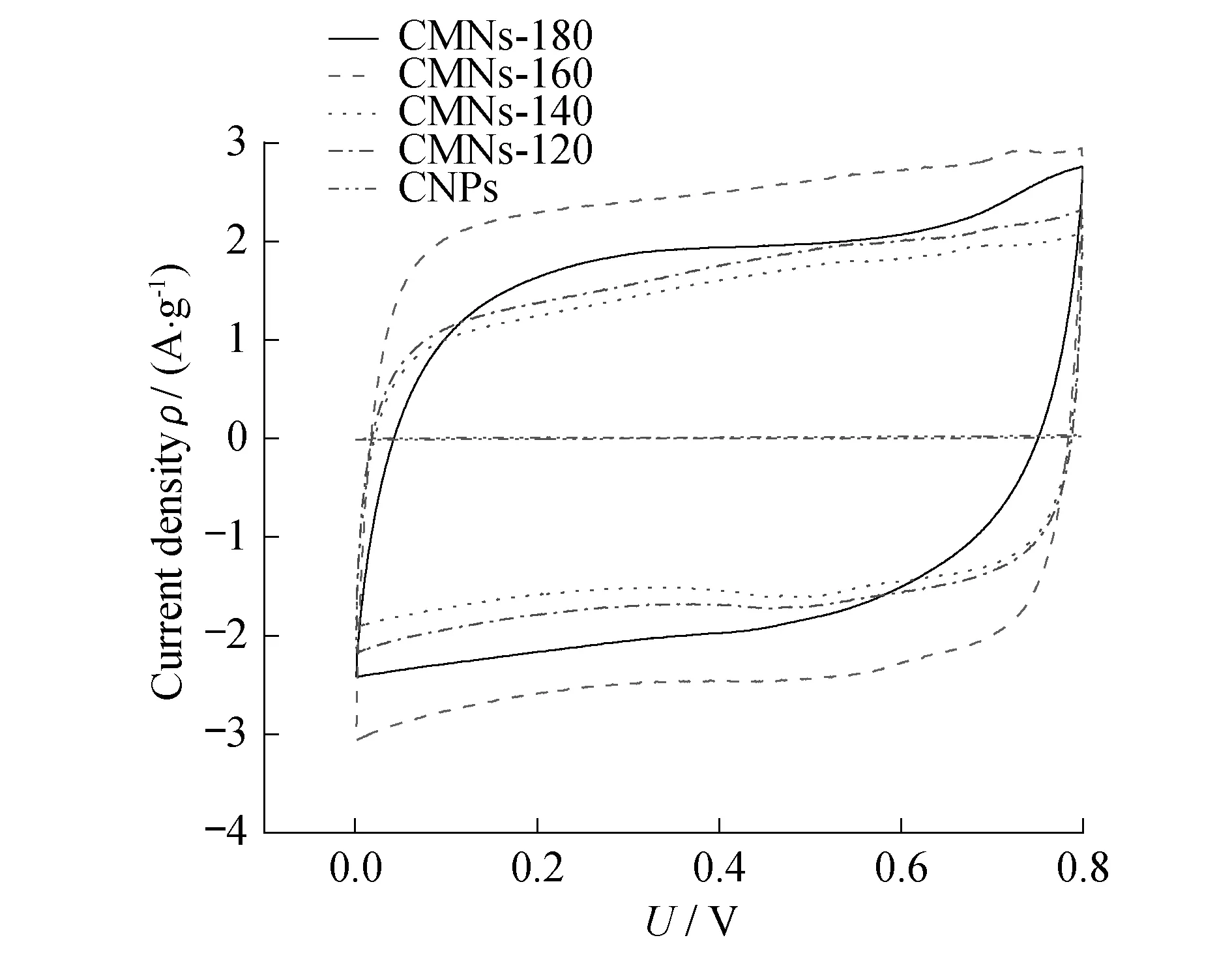
图5 碳球和CMNs-180,CMNs-160,CMNs-140,CMNs-120在10 mV/s扫描速度下的循环伏安曲线
图5是碳球和不同温度下合成的MnO2/CNPs复合材料在1 mol/L Na2SO4电解液中,电压窗口为0~0.8 V,扫描速度是10 mV/s时的循环伏安曲线.从CV曲线可知,对于碳球,在曲线上没有明显的氧化还原峰,并且CMNs-180,CMNs-160,CMNs-140,CMNs-120的循环伏安曲线接近对称的矩形形状,这表明活性电极材料具有良好的双电层电容特性以及可逆的氧化还原反应.
2.6 恒电流充放电测试
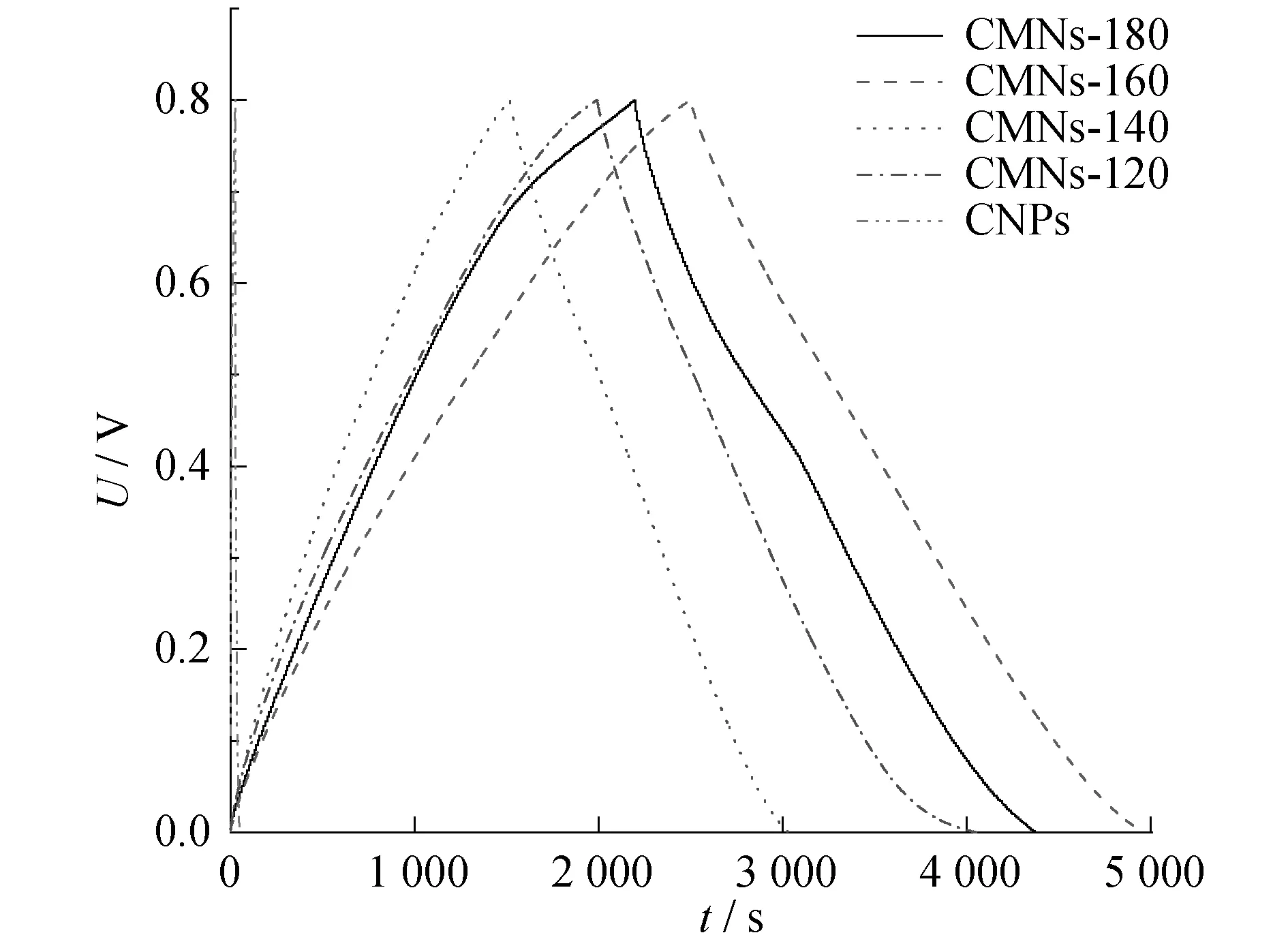
图6 碳球和CMNs-180,CMNs-160,CMNs-140,CMNs-120在100 mA/g电流密度下的恒电流充放电曲线
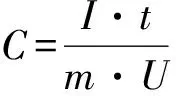
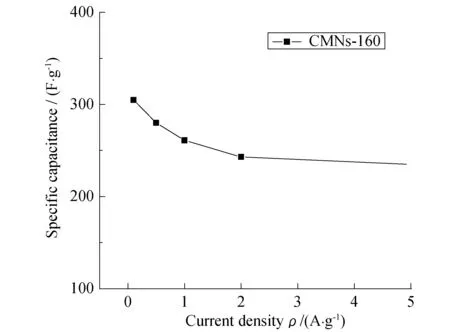
图7 CMNs-160在不同电流密度下的比电容计算值
图7为在0.1~5 A/g电流密度下CMNs-160的比电容计算值.在5、2、1、0.5和0.1 A/g电流密度下,通过比电容公式计算得到CMNs-160的比电容值分别为235、243、261、280和305.6 F/g.在5 A/g的电流密度下电容量仍能保持76.9%.在高的电流密度下,活性材料具有较小的比电容值,这是因为电极材料在高的电流密度下有一定的欧姆电压降[18].
2.7 循环稳定性测试
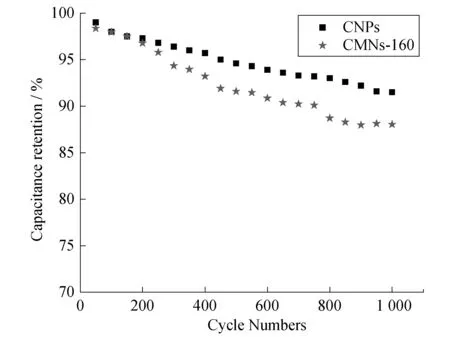
图8 碳球和CMNs-160的1 000次循环稳定测试
电极活性材料的循环稳定性测试是在1 mol/L Na2SO4电解液中,1 A/g的电流密度,0~0.8 V的电位窗口下进行的1 000次循环测试.图8为碳球和CMNs-160的1 000次循环稳定性测试,经过1 000次循环测试后,碳球比电容保持率为91.5%,CMNs-160比电容保持率为88.04%.由图8可知,碳球比CMNs-160复合材料的循环稳定性要好,这是因为碳材料在电解液中通过静电电荷吸附储存能量,MnO2/CNPs复合材料不仅通过静电电荷吸附储存电荷也通过MnO2的氧化还原反应储存电荷,所以复合材料的循环稳定性较差.
3 结 论
采用水热法合成了纳米棒状MnO2与纳米碳球的复合材料.研究发现,这种独特的结构提高了复合材料的电化学性能,在0.1 A/g的电流密度下,纯纳米碳球的比电容为49.3 F/g,而纳米棒状MnO2与碳球复合材料比电容为305.6 F/g,即使在5 A/g的电流密度下复合材料的电容量仍能保持76.9%.纳米棒状MnO2/CNPs优异的电容性能表明其是理想的电化学电容器电极材料.
[1] Yuan L Y,Lu X H,Xiao X,et al.Flexible solid-state supercapacitors based on carbon nanoparticles/MnO2nanorods hybrid structure [J].Acs Nano,2012,6(1):656-661.
[2] Zhao Y,Meng Y N,Jiang P.Carbon@MnO2core-shell nanosphere for flexible high-performance supercapacitor electrode materials [J].Journal of Power Sources,2014,259:219-226.
[3] Jiang H,Ma J,Li C Z.Mesoporous carbon incorporated metal oxide nanomaterials as supercapacitor electrodes [J].Advanced Materials,2012,24(30):4197-4202.
[4] Zhou H,Zhang Y R.Electrochemically self-doped TiO2nanotube arrays for supercapacitors [J].Journal of Physical Chemistry C,2014,118(11):5626-5636.
[5] Tang Q Q,Chen M M,Yang C Y,et al.Enhancing the energy density of asymmetric stretchable supercapacitor based on wrinkled CNT@MnO2cathode and CNT@Polypyrrole anode [J].Acs Applied Materials & Interfaces,2015,7(28):15303-15313.
[6] Chen S,Zhu J W,Wu X D,et al.Graphene oxide-MnO2nanocomposites for supercapacitors [J].Acs Nano,2010,4(5):2822-2830.
[7] Jiang H,Dai Y H,Hu Y J,et al.Nanostructured ternary nanocomposite of rGO/CNTS/MnO2for higigh-rate supercapacitors. [J].Acs Sustainable Chemistry & Engineering,2014,2(1):70-74.
[8] Wei W F,Cui X W,Chen W X,et al.Manganese oxide-based materials as electrochemicals supercapacitor electrodes [J].Chemical Society Reviews.2011,40(3):1697-1721
[9] Zhang S W,G Chen Z.Manganese oxide based materials for supercapacitors[J].Advanced Energy Materials,2008,3(3):186-200.
[10] Zhang X Y,Han L Q,Sun S,et al.MnO2/C composite electrode free of conductive enhance for supercapacitors [J].Journal of Alloys and Compounds,2015,653:539-545.
[11] Rakhi R B,Chen J W,Cha D,et al.Nanostructured ternary electrodes for energy-storage applications [J].Advanced Energy Materials,2012,2(3):381-389.
[12] Jin X,Zhou W,Zhang S,et al.Nanoscale microelectrochemical cells on carbon nanotubes [J].Small,2007,3(9):1513-1517.
[13] Yoo S M,Choi W M,Baik H,et al.Synthesis of multilayer graphene balls by carbon segregation from nickel nanoparticles [J].Acs Nano,2012,6(8):6803-6811.
[14] Zhu J Y,He J H.Facile synthesis of graphene-wrapped honycomb MnO2nanospheres and their aplication in supercapacitors [J].Acs Applied Materials & Interfaces,2012,4(3):1770-1776.
[15] Li H P,Wang B,He X Y,et al.Composite of hierarchical interpenetrating 3D hollow carbon skeleton from lotus pollen and hexagonal MnO2nanosheets for high-performance supercapacitors [J].Journal of Materials Chemistry A,2015,3(18):9754-9762.
[16] Liu Z Q,Xiao K,Xu Q Z,et al.Fabrication of hierarchical flower-like super-structures consisting of porous NiCo2O4nanosheets and theirs electrochemical and magnetic properties [J].Rsc Advances,2013,3(13):4372-4380.
[17] Prathap M U A,Srivatava R,Satpati B.Simultaneous detection of guanine adenine,thymine and cytosine at polyaniline/MnO2modified electrode [J].Electerchimica Acta,2013,114:285-295.
[18] Pendashteh A,Rahmanifar M S,Kaner R B,et al.Facile synthesis of nanostructured CuCo2O4as a novel electrode material for high-rate supercapacitors [J].Chemical Communications,2014,50(16):1972-1975.
(责任编辑:包震宇,郁 慧)
Preparation and property study of MnO2/CNPs as electrode materials of electrochemical supercapacitors
JIANG Chao, LI Jun, TAO Lingling, HUANG Jinping
(College of Life and Environmental Sciences,Shanghai Normal University,Shanghai 200234,China)
MnO2nanorods deposited on carbon nanospheres (MnO2/CNPs) as electrode materials of electrochemical supercapacitors have been synthesized via a hydrothermal synthesis.The micro morphologies and phases of the as-prepared MnO2/CNPs were characterized by field emission scanning electro microscopy(FESEM) and X-ray diffraction(XRD).The electrochemical properties of nanomaterials were tested by cyclic voltammetry and galvanostatic charge-discharge.At a current density of 0.1 A/g using 1 mol/L Na2SO4as electrolyte,the as-prepared MnO2/CNPs exhibit excellent specific capacitance of 305.6 F/g,far larger than carbon nanospheres (49.3 F/g).At a current density of 5 A/g,the specific capacitance of MnO2/CNPs is 235 F/g,which is 76.9% of the specific capacitance under 1 A/g current density.These results demonstrated that MnO2/CNPs may show potential application for electrode materials in electrochemical supercapacitors.
hydrothermal synthesis; MnO2/CNPs; electrochemical supercapacitor; electrode material
2016-09-22
黄金萍,中国上海市徐汇区桂林路100号,上海师范大学生命与环境科学学院,邮编:200234,E-mail:hjinping@shnu.edu.cn
O 611.3
A
1000-5137(2016)06-0663-07

