聚乙二醇干扰素α-2b联合利巴韦林治疗不同发病时间急性丙型肝炎的疗效评价
聚乙二醇干扰素α-2b联合利巴韦林治疗不同发病时间急性丙型肝炎的疗效评价
赵华1,金航芸2,潘统桧1,方玉才1
(1.桐庐县第一人民医院检验科,浙江 桐庐 311500;2.桐庐富春江医院检验科,浙江 桐庐 311504)
摘要:目的探讨治疗时机对聚乙二醇干扰素α-2b(PEG-IFNα-2b)联合利巴韦林治疗急性丙型肝炎(AHC)疗效的影响。方法将40例AHC患者按发病时间分为Ⅰ组(病毒血症持续3个月以内)23例、Ⅱ组(病毒血症持续3至6个月)17例,应用PEG-IFNα-2b(80 μg/周)联合利巴韦林(800 mg/d)治疗24周。于治疗前(第0周)及治疗后第12、24、48周检测血清丙型肝炎病毒(HCV)RNA、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、透明质酸(HA)及层黏连蛋白(LN)的水平,并对所得数据进行统计学分析。结果Ⅰ组和Ⅱ组在治疗前HCV RNA、ALT、AST、HA、LN水平差异有统计学意义(P<0.05)。治疗后Ⅰ组HCV RNA载量和ALT、AST、HA、LN水平均下降,与治疗前及Ⅱ组治疗后比较,差异有统计学意义(P<0.05)。治疗后Ⅰ组的早期病毒学应答(EVR)率、治疗结束时病毒学应答(ETVR)率、持久病毒学应答(SVR)率、生化学应答(BR)率和HA、LN的复常率均明显高于Ⅱ组治疗后(P均<0.05),治疗后Ⅱ组的复发率明显高于Ⅰ组治疗后(P<0.05)。结论PEG-IFNα-2b联合利巴韦林治疗AHC能在一定程度上阻止其慢性化及肝纤维化,病毒血症持续3个月以内的AHC患者用上述方案治疗效果显著好于病毒血症持续3至6个月的患者。病毒血症持续3至6个月的AHC患者治疗后病情容易复发。
关键词:聚乙二醇干扰素α-2b;利巴韦林;治疗时机;疗效;急性丙型肝炎
中图分类号:
文章编号:1673-8640(2015)10-0975-05R446.61
文献标志码:A
DOI:10.3969/j.issn.1673-8640.2015.10.002
Abstract:ObjectiveTo investigate the efficacy influence of polyethylene glycol interferon alpha-2b(PEG-IFNα-2b)plus ribavirin treatment for acute hepatitis C(AHC) in different times. MethodsAll 40 patients with AHC were classified into Ⅰ(viremia lasted less than 3 months, 23 cases) and Ⅱ(viremia lasted for 3 months to 6 months, 17 cases) groups, and they were administrated PEG-IFNα-2b (80 μg/week) combined with ribavirin (800mg/d) for 24 weeks. Before the treatment(at the end of week 0) and after the treatment (at the ends of week 12, 24 and 48), serum hepatitis C virus (HCV) RNA, alanine aminotransferase (ALT), aspartate aminotransferase (AST), hyaluronic acid (HA) and laminin (LN) were determined. The results were analyzed statistically. ResultsThe HCV RNA, ALT, AST, HA and LN before the treatment in Ⅰ and Ⅱ groups were different statistically(P<0.05). After the treatment, the levels of HCV RNA, ALT, AST, HA and LN in Ⅰ group decreased. Compared with those before the treatment of Ⅰ group and after the treatment of Ⅱ group, there was statistical significance (P<0.05). After the treatment, the early virological response(EVR)rate and virological response at end of therapy(ETVR) rate, sustained virological response(SVR)rate, biochemical response(BR) rate and the recovery rates of HA and LN of Ⅰ group were higher than those after the treatment of Ⅱ group (P<0.05). The relapse rate in Ⅱ group after the treatment was higher than that in Ⅰ group after the treatment(P<0.05). ConclusionsThe PEG-IFNα-2b plus ribavirin treatment for AHC could prevent the occurrence of chronic hepatitis C and liver fibrosis. The clinical curative efficacy of AHC with viremia lasted less than 3 months with this therapeutic schedule is better than that with viremia lasted for 3 months to 6 months. It is easy to relapse in AHC patients with viremia lasted for 3 months to 6 months after the treatment.
作者简介:赵华,男,1989年生,学士,技师,主要从事临床检验工作。
通讯作者:方玉才,联系电话:0571-64399760。
收稿日期:(2014-11-27)
Evaluation on the efficacy of PEG-IFNα-2b plus ribavirin treatment for acute hepatitis C in different timesZHAOHua1,JINHangyun2,PANTonghui1,FANGYucai1.(1.DepartmentofClinicalLaboratory,TongluCountyFirstPeople′sHospital,ZhejiangTonglu311500,China; 2.DepartmentofClinicalLaboratory,TongluFuchuanjiangHospital,ZhejiangTonglu311504,China)
Key words: Polyethylene glycol interferon alpha-2b; Ribavirin; Treatment time; Curative efficacy; Acute hepatitis C

丙型肝炎病毒(hepatitis C virus,HCV)是一种单股线性正链RNA病毒,是引起人类急性丙型肝炎(acute hepatitis C,AHC)的病原,成人AHC演变成慢性者的比例为60%~85%,甚至更高,20%的慢性丙型肝炎患者逐步演变为肝硬化[1]。目前,临床上主要采用《丙型肝炎防治指南》[2]建议的聚乙二醇干扰素α-2b(polyethylene glycol interferon alpha-2b,PEG-IFNα-2b)联合利巴韦林治疗AHC。为了解不同治疗时机对PEG-IFNα-2b联合利巴韦林治疗AHC疗效的影响,我们对40例AHC患者治疗前后血清HCV RNA载量、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、透明质酸(hyaluronic acid ,HA)、层黏连蛋白(laminin,LN)的水平进行检测,以观察病毒血症持续不同时间规范化治疗疗效的差别。
材料和方法
一、材料
1.研究对象收集桐庐县第一人民医院2012年1月至2013年12月间门诊及住院的AHC患者40例,其中男26例,女14例,年龄(37±5)岁。40例AHC患者按发病时间分为Ⅰ组(病毒血症持续3个月以内)23例、Ⅱ组(病毒血症持续3至6个月)17例。对Ⅰ组、Ⅱ组患者的年龄、性别进行比较,差异无统计学意义(P均>0.05)。
2.病例入选标准和排除标准AHC患者按2004年中华医学会肝病学分会和中华医学会传染病与寄生虫病学分会联合制定的《丙型肝炎防治指南》的标准[2]纳入研究对象:临床上有全身乏力、食欲减退、恶心和右季肋部疼痛等表现,少数伴低热,轻度肝脾肿大。实验室检查显示ALT呈轻度或中度升高,HCV RNA阳性且阳性持续时间不超过6个月。排除标准:6个月内曾接受过抗病毒药物及免疫调节剂治疗者,肝硬化、肝癌、脂肪肝、药物性肝损害及丙型肝炎病毒以外的其它肝炎病毒感染者。
3.仪器与试剂Light Cyclcer 480荧光定量聚合酶链反应(polymerase chain reaction,PCR)扩增仪;OLYMPUS 2700生化分析仪;MAGLUMI 2000 Plus全自动化学发光免疫分析仪。HCV RNA定量检测试剂盒由上海科华生物工程股份有限公司提供(批号20111220);ALT和AST检测试剂盒由宁波瑞源生物科技有限公司提供(批号均为20120101);HA和LN检测试剂盒由深圳市新产业生物医学工程股份有限公司提供(批号分别为051120101和049120101)。
二、方法
1.检测方法 HCV RNA检测采用实时荧光定量PCR,定量测定范围为103~107拷贝/mL,低于103拷贝/mL判定为HCV RNA阴性;ALT检测采用酶速率法,参考值范围为5~40 U/L;AST检测采用酶速率法,参考值范围为5~40 U/L;HA检测采用化学发光法,参考值范围为0.0~100.0 ng/mL;LN检测采用化学发光法,参考值范围为0.5~50.0 ng/mL。上述项目的检测方法及结果判断严格按照试剂盒说明书进行。所有患者于治疗前(第0周)及治疗后第12、24、48周检测HCV RNA、ALT、AST、 HA及LN水平。
2.治疗方法所有患者签署知情同意书,全部采用皮下注射PEG-IFNα-2b(商品名:佩乐能,美国先灵葆雅公司生产),剂量80 μg,每周1次,同时服用利巴韦林800 mg/d,疗程24周,若白细胞总数低于1.5×109/L或中性粒细胞数低于0.75×109/L时,则适当减量或暂停1~2周,或使用升白细胞药,待白细胞总数回升至正常后再恢复原用量。
3.疗效标准按2004年中华医学会肝病学分会和中华医学会传染病与寄生虫病学分会联合制定的标准,即ALT和AST回复正常为生化学应答(biochemical response,BR);治疗12周时血清定量检测小于最低检测限或定量检测降低2个对数级(Log)以上为早期病毒学应答(early virological response,EVR);治疗结束时HCV RNA定量检测<最低检测限为治疗结束时病毒学应答(virological response at end of therapy,ETVR);治疗结束至少随访24周时,HCV RNA定量检测<最低检测限为持久病毒学应答(sustained virological response,SVR);从未获得EVR、ETVR及SVR者为无应答(nonresponse,NR);治疗结束时HCV RNA定量检测<最低检测限,但停药后HCV RNA又转为阳性称为复发。
三、统计学方法
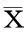
结果
一、Ⅰ组和Ⅱ组AHC患者治疗前后病毒学指标、生化学指标及肝纤维化指标的比较
治疗前Ⅱ组的HCV RNA载量和ALT、AST、HA、LA水平均高于Ⅰ组(P<0.05);治疗后Ⅰ组HCV RNA载量和ALT、AST、HA、LN水平均下降,与治疗前及Ⅱ组治疗后比较,差异有统计学意义(P<0.05)。见表1。
二、Ⅰ组和Ⅱ组AHC患者治疗后病毒学应答率的比较
治疗后Ⅰ组的EVR率、ETVR率、SVR率均达到了100.0%明显高于Ⅱ组治疗后(P<0.05),但复发率低于Ⅱ组(P<0.01)。见表2。
三、Ⅰ组和Ⅱ组AHC患者治疗前后生化学应答率及肝纤维化指标复常率的比较
治疗后Ⅰ组和Ⅱ组AHC患者的生化学应答率及肝纤维化指标复常率均明显升高(P<0.01);治疗后 Ⅰ 组的BR率和HA、LN的复常率均明显高于治疗后同期的Ⅱ组(P<0.05)。见表3。

表1 Ⅰ组和Ⅱ组AHC患者治疗前后病毒学指标、生化学指标及肝纤维化指标的比较

表2 Ⅰ组和Ⅱ组AHC患者治疗后病毒学应答率的比较 [%(例)]
表3 Ⅰ组和Ⅱ组AHC患者治疗前后BR率及肝纤维化指标复常率的比较 [%(例)]
四、毒副作用
本研究中发现所有患者在注射PEG-IFNα-2b后1~4 d内均有发热,大部分患者感到乏力、全身不适、轻度头晕,1至2周症状缓解或消失。所有AHC患者在治疗过程中共有3例出现白细胞减少,其中Ⅰ组1例、Ⅱ组2例。3例患者出现白细胞减少后,PEG-IFNα-2b适当减量,1周后白细胞总数回升至正常,随后PEG-IFNα-2b恢复原用量直至治疗结束。
讨论
AHC的主要发病机制是HCV直接细胞毒作用、宿主免疫因素、自身免疫和细胞凋亡[3]。有研究显示,当HCV RNA在肝细胞内复制时可引起肝细胞结构和功能改变或干扰肝细胞内蛋白的合成,造成肝细胞变性坏死[4]。一部分HCV感染呈自限性经过,血清HCV RNA在感染后3至4个月内检测不到[5]。RAO等[6]在一项大样本人群的研究中发现,在AHC患者中女性患者疾病自愈的概率明显高于男性,本次研究中未发现这样的自愈患者。
现在医学认为,干扰素具有抑制HCV复制、减轻肝脏炎症、阻止肝纤维化的发生和发展以及预防肝细胞癌发生的作用。PEG是一种安全、无活性、无毒的聚合物,与重组IFNα-2b结合形成长效干扰素,它封闭了一些干扰素抗原位点,减低了免疫原性,减少了干扰素抗体的产生,给药后血药浓度稳定,半衰期可长达96 h,从而使治疗周期延长为每周1次,且药物浓度波动小,对病毒的抑制作用持久[7]。利巴韦林是一种广谱抗DNA和RNA病毒的鸟嘌呤核苷类似物,可抑制病毒依赖RNA多聚酶,口服吸收好,两者联合使用的效果比单用干扰素好[8]。
本研究显示,AHC患者采用PEG-IFNα-2b联合利巴韦林治疗后,血清HCV RNA载量和ALT、AST、HA、LN水平较治疗前均明显降低(P<0.05),说明PEG-IFNα-2b联合利巴韦林能有效减少肝脏组织内和血液中病毒载量,抑制HCV复制,减轻肝脏炎症、坏死。治疗后Ⅰ组的EVR率、ETVR率和SVR率要明显高于Ⅱ组治疗后(P<0.05)。这与DETERDING等[9]对随访12周的HCV RNA仍为阳性的延迟治疗依从性良好的AHC患者应用PEG-IFNα-2b联合利巴韦林可以获得与早期治疗患者相似的应答率这一结论不符。Ⅱ组中2例患者在治疗后第24周至治疗后第48周内出现了复发,同时ALT、AST指标出现了反跳,而Ⅰ组治疗后却没有出现复发及反跳现象。这一结果与MICHAEL等[10]的HCV感染的AHC未经治疗发展为慢性者的概率高达80%,如及时诊断和早期治疗则可防止慢性化,且90%以上患者可治愈这一结论相符。Ⅱ组中出现复发的2例患者在治疗过程中出现了白细胞减少,而Ⅰ组中出现白细胞减少的患者在治疗后并未复发。上述结果说明AHC患者在病毒血症持续3个月以内时采用PEG-IFNα-2b联合利巴韦林治疗的临床疗效较病毒血症持续3至6个月以内明显。对于初始治疗后未取得SVR患者的再治疗疗程建议为48周,可加用利巴韦林联合治疗[11]。
医学研究发现,HA、基质金属蛋白酶抑制因子1、转化生长因子β1、血小板衍生生长因子BB、肿瘤坏死因子α、IV型胶原、LN等均与肝纤维化相关[12]。我们观察发现Ⅰ组和Ⅱ组治疗后HA、LN复常率和BR率均明显高于治疗前(P<0.05),且Ⅰ组治疗后HA、LN复常率和BR率均高于Ⅱ组治疗后(P<0.05)。提示PEG-IFNα-2b联合利巴韦林治疗AHC能减轻肝脏炎症和坏死,且在病毒血症持续3个月以内时采用联合治疗能更有效地阻止肝纤维化的发生。
HCV核心抗原检测是新近发展的一种HCV感染的检测方法,在HCV感染诊断中的价值越来越受到重视。HCV核心抗原于HCV感染后12~15 d即可检测到,仅较HCV RNA晚1 d[13],且与血清中HCV RNA载量呈正相关,并在HCV感染治愈或康复后消失。因此,HCV核心抗原检测理论上也可作为AHC临床疗效的评价指标,此方面有待进一步研究。
参考文献
[1]张青文.急性丙型病毒性肝炎19例临床分析[J].实用医技杂志,2014,21(2):184-185.
[2]中华医学会肝病学分会,中华医学会传染病与寄生虫病学分会.丙型肝炎防治指南[J].中华传染病杂志,2004,22(2):135-136.
[3]段学章,张敏.丙型病毒性肝炎防治新进展[M].北京:人民军医出版社,2010:57-65.
[4]LOGUERCIO C, FEDERICO A, MASARONE M, et al. The impact of diet on liver fibrosis and on response to interferon therapy in patients with HCV-related chronic hepatitis[J]. Am J Gastroenterol, 2008, 103(12): 3159-3166.
[5]SANTANTONIO T, WIEGAND J, GERLACH JT. Acute hepatitis C: current status and remaining challenges[J]. J Hepatol, 2008, 49(4): 625-633.
[6]RAO HY, SUN DG, JIANG D, et al. IL28B genetic variants and gender are associated with spontaneous clearance of hepatitis C virus infection[J]. J Viral Hepat, 2012, 19(3): 173-181.
[7]ZHANG YX, WU WJ, ZHANG YZ, et al. Noninvasive assessment of liver fibrosis with combined serum aminotransferase/platelet ratio index and hyaluronic acid in patients with chronic hepatitis B[J]. World Gastroenterol, 2008, 14(46): 7117-7121.
[8]曾颖玲,毛惠南.安络化纤丸联合干扰素和利巴韦林治疗丙型肝炎肝纤维化的临床研究[J].国际医药卫生导报,2013,19(4):543-545.
[9]DETERDING K, GRÜNER N, BUGGISCH P, et al. Delayed versus immediate treatment for patients with acute hepatitis C: a randomized controlled non-inferiority trial[J]. Lancet Infect Dis, 2013, 13(6): 497-506.
[10]MICHAEL PM,钱燕.丙型肝炎治疗进展[J].肝脏,2008,13(1):56.
[11]European Association for Study of Liver. EASL clinical practice guidelines: management of hepatitis C virus infection[J]. J Hepatol, 2014, 60(2): 392-420.
[12]田玉岭, 赵伟, 沈玲, 等.聚乙二醇干扰素α-2a对乙型肝炎病毒复制及肝纤维化指标的影响[J].中华传染病杂志,2007,25(9):553-557.
[13]GU S, LIU J, ZHANG H, et al. Core antigen tests for hepatitis C virus: a meta-analysis[J]. Mol Biol Rep, 2012, 39(8): 8197-8208.
(本文编辑:姜敏)
上海市临检中心通过两大体系复评审及扩项评审
金秋九月,上海市临检中心迎来了中国合格评定国家认可委员会(CNAS)评审专家对检测实验室(ISO17025)复评审和能力验证提供者(ISO17043)复评审及其扩项评审,两大体系均顺利通过现场评审。
检测实验室(ISO17025)复评审中,评审组依据CNAS-CL01:2006《检测和校准实验室能力认可准则》,并结合3个应用说明CNAS-CL09:2006《检测和校准实验室能力认可准则在微生物检测领域的应用说明》和CNAS-CL21:2006《检测和校准实验室能力认可准则在卫生检疫领域的应用说明》以及CNAS-CL52:2014 《CNAS-CL01<检测和校准实验室能力认可准则>应用要求》,采用现场常规试验、留样再测、人员比对、现场询问、现场演示、查阅能力验证结果、查阅原始记录等方式,对中心检测实验室质量管理体系运行情况以及技术能力进行了全面而细致的审核。评审专家组对实验室的工作予以充分肯定,认为实验室的管理体系运行有效,承担实验的检测人员操作技术规范娴熟,实验条件和技术能力达到了认可的要求;同时评审组也对中心检测实验室提出了9个不符合项和持续改进的建议,对中心实验室的运行和完善提供了很好的帮助。评审组同意继续维持上海市临检中心检测实验室申请的72个项目的检测能力(详见CNAS网站“获认可机构名录”)。
能力验证提供者(ISO17043)复评审及其扩项评审中,评审组依据准则CNAS-CL03:2010《能力验证提供者认可准则》全部要素和其它相关规则、准则的要求对中心进行了3 d的现场评审,评审共确认申请认可的细菌学(0703)、病毒学(0705)、真菌学(0706)、血液学(0711)、化学病理学(0720)、医学应用病理学(0726)检测领域。血液学(0711)、化学病理学(0720)、医学应用病理学(0726)检测领域的118个项目/参数,涉及血清基质制备物、全血、溶液、血浆基质制备物、尿液基质制备物、冻干菌株等样品。经过现场评审,评审专家组对中心能力验证提供者工作充分肯定,并认为实验室的管理体系运行有效;评审组也提出了8个不符合项和持续改进的建议,进一步促进和完善能力验证的组织工作。中心所提供的118个医学检验项目(详见CNAS网站“获认可机构的名录”)的技术能力满足CNAS认可要求,评审组同意将向CNAS推荐认可。
(本刊编辑部)

