粘弹性本构对人耳动力学特性影响的数值研究
粘弹性本构对人耳动力学特性影响的数值研究
田佳彬1,饶柱石1,塔娜1,许立富1,黄新生2
(1.上海交通大学振动、冲击噪声研究所 机械系统与振动国家重点实验室,上海200240;2.复旦大学附属中山医院,上海200032)
摘要:为分析中耳软组织粘弹性材料特性对人耳系统动力学特性影响,建立包括外耳道、中耳及耳蜗的整耳有限元模型。外耳道及中耳模型用微CT扫描与逆向成型技术建立,耳蜗采用双腔导管形式简化模型。基于该模型,中耳部分软组织材料属性采用线性粘弹性,以表征动态分析中能量损耗。在外耳道施加90 dB SPL声压模拟声激励,并在计算中考虑外耳道气体、中耳固体及耳蜗流体多场耦合作用。中耳结构响应包括鼓膜脐部与镫骨底板位移及镫骨底板速度传递函数,耳蜗流体压力响应用于计算中耳压力增益、耳蜗输入声阻抗及压力逆向传递函数。结果表明,考虑粘弹性后,人耳系统动态响应参数较线弹性有一定程度改善,尤其在高频段提升较明显,与实验测量数据匹配效果更好。
关键词:粘弹性;动态能耗;耳蜗;动力学建模;多场耦合;有限元分析
中图分类号:R318.01文献标志码:A
Numerical analysis on the effects of viscoelastic constitutive relation on dynamic characteristics of human ear
TIANJia-bin1,RAOZhu-shi1,TANa1,XULi-fu1,HUANGXin-sheng2(1. Institute of Vibration, Shock and Noise, State Key Laboratory of Mechanical System and Vibration,Shanghai Jiao Tong University, Shanghai 200240, China; 2. Zhongshan Hospital A?liated to Fudan University, Shanghai 200032, China)
Abstract:To analyze the effects of viscoelastic properties of middle ear soft tissues on the dynamic characteristics of human ear system, a finite element (FE) model of the human ear consisting of the external ear canal, middle ear and cochlea was developed. The geometric configuration of the external ear canal and middle ear was constructed via micro-CT scanning and reverse engineering technology, and the cochlea was simplified as an uncoiled, two-chambered and fluid-filled duct. The viscoelastic material effect was introduced into the behaviors of middle ear soft tissues to represent the energy dissipation in dynamic analysis. A multiphysics coupled analysis was conducted on the model in which the coupling effects among the air in the ear canal, the fluid in the cochlea and the middle ear structures were concerned. Then a sound pressure of 90 dB SPL was applied on the ear canal to simulate the sound stimulus on normal human ear. Middle ear structural responses such as movements of the tympanic membrane and stapes footplate in response to the sound stimulus were derived by this model. Meanwhile, based on calculating the pressure of the fluid in the cochlea, the sound pressure gain across the middle ear, the cochlear input impedance and the reverse pressure transfer function of cochlea were also obtained. The results show that taking into account the viscoelastic properties of middle ear soft tissues can improve the dynamic responses of the human ear system as compared with the results of a linear elastic model, especially at the high-frequency range. The better agreements between the model results and the experimental data in the literature illustrate the necessity of considering viscoelasticity for dynamic modeling of human ear.
Key words:viscoelasticity; dynamic energy dissipation; cochlea; dynamic modeling; multiphysics coupling; finite element analysis
人耳系统主要由耳廓、外耳道、中耳及耳蜗构成。该系统具有复杂几何形态、超微型结构特征及非同质材料特性,且在正常生理过程中伴随声固耦合、流固耦合等复杂机理。基于此,采用有限单元法建立人耳数值模型已成为人耳生物力学研究的重要方法[1]。
中耳声传导模型主要用于模拟声音经外耳道、鼓膜、中耳听骨链至镫骨底板的传递机制[1-2],其与耳蜗的耦合模型则可用于分析耳蜗内部淋巴液的压力响应及基底膜沿长度方向位移分布[3]等特性。人耳数值模型与实验测量数据的匹配程度及声传导机理研究已取得一定成果。力学实验[4-5]研究结果显示,人耳部分组织与器官如鼓膜、中耳软组织等均具有粘弹性材料特性,故动态分析中的材料属性普遍采用线弹性及瑞利阻尼的假设形式[6],与实验结果有出入,不能反映人耳各部分结构真实力学特性。而准确的人耳动力学建模需考虑软组织粘弹性特性的实际影响。
人耳的主要功能在于将耳廓收集的动态声压传递到耳蜗淋巴液转化成电信号刺激耳蜗的听神经。此动态过程具有较大的频率相关性,并取决于耳蜗基底膜的选频特性[7],使人耳对高频声压幅值较敏感。对具有粘弹性特性材料,动态过程中能量耗散通常通过复模量虚部即损耗模量形式引入,而复模量则采用粘弹性本构模型方式表达成频率的函数。因此,人耳力学模型中考虑粘弹性材料属性,必对人耳系统频率相关性产生影响。现有大部分人耳有限元模型的人耳结构能量损耗通常用瑞利阻尼定义[8],阻尼系数设为α=0,β≠0,因而会导致系统阻尼随频率提高显著增加,降低系统的高频响应。有限元模型中,中耳模型[9]及含耳蜗的整耳模型均出现位移响应的高频幅值相对较低现象,尤其镫骨底板的高频位移明显低于实验结果,故在人耳动力学建模中应以更真实的本构关系取代线弹性假设条件。
完整的人耳声传导路径应含外耳道气体、中耳固体、耳蜗流体及基底膜等结构。耳蜗流体压力响应为耳蜗生物力学特性的重要参数,Stieger等[10]研究中耳蜗底部隔膜压力差被认为耳蜗的输入信号,为声传导驱动因素。基于正、逆向激励的耳蜗隔膜压力差相等方法,圆窗激励式人工中耳在理论与实际应用中也取得一定进展[11]。因此,研究粘弹性特性引入对耳蜗流体压力响应等参数影响尚需建立外耳道、中耳及耳蜗的耦合模型。为此,本文基于耳蜗建模中普遍采用的双腔导管模型对耳蜗实际螺旋形结构进行几何简化。而外耳道、中耳的几何模型基于逆向成型技术建立,并通过定义流固耦合面方式实现外耳、中耳、耳蜗整体集成。在此基础上,考虑鼓膜、中耳软组织的粘弹性材料属性,计算中耳结构位移及耳蜗流体压力等动力学参数,比较线弹性与粘弹性响应的异同点,分析引入粘弹性本构在人耳动力学建模中的必要性。可为建立完整、准确的人耳动力学模型提供思路。
1方法
1.1整耳网格模型
用微CT扫描仪(GE Healthcare,eXplore Locus SP)扫描人体颞骨标本(男,45岁,右耳),获得882张医疗影像图片,扫描层厚度43.5 μm。将所得图片文件导入Simpleware软件进行逆向成型,建立外耳道及中耳的三维几何模型。将模型尺寸与模型数据[12]进行比对,验证所建模型尺寸与结构特征处于合理范围内。用有限元前处理软件Hypermesh划分网格,获得人体外耳道及中耳模型。其中外耳道气体采用四面体单元AC3D4,单元数22 366,中耳结构包括听骨链、中耳韧带与肌腱亦用四面体单元C3D4,总单元数为48 043。鼓膜、鼓膜环韧带采用壳单元S3划分,单元数804;鼓膜环韧带及鼓膜张紧、松弛部厚度分别取0.2 mm、0.05 mm及0.1 mm。
耳蜗采用非螺旋状、充满液体的双腔导管模型,包括前庭阶、鼓阶、基底膜、卵圆窗、圆窗及蜗孔,模型整体尺寸见文献[6],与人体耳蜗实际尺寸相近。基底膜尺寸由底部厚度7.5 μm、宽度150 μm线性变化到顶部厚度2.5 μm、宽度500 μm[13],总长度34 mm,划分成482个S3、S4壳单元。前庭阶及鼓阶的液体容积分别为92.781 μL、93.270 μL,用六面体单元AC3D4及AC3D8划分网格,单元数分别为17 577及13 802。圆窗直径基于文献[8]圆窗膜面积2.1 mm2确定为1.6 mm。所建人耳有限元模型见图1、图2。为显示耳蜗内部的基底膜结构,耳蜗流体设置成半透明形式。中耳几何参数及见表1。

图1 外耳、中耳与耳蜗耦合模型 Fig.1 Coupled model of human ear consisting of external ear canal, middle ear and cochlea
1.2材料属性
人耳有限元模型材料参数按外耳道气体、中耳及耳蜗三部分设定。外耳道气体材料属性与空气相同,体积模量0.142 MPa,密度1.21 kg/m3。中耳各部分结构采用均匀及各向同性弹性材料,泊松比均为0.3。鼓膜、听骨链材料及韧带、肌腱材料参数采用交叉调试[12]方法确定,获得鼓膜、听骨链、中耳韧带及肌腱材料属性见表2。动态分析中的能量损耗通过两种形式实现,鼓膜张紧部、鼓膜松弛部、砧锤关节、砧镫关节、镫骨环韧带及圆窗用线性粘弹性材料模型,动态能耗通过粘性部分表达,材料参数见表3。中耳其它部分能量损耗采用瑞利阻尼形式,阻尼系数α=0 s-1,β=0.75×10-4s。

图2 中耳各部分结构说明 Fig.2 Illustration of components in the middle ear

部件尺寸模型尺寸参考尺寸[14]鼓膜沿着锤骨柄方向的直径/mm8.6678.0-10.0垂直锤骨柄方向的直径/mm7.5747.5~9.0锥形高度/mm1.7742.0表面积/mm263.77755.8~85.0厚度/mm0.050.04~0.075锤骨锤骨柄底部到外侧突底部的距离/mm4.0425.8总长度/mm7.4537.6~9.1砧骨砧骨长突的长度/mm6.8437.0砧骨短突的长度/mm4.7385.0镫骨高度/mm3.4512.5~4.0镫骨底板的长度/nn2.7472.64~3.36镫骨底板的宽度/mm1.4060.7~1.66外耳道长度(鼓膜脐部到外耳道入口)/mm25.32925~31体积/mm3865.927830~1972
耳蜗部分前庭阶及鼓阶流体材料特性与水相同,即体积模量2 250 MPa、密度1 000 kg/m3。为模拟耳蜗基底膜沿长度方向刚度渐变的特性,用定义温度场变量方式将基底膜杨氏模量设为由底部40 MPa线性减小中间15 MPa,再依次线性减小到顶部的3 MPa,瑞利阻尼系数取α=0 s-1,β=0.1×10-3s。基底膜支撑部分与圆窗的杨氏模量分别取1.41×104MPa及0.3 MPa。耳蜗流体粘度以间接方式引入,表达成流体的体积阻力,表达式为
(1)
式中:ω为圆频率;ρ为耳蜗流体密度;K为耳蜗流体体积模量;η为体积粘度系数,大小为0;μ为剪切粘度系数,大小为1×10-3N·s/m2。

表2 中耳结构的材料参数
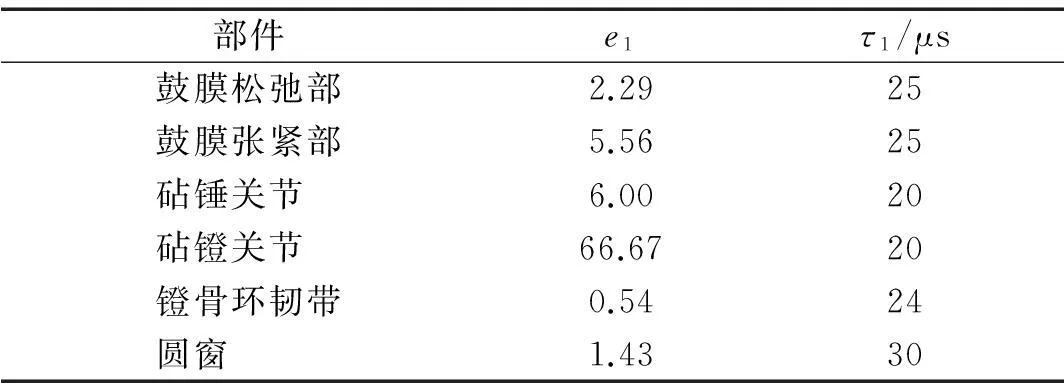
表3 中耳软组织的粘弹性材料参数
1.3结构与流体边界设定
人耳有限元模型中结构边界条件均采用节点位移固支形式,具体包括:鼓膜环韧带环向节点、中耳韧带及肌腱端部节点、基底膜支撑部分外侧节点及圆窗外侧周向节点。模型流体边界按流体内、外边界分别设定。模型的流体外边界设定中,外耳道气体毗邻耳道壁面流体单元表面及耳蜗流体毗邻耳蜗骨壁的流体单元表面定义成Wall边界,即流体压力的法向梯度为零。外耳道的流体单元则施加固定幅值的压力载荷用于模拟正常人耳的声激励。对模型的流体内边界,通过定义流固耦合面实现流体压力的法向梯度与结构力的相互传导。流固耦合面包括:外耳道气体与鼓膜外侧面的耦合、镫骨底板表面与耳蜗流体的耦合、圆窗与耳蜗流体耦合、耳蜗隔膜(含基底膜)两侧与前庭阶流体与鼓阶流体的耦合。需指出的是,由于耳蜗流体与镫骨底板表面及圆窗膜表面间网格节点并非一一对应,故实际建模时采用Abaqus中的Tie命令完成各结合面的连接处理。
1.4粘弹性本构关系
为表达软组织粘弹性材料特性,采用广义的线性固体模型或Weichert模型[19]进行模拟,见图3。

图3 Weichert粘弹性模型 Fig.3 Weichert model for viscoelastic material
基于图3模型,软组织的时域松弛模量E(t)可表达成Prony级数[20],即
(2)
式中:E∞为t→∞时长期模量;Ei为第i个弹簧的松弛模量;τi为第i个阻尼器松弛时间。
为计算松弛模量的傅里叶变换,定义无量纲松弛函数e(t)为
(3)
式中:ei=Ei/E∞。
本文采用一阶Prony级数(n=1)模拟人耳软组织的粘弹性特性。对稳态动力学分析而言,时域的松弛模量转换化成频域复模量为
E*(ω)=E′(ω)+iE″(ω)
(4)
式中:ω为圆频率;E′(ω),E″(ω)分别为存储模量及损耗模量,表达式为
(5)
复模量E*(ω)表达动态分析中随频率变化的材料特性,能量损耗机制通过损耗模量E″(ω)反映到复模量虚部。
对人耳系统,由于动态声压幅值较小,因此,采用稳态小振幅振动分析假设,参数e1及τ1保持不变。而长期模量E∞则对应表2的杨氏模量。本文所建有限元模型中,中耳软组织的5个部分均采用线性粘弹性本构模型,即鼓膜张紧部、鼓膜松弛部、砧锤关节、砧镫关节及镫骨环韧带。材料参数e1,τ1见文献[21],圆窗材料参数见文献[22](表3)。
2结果分析
用有限元分析软件Abaqus 6.10于外耳道距离鼓膜约1.7 mm处,施加90 dB SPL(0.632 Pa,有效值)的声压激励,分析频率范围250~8 000 Hz。计算包括鼓膜脐部与镫骨底板位移、镫骨底板速度传递函数、中耳压力增益及耳蜗输入声阻抗等动态参数。在此基础上,于圆窗膜中耳腔一侧施加1 Pa的压力载荷,计算耳蜗压力逆向传递函数。在与相关实验测量数据对比同时将线弹性+瑞利阻尼及粘弹性计算结果进行比对。其中瑞利阻尼系数取α=0 s-1,β=0.75×10-4s。
2.1鼓膜脐部与镫骨底板位移
模型计算的鼓膜脐部与镫骨底板位移响应幅值及与10组人体颞骨实验数据平均值[23]比较见图4。由图4看出,模型计算结果与实验数据均值一致性较好,鼓膜脐部与镫骨底板位移均在1 000 Hz处取得最大值,且频率大于1 000 Hz时位移幅值随频率增大逐渐减小。通过粘弹性与线弹性比对知,用粘弹性本构模型时鼓膜脐部与镫骨底板位移响应在250~1 000 Hz低频段相差不大,随频率增大粘弹性计算结果逐渐趋近实验曲线,并高于线弹性计算结果。其中鼓膜脐部位移曲线从2 000 Hz处开始高于线弹性计算曲线,而镫骨底板则始于1 500 Hz频率处。图4(b)为模型计算结果,有限元模型基于外耳道、中耳及耳蜗的集成,且中耳软组织采用线弹性本构模型。粘弹性位移曲线高于1 000 Hz时明显高于文献[8]结果,与实验数据更接近。镫骨底板作为连接中耳与耳蜗的关键部位,其位移响应为衡量人耳模型有效性、评价植入式中耳助听装置[24]的重要指标。因此,较好匹配镫骨底板位移实验曲线,会为模型进一步应用提供基础条件。
2.2镫骨底板速度传递函数
模型计算的镫骨底板速度传递函数及文献[25]的实验曲线均值及上、下限见图5,用于表征中耳的声传递特性,定义为镫骨底板速度与外耳道内鼓膜附近声压之比。实验数据取自12例人体颞骨样本。用粘弹性本构计算结果总体趋势与实验曲线一致,尤其在250~4 500 Hz频段内,计算、实验曲线一致性较好。较线弹性,粘弹性计算结果亦在高于1 500 Hz时出现较明显的增幅现象,处于实验曲线范围内。

图4 中耳位移响应Fig.4Displacementresponseofthemiddleear图5 镫骨底板速度传递函数Fig.5Stapesfootplatevelocitytransferfunction
2.3中耳压力增益
中耳压力增益定义为前庭阶靠近卵圆窗处的压力值与外耳道内鼓膜附近的压力值之比,并以dB形式表达。本文前庭阶压力提取点为耳蜗内部距卵圆窗0.23 mm,距耳蜗隔膜1.5 mm,与文献[26]实测点0.2 mm及2~3 mm较接近。计算结果、相关实测数据[27]及其它有限元模型的仿真曲线见图6。由图6看出,中耳软组织采用粘弹性材料特性时模型计算的中耳压力增益曲线与Puria等实验结果较接近,尤其在频率高于2 000 Hz时。在250~850 Hz低频段及3000~8 000 Hz高频段内,模型计算结果均高于仿真曲线,与实验数据更吻合。
对比图6中线弹性与粘弹性结果曲线可知,二者差异主要集中在2 000~8 000 Hz频率范围内。在8 000 Hz频率点处,对应线弹性压力增益值为1.99 dB,而对应粘弹性增益值为11.88 dB,相差量值达9.89 dB。结果表明,中耳软组织采用粘弹性本构关系亦会对耳蜗压力响应产生显著影响。由模型计算知,仅考虑圆窗粘弹性特性时前庭阶的压力响应与线弹性基本相同。研究表明,耳蜗前庭阶及鼓阶压力差可作为耳蜗的输入信号,并用于圆窗激励式人工中耳的植入性能评价[28],因此,图6中前庭阶压力响应的高频改善会益于研究。
2.4耳蜗输入声阻抗
耳蜗输入声阻抗为理解声能量由中耳传递到耳蜗的重要参数,定义式[29]为
(6)
式中:PSV为前庭阶近卵圆窗处压力(提取点用与中耳压力增益计算中相同位置);VS为镫骨底板速度;AS=3.2 mm2为镫骨底板面积。
模型计算的耳蜗输入声阻抗及实验曲线[30]见图7。由图7看出,计算结果在总趋势上与实验曲线相似,虽不同实验数据偏差较大,但结果曲线基本位于各组实验曲线范围之内。对应线弹性与粘弹性不同材料属性,声阻抗最小值均位于1 000 Hz频率点处,大小为17.89 GΩ。与图4~图6计算结果不同,在声阻抗计算曲线高频段未出现较明显的粘弹性高于线弹性现象,且在250~750 Hz频率范围内线弹性计算结果却高于粘弹性。需进一步指出的是,耳蜗输入声阻抗需综合考虑中耳结构与耳蜗流体的动态响应,而在人耳数值仿真中不易准确计算,人耳软组织材料属性变化对声阻抗影响。研究表明[31],前庭阶截面积也是影响声阻抗的重要因素,故准确仿真计算尚需实验、建模的深入研究。
2.5耳蜗压力逆向传递函数
为进一步分析引入粘弹性材料特性对人耳动力学响应影响,基于所建整耳模型计算耳蜗压力逆向传递函数。此时激励压力加载于圆窗膜中耳腔一侧,大小为1 Pa,用于计算逆向激励下耳蜗前庭阶及鼓阶的流体压力响应。其中,前庭阶与鼓阶压力提取点分别为:距卵圆窗、圆窗中心点0.23 mm,距耳蜗隔膜1.5 mm。耳蜗压力逆向传递函数为
(7)

模型计算耳蜗压力逆向传递函数与三组实验结果[32](单位dB)见图8。由图8看出,模型计算曲线基本处于三组实验曲线范围之内,且波动主要在低于1 000 Hz频率处,在1 000~8 000 Hz频率内,结果曲线较平坦且接近0 dB。由线、粘弹性结果比对可知,引入粘弹性材料特性对耳蜗压力逆向传递函数影响主要集中在250~1 000 Hz低频段,最大差异量为250 Hz的3 dB;而频率高于1 000 Hz时最大差异量仅8 000 Hz的1.52 dB。此外,对计算结果,逆向激励下鼓阶压力值普遍大于前庭阶,因此,粘弹性曲线在低频段下降现象表明,引入粘弹性会一定程度上提高逆向激励的前庭阶压力响应。需指出的是,现阶段将人工中耳植入圆窗,采用逆向激励形式进行人耳听力补偿,已取得较佳实验效果。在圆窗激励评价中,耳蜗压力逆向传递函数通常可用于计算等效驱动力、驱动位移等重要参数[32],故该计算结果有助于提高圆窗激励的数值评价精度。
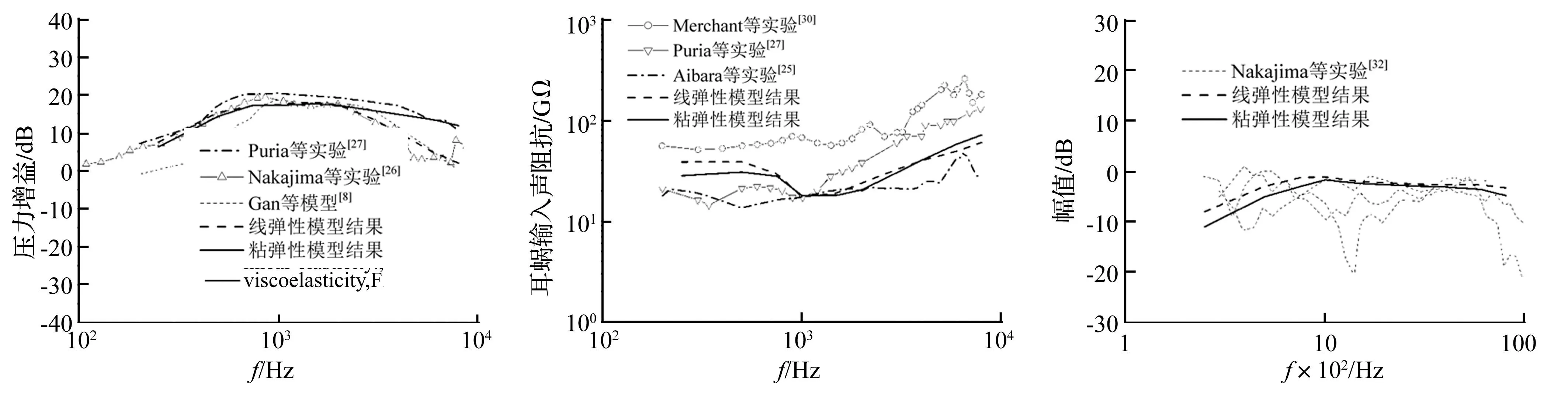

图6 中耳压力增益Fig.6Middleearpressuregain图7 耳蜗输入声阻抗Fig.7Cochlearinputimpedance图8 耳蜗压力逆向传递函数Fig.8Reversepressuretransferfunctionofcochlea
3讨论
本文研究主要目的在于分析中耳软组织引入粘弹性材料属性对人耳动力学特性影响。图4、图5分别从鼓膜脐部与镫骨底板位移及镫骨底板速度传递函数三方面,反映粘弹性本构关系能改善中耳结构的高频响应,图6的中耳压力增益则表明,耳蜗流体压力响应同样可通过考虑粘弹性达到与实验数据的较佳匹配。由此表明,用粘弹性表征人耳系统动态过程中能量损耗机制更合适。而模型中采用粘弹性材料属性的人耳结构数量较有限,虽中耳韧带、肌腱对人耳动力学特性具有重要影响[33],但关于结构的粘弹性材料实验仍无报道,因此模型中仍采用线弹性本构模型。实验研究[34-35]表明,人体与豚鼠的鼓膜不仅具有频率相关的粘弹性特性,在准静态域亦呈较明显的超弹性特性。本文的人耳动力学建模,未考虑软组织超弹性材料属性,在动态分析中人耳系统的平衡位置始终保持不变。因此,综合考虑人耳软组织的超弹性、粘弹性特性,分析不同中耳静压加载下的人耳动力学特性,将成为新的研究重点。

图9 基底膜峰值响应位置与频率关系 Fig.9 Place of maximum response on the basilar membrane vs. frequency
本文的整耳有限元模型,耳蜗部分采用简化的双腔导管形式,并未对蜗管及柯蒂氏器进行实际建模,因此仍为被动的耳蜗模型。基底膜沿长度方向刚度渐变特性主要通过厚度尺寸、宽度尺寸及杨氏模量变化表达。目前关于基底膜厚度、宽度方向尺寸已有较多研究,并被相关耳蜗模型采用,但由于耳蜗内部复杂的生理条件及基底膜螺旋形结构特点,关于基底膜材料属性实验研究仍较少。为此,参考文献[7]实验数据,以基底膜杨氏模量为调节参数,通过匹配实验曲线确定基底膜最终的模量参数。基底膜峰值位移位置与频率的对应关系见图9,表示出基底膜的选频特性。由图9看出,沿基底膜长度方向,共振频率位置随频率增加逐渐由基底膜顶部32.2 mm移到底部7 mm处,并与实验曲线具有较好的一致性。需指出的是,由于基底膜厚度方向尺寸(2.5~7.5 μm)远小于另两方向尺寸(0.15~34 mm),用实体单元划分网格会导致过多单元数量,导致计算困难。为此,基底膜采用壳单元进行网格划分,而沿长度方向变化的厚度尺寸及杨氏模量则通过定义温度场变量方式实现。图9计算结果亦表明设定的合理性。
4结论
(1)通过所建含外耳道、中耳及简化耳蜗的集成人耳有限元模型,分析中耳软组织粘弹性材料特性引入对人耳动力学特性影响。并计算包括鼓膜脐部与镫骨底板位移、镫骨底板的速度传递函数、中耳压力增益、耳蜗输入声阻抗及耳蜗压力逆向传递函数等动态响应参数。
(2)模型计算结果显示,较线弹性,粘弹性材料属性不仅能明显提高中耳结构的高频响应,对耳蜗流体压力响应亦影响显著。模型计算曲线与实验测量曲线比较表明,基于粘弹性本构关系的动态响应能取得与实验结果更佳的匹配效果、用粘弹性表征人耳系统动态能量损耗更合理。该研究有助于建立更贴近实际生理条件的人耳有限元模型。
参考文献
[1]姚文娟,陈懿强,叶志明,等. 耳听力系统生物力学研究进展[J]. 力学与实践, 2013, 35(6): 1-10.
YAO Wen-juan, CHEN Yi-qiang, YE Zhi-ming, et al. Advance in biomechanics of human ear as hearing system [J]. Mechanics in Engineering, 2013, 35(6): 1-10.
[2]Nie X, Liu H, Huang X, et al. Finite element model of human ear reconstruction through micro-computer tomography[J]. Acta Oto-Laryngologica, 2011, 131(3):269-276.
[3]王学林,胡于进. 蜗窗激励评价的有限元计算模型研究 [J]. 力学学报, 2012, 44(3): 622-630.
WANG Xue-lin, HU Yu-jin. Evaluation of round window stimulation by a FE model of human auditory periphery [J]. Chinese Journal of Theoretical and Applied Mechanics, 2012, 44(3): 622-630.
[4]Cheng T, Gan R Z. Experimental measurement and modeling analysis on mechanical properties of tensor tympani tendon [J]. Medical Engineering & Physics, 2008, 30(3): 358-366.
[5]Zhang X, Gan R Z. Dynamic properties of human tympanic membrane based on frequency-temperature superposition [J]. Annals of Biomedical Engineering, 2012, 41(1):205-214.
[6]Kim N, Homma K, Puria S. Inertial bone conduction: symmetric and anti-symmetric components[J]. Journal of the Association for Research in Otolaryngology, 2011, 12(3): 261-279.
[7]Greenwood D D. A cochlear frequency-position function for several species-29 years later[J]. Journal of the Acoustical Society of America, 1990, 87(6): 2592-2605.
[8]Gan R Z, Reeves B P, Wang X L. Modeling of sound transmission from ear canal to cochlea[J]. Annals of Biomedical Engineering, 2007, 35(12): 2180-2195.
[9]刘后广,塔娜,饶柱石. 悬浮振子对中耳声传播特性影响的数值研究 [J]. 力学学报, 2010, 42(1): 109-114.
LIU Hou-guang, TA Na, RAO Zhu-shi. Numerical study on the effect of the floating mass transducer on middle ear sound transmission [J]. Chinese Journal of Theoretical andApplied Mechanics, 2010, 42(1):109-114.
[10]Stieger C, Rosowski J J, Nakajima H H. Comparison of forward (ear-canal) and reverse (round-window) sound stimulation of the cochlea[J]. Hearing Research, 2013, 301: 105-114.
[11]Nakajima H H, Dong W, Olson E S, et al. Evaluation of round window stimulation using the floating mass transducer by intracochlear sound pressure measurements in human temporal bones [J]. Otology & Neurotology, 2010, 31(3): 506-511.
[12]Sun Q, Gan R Z, Chang K H, et al. Computer-integrated finite element modeling of human middle ear[J].Biomechanics and Modeling in Mechanobiology, 2002,2(1): 109-122.
[13]Kwacz M, Marek P, Borkowski P, et al. A three-dimensional finite element model of round window membrane vibration before and after stapedotomy surgery [J]. Biomechanics and Modeling in Mechanobiology, 2013: 1-19.
[14]Wang J, Zhao F, Li Y, et al. Effect of anterior tympanomeatal angle blunting on the middle ear transfer function using a finite element ear model[J]. Medical Engineering & Physics, 2011, 33(9): 1136-1146.
[15]Koike T, Wada H, Kobayashi T. Modeling of the human middle ear using the finite-element method [J]. The Journal of the Acoustical Society of America, 2002, 111(3): 1306-1317.
[16]Gan R Z, Sun Q, Feng B, et al. Acoustic-structural coupled finite element analysis for sound transmission in human ear-Pressure distributions[J]. Medical Engineering & Physics, 2006, 28(5): 395-404.
[17]Zhang X, Gan R Z. Finite element modeling of energy absorbance in normal and disordered human ears[J]. Hearing Research, 2013,301:146-155.
[18]Gan R Z, Yang F, Zhang X, et al. Mechanical properties of stapedial annular ligament [J]. Medical Engineering & Physics, 2011, 33(3): 330-339.
[19]Machiraju C, Phan A V, Pearsall A, et al. Viscoelastic studies of human subscapularis tendon: Relaxation test and a Wiechert model [J]. Computer Methods and Programs in Biomedicine, 2006, 83(1): 29-33.
[20]Park S, Schapery R. Methods of interconversion between linear viscoelastic material functions.part I-a numerical method based on prony series [J]. International Journal of Solids and Structures, 1999, 36(11): 1653-1675.
[21]Zhang X, Gan R Z. A comprehensive model of human ear for analysis of implantable hearing devices [J]. Biomedical Engineering, IEEE Transactions on, 2011, 58(10): 3024-3027.
[22]Zhang X, Gan R Z. Dynamic properties of human round window membrane in auditory frequencies running head: Dynamic properties of round window membrane[J]. Medical Engineering & Physics, 2013, 35(3): 310-318.
[23]Gan R Z, Wood M W, Dormer K J. Human middle ear transfer function measured by double laser interferometry system [J]. Otology & Neurotology, 2004, 25(4): 423-435.
[24]Wang X L, Hu Y J, Wang Z L, et al. Finite element analysis of the coupling between ossicular chain and mass loading for evaluation of implantable hearing device[J]. Hearing Research, 2011, 280(1): 48-57.
[25]Aibara R, Welsh J T, Puria S, et al. Human middle-ear sound transfer function and cochlear input impedance [J]. Hearing Research, 2001, 152(1): 100-109.
[26]Nakajima H H, Dong W, Olson E S, et al. Differential intracochlear sound pressure measurements in normal human temporal bones [J]. Journal of the Association for Research in Otolaryngology, 2009, 10(1): 23-36.
[27]Puria S, Peake W T, Rosowski J J. Sound-pressure measurements in the cochlear vestibule of human-cadaver ears [J]. The Journal of the Acoustical Society of America, 1997, 101(5): 2754-2770.
[28]王学林. 蜗窗激励与外耳道激励产生的耳蜗压力差的比较分析[J].生物医学工程学杂志,2012,29(6): 1109-1113.
WANG Xue-lin. Comparison of differential intracochlear pressures between round window stimulation and ear canal stimulation[J]. Journal of Biomedical Engineering, 2012,29(6):1109-1113.
[29]Zwislocki J. The role of the external and middle ear in sound transmission[J]. The Nervous System,1975, 3: 45-55.
[30]Merchant S N, Ravicz M E, Rosowski J J. Acoustic input impedance of the stapes and cochlea in human temporal bones [J]. Hearing Research, 1996, 97(1): 30-45.
[31]Wang X, Wang L, Zhou J, et al. Finite element modelling of human auditory periphery including a feed-forward amplification of the cochlea[J]. Computer Methods in Biomechanics and Biomedical Engineering, 2012,17(10): 1096-1107.
[32]Nakajima H H, Merchant S N, Rosowski J J. Performance considerations of prosthetic actuators for round-window stimulation [J]. Hearing Research,2010,263(1):114-119.
[33]Gentil F, Parente M, Martins P, et al. The influence of muscles activation on the dynamical behaviour of the tympano-ossicular system of the middle ear[J]. Computer Methods in Biomechanics and Biomedical Engineering, 2013, 16(4): 392-402.
[34]Aernouts J, Dirckx J J. Static versus dynamic gerbil tympanic membrane elasticity: derivation of the complex modulus[J].Biomechanics and Modeling in Mechanobiolo-gy, 2012,11(6): 829-840.
[35]Aernouts J, Aerts J R, Dirckx J J. Mechanical properties of human tympanic membrane in the quasi-static regime from in situ point indentation measurements [J]. Hearing Research, 2012, 290(1): 45-54.


