LiNi0. 5Mn1. 5O4正极材料的γ-Al2O3包覆及其性能
杨建文,叶 璟,何世丽,颜 波,刘彦生,张灵志( .桂林理工大学化学与生物工程学院,广西桂林 54006; .广西有色金属集团,广西梧州 54303)
LiNi0. 5Mn1. 5O4正极材料的γ-Al2O3包覆及其性能
杨建文1,叶璟1,何世丽2,颜波1,刘彦生1,张灵志1
( 1.桂林理工大学化学与生物工程学院,广西桂林541006; 2.广西有色金属集团,广西梧州543103)
摘要:以氢氧化铝溶胶为前驱体在LiNi0. 5Mn1. 5O4正极材料表面制备尖晶石结构γ-Al2O3包覆层,借助XRD、SEM、TEM及电化学方法对电极材料的主要性能进行了研究。结果表明: LiNi0. 5Mn1. 5O4表面γ-Al2O3包覆层形成条件为600℃下煅烧0. 5 h,较佳包覆量约为3 % (摩尔比) ;γ-Al2O3包覆层形貌完整,厚度约为5~10 nm,( 311)晶面间距约0. 24 nm;γ-Al2O3包覆的LiNi0. 5Mn1. 5O4正极材料30周充放电循环( 0. 2 C)后的比容量为112. 1 mAh/g,4 C倍率下的比容量为82. 0 mAh/g,容量保持率较基体分别提高了约10%和17. 2%。因此,γ-Al2O3包覆层减小了LiNi0. 5Mn1. 5O4与电解液的接触,有效抑制了基体与电解液之间的副反应,其电化学反应可逆性、循环稳定性及倍率性能得到了提高,有望用作动力锂离子电池正极材料。
关键词:LiNi0. 5Mn1. 5O4;γ-Al2O3;包覆;锂离子电池
锂离子电池具有工作电压高、比能量高、自放电率小、循环寿命长、绿色环保等优势,在便携式电子产品中已得到广泛应用,发展动力型锂离子电池是目前研究的热点。在LiCoO2、LiMn2O4、LiNi1/3Co1/3Mn1/3O2、LiFePO4等商业化的锂离子电池正极材料中,LiMn2O4具有资源丰富、价格低、电位高、安全性好、低温性能和倍率性能好等优点,是理想的动力电池正极材料[1-4]。
LiMn2O4正极材料规模化应用尚需解决Jahn-Teller效应、与电解液的副反应等问题,化学掺杂和表面包覆是改善这些不利因素的有效途径[3]。比较成功的LiMn2O4掺杂产物是尖晶石结构LiNi0. 5Mn1. 5O4( LNMO),其嵌锂电位为4. 7 V,理论容量146. 7 mAh·g-1,实际容量可达120 mAh·g-1,不存在Jahn-Teller效应,与安全型负极材料如钛酸锂、氧化物、氮化物等可以组成工作电压较高的新型电池体系[5-6]。LNMO的表面包覆改性材料主要有ZnO、Li3PO4、SiO2、Bi2O3、Al2O3、ZrP2O7、ZrO2、LiCoO2、LiAlO2、GaF3、FePO4、AlPO4、LiFe-PO4、Li4P2O7、BiOF、Li4Ti5O12、高分子聚合物等[7-20]。其中,Al2O3廉价、易制备,仅有Liu等[8]研究了无定形纳米多孔Al2O3对LNMO的表面包覆特性,对晶态Al2O3的包覆性能未见报道。笔者认为,γ-Al2O3为尖晶石结构,与LNMO基体具有一定的结构相似性,借助于氢氧化铝溶胶,有望形成微观界面结合良好的包覆层。据此,笔者以氢氧化铝溶胶为前驱体,探讨了γ-Al2O3的制备及其对LNMO正极材料的表面包覆性能。
1 实验部分
1. 1 LNMO的制备
以醋酸锂、醋酸镍、醋酸锰(均为分析纯)为原料,按化学计量比将三者溶于一定量去离子水中,在85℃下干燥1 h,再升温至130℃干燥2 h,得到淡绿色干凝胶,转入镍坩埚中加热燃烧完全后自然冷却,研磨成粉末,在通空气的管式炉内于800℃煅烧10 h,以1℃/min冷却至600℃,继续煅烧20 h,然后随炉冷却,研磨得到LNMO基体。
1. 2 LNMO的γ-Al2O3包覆
将分析纯硝酸铝溶解于去离子水中,滴加氨水至pH为9. 2,将氢氧化铝沉淀进行减压过滤,重新分散于水中,滴加硝酸,85℃老化24 h,得到氢氧化铝溶胶[21]。将LNMO基体置于小烧杯中,滴加氢氧化铝溶胶,超声波震荡使之分散均匀。然后转入100℃的烘箱中干燥、研磨,在管式炉中于600℃煅烧一定时间,随炉冷却,得到γ-Al2O3包覆的LNMO正极材料。按氢氧化铝溶胶的加入量计算γ-Al2O3包覆量,制备了包覆量为x的样品。
1. 3性能测试
本实验用荷兰产X’Pert Pro型X射线衍射仪对合成产物进行物相分析( Cu Kα,λ= 0. 154 056 nm,管压40 kV,管流10 mA,扫速4°/min,扫描范围2θ=10°~80°) ;日本产HITACHI S4800型场发射扫描电子显微镜( FESEM)观察合成样品的表面形貌;日本产JEM-2100F透射电子显微镜( TEM)观察包覆样品的组成结构。
将正极材料、乙炔黑和PVDF按质量比8∶1∶1混匀,加入适量的N-甲基吡咯烷酮制成浆料,涂敷在10 μm厚的铝箔上,在120℃下干燥12 h以上,裁剪成直径为14 mm的正极片。以金属锂为负极和参比电极,1 mol/L LiPF6/EC + DMC + DEC(体积比2∶2∶1)为电解液,Celgard 2400膜为隔膜,在充满氩气的手套箱中组装成CR2025型纽扣电池。在室温下,采用武汉蓝电Land 2001A电池性能测试仪测试电池的恒电流充放电性能,电压范围为3. 5~4. 9 V;上海辰华CHI860D电化学工作站测试电池的循环伏安曲线( CV,扫速0. 1 mV ·s-1)和电化学阻抗谱( EIS,频率10 kHz~0. 1 Hz,振幅5 mV)。
2 结果与讨论
2. 1 XRD分析
煅烧温度对氢氧化铝干凝胶结构的影响如图1所示。可见,氢氧化铝凝胶在450℃下焙烧4 h已经形成尖晶石结构γ-Al2O3,当温度提高至600、800℃时,衍射峰趋于清晰、尖锐,表明此时晶体结构发育更加完整,但是600℃以上变化并不显著。为了兼顾LNMO的退火温度,考察了600℃下焙烧时间对γ-Al2O3晶体结构的影响(图2)。可以看出,600℃下分别煅烧0. 5、4、8 h所得产物均为尖晶石结构γ-Al2O3( PDF#00-050-0741),时间依次延长,衍射峰的位置和强度均未发生显著变化,表明氢氧化铝干凝胶在600℃下煅烧时能够较快地生成结构稳定的γ-Al2O3。图3是基体LNMO及3%的γ-Al2O3包覆后的XRD谱,所有衍射峰均与LNMO的标准卡( PDF#80-2162)相对应[22]。图3b较图3a的衍射峰强度略有增大,可能因包覆层制备时热处理过程使基体的晶形继续发育所致。图3b中未见γ-Al2O3的衍射峰,这可能是γ-Al2O3包覆量较少的缘故[23]。

图1 氢氧化铝凝胶不同煅烧温度的XRD谱Fig. 61XRD patterns of aluminum hydroxide gel sintered at different temperatures

图2 氢氧化铝凝胶不同煅烧时间的XRD谱Fig. 62XRD patterns of aluminum hydroxide gel sintered for different times
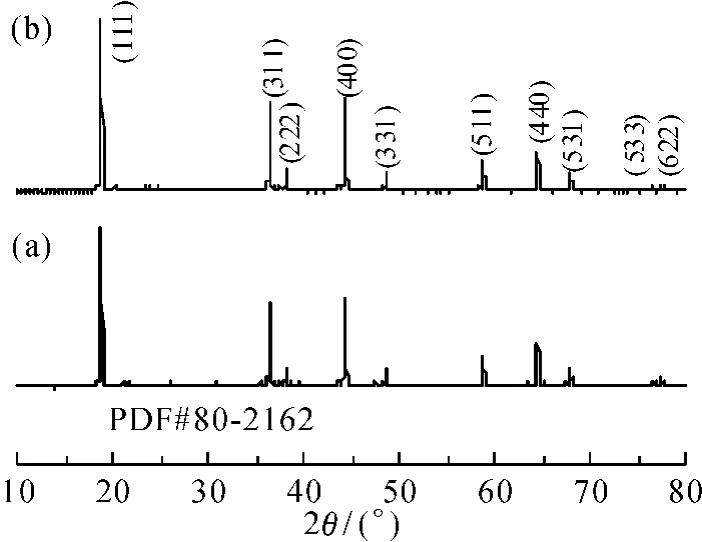
图3 LNMO ( a)及3%γ-Al2O3/LNMO( b)的XRD谱Fig. 63XRD patterns of bare LNMO ( a) and 3%γ-Al2O3/LNMO ( b)
2. 2 SEM和TEM分析
用FESEM观察基体和含3 %的γ-Al2O3包覆层样品的表面形貌,在图4a中,基体LNMO由大量粒度为200~400 nm的大颗粒和少量大小不等的小颗粒组成。粒度较大颗粒的晶形发育规整,晶棱、晶角尖锐清晰,晶面平整光滑;粒度较小颗粒的晶形特征不明显。在图4b中,γ-Al2O3包覆大颗粒LNMO仍然保持较规整的形貌,但是其晶棱、晶角模糊,不够清晰,晶面粗糙;小颗粒有增大、增多的趋势,这可能是由于小颗粒被γ-Al2O3包覆和部分γ-Al2O3未附着在基体表面的缘故。

图4 LNMO( a)及3%γ-Al2O3/LNMO( b)的SEM图Fig. 64SEM images of LNMO ( a) and 3%γ-Al2O3/LNMO ( b)
TEM测试结果见图5。图5a显示,基体LNMO表面有清晰的覆盖层,其厚度为5~10 nm。在高分辨率图(图5b)中,可以看到LNMO清晰的( 111)晶面和γ-Al2O3的( 311)晶面,其晶面间距分别为0. 47和0. 24 nm。包覆层和基体之间没有明显的界面,这表明包覆层与基体结合的比较紧密,可以较好地减少基体与电解液的接触;但是,包覆层并非致密连续的一个整体,包覆层颗粒之间存在边界或通道。同时,对比文献[9]可以发现,部分包覆层(图5b左上部分)也具有可供锂离子通过的多孔通道。

图5 γ-Al2O3/LNMO的TEM( a)和HRTEM( b)图Fig. 65TEM ( a) and HRTEM ( b) images of 3%γ-Al2O3/LNMO
2. 3电化学性能分析
图6为LNMO与其包覆样品的CV曲线。可以看出,基体及包覆样品在4. 7 V附近均具有较强的氧化还原峰,对应Ni2 +/Ni4 +电对的氧化还原过程[24];在4 V附近的氧化还原峰较弱,对应于Mn3 +/Mn4 +电对的氧化还原过程[24]。同时,包覆样品的CV峰形尖锐,峰电位差为0. 202 V,而基体的峰电位差较大( 0. 267 V),表明γ-Al2O3包覆层使LNMO脱/嵌锂过程的可逆性有所提高。γ-Al2O3包覆量对LNMO充放电性能的影响如图7所示,样品的充放电平台主要在4. 7 V附近[25]。γ-Al2O3包覆量为0、2%、3%、4%时,样品的放电容量依次为119. 2、117. 5、116. 4和111 mAh· g-1,其容量依次递减,充放电平台电位差有增大趋势,可能因包覆层质量增加导致电极过程极化增大所致。
γ-Al2O3包覆量对LNMO循环性能的影响如图8所示。可以看出,充放电循环次数增加,基体容量缓慢衰减,30周循环后容量从初始的120 mAh·g-1衰减到103. 4 mAh·g-1,容量保持率为85. 4%。γ-Al2O3的包覆量为2%、3%、4%时,初始容量依次为116、117和110 mAh·g-1,其30周循环后的容量为106. 1、112. 1和105. 3 mAh·g-1,容量保持率为91. 7%、96. 5%、96. 0%。可见,γ-Al2O3包覆使LNMO的循环性能得到了提高。这可能是包覆层有效的减少了LNMO在充放电过程中与电解液的副反应所致[8]。
γ-Al2O3包覆层对LNMO倍率性能的影响如图9所示。可以看出,当放电倍率从0. 2 C提高至0. 5、1、2、4 C时,样品容量均呈下降趋势。其中,基体容量下降幅度最大,对应容量分别为115. 1、102. 3、85. 9和58. 1 mAh·g-1;相反,3%γ-Al2O3包覆样品的容量下降幅度最小,对应容量分别为119、112、101. 5和81. 1 mAh·g-1,其对应容量保持率分别比基体高2. 4%、6. 9%、11. 3%、18. 3%。可见,γ-Al2O3包覆层的存在对基体的倍率性能有利,这可能由于包覆层减弱了基体与电解液之间的SEI膜效应,提高了锂离子的脱嵌速度,从而降低了活性材料在高倍率下的极化[17]。

图6 LNMO及3%γ-Al2O3/LNMO的CV曲线Fig. 66CV profiles of bare LNMO and 3%γ-Al2O3/LNMO

图70 .2C下LNMO和γ-Al2O3包覆LNMO的充放电曲线Fig. 67Charge and discharge curves of the bare and γ-Al2O3-coated-LNMO at 0.2 C

图80 . 2C下LNMO和γ-Al2O3包覆LNMO的循环性能Fig. 68Cycling performance of the bare and γ-Al2O3-coated LNMO at 0.2C
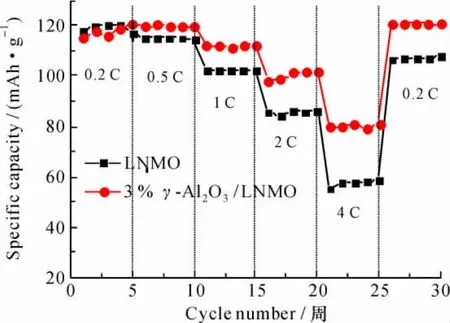
图9 LNMO和3%γ-Al2O3/LNMO的倍率性能Fig. 69Rate performance of the bare LNMO and 3%γ-Al2O3/LNMO
γ-Al2O3包覆层对LNMO的电化学阻抗谱的影响如图10所示。样品电池的阻抗谱(图10a)均由1个半圆和1段斜线组成。半圆代表电化学反应过程,与电荷传递电阻和双电层电容有关;半圆高频区与实轴的截距代表体系的欧姆电阻( Rs),与电解液、隔膜及电极接触电阻等因素有关;半圆低频区的截距( R1)代表嵌入反应电荷传递极化电阻,与电极形变、反应可逆程度、电极表面反应等因素有关;斜线代表电极活性材料体相中的离子扩散过程,此过程是电池反应的控制步骤。高频区不存在明显的固体电解质( SEI)膜阻挡层半圆,可能因γ-Al2O3覆盖层有效减少了基体的裸露表面。阻抗谱的等效模拟电路由图10b给出[26-27]。从图10a还可以看出,基体循环充放电过程中R1值从3周时的125. 2 Ω增长至30周时的298. 3 Ω,而γ-Al2O3包覆样品对应R1值仅从138. 8 Ω增长至195. 2 Ω,这表明γ-Al2O3包覆层较好地降低了LNMO电极材料的电荷转移极化电阻。
3 结论
( 1)以氢氧化铝溶胶为前驱体在LiNi0. 5Mn1. 5O4正极材料表面包覆γ-Al2O3,γ-Al2O3的用量(摩尔比)为基体的3%,制备条件为600℃下煅烧0. 5 h。包覆层为尖晶石结构,其形貌完整致密,晶面清晰,厚度为5~10 nm,( 311)晶面间距约0. 24 nm。
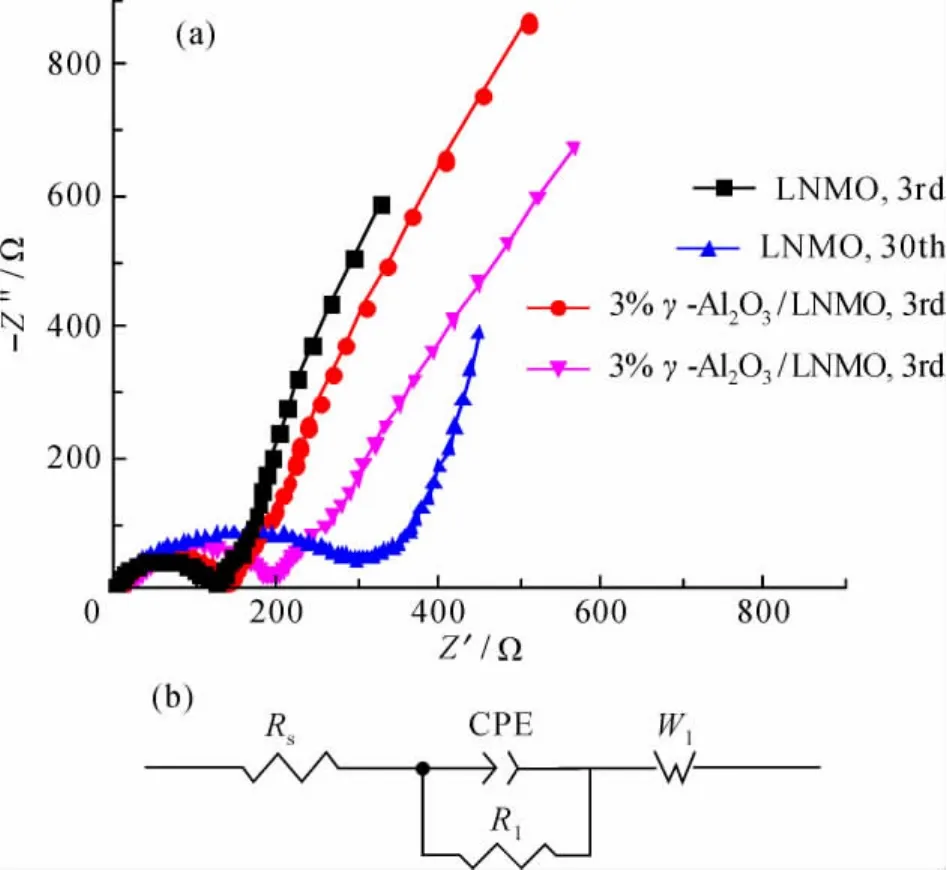
图10 LNMO与3%γ-Al2O3/LNMO的交流阻抗谱( a)及模拟电路( b)Fig. 610Nyquist plots ( a) and equivalent circuit ( b) of LNMO and 3%γ-Al2O3/LNMO
( 2)γ-Al2O3包覆层减少了LNMO与电解液的接触,较好地抑制了基体与电解液之间的副反应,从而使电极材料的电化学反应可逆性、循环稳定性和倍率性能得到提高。
参考文献:
[1]Thackeray M M,David W I F,Bruce P G,et al.Lithium insertion into manganese spinels[J].Mater.Res.Bull.,1983,18 ( 4) : 461-472.
[2]Padhi A K,Nanjundaswamy K S,Goodenough J B.Phosphoolivines as positive-electrode materials for rechargeable lithium batteries[J].J.Electrochem.Soc.,1997,144 ( 4) : 1188 -1194.
[3]Xia Y Y,Zhou Y H,Yoshio M.Capacity fading on cycling of 4 V Li/LiMn2O4cells[J].J.Electrochem.Soc.,1997,144 ( 8) : 2593-2601.
[4]Ohzuku T,Makimura Y.Layered lithium insertion material of LiCo1/3Ni1/3Mn1/3O2for lithium-ion batteries[J].Chem.Lett.,2001,30 ( 7) : 642-643.
[5]杨杰,杨建文,石阳,等.锂离子电池正极材料LiNi0. 5Mn1. 5O4的研究现状[J].化工新型材料,2012,40 ( 3) : 9 -11.
[6]Kunduraci M,Amatucci G G.Synthesis and characterization of nanostructured 4. 7 V LixMn1. 5Ni0. 5O4spinels for high-power lithium-ion batteries[J].J.Electrochem.Soc,2006,153 ( 7) : A1345-A1352.
[7]Sun Y K,Yoon C S,Oh I H.Surface structural change of ZnO-coated LiNi0. 5Mn1. 5O4spinel as 5 V cathode materials at elevated temperatures[J].Electrochimca Acta,2003,48 ( 5) : 503-506.
[8]Liu J,Manthiram A.Kinetics study of the 5 V spinel cathode LiMn1. 5Ni0. 5O4before and after surface modifications[J].J.Electrochem.Soc.,2009,156 ( 11) : A833-A838.
[9]Liu J,Manthiram A.Publisher's note: Kinetics study of the 5 V spinel cathode LiMn1. 5Ni0. 5O4before and after surface modifications[J].J.Electrochem.Soc.,2009,156 ( 12) : S13 -S13.
[10]Chong J,Xun S D,Song X Y,et al.Surface stabilized LiNi0. 5Mn1. 5O4cathode materials with high-rate capability and long cycle life for lithium ion batteries[J].Nano Energy,2013,2 ( 2) : 283-293.
[11]Sun Y K,Lee Y S,Yoshio M,et al.Synthesis and electrochemical properties of ZnO-coated LiNi0. 5Mn1. 5O4spinel as 5 V cathode material for lithium secondary batteries[J].Electrochem.Solid-State Lett.,2002,5 ( 5) : A99-A102.
[12]Kobayashi Y,Miyashiro H,Takei K,et al.5 V class all-solid-state composite lithium battery with Li3PO4coated LiNi0. 5Mn1. 5O4[J].J.Electrochem.Soc.,2003,150 ( 12) : A1577-A1582.
[13]Fan Y K,Wang J M,Tang Z,et al.Effects of the nanostructured SiO2coating on the performance of LiNi0. 5Mn1. 5O4cathode materials for high-voltage Li-ion batteries[J].Electrochimica.Acta,2007,52 ( 11) : 3870-3875.
[14]Wu H M,Belharouak I,Abouimrane A,et al.Surface modification of LiNi0. 5Mn1. 5O4by ZrP2O7and ZrO2for lithium-ion batteries[J].J.Power Sources,2010,195 ( 9) : 2909-2913.
[15]Hyo-Ree S,Cheol-Woo Y,Keon K.Improved electrochemical properties of LiNi0. 5Mn1. 5O4spinel material by surface modification with LiCoO2[C]/ / ACS National Meeting Book of Abstract,2011: 644.
[16]Cheng F Q,Xin Y L,Huang Y Y,et al.Enhanced electrochemical performances of 5 V spinel LiMn1. 58Ni0. 42O4cathode materials by coating with LiAlO2[J].J.Power Sources,2013,239: 181-188.
[17]Huang Y Y,Zeng X L,Zhou C,et al.Electrochemical performance and thermal stability of GaF3-coated LiNi0. 5Mn1. 5O4as 5 V cathode materials for lithium ion batteries[J].J.Mater.Sci.,2013,48 ( 2) : 625-635.
[18]Liu D L,Bai Y,Zhao S,et al.Improved cycling performance of 5 V spinel LiMn1. 5Ni0. 5O4by amorphous FePO4coating[J].J.Power Sources,2012,219: 333-338.
[19]Shi J Y,Yi C W,Kim K.Improved electrochemical performance of AlPO4-coated LiMn1. 5Ni0. 5O4electrode for lithium-ion batteries[J].J.Power Sources,2010,195 ( 19) : 6860-6866.
[20]Liu D Q,Trottier J,Charest P,et al.Effect of nano LiFePO4coating on LiMn1. 5Ni0. 5O45 V cathode for lithium ion batteries[J].J.Power Sources,2012,204: 127-132.
[21]吴建锋,徐晓虹,张欣.以硝酸铝为原料制备铝溶胶的研究[J].陶瓷学报,2007,28 ( 3) : 155-159.
[22]Liu D Q,Han J T,Goodenough J B.Structure,morphology,and cathode performance of Li1-x[Ni0. 5Mn1. 5]O4prepared by coprecipitation with oxalic acid[J].J.Power Sources,2010,195 ( 9) : 2918-2923.
[23]Lee Y H,Mun J Y,Kim D W,et al.Surface modification of LiNi0. 5Mn1. 5O4cathodes with ZnAl2O4by a sol-gel method for lithium ion batteries[J].Electrochimica Acta,2014,115: 326-331.
[24]杜国栋,努丽燕娜,冯真真,等.LiNi0. 5Mn1. 5O4-xFx高电压电极高温保存下的电化学行为[J].物理化学学报,2008,24 ( 1) : 165-170.
[25]唐致远,胡冉,王雷.5 V锂离子电池正极材料LiNi0. 5Mn1. 5O4的研究进展[J].化工进展,2006,25( 1) : 31-34.
[26]Chung S Y,Chiang Y M.Microscale measurements of the electrical conductivity of doped LiFePO4[J].Electrochemical.and Solid-State Letters,2003,6 ( 12) : A278-A281.
[27]Kim Y G,Dudney N J,Chi M F,et al.A perspective on coatings to stabilize high-voltage cathodes: LiMn1. 5Ni0. 5O4with sub-nanometer lipon cycled with LiPF6electrolyte[J].J.Electrochem.Soc.,2013,160 ( 5) : A3113-A3125.
Preparation and characteristics of γ-Al2O3coating on LiNi0. 5Mn1. 5O4cathode materials
YANG Jian-wen1,YE Jing1,HE Shi-li2,YAN Bo1,ZHANG Ling-zhi1
( 1. College of Chemistry and Bioengineering,Guilin University of Technology,Guilin 541006,China; 2. Guangxi Nonferrous Metals Group Co.Ltd.,Wuzhou 543103,China)
Abstract:γ-Al2O3-coated LiNi0. 5Mn1. 5O4cathode material was prepared using aluminum hydroxide sol as precursors.The properties of samples were characterized by XRD,SEM,TEM and electrochemical methods.The results indicate that the complete and compact γ-Al2O3nanoshell can be obtained by sintering at 600℃for 0. 5 h with Al2O3/LiNi0. 5Mn1. 5O4mole ratio of 3%.The coating thickness is about 5-10 nm.The crystal face is clear and the interplanar spacing of ( 311) is about 0. 24 nm.Al2O3-coated samples can still deliver a discharge capacity of 112. 1 mAh/g and 82. 0 mAh/g respectively after 30 full charge-discharge cycles at constant rates of 0. 2 C and 4 C.Al2O3-coated LiNi0. 5Mn1. 5O4samples show outstanding cyclability.The capacities of Al2O3-coated samples are 10% and 17. 2% higher than that of the bare ones after 30 charge-discharge cycles at rates of 0. 2 C and 4 C respectively.These mean that the Al2O3coating can effectively separate the electrolyte and LiNi0. 5Mn1. 5O4,which depresses the side reactions,resulting in better cycling performance,better rate capability,and better rate capability retention during cycling.These results prove that γ-Al2O3-coated LiNi0. 5Mn1. 5O4is a very promising cathode material.
Key words:LiNi0. 5Mn1. 5O4;γ-Al2O3; coating; Li-ion battery
作者简介:杨建文( 1968—),博士,研究员,研究方向:新能源材料,zhnyjw@163. com。
基金项目:国家自然科学基金项目( 51164006) ;广西科学研究与技术开发项目(桂科能1298025-9) ;广西建筑新能源及节能重点实验室项目( 110310802)
收稿日期:2014-03-14
doi:10. 3969/j.issn. 1674-9057. 2015. 01. 020
文章编号:1674-9057( 2015) 01-0126-06
文献标志码:A
中图分类号:TM912. 9
引文格式:杨建文,叶璟,何世丽,等.LiNi0. 5Mn1. 5O4正极材料的γ-Al2O3包覆及其性能[J].桂林理工大学学报,2015,35 ( 1) : 126-131.

