三七总皂苷对丙泊酚麻醉大鼠术后认知功能及海马NGF、BDNF表达的影响
三七总皂苷对丙泊酚麻醉大鼠术后认知功能及海马NGF、BDNF表达的影响
冯念海唐俊霞
(淄博市中心医院麻醉科,山东淄博255036)
摘要〔〕目的探究三七总皂苷对对丙泊酚麻醉大鼠术后认知功能及海马组织神经生长因子(NGF)、脑神经营养因子(BDNF)表达变化的影响。方法80只雄性大鼠随机分为正常对照组(N组),正常大鼠丙泊酚麻醉2 h组(B组),腹部探查组(P组),丙泊酚麻醉2 h腹部探查后给予三七总皂苷组(S组)。麻醉各组给予大鼠丙泊酚100 mg/kg腹腔注射。S组三七总皂苷剂量为10 mg/d,浓度为10 mg/ml,1次/d,连续7 d,检测各组大鼠的认知功能和NGF、BDNF的表达水平。结果术后3 d麻醉各组大鼠的逃逸潜伏期均明显增加(P<0.05);B组和S组术后7 d与术后3 d结果有显著差异(P<0.05)。与术前1 d相比,术后3 d麻醉各组穿台次数均明显减少(P<0.05);术后7 d与术后3 d相比,B组和S组的穿台次数均增加(P<0.05)。术后3 d,B、P、S组的NGF、BDNF mRNA相对表达量较N组显著降低(P<0.05);与术后3 d相比,术后7 d B、S、P组的NGF、BDNF mRNA相对表达量明显上升(P<0.05)。结论三七总皂苷对丙泊酚麻醉大鼠术后认知功能有改善作用,促进海马NGF、BDNF表达。
关键词〔〕三七总皂苷;丙泊酚;术后认知功能;神经生长因子;脑神经营养因子
中图分类号〔〕R614〔文献标识码〕A〔
第一作者:冯念海(1968-),男,副主任医师,主要从事老年麻醉研究。
丙泊酚通过激活GABA受体-氯离子复合物发挥镇静催眠作用〔1〕,普遍用于麻醉诱导、麻醉维持、ICU危重病人镇静,因为其起效迅速、诱导平稳、苏醒快且功能恢复完善、术后恶心呕吐发生率低〔2〕,现被广泛用于临床麻醉的诱导及维持、区域麻醉的镇静、门诊小手术和内镜检查的短时间麻醉。随着医疗水平的不断提高,围术期的并发症和死亡率明显降低,但术后认知功能障碍(POCD)的发生率一直居高不下〔3〕。但现在临床上还没有防止POCD发生的特别有效的措施。三七(Panaxnotoginseng),味甘、苦、性温,归肝、胃经,能散癖止血,消肿止痛〔4〕;主要成分包括阜苷、多糖、黄酮、三七素等,其中的主要活性成分是三七总皂苷(PNS)。现代药理学研究表明,PNS具有扩张外周血管、抑制血栓形成、降低血压等作用。已经证实PNS对脑神经细胞的损伤具有保护作用〔5〕,但其对于丙泊酚麻醉后POCD的影响研究尚少。本研究通过观察丙泊酚麻醉大鼠术后认知功能及海马组织神经生长因子(NGF)、脑神经营养因子(BDNF)表达变化,探究PNS对丙泊酚麻醉后POCD的影响。
1资料与方法
1.1实验动物健康清洁级SD大鼠85只,雄性,8~10周龄,体重200~220 g,购于中国科学院上海动物中心,光/暗周期为12 h/12 h,动物自由饮水进食。
1.2仪器及试剂丙泊酚(AstraZeneca UK Limited)、PNS、头孢曲松钠(苏州东瑞制药有限公司)、Morris水迷宫视频分析系统(上海吉量软件科技有限公司)、盐酸布比卡因注射液。
1.3分组及给药方案80只大鼠随机分为正常对照组(N组),正常大鼠丙泊酚麻醉2 h组(B组),腹部探查组(P组),丙泊酚麻醉2 h腹部探查后给予PNS组(S组),每组各19只。麻醉各组给予大鼠丙泊酚100 mg/kg腹腔注射。S组PNS剂量为10 mg/d,浓度为10 mg/ml,1次/d,连续7 d。
1.4实验方法
1.4.1术前Morris水迷宫训练及测试术前5 d开始对85只大鼠进行Morris水迷宫训练。训练第1天将大鼠放入水温为(24±2℃)的水中自由游泳,以熟悉环境,减少应激反应。待大鼠熟悉环境后引导大鼠上固定平台,平台固定于第3象限,停留20 s后推入水中,待其再次找到平台。训练3 d后,第4天Morris水迷宫选出训练合格的大鼠。以40 s内找到固定平台为合格。共选出76只合格大鼠,每组19只。第5天测试每组大鼠的定位航行能力和空间探索能力。
定位航行实验:将每组大鼠分别从NE(Ⅰ)、SE(Ⅱ)、NW(Ⅳ)坐标象限内标定的入水点将大鼠面放入水中,头朝向同侧,记录其寻找平台的时间,即逃避潜伏期(代表认知能力中的学习能力)。如超过120 s未能找到平台,按120 s计算。最终结果取平均值。
空间探索实验:定位航行实验后,实验参数不变,撤去平台,取第Ⅰ象限为入水点,将大鼠放入水中,记录其在120 s内运动轨迹及相应参数(第Ⅲ象限时间百分比、第Ⅲ象限路程、穿越平台次数),代表认知能力中的记忆能力。
1.4.2麻醉及手术测试结束后第2日对每组大鼠进行干预,前一晚所有大鼠禁食水。给药方式为腹腔注射。N组给予生理盐水;B组大鼠给予丙泊酚100 mg/kg麻醉诱导,保持大鼠自主呼吸,注意保暖,维持麻醉2 h,如有体动反应追加丙泊酚50 mg/kg。P组大鼠腹腔注射丙泊酚100 mg/kg行麻醉诱导,保持自主呼吸,观察呼吸动度等,注意保暖。对大鼠进行腹部探查术,时间为2 h,术中丙泊酚维持麻醉,并给予吸氧支持,术后腹腔注射头抱,预防感染。S组大鼠丙泊酚100 mg/kg麻醉诱导,保持大鼠自主呼吸,观察大鼠呼吸动度等生命指标,注意保暖。对大鼠进行开腹探查手术,丙泊酚维持麻醉2 h,麻醉过程中给予吸氧支持。过程中腹腔注射 PNS10 mg,术毕腹腔注射头孢,预防感染。苏醒后1 h常规进食饮水。
1.4.3术后用药及Morris水迷宫测试术后前3 d每天给予腹部探查各组大鼠腹部注射头孢曲松钠,1次/d,S组腹腔注射PNS 10 mg,连续1 w。各组大鼠于术后第3天及第7天进行Morris水迷宫测试(包括定位航行实验和空间探索实验)。
1.5海马NGF、BDNF表达水平沿大鼠双耳前连线剪开头皮,自枕骨大孔掀开头骨,暴露大脑组织,自大脑中段找到海马组织,仔细分离右侧海马组织,加入300 μl Trizol,匀浆后提取总RNA,进行逆转录。采用实时定量PCR法测定 NGF和BDNF的表达。引物序列:NGF正义:5' TGCCAAGGCGCAGCTTTCTATC3',反义:5'GTTTAGTCCAGTGGGCTTCAGGG3';BDNF正义:5'CTTCATAGGAGACCCTCCGCAAC3',反义:5'TCTGCCAAAAAGAGACCACAGCA3'。
1.6海马病理切片自大脑中段找到海马组织,仔细分离左侧海马组织,洗去血液,置于100 ml/L甲醛溶液中浸泡、固定24 h,脱水、透明、浸蜡、常规石蜡包埋,切片,苏木素-伊红(HE)染色,光镜下进行常规组织学检查。
1.7统计学方法应用SPSS19.0软件,计量资料采用t检验,计数资料采用χ2检验。
2结果
2.1各组大鼠逃逸潜伏期术后3 d的逃逸潜伏期均明显增加(P<0.05)。手术组术后7 d后逃逸潜伏期均有下降;B组和S组术后7 d与术后3 d结果有显著差异(P<0.05)。见表1。
2.2各组大鼠原平台穿越次数与术前1 d相比,术后3 d麻醉各组穿台次数均明显减少(P<0.05);术后7 d与术后3 d相比,B组和S组的穿台次数均增加(P<0.05);B组与S组相比无统计学差异(P>0.05)。见表2。
2.3海马NGF、BDNF表达水平见表3。术后3 d,与N组比较,B、P、S组的NGF、BDNF mRNA相对表达量显著降低(P<0.05);与术后3 d相比,术后7 d B、S、P组的NGF、BDNF mRNA相对表达量明显上升(P<0.05)。
表1 各组大鼠治疗前后逃逸潜伏期对比 ± s, n=19,s)
与术前1 d比较:1)P<0.05;与术后3 d比较:2)P<0.05;表2同
表2 各组大鼠治疗前后原平台穿越次数对比 ± s, n=19,次)
表3 各组大鼠术后NGF、BDNF表达水平比较
与N组相比:1)P<0.05,与术后3 d比较:2)P<0.05
2.4海马病理学改变N组海马锥体细胞排列紧密均匀;B组大鼠排列较紧密,少见固缩的神经元;P组大鼠锥体细胞排列疏松,胞核深染,固缩,胞间距较大;S组大鼠锥体细胞排列疏松,胞核淡染。见图1。
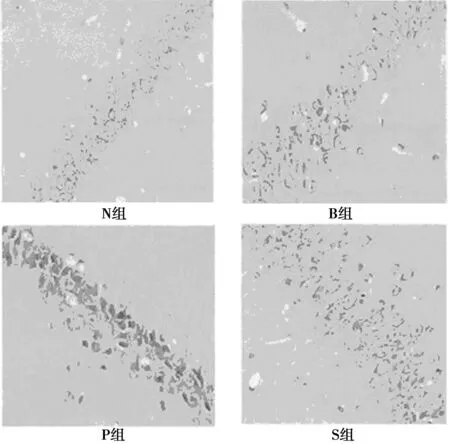
图1 各组大鼠海马病理学切片
3讨论
POCD临床表现为:记忆力、语言理解能力、注意力等的损害和社交能力的降低,可在术后数天到数周发生,也可能持续长久〔6〕。NGF是一类能促进中枢和外周神经分化和存活的活性蛋白质,在神经系统的发育和正常的生理功能中起着重要作用〔7〕。NGF主要分布于神经系统,而且在中枢神经系统(CNS)中海马内NGF蛋白水平也是整个脑中最高的,其主要作用是维持神经元存活,促进神经细胞的生长发育,促进神经元分化〔8〕。BDNF是一种分泌性蛋白,由人类脑源性神经营养因子基因编码,作为“神经营养因子”家族的成员〔9〕,可出现在大脑和外围神经系统,但BDNF在大脑皮质和海马中有的浓度很高〔10〕。BDNF在基底前脑区很活跃,这对于学习、记忆和高等思维至关重要。PNS能提高脑皮质内去甲肾上腺素(NE)、5-羟色胺(5-HT)和多巴胺(DA)的含量,提高突触素(Syp)的表达,改善痴呆模型的病理损伤和学习功能障碍。
本研究结果表明,丙泊酚麻醉会导致POCD,通过引起NGF、BDNF表达下降而发挥作用。术后长期使用PNS治疗,可明显促进海马内的NGF、BDNF表达,抑制神经细胞凋亡,提高学习能力和记忆能力,从而显著改善认知功能。
4参考文献
1Zhang H,Wang W,Gao W,etal.Effect of propofol on the levels of neurotransmitters in normal human brain;a magnetic resonance spectroscopy study 〔J〕.Neurosci Lett,2009;467(3):247-51.
2Moller JT,Cluitmans P,Rasmussen LS,etal.Long-term postoperative cognitive dysfunction in the elderly ISPOCD1 study〔J〕.Lancet,1998;351(9106):857-61.
3Alkire MT,Hudetz AG,Tononi G.Consciousness and anesthesia〔J〕.Science,2008;322(5903):876-80.
4鲍建才,刘刚,丛登立,等.三七的化学成分研究进展〔J〕.中成药,2006;28(2):246-53.
5马河,汤金土.三七皂苷的实验研究进展〔J〕.浙江中西医结合杂志,2002;12(3):197-9.
6Rudolph JL,Marcantonio ER,Culley DJ,etal.Delirium is associated with early postoperative cognitive dysfunction〔J〕.Anaesthesia,2008;63(9):941-7.
7路露,陈美婉,罗焕敏,等.神经营养因子受体的研究进展〔J〕.中国老年学杂志,2010;30(1):126-31.
8Harrison FE,Hosseini AH,McDonald MP.Endogenous anxiety and stress responses in water maze and Barnes maze spatial memory tasks 〔J〕.Behav Brain Res,2009;198(1):247-51.
9魏均娴,杜元冲.三七的现代科学与应用〔M〕.昆明:云南科技出版社,1996:19-47.
10宋希贵,王秀云,张书燕.中药调剂与鉴别彩色图谱〔M〕.北京:中国医药科技出版社,2009:137-8.
〔2014-09-17修回〕
(编辑袁左鸣)

