超高效液相色谱-四极杆-飞行时间质谱检测和鉴定猪尿中氯丙那林的主要代谢产物
毕言锋 , 王亦琳, 叶 妮, 孙 雷, 王鹤佳, 徐士新, 肖希龙
(1. 中国兽医药品监察所,国家兽药残留基准实验室,北京100081;2. 中国农业大学动物医学院,北京100193)
β-肾上腺受体激动剂(β-adrenergic agonists,β-AAs)是临床上常用的一类平喘药物。有研究发现,当使用剂量是推荐治疗剂量的5 ~10 倍时,克伦特罗、西马特罗等β-AAs 能促进动物脂肪代谢,并增加蛋白合成,具有明显的“营养再分配”作用[1-3]。因此,多种β-AAs 类化合物先后在养殖中作为促生长剂被大量使用,在我国也被称为“瘦肉精”。然而,由于克伦特罗残留在欧洲多个国家导致了多起食品中毒事故,欧盟、中国等先后禁止β-AAs 物质用作食品动物促生长剂[4,5]。近年来,作为新的“瘦肉精”替代品,β-AAs 类化合物氯丙那林(CLO)也被发现非法添加于饲料中[6]。同时,还出现了兽药制剂中添加氯丙那林的违法事件。为了保障动物源食品安全,农业部1519 号公告已经禁止盐酸氯丙那林等在饲料和动物饮水中使用[7]。
在分子结构上,β-AAs 类化合物一般具有苯乙醇胺(phenylethanolamine,PEA)母核以及不同的N-取代基(见图1)。Smith 等[8]的研究表明,苯环取代基类型是决定β-AAs 类化合物代谢特点的关键因素。当PEA 的苯环上有羟基(苯酚型,如莱克多巴胺、沙丁胺醇等)时,动物体内的主要代谢途径是酚羟基的葡萄糖醛酸或硫酸轭合,且轭合代谢产物是体内的主要残留形式。而对于克伦特罗等苯环取代基为氨基(苯胺型)的β-AAs,在动物体内可能发生氧化、轭合代谢,但主要残留形式为未代谢的原形。在检测动物尿液和组织中β-AAs 残留时,一般先对样品进行水解,然后测定游离态β-AAs 原形的总量[9-12]。
氯丙那林分子(结构式见图1a)的苯环上只有一个氯取代基,既不属于苯胺型,也不属于苯酚型。因此,氯丙那林在动物体内的主要代谢途径可能与其他β-AAs 类化合物不同。目前,氯丙那林在猪、牛等家畜体内的代谢研究还是空白,而在一些专门针对氯丙那林的残留分析方法中[13,14],并未对样品进行酶解,且直接将原形作为检测目标物。在本研究中,将利用超高效液相色谱-四极杆-飞行时间质谱(UPLC/Q-TOF MS)技术,检测和鉴定猪口服氯丙那林后尿液中的主要代谢产物,研究氯丙那林在猪体内的主要代谢途径。

图1 (a)氯丙那林、(b)克伦特罗和(c)莱克多巴胺的分子结构Fig.1 Structures of (a)clorprenaline,(b)clenbuterol and (c)ractopamine
1 实验部分
1.1 仪器与试剂
超高效液相色谱-四极杆-飞行时间质谱仪(Waters Acquity UPLC-SYNAPT HDMS,美国Waters公司);猪代谢笼(北京人和机械厂);高速离心机(德国Thermo 公司);涡旋振荡器(MS-3,德国IKA公司);氯丙那林(含量>95%,中国食品药品检定研究院);乙腈(HPLC 级,美国Thermo Fisher Scientific 公司);甲酸(分析纯,北京试剂公司)
1.2 样品采集及处理
长白猪(购自北京市苏家坨养殖场),体重30 ~40 kg。代谢实验前,动物在代谢笼中适应一周,饲喂空白饲料,自由饮水。给药前禁食12 h,不禁水。按10 mg/kg (b. w.)的剂量,口服给药一次。给药后,自由采食进水。收集给药前12 h 内的尿液,作为空白样品。收集给药后24 h 内的尿液,8 000 r/min 离心10 min,取上清液于-20 ℃冷冻保存。
取以上样品500 μL 于5 mL 塑料离心管中,加入乙腈溶液2.0 mL,充分涡旋振荡后,以5 000 r/min 离心10 min,转移上清液。按照以上方法,重复提取一次。合并上清液,在50 ℃氮气流下浓缩至小于0.5 mL。用水定容至0.5 mL 后,以12 000 r/min 离心10 min,取上清液过0.22 μm 滤膜后,供UPLC/Q-TOF MS 分析。
1.3 UPLC/Q-TOF MS 条件
色谱柱采用ACQUITY HSS T3柱(100 mm×2.1 mm,1.7 μm),柱 温30 ℃,流 速0.400 mL/min,进样体积2 μL。流动相A 为含0.1% 甲酸的乙腈,流动相B 为含0.1% 甲酸的水溶液,梯度洗脱程序如下:0 ~1.0 min,保持2% A;1.0 ~5.0 min,流动相A 的比例由2% 线性变化至30%;5.0~7.0 min,流动相A 的比例由30% 线性变化至60%;7.0 ~9.0 min,流动相A 的比例保持95%;9.0 ~11.0 min,保持流动相A 的比例为2%。
Q-TOF MS 采用电喷雾正离子源(ESI+);毛细管电压3.0 kV;电离源温度120 ℃,锥孔电压20 V,数据采集质量范围为50 ~1 000 Da;数据采集方式为MSE模式,一级质谱(MS)碰撞能量为4 eV,二级质谱(MS/MS)碰撞能量为10 ~30 eV。检测前,采用甲酸钠溶液进行精确质量校正,并用亮氨酸-脑啡肽溶液([M+H]+,m/z 556.277 1 Da)进行实时质量锁定。
1.4 代谢物检测和结构鉴定
采用MetaboLynx XS 软件对UPLC/Q-TOF MS 采集的数据进行处理。首先,对数据进行质量亏损过滤(MDF)处理,消除内源性代谢物的干扰。在MDF 处理时,以氯丙那林(C11H17NOCl,[M +H]+=214.099 9 Da)为模板(template),MDF 的阈值为±50 mDa。然后,根据氯丙那林可能代谢途径的精确质量变化,进行离子色谱峰提取(EIC),筛查可能的代谢产物。其中,在EIC 处理中,保留时间和精确质量的误差分别为±0.05 min 和±10 mDa。最后,根据MSE采集的MS/MS 信息,对比代谢产物和原形的主要碎片离子,对代谢产物的结构进行鉴定。
1.5 相对含量计算
由于无法得到所有代谢物的对照品,因此,只能根据EIC 的峰面积估算氯丙那林原形或代谢物的相对含量。具体计算公式如下:氯丙那林或代谢物相对含量=峰面积CLO或代谢物/(峰面积CLO+峰面积CLO_M1+……+峰面积CLO_M9)×100%。
2 结果与讨论
2.1 氯丙那林的质谱裂解特征
根据UPLC/Q-TOF MS 采集的MS/MS 信息(见图2),氯丙那林的准分子离子([M+H]+)可以产生4 个主要的碎片离子,分别为m/z 196、m/z 154、m/z 118 和m/z 91,其元素组成、精确质量数(exact mass,EM)和不饱和度(double bond equivalent,DBE)分别见表1。
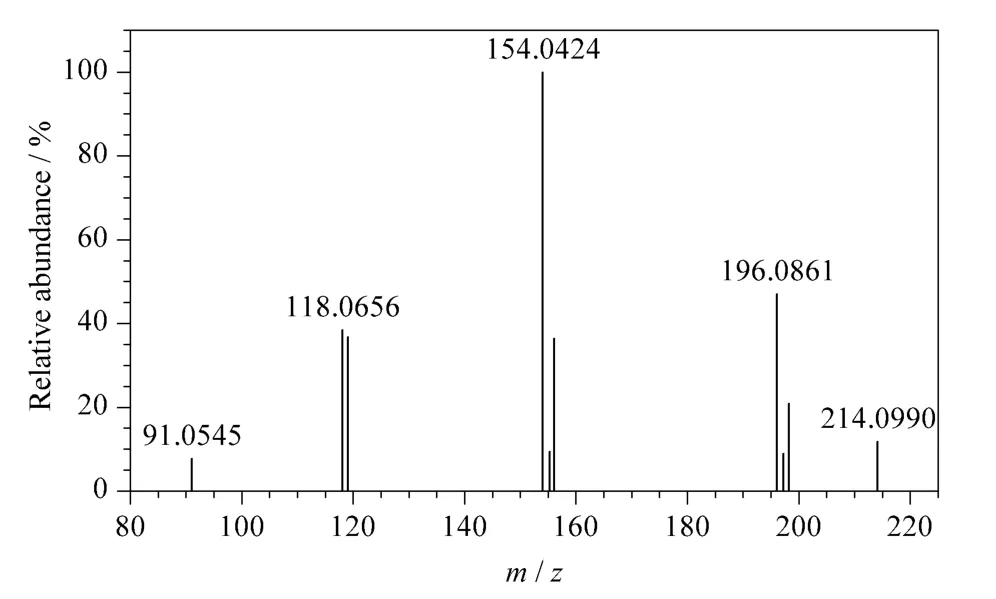
图2 氯丙那林的MS/MS 图Fig.2 MS/MS spectrum of clorprenaline

表1 氯丙那林的[M+H]+及其主要碎片离子的元素组成、EM 理论值及测量值、不饱和度(DBEs)和质量偏差Table 1 Element compositions,exact masses,DBEs and mass errors of[M+H]+and fragment ions of clorprenaline


图3 氯丙那林的质谱碎裂途径Fig.3 Proposed fragmentation pathways of clorprenaline
2.2 代谢产物鉴定
除氯丙那林原型外,在猪尿液中还检测到9 种主要代谢产物,其中,Ⅰ相代谢产物2 种,Ⅱ相代谢产物7 种。氯丙那林及其代谢产物的UPLC 保留时间(RT)、精确质量数、元素组成和相对含量等见表2。另外,9 种代谢产物(CLO_M1 ~ CLO_M9)的EICs 谱图和MS/MS 谱图分别见图4 和图5。
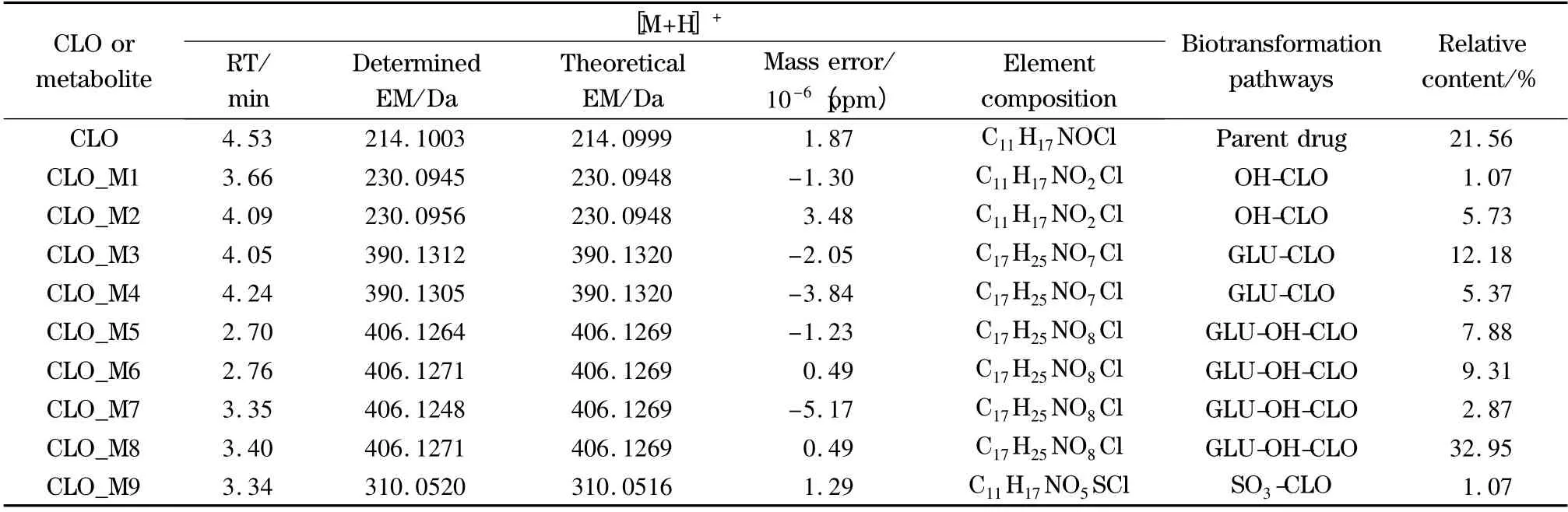
表2 猪尿样品中氯丙那林及其代谢产物的色谱-质谱信息、代谢途径和相对含量Table 2 LC-MS information,biotransformation pathways and relative contents of clorprenaline and its metabolites in swine urine

图4 猪尿中氯丙那林代谢产物(CLO_M1 ~CLO_M9)的EIC 图Fig.4 EICs of clorprenaline metabolites (CLO_M1-CLO_M9)in swine urine
2.2.1 Ⅰ相代谢产物
代谢物CLO_M1(m/z 230.094 5,RT =3.66 min)与CLO_M2(m/z 230.095 6,RT =4.09 min)的[M+H]+的元素组成都为C11H17NO2Cl(EM 理论值为230.094 8 Da),比氯丙那林(C11H17NOCl)多一个氧原子。MS/MS 图(图5)显示,M1 和M2 具有相同的碎片离子m/z 212、m/z 170 和m/z 134,比氯丙那林的特征碎片离子m/z 196、m/z 154 和m/z 118 大16 Da,说明CLO_M1 和CLO_M2 是氯丙那林的氧化产物。另外,碎片离子m/z 170(C8H9NOCl)和m/z 134(C8H8NO)的存在,说明氧化代谢反应发生在苯环上,而不是侧链的N-异丙基上。因此,CLO_M1 和CLO_M2 被确定为氯丙那林的苯环羟基化代谢产物(OH-CLO),可能的质谱裂解途径见图6。
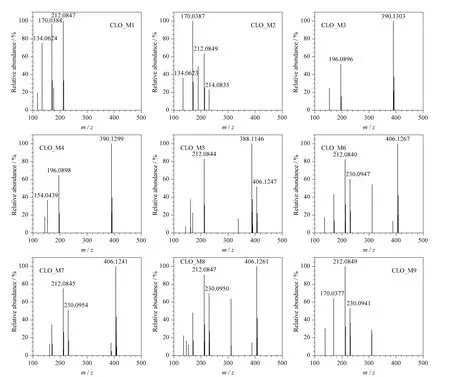
图5 氯丙那林代谢产物(CLO_M1 ~CLO_M9)的MS/MS 图Fig.5 MS/MS spectra of clorprenaline metabolites (CLO_M1-CLO_M9)
2.2.2 Ⅱ相代谢产物
代谢物CLO_M3(m/z 390.131 2,RT =4.05 min)和CLO_M4(m/z 390.130 5,RT =4.24 min)的[M+H]+的元素组成为C17H25NO7Cl(EM 理论值为390.132 0 Da),比氯丙那林多C6H8O6(EM 理论值为176.032 1 Da)。同时,CLO_M3 和CLO_M4都具有与氯丙那林相同的特征碎片离子m/z 196和m/z 154(见图5),因此,可以确定它们为氯丙那林的葡萄糖醛酸轭合产物(GLU-CLO),可能的轭合反应位点为β-羟基或脂肪仲胺。

图6 OH-CLO 可能的质谱裂解过程Fig.6 Proposed fragmentation pathways of OH-CLO
代谢物CLO_M5(m/z 406.126 4,RT =2.71 min)、CLO_M6(m/z 406.127 1,RT =2.75 min)、CLO_M7(m/z 406.124 8,RT =3.35 min)和CLO_M8(m/z 406.127 1,RT =3.41 min)的[M+H]+的元素组成全部为C17H25NO8Cl(EM 理论值为406.126 9 Da),比OH-CLO(CLO_M1 和CLO_M2)多C6H8O6(EM 理论值为176.032 1 Da)。同时,它们都具有与OH-CLO(CLO_M1 和CLO_M2)相同的特征碎片离子m/z 212 和m/z 170(见图5)。因此,CLO_M5、CLO_M6、CLO_M7 和CLO_M8 是OH-CLO 的4 种葡萄糖醛酸轭合物(GLU-OHCLO)。
在OH-CLO 分子中,β-羟基、脂肪仲胺或酚羟基都可能与葡萄糖醛酸轭合。有研究[8]表明,对于苯环上有羟基的β-AAs 化合物(如莱克多巴胺等),酚羟基比β-羟基和仲氨基更容易与葡萄糖醛酸发生轭合反应。从图4 可以看出,CLO_M8 的质谱响应明显大于其他GLU-OH-CLO 的同分异构体。因此,可以推测CLO_M8 的轭合位点可能在苯环上的羟基上。然而,只根据质谱所采集的碎片离子信息,还无法准确确定轭合反应发生的具体位置。
代谢物CLO_M9(m/z 310.052 0,RT =3.34 min)的[M+H]+对应的元素组成为C11H17NSO5Cl(EM 理论值为310.051 6 Da),比OH-CLO(CLO_M1 和CLO_M2)多SO3(EM 理论值79.956 8 Da)。同时,CLO_M9 可以失去SO3生成碎片离子m/z 230(C11H17NO2Cl),并具有与OH-CLO 相同的特征碎片离子m/z 212 和m/z 170(图5)。因此,可以确定CLO_M9 为OH-CLO 的硫酸轭合产物(SO3-OH-CLO)。另外,在尿液中没有发现氯丙那林的硫酸轭合产物(C11H17NSO4Cl,[M+H]+=294.056 7 Da),说明β-羟基和脂肪仲胺不易与硫酸轭合。由此可以推测,CLO_M9 的硫酸轭合位点在苯环羟基化引入的酚羟基上。
2.3 氯丙那林在猪体内的主要代谢途径
在本研究中,利用UPLC/Q-TOF MS 在猪尿中检测和鉴定了氯丙那林的2 种Ⅰ相代谢产物和7 种Ⅱ相代谢产物。根据代谢物鉴定结果,推测氯丙那林在猪体内先发生苯环羟基化和葡萄糖醛酸轭合,而羟基化氯丙那林(OH-CLO)还能继续与葡萄糖醛酸和硫酸轭合(见图7)。

图7 氯丙那林在猪体内的主要代谢途径Fig.7 Proposed metabolic pathways of clorprenaline in swine
本研究的结果表明,与其他β-AAs 化合物相似,氯丙那林在猪体内的主要代谢途径也是氧化和轭合反应。以前的研究显示,苯胺型的克伦特罗在牛和猪体内的氧化代谢主要发生在苯胺上[14,15]。然而,由于苯环上的取代基类型不同,氯丙那林的氧化代谢主要是苯环的羟基化。另外,氯丙那林也能通过β-羟基和仲氨基与葡萄糖醛酸轭合,但没有发现其硫酸轭合产物。
氯丙那林的羟基化代谢产物(OH-CLO)含有一个酚羟基,结构特点与苯酚型β-AAs(如莱克多巴胺)相似。本研究发现,OH-CLO 的代谢特征与莱克多巴胺相同[8,16],可 以生成 葡萄糖 醛酸轭 合物(GLU-OH-CLO)和硫酸轭合产物(SO3-OH-CLO)。另外,OH-CLO 及其轭合物(GLU-OH-CLO 和SO3-OH-CLO)的相对含量为60.9%,明显高于氯丙那林原形及其轭合产物(39.1%)。因此,羟基化及轭合反应是氯丙那林在猪体内的主要代谢途径。
3 结论
本文采用UPLC/Q-TOF MS 鉴定了猪尿中氯丙那林的9 种代谢产物,并推测了氯丙那林在猪体内的主要代谢途径——苯环羟基化、葡萄糖醛酸轭合和硫酸轭合。本研究还发现,羟基化氯丙那林及其轭合物是尿液中的主要代谢产物,这将为确定氯丙那林在动物体内的残留标示物提供科学依据。
[1] Williams P E,Pagliani L,Innes G M,et al. Brit J Nutr,1987,57:417
[2] Bergen W G,Johnson S E,Skjaerlund D M,et al. J Anim Sci,1989,67:2255
[3] Chikhou F H,Moloney A P,Allen P,et al. J Anim Sci,1993,71:906
[4] Council Directive 96/22/EC
[5] Announcement of the Ministry of Agriculture No. 176 of P.R. China (中华人民共和国农业部公告第176 号),2002
[6] Cao Y,Huang S X,Li D N. Chinese Journal of Veterinary Drug (曹莹,黄士新,李丹妮. 中国兽药杂志),2007,41(12):30
[7] Announcement of the Ministry of Agriculture No. 1519 of P.R. China (中华人民共和国农业部公告第1519 号),2010
[8] Smith D J. J Anim Sci,1998,76(1):173
[9] Miao H,Zou J H,Fan S,et al. Chinese Journal of Chromatography (苗虹,邹建宏,范赛,等. 色谱),2010,28(6):572
[10] Cai Q R,Wu J S,Qian Z J,et al. Chinese Journal of Chromatography (蔡勤仁,吴洁珊,钱振杰,等. 色谱),2013,31(3):200
[11] Li D,Sun L,Bi Y F,et al. Chinese Journal of Veterinary Drug (李丹,孙雷,毕言锋,等. 中国兽药杂志),2013,47(12):50
[12] Nie J R,Zhu M L,Lian J,et al. Chinese Journal of Chromatography (聂建荣,朱铭立,连槿,等. 色谱),2010,28(8):759
[13] Zou Y D,Ren T T,Wu Y B,et al. Journal of Analytical Science (邹永德,任甜甜,吴银宝,等. 分析科学学报),2014,30(1):119
[14] Zalko D,Bories G,Tulliez J. J Agric Food Chem,1998,46(5):1935
[15] Zalko D,Debrauwer L,Bories G,et al. Chem Res Toxicol,1997,10(2):197
[16] Smith D J,Feil V J,Paulson G D. Xenobiotica,2000,30(4):427
——α-葡萄糖醛酸酶的研究进展*

