酱油中甜蜜素应用气相色谱法的含量测定
◎刘清清
(江苏省食品药品监督检验研究院,江苏 南京 210008)
甜蜜素的化学名称为环已基氨基磺酸钠(C6H12NaO3S),其主要的用途是提升食品中的甜度,其属于化学类的调味品。而且它的口感非常好,且价格非常低。所以,经常被人们使用在饮料、糕点等生产中。而且,它的甜度只有人们日常生活中所见的糖精的1/30。所以,添加到饮料或者是糕点等食品中并不会让人们在适用的时候感觉非常甜腻。但是,这种甜蜜素毕竟是一种化学产品,使用过量的情况下,一定会使得人体的健康受到影响,比如肝脏及神经系统等都会受到一定程度的影响。所以,我国颁布了一个强制性的条例,其中明确地规定了甜味剂等的使用范围和使用剂量等,而且甜味剂等本身的质量我国也有相应的规定。我国的酱油中也含有一定程度的甜蜜素,按照我国的检测标准来说,是不能够检测到甜蜜素在酱油中存在的。
1 材料与方法
实验所使用的检测仪器主要有岛津的GC2010带FID检测器等。使用的试剂主要有正己烷、氯化钠、亚硝酸钠等物质,按照标准来配置溶液,使用RO水加上甜蜜素标准品混合配置成10 mg/mL的储备液。而试验中所使用的气相色谱柱是使用的岛津公司的30 m×0.25 μm×0.25 rm、分流/不分流进样口、温度大约在200 ℃的毛细管色谱柱,其分流进样的比例为10∶1。而且需要使用纯度在99%的氮气,其流速大约在40 mL/min。此外,还对空气、氢气等方面有一定的要求。对于标准曲线的制作则需要按照国家的标准,先将固体的甜蜜素标准样品通过精确称称出1.000 0 g的量,然后加入到水中溶解后放入100 mL的量瓶中,然后将其配置成10 mg/mL浓度的标准溶液,然后在按照标准分别得吸取这个溶液加入到100 mL带塞的比色管中,再往里加入蒸馏水大约在20 mL即可,然后将其混合均匀后放置到冰浴中。再依次分别加入5 mL的亚硝酸溶液及硫酸溶液,均匀摇晃后放在冰浴中大约30 min即可,这个时间段注意应不停地摇晃溶液,然后在加入10 mL的正己烷和5 g的氯化钠摇匀,并放置到仪器上振动1 min,待己烷层分离出来后,再吸取2 L样品放入到仪器中进行检测即可。
2 结果与讨论
2.1 改进样品处理方式
将准确的20.0 g样品放在100 mL带塞的比色管中,并放置于冰浴中,再按照上述的添加亚硝酸溶液等方式进行添加,待静置后将正己烷吸出,并放入10 mL带塞的离心管中进行分离,上层的正己烷则放入气相色谱进行分析。但在实际的操作过程中,会出现大量泡沫的问题,从而使得静置后无法分层,也就无法将上层的正己烷吸出。因此,改善的方式是将样品的量和试剂的量减少,并直接将正己烷进行离心,不需要将其含有的环乙醇亚硝酸酯分离后在进行离心。这样不仅简化了操作过程,还使得乳化不分层的问题得到了解决。
2.2 试验结果
表1为20 g样品放入100 mL比色管中分析后的结果。
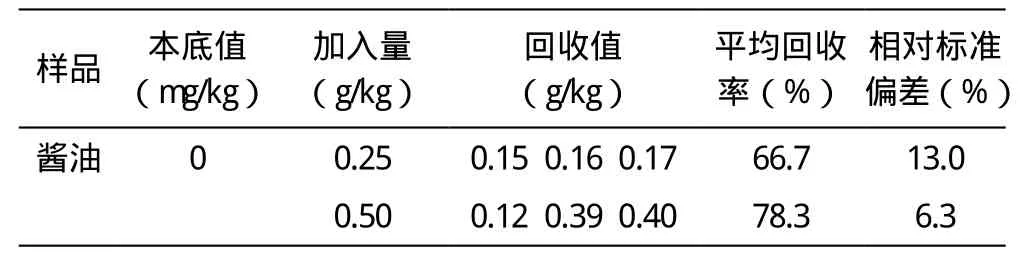
表1 酱油中甜蜜素应用气相色谱法的含量测定结果
2.3 标准曲线的线性范围
上文中的实验条件下,将甜蜜素的含量作为横坐标,而峰面积则作为纵坐标,绘制标准曲线,其具 体 为 Y=8.944e-0.07×X-4.601 77-0.02,R=0.998 7,R2=0.997 568。由此可知,甜蜜素的含量范围大约在0.1~1.0 mg/mL。
2.4 注意事项
在实验过程中,实验人员要注意对样品的处理,要加入5 mL 50 g/L的亚硝酸溶液,以及5 mL 100 g/L的硫酸溶液,然后要摇匀,在摇匀的时候一定要注意刚开始时要保持缓慢,并且随时打开瓶盖进行放气处理,以防瓶内气压过大使得瓶子破裂,从而液体飞溅使得实验人员受到伤害。
3 结论
在实验的过程中,对于样品的处理可以按照上文中所使用的方式。此外,要注意提前将正己烷进行离心,然后将正己烷吸出后,能够有效解决掉溶液乳化不分层的问题。而且通过气相色谱分析,发现甜蜜素的回收率比较高,而且气相色谱法的精准度也很高。此外,使用石英的毛细管柱及程序的升温可以很有效地将溶剂峰与甜蜜素峰进行分离,而且还能够减少沸点高的残留物,从而对色谱柱提供一个保障,并且降低杂质的干扰。通过本文中的实验可以看出,酱油中甜蜜素的平均回收率较高,变差相对而言不是很大。所以,按照这种实验方式,并适当地进行改良可以用于检测酱油中的甜蜜素是否达标。
[1]洪晓峰.气相色谱法测定酱油中甜蜜素含量的探讨[J].福建分析测试,2012(2):42-44.
[2]肖聪伟,王磊,陈建芳,等.程序升温毛细管气相色谱法测定食品中甜蜜素含量方法研究[J].科技广场,2012(12):145-147.
[3]王悦宏.快速测定HVP和酱油中3-MCPD方法的研究与应用[D].长春:东北师范大学,2008.
[4]李秀勇.色谱法在食品分析中的应用研究[D].兰州:兰州大学,2008.
[5]刘波.甜蜜素检测方法研究进展[J].中国食品添加剂,2007(2):218-222.
[6]潘一,郭泽,王春龙,等.酱油成分检测方法的研究进展[J].中国调味品,2013(3):14-17.

