双酚A在离子液体修饰碳糊电极上的电化学行为及测定
花小霞,郑香丽,刘 珊,夏方诠,周长利*
(济南大学化学化工学院,山东 济南 250022)
双酚A在离子液体修饰碳糊电极上的电化学行为及测定
花小霞,郑香丽,刘 珊,夏方诠,周长利*
(济南大学化学化工学院,山东 济南 250022)
制备1-氰乙基-3-甲基咪唑六氟磷酸盐离子液体修饰碳糊电极,研究双酚A(bisphenol A,BPA)在离子液体修饰碳糊电极上的电化学行为。结果表明,在0.1 mol/L B-R缓冲液(pH 10.0)中,BPA在0.415 V处产生一良好的氧化峰,具有明显的电催化增敏作用。BPA的氧化过程为伴随有质子转移的表面吸附控制的不可逆过程,其电极反应速率为0.32/s。建立了示差脉冲伏安法测定痕量BPA的方法,线性范围为3.0×10-7~6.0×10-5mol/L,检出限为5.0×10-8mol/L(RSN=3)。并将其用于奶瓶样品中迁移BPA的测定,结果表明该传感方法为直接电化学检测BPA提供了一种新的思路。
离子液体;化学修饰电极;双酚A;食品检测
双酚A(bisphenol A,BPA)是一种类雌激素,可对人类的生殖以及后代的生存能力产生负面影响[1],长期接触BPA对于脑部和心血管系统有很大的危害[2-5]。而作为一种添加剂,BPA普遍存在于罐头包装的内衬、饮料和食品的包装袋及奶瓶中。因此建立一种快速、灵敏、简便、准确检测BPA的方法非常有意义。目前,许多技术已用于BPA的检测,如:色谱及其联用技术[6-9]、荧光分析法[10-11]、酶联免疫分析法[12-13]等。但这些方法存在仪器设备昂贵、前处理复杂和线性范围窄等缺陷。近年来,化学修饰电极由于其具有仪器简单、低消耗、简捷快速、灵敏度高、选择性好和原位分析等优点,获得了广泛应用[14-18]。Tu Xinman等[3]构建了基于多壁碳纳米管/金纳米粒子复合膜修饰的玻碳电极,检测塑料中的BPA。利用带有正电荷的表面活性剂的静电吸附作用将带负电荷的多壁碳纳米管和金纳米颗粒层层自组装在玻碳电极表面。Poorahong等[5]采用聚苯胺纳米棒/多壁碳纳米管修饰的石墨电极检测婴儿奶瓶中的BPA。Zhou Jianqing等[12]用酶标记的BPA与目标物BPA竞争的方式,通过测定酶底物显色强度来测定目标BPA的浓度。Niu Xiuli等[16]制备了多层石墨烯纳米纤维/金纳米粒子复合物修饰的玻碳电极,检测奶瓶中BPA。针对BPA小分子,通常电极制备都比较复杂,同时纳米材料的制备要求较高,酶的活性不易维持,实际应用效果也不尽如意。因此发展一种简捷的电极修饰技术,建立快速、灵敏的测定方法成为研究重点。离子液体导电率高、电化学窗口宽、黏结性和机械性好的特点[19-20],使其在电化学和电分析化学领域中具有较明显的优点,在修饰电极与传感器中的应用也越来越引起人们的关注[21-23]。
本实验组装了离子液体1-氰乙基-3-甲基咪唑六氟磷酸盐(1-cyanoethyl-3-methylimidazolium hexafl uorophosphate,CMΙMPF6)离子液体碳糊修饰电极(ionic liquid carb on paste electrodes,ΙLCPE),研究了BPA在修饰电极上的电化学行为及其电极过程,建立了BPA灵敏快速的分析方法,应用于奶瓶中迁移BPA含量的测定,结果满意。该工作为进一步研究功能化离子液体修饰电极在电分析化学中的应用,提供了良好的基础。
1 材料与方法
1.1 试剂与仪器
CMΙMPF6上海成捷化学有限公司;石墨粉(光谱纯)、BPA(化学纯),其他试剂均为分析纯,实验用水均为二次石英亚沸重蒸水。
ΙM6x电化学工作站 德国Zahner公司;CHΙ842C电化学分析仪 上海辰华仪器公司。
实验使用三电极系统,碳糊电极或离子液体修饰碳糊电极为工作电极,Ag/AgCl电极为参比电极,铂丝为对电极。
1.2 方法
1.2.1 电极的制备
将石墨粉和离子液体混合(4∶1,m/m)后,取1 g混合物于研钵中,混匀。加入200 μL液体石蜡,充分研匀后装入玻璃管(Φ=5 mm)中,压紧,用铜丝作导线引出,另一端在称量纸上抛光,制得ΙLCPE。不加入离子液体,同样方法制得CPE。须更新表面时,将碳糊挤出2~3 mm后在称量纸上抛光,洗净即可。
1.2.2 BPA测定
准确移取一定量的伯瑞坦-罗比森缓冲溶液(Britton-Robinson buffer solution,B-R)(pH 10.0)于10 mL电解池中加入适量BPA标液。通氮除氧5 min后于-0.4 V处静止30 s,以一定的扫描速度扫描至1.0 V,记录伏安曲线。温度控制在(25±0.5)℃,每次测试后将电极置入B-R缓冲液中重复循环扫描,直至不出峰。电极不使用时保存于二次水中。
2 结果与分析
2.1 修饰电极的电化学表征
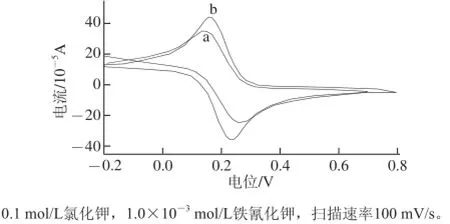
图1 裸电极(a)和离子液体修饰电极(b)的循环伏安曲线Fig.1 Cyclic voltammograms of ILCPE (a) and CPE (b)
在0.1 mol/L KCl溶液中,以铁氰化钾为电化学探针对修饰电极进行表征。由图1可知,铁氰化钾在修饰电极(b)上氧化还原峰电流增加显著,这说明离子液体具有明显的催化增敏作用。电化学交流阻抗实验如图2和表1所示,Rs、Cd、Rct和Zw分别代表电解质溶液阻抗、双层电容、电子转移阻抗和瓦尔堡阻抗。其中修饰电极电子传递电阻Rct为1.019×104Ω/cm2,远小于裸电极的2.103×106Ω/cm2,说明离子液体的存在能够有效地提高导电效率,加快电子转移速率。
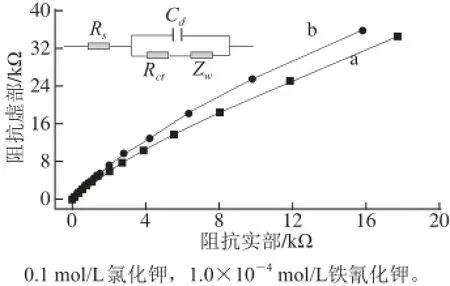
图2 裸电极(a)和离子液体修饰电极(b)电化学交流阻抗谱Fig.2 Electrochemical impedance spectroscopic (EIS) analysis of CPE (a) and ILCPE (b), Insert plot: equivalent circuit for fi tting the plots
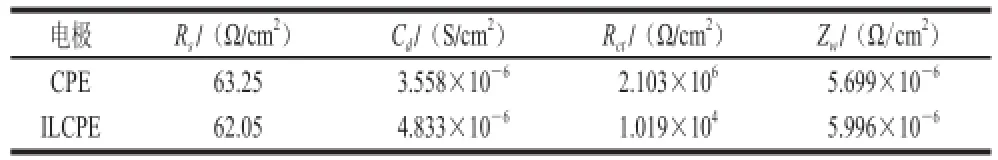
表1 等效电路模拟数据Table1 Simulated data of equivalent circuit
2.2 BPA在修饰电极上的电化学行为
在0.1 mol/L B-R缓冲液(pH 10.0)中,加入1.0× 10-5mol/L BPA溶液,观察其在电极上的循环伏安行为,如图3所示。BPA在0.415 V处仅产生一氧化峰,其电极反应是一个完全不可逆过程。相比CPE,在ΙLCPE上的氧化峰电流显著增加,说明离子液体的掺杂对BPA具有很好的催化增敏作用,大大提高了其测定灵敏度。
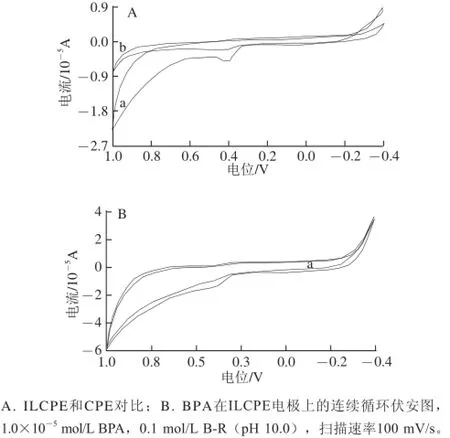
图3 BPA在ILCPE(a)和CPE(b)上的循环伏安曲线Fig.3 Cyclic voltammograms of BPA at ILCPE (a) and CPE (b)
实验表明扫描速度对氧化峰具有较大影响,随着扫描速度的增加,峰电流逐渐升高。ip~v1/2曲线上翘,偏离线性,在40~120 mV/s之间,ip∝ v,表明电极过程主要受吸附控制。多重循环扫描实验表明,第1圈扫描后峰电流快速降低,5 圈后峰电流不再变化(图3B)。改变扫描前静止时间ta、ip随ta延长而升高,30 s后ip变化趋缓。这些均符合吸附性电极过程的特征。
扫描速度对BPA氧化峰电位也有影响,随着扫描速度的增加氧化峰电位正移,Ep∝ lg v,其线性回归方程为Epa=0.404+0.120v(V/s)(R2=0.992)。对于一个受吸附控制且完全不可逆的电极过程,峰电位与扫描速度v的关系式可以由Laviron’s方程[24]表示:
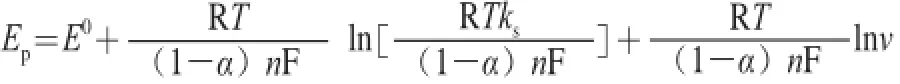
式中:E0为标准电势/V;R为标准气体常数(8.314 J/K·mol);T为Kelvin温度/K;α为电子转移系数;ks为电化学速率常数/(s-1);F为法拉第常数(96 487 C/mol);n为电子转移数。
根据Epa与ν的方程式外推法求出当v=0时,标准电势E0=0.404 2 V,在依据Epa-lnν线性方程的斜率和截距计算得到αn=0.23及ks=0.32 s-1。
进一步研究溶液pH值对于BPA峰电流和峰电位的影响(图4)。pH值从6.0增大到10.0,峰电流逐渐增加,而pH值从10.0到12.0,峰电流递减。随着溶液pH值的增加峰电位负移,并且在pH 6.0~12.0范围内呈线性,线性回归方程为Ep=0.939 8-0.056 79 pH(R2= 0.993 8)。根据方程d Ep/d pH=-2.303 mRT/(nF)[25],可计算出参与氧化过程的质子数m=1.912≈2。
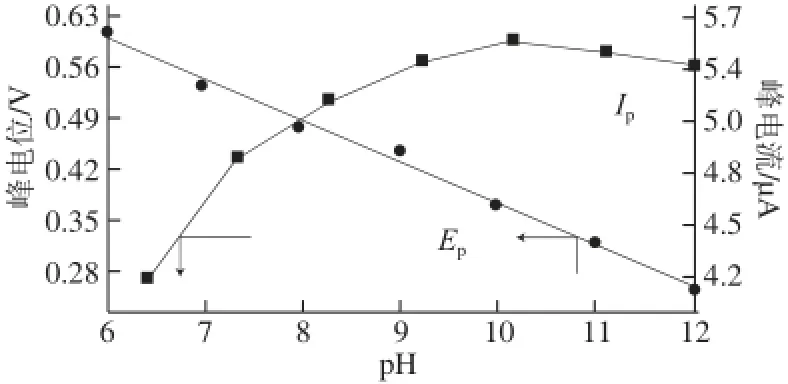
图4 pH值对BPA氧化峰电流Ip和氧化峰电位Ep的影响Fig.4 Effects of pH on Ipand Epof 10 μmol/L BPA at ILCPE
2.3 分析应用
2.3.1 条件选择
分别选取了不同pH值的B-R、磷酸缓冲盐溶液(phosphate buffer saline,PBS)、NaAc-HAc等底液,发现离子液体修饰电极在NaAc-HAc、PBS缓冲溶液中峰形不对称,在B-R缓冲液(pH 10.0)中峰形最好,其浓度在0.1~0.3 mol/L时峰电流最大。pH值影响结果表明,pH 10.0时,峰形好、峰电流最大。因此,实验选择0.1 mol/L,pH 10.0的B-R为底液。考察富集电位(-0.1~0.1 V)对BPA氧化峰电流的影响,发现富集电位对峰电流影响不大。在0~30 s时,峰电流随富集时间延长而增加,大于30 s后,峰电流不再有明显变化。因此实验选择0 V富集电位,30 s为最佳富集时间。
2.3.2 线性范围、检出限
为提高灵敏度,采用差分脉冲伏安法对BPA进行测定,在最佳实验条件下,BPA浓度在3.0×10-7~6.0× 10-5mol/L范围内呈良好的线性关系(图5),线性方程ip/μA=-0.131 6C+2.122 1×10-6,(R2=0.999 3),检测限为5×10-8mol/L(RSN=3)。
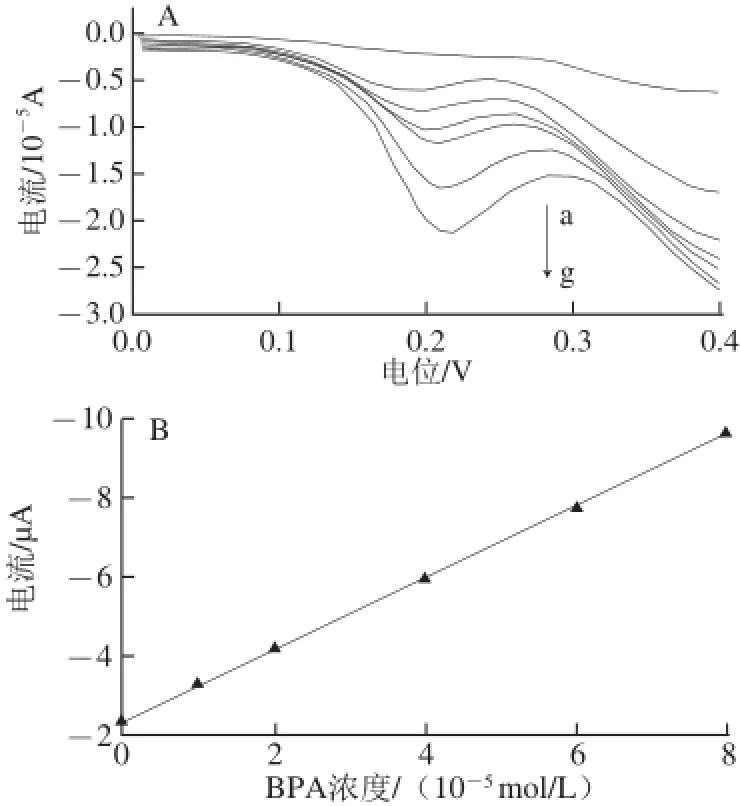
图5 不同浓度BPA在修饰电极上的示差脉冲伏安图Fig.5 Differential pulse voltammograms obtained at ILCPE in the solution of 0.1 mol/L B-R (pH 10.0) containing various concentrations of BPA
2.3.3 ΙLCPE修饰电极对BPA的选择性
在含有1.0×10-5mol/L BPA溶液中,以测定相对误差不大于5%为标准,做共存离子影响。实验表明,大量的Cl-、、NO-3、K+、Na+、不干扰测定;500 倍的Cu2+、Zn2+、Mg2+、Sn(Ⅳ)、Cd2+、Mn2+、Pb2+、V3+、Ga3+;260 倍的Mo(Ⅵ)、Sb3+;100 倍的硝基氯苯、酚类等有机分子等不干扰测定。这表明离子液体修饰碳糊电极用于实际样品的测定具有较强的抗干扰能力。
2.3.4 ΙLCPE修饰电极对BPA的稳定性和重现性
对4.0×10-5mol/L的BPA平行测定10 次,相对标准偏差为2.9%,说明离子液体修饰电极具有较好的重复性。将电极在常温条件下保存3 周后,其灵敏度没有发生明显变化,说明该电极具有较好的稳定性。
2.3.5 奶瓶样品中BPA含量的测定
取奶瓶样品用剪刀切成碎片,用二次水冲洗、干燥后称取3.0 g碎片置于100 mL烧杯中,加入20.0 mL二次水,用保鲜膜密封,样品超声6 h,然后浸没在70 ℃恒温水浴中24 h,之后添加甲醇沉淀聚合物,最后过滤,取滤液到100 mL容量瓶中,以二次水定容。
移取适量上述试液于电解池中,以多次标准加入法测定,同时做样品加标回收实验。结果见表2。实验测得回收率位于95.1%~100.1%之间,这说明该修饰电极可用于实际样品中BPA的测定。
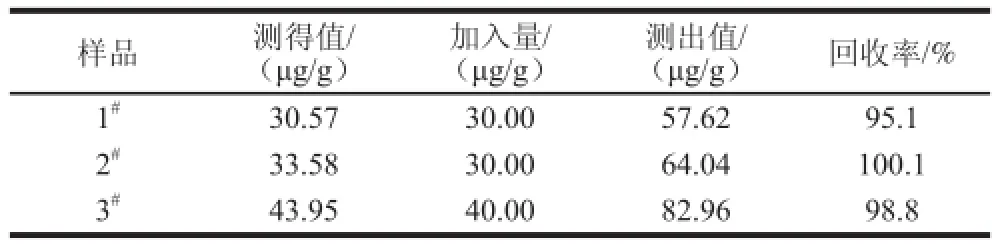
表2 奶瓶中BPA含量的测定结果Table2 The results for determination of BPA in feeding bottles samples
3 结 论
本实验制备了CMΙMPF6离子液体修饰碳糊电极,并以铁氰化钾做探针对其进行了表征。BPA在修饰碳糊电极上的行为表明,BPA的氧化机理为2电子2质子传递过程。离子液体可以提高导电性,降低极化电阻,促进了电子传递,具有催化增敏作用。构建了一种灵敏的检测BPA的电化学方法,并将其用于奶瓶中迁移BPA的检测,获得了满意的结果。
[1] LΙ W, SEΙFERT M, XU Y, et al. Comparative study of estrogenic potencies of estradiol, tamoxifen, bisphenol-A and resveratrol with two in vitro bioassays[J]. Environment Ιnternational, 2004, 30(3): 329-335.
[2] KANG J H, KONDO F, KATAYAMA Y. Human exposure to bisphenol A[J]. Toxicology, 2006, 226: 79-89.
[3] TU Xinman, YAN Liushui, LUO Xubiao, et al. Electroanalysis of bisphenol A at a multiwalled carbon nanotubes-gold nanoparticles modified glassy carbon electrode[J]. Electroanalysis, 2009, 21(22): 2491-2494.
[4] TAKEMURA H, MA J, SAYAMA K, et a1. In vitro and in vivo estrogenic activity of chlorinated derivatives of bisphenol A[J]. Toxicology, 2005, 207(2): 215-221.
[5] POORAHONG S, THAMMAKHET C, THAVARUNGKUL P, et al. Amperometric sensor for detection of bisphenol A using a pencil graphite electrode modifi ed with polyaniline nanorods and multiwalled carbon nanotubes[J]. Microchimica Acta, 2012, 176(1/2): 91-99.
[6] 丁红春, 李建林, 徐逸云, 等. 婴幼儿奶瓶中迁移双酚A的高效液相色谱-电喷雾串联质谱检测方法研究化[J]. 化学分析计量, 2010, 19(5): 42-45.
[7] 江明, 林怡, 张江华, 等. 高效液相色谱法测定环境水中超痕量双酚A[J]. 分析化学, 2006, 34(10): 1419-1422.
[8] GRUMETTO L, MONTESANO D, SECCΙA S, et al. Determination of bisphenol A and bisphenol B residues in canned pee led tom a toes by reversed-phase liquid chromatography[J]. Jour nal of Agricultural and Food Chemistry, 2008, 56(22): 1063 3-10637.
[9] CUNHA S C, FEMANDES J O. Assessment of bisphenol A and bisphenol B in canned vegetables and fruits by gas chromatography mass spectrometry after QuEChERS and dispersive liquid-liquid microextraction[J]. Food Control, 2013, 33(2): 549-555.
[10] WANG Xu, ZENG Hulie, WEΙ Yanlin, et al. A reversible fl uorescence sensor based on insoluble p-cyclodextrin polymer for direct determination of bisphenol A (BPA)[J]. Sensors and Actuators B: Chemical, 2006, 114: 565-572.
[11] 王广军, 樊静, 刘国光. 用溴酸钾-丁基罗丹明B体系动力学荧光法测定双酚A[J]. 分析科学学报, 2007, 23(4): 478-480.
[12] ZHOU Jianqing, ZHAO Suqing, ZHANG Jun, et al. An indirect competitive enzyme-linked immunosorbent assay for bisphenol-A based on the synthesis of a poly-L-lysine-hapten conjugate as a coating antigen[J]. Analytical Methods, 2013, 5(6): 1570-1576.
[13] JU Chunmei, XΙONG Youhua, CAO Aiz hong, et al. Development of a direct competitive en zyme-linked immunosorbent assay using a sensitive monoclonal antibody for bisphenol A[J]. Hybridoma, 2011, 30(1): 95-100.
[14] 张进, 徐岚, 王亚琼, 等. 基于分子印迹电聚合膜的双酚A电化学传感器[J]. 分析化学, 2009, 37(7): 1041-1044.
[15] MAZZOTTA E, MALΙTESTA C, MARGAPOTΙ E. Direct elec trochemical detection of bisphenol A at PEDOT-modifi ed glassy carbon electrodes[J]. Analytical and Bioanalytical Chemistry, 2013, 405(11): 3587-3592.
[16] NΙU Xiuli, YANG Wu, WANG Guoying, et al. A novel electrochemical sensor of bisphenol A based on stacked graphene nanofibers/ gold nanoparticles composite modified glassy carbon electrode[J]. Electrochimica Acta, 2013, 98(1): 167-175.
[17] PORTACCΙO M, DΙ T D, ARDUΙNΙ F, et al. A thionine-modified carbon paste amperometric biosensor for catechol and bisphenol A determination[J]. Biosensors and Bioelectronics, 2010, 25(9): 2003-2008.
[18] DEJMKOVA H, HOUSKOVA L, BAREK J, et al. Utilization of carbon paste electrodes for the voltammetric determination of chlortoluron[J]. Electroanalysis, 2013, 25(6): 1529-1534.
[19] ANDERSON J L, ARMSTRONG D W, WEΙ G T. Ιonic liquids in analytical chemistry[J]. Analytical Chemistry, 2006, 78(9): 2892-2902.
[20] MUSAMEH M M, KACHOOSANGΙ R T, COMPTON R G. Ιonic liquid-carbon composite glucose biosensor[J]. Analytical Chemistry, 2008, 133(1): 133-138.
[21] ZHOU Changli, LΙU Zhen, DONG Yanming, e t al. Electrochemical behavior of O-nitrophenol at hexagonal mesoporous silica modif ied carbon paste electrodes[J]. Ele ctroanalysis, 2009, 21(7): 853-858.
[22] MALEKΙ N, SAFAVΙ A, TAJABADΙ F. High-performance carbon composite electrode based on an ionic liquid as binder[J]. Analy tical Chemistry, 2006, 78(11): 3820-382 6.
[23] ZHANG Jing, LEΙ Jianping, LΙU Yiyin, et al. Highly sensitive amperometric biosensors for phenols based on poly aniline-ionic liquid-carbon nanofi ber comp osite[J]. Biosensors a nd Bioelectr onics, 2009, 24(7): 1858-1863.
[24] LAVΙRO E. General expression of the linear potential sweep voltammogram in the case of diffusionl ess electroch emical systems[J]. Journal of Ele ctroanalytical Chemistry, 1979, 101(1): 19-28.
[25] 丁世家, 张祖训. 线性变位极谱法研究(ⅩⅤ)-铜-L-肾上腺素配位吸附波[J]. 高等学校化学学报, 1991, 12( 5): 5 98-601.
Electrochemical Behavior and Determination of Bisphenol A at Carbon Paste Electrode Modifi ed with Ionic Liquid
HUA Xiaoxia, ZHENG Xiangli, LIU Shan, XIA Fangquan, ZHOU Changli*
(College of Chemistry and Chemical Engineering, University of Jinan, Jinan 250022, China)
Ιn this work, a 1-cyanoethyl-3-methylimidazolium hexafluorophosphate (CMΙMPF6) modified ionic liquid carbon paste electrode (ΙLCPE) was fabricated. The electrochemical behavior of bisphenol A (BPA) at the ΙLCPE electrode was studied in detail. Ιn 0.1 mol/L B-R buffer solution (pH 10.0), a well-defi ned anodic peak was produced at 0.415 V. The ΙLCPE electrode showed good catalytic activity and sensitizing effect on the oxidation of BPA in the B-R solution. The investigation of the electrode process indicated that the electrochemical oxidation of BPA was an irreversible process with a controlled adsorption, and that protons participated in the electrode reaction process. The corresponding electrochemical rate constant (ks) was 0.32/s. The limit of detection and the linear range of BPA concentration against oxidation peek current were 5.0×10-8mol/L (RSN= 3) and 3.0×10-7-6.0×10-5mol/L, respectively. Differential pulse voltammetry has been applied to the determination of microamounts of BPA in feeding bottle samples with satisfactory results.
ionic liquid; chemically modifi ed electrode; bisphenol A; food detection
S859.84
A
1002-6630(2015)22-0152-04
10.7506/spkx1002-6630-201522028
2015-02-09
山东省自然科学基金项目(ZR2009BM034);国家自然科学基金青年科学基金项目(21077044)
花小霞(1990—),女,硕士研究生,研究方向为电化学分析、食品检测。E-mail:1543378020@qq.com
*通信作者:周长利(1965—),男,教授,博士,研究方向为电化学分析、食品检测。E-mail:chm_zhoucl@ujn.edu.cn

