高效液相色谱法测定还原型谷胱甘肽钠的含量
宗春燕,朱 娜,苏学军
(泰州职业技术学院,江苏 泰州 225300)
还原型谷胱甘肽钠商品名为松泰斯,化学名称为N-(N-L-谷氨酰基-L-半胱氨酰基)甘氨酸钠盐,白色结晶性粉末,具有轻微的特征气味。谷胱甘肽制剂可用于酒精中毒或某些药物中毒的治疗,亦具有抗过敏、抗氧化、增强免疫力、延缓衰老、抗癌、抗辐射及辅助化疗等功效,因而在医药工业中得到了广泛的应用[1,2]。另外,还原型谷胱甘肽钠在食品中的应用也令人瞩目[3],如添加到乳制品中有相当于维生素C的功效,可防止水果褐变,还可用作食品风味剂,是重要的食品功能因子。
谷胱甘肽钠的生产方法主要有化学合成法、酶转化法、发酵法和溶剂提取法[3]。目前,化学合成法和提取法已经工业化,酶转化法正在进行广泛研究。由于国内谷胱甘肽钠的研究起步较晚,对还原型谷胱甘肽钠的分离分析一直是研究的热点[4,5]。文献报道采用的紫外分光光度法测定谷胱甘肽钠的含量,准确度不高,且干扰严重[6]。毛细管区带电泳分析法虽可实现快速检测,精密度及准确度较高,但对操作要求较高[7]。本文采用高效液相色谱仪附紫外检测器,以磷酸二氢钠盐溶液为流动相,在210nm波长下测定还原型谷胱甘肽钠的含量,能准确检测出样品中的主要成分,适用于注射用还原型谷胱甘肽钠制剂含量的测定。
1 实验部分
1.1 仪器与试剂
Waters2695高效液相色谱仪,配有紫外检测器及数据处理软件,Waters公司;Sartorius电子天平,北京赛多利斯仪器有限公司;PS-30A超声波清洗器,东莞洁康超声波设备有限公司。二水合磷酸二氢钠(分析纯,国药集团化学试剂有限公司);乙腈、磷酸(色谱纯,购自MERCK公司)、谷胱甘肽对照品(纯度≥99.0%,自制);二次蒸馏水。
1.2 色谱条件
色谱柱:Synergi4u Hydro-RP 80A 250×4.60mm;流动相:称取二水合磷酸二氢钠3.90g,溶解到500mL二次蒸馏水中,用85%磷酸调节pH值至2.8,加二次蒸馏水稀释到1000mL,过滤,经超声波清洗器脱气冷却后即得。检测波长选择210nm,柱温为30℃,流速为1.5 mL/min;进样体积 20μL。
1.3 测定方法
1.3.1 对照品溶液的制备
准确称取谷胱甘肽钠50.0mg,置于100mL容量瓶中,加流动相稀释至刻度并摇匀备用。因还原型谷胱甘肽钠不稳定,受温度和光线影响后极易氧化成氧化型谷胱甘肽钠,因而本品应临用现配。
1.3.2 样品溶液的制备
准确称取还原型谷胱甘肽钠样品50.0mg,加流动相配制成每1mL含还原型谷胱甘肽钠0.5mg的溶液,摇匀后备用。
1.3.3 样品的测定
分别取已制备好的样品溶液和标准对照品溶液20μL,在相同色谱条件下待基线稳定后,连续数针进样,调节好检测灵敏度,以保留时间定性,峰面积定量。根据样品峰的峰面积,按下式公式计算出样品中谷胱甘肽钠的含量。
样品中还原型谷胱甘肽钠的含量:
式中:A—对照品溶液中还原型谷胱甘肽钠的峰面积;A'—样品溶液中还原型谷胱甘肽钠的峰面积;m1—还原型谷胱甘肽钠对照品的质量,mg;m2—还原型谷胱甘肽钠样品的质量,mg;χs—对照品中还原型谷胱甘肽钠的质量分数。
2 结果与讨论
2.1 色谱条件的选择及系统适用性色谱柱
2.1.1 色谱条件的选择
将配制好的对照品溶液,利用可变波长检测器进行全波长扫描,结果发现,还原型谷胱甘肽钠在210m处有最大吸收值,故选择210nm作为检测波长,与文献一致[5]。
2.1.2 流动相的选择
通过选用磷酸二氢钠和乙腈的混合溶液及磷酸二氢钠盐溶液进行了多次比对试验,结果表明,采用磷酸二氢钠盐溶液的检测灵敏度可满足检测要求,且乙腈混合液有毒,成本高。对盐溶液的浓度配比进行了考查,发现浓度为0.0325mol/L时保留时间适当且峰形对称完整,故最终选定以磷酸二氢钠和水的盐溶液作为流动相。
2.1.3 流速的选择
实验发现,流速对还原型谷胱甘肽钠的分离有一定影响,当流速增大时,色谱峰变窄,分离度变小;当流速减小时,色谱峰变宽,分离度变大。考虑到峰宽和分离度的要求,合适的流速选为1.5mL/min。
2.1.4 流动相pH值的选择
考查不同pH值的流动相对实验的影响,结果显示,pH值的变化会引起谷胱甘肽钠峰面积的变化,pH值在2.8~3.0之间,谷胱甘肽钠的吸收程度高,灵敏度也比较高,最终选择流动相的pH值为2.8。
2.1.5 系统适用性
系统适用性色谱柱的理论塔板数不低于3000,对照品色谱图中色谱峰的分离度符合要求。
2.1.6 线性关系的确定
将配制的对照样按5个不同浓度梯度进样,进行液相色谱分析。以谷胱甘肽钠质量浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程为y=40.25x+53.84,相关系数为R=0.9998。
2.2 专属性试验
取上述选定的色谱条件,将配制好的谷胱甘肽钠对照品溶液、还原型谷胱甘肽钠试样溶液以及用流动相作为稀释液的空白溶液,进样,记录图谱。
实验之前需进一针空白,保证流动相无污染,无其它杂质,以防止影响样品含量的计算,对照品图谱如图1所示,样品图谱如图2所示。
2.3 精密度试验
取还原型谷胱甘肽钠对照品溶液一份,连续进样5次,记录峰面积,结果如表1所示,RSD=0.03%。同样条件下,再测定两份样品,RSD均小于1.00%。
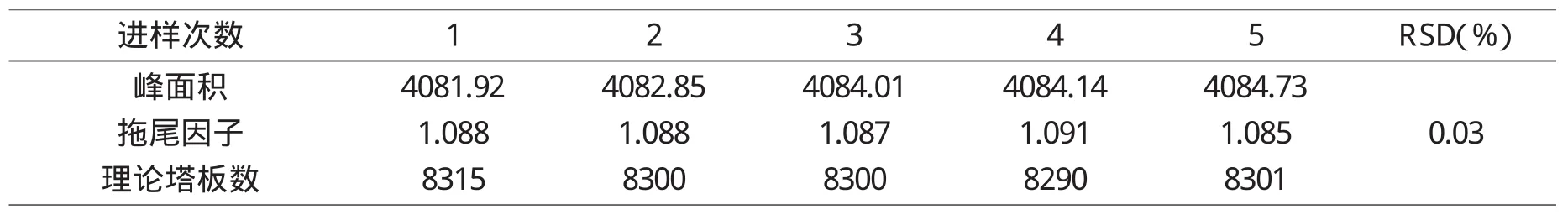
表1 精密度试验结果
2.4 含量测定
平行取供试品2批,一式两份,加入流动相配制成每1mL含还原型谷胱甘肽钠0.5mg的溶液,取适量注入色谱仪,记录色谱图,结果见表2。由表2可见,该法的准确度良好。
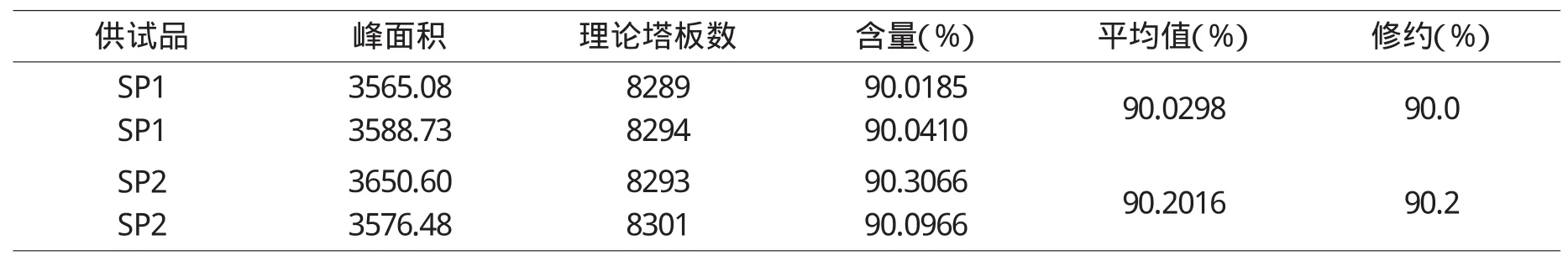
表2 供试品含量测定结果
还原型谷胱甘肽钠含量的企业指标含量大于或等于90.0%,因此测定两批供试品的还原型谷胱甘肽钠的含量符合要求,为合格品。
3 结论
目前国内关于还原型谷胱甘肽钠含量的高效液相色谱法分析报道相对较少,本文通过实验探索的分析方法,其精密度和准确度较高,峰分离度表现良好,可用于还原型谷胱甘肽钠制剂含量的测定,为企业产品质量控制提供了检测依据。
[1]国家药典委员会.中华人民共和国药典(第一部)[M].北京:化学工业出版社,2005.
[2]颜鸣,史国兵,郭涛,等.高效液相色谱法测定人血浆中还原型谷胱甘肽浓度[J].解放军药学学报,2008,24(3):251-253.
[3]江洁,单立峰.谷胱甘肽的生产及其在食品工业中的应用[J].中国调味品,2009,34(2):40-44.
[4]张现涛,沈小钟,张雷红,等.氧化型谷胱甘肽二钠及其有关物质的高效液相色谱分析 [J].广东微量元素科学,2009,16(8):57-59.
[5]王爱月,解魁,李发生.高效液相色谱法测定保健食品中谷胱甘肽含量的方法研究 [J].中国卫生检验杂志,2007,17(7):1181-1182.
[6]翟文慧,王爱月.紫外分光光度法测定保健食品中谷胱甘肽[J].预防医学论坛,2005,11(5):560-561.
[7]赵绍林,吴惠毅,杨晋,等.注射用还原型谷胱甘肽钠的毛细管区带电泳分离及其光学纯度分析[J].分析科学学报,2011,27(6):770-772.□

