黄芩苷对四氧嘧啶致糖尿病小鼠学习记忆功能的影响
常 鹏, 马 岩, 胡雪剑, 李建雄
(1.兰州大学第二医院药学部,甘肃 兰州730030;2.郑州大学附属郑州中心医院药学部,河南 郑州450007;3.兰州大学第二医院内分泌科,甘肃兰州730030;4.兰州大学第二医院神经内科,甘肃兰州730030)
黄芩苷对四氧嘧啶致糖尿病小鼠学习记忆功能的影响
常 鹏1, 马 岩2, 胡雪剑3, 李建雄4*
(1.兰州大学第二医院药学部,甘肃 兰州730030;2.郑州大学附属郑州中心医院药学部,河南 郑州450007;3.兰州大学第二医院内分泌科,甘肃兰州730030;4.兰州大学第二医院神经内科,甘肃兰州730030)
目的 观察黄芩苷对四氧嘧啶致糖尿病小鼠学习记忆功能及去甲肾上腺素能神经活动的影响。方法实验分正常对照组、模型组、黄芩苷组 (12.5 mg/kg)和尼莫地平组 (15 mg/kg),采用腹腔注射四氧嘧啶 (70 mg/kg)复制糖尿病模型,造模第4天起药物处理,每天一次,持续至第56天。采用血糖仪检测小鼠血糖,采用Morris水迷宫测试小鼠学习记忆功能,采用酶联免疫吸附法测定小鼠大脑海马区和额叶皮层区去甲肾上腺素 (NE)和间羟去甲肾上腺素 (NMN)的量。结果 造模后第28天和56天,与对照组相比,模型组潜伏期均明显延长 (P<0.01);穿台次数和目标象限停留时间比均显著性减少 (P<0.01)。与模型组比较,黄芩苷组潜伏期缩短 (P<0.05,P<0.01),穿台次数和目标象限停留时间比明显增加 (P<0.05),且黄芩苷组和尼莫地平组之间差异无统计学意义。黄芩苷能够有效抑制糖尿病小鼠大脑海马区和额叶皮层区NE和NMN的量的降低 (P<0.05,P<0.01)。结论 黄芩苷能够有效改善四氧嘧啶致糖尿病小鼠学习记忆功能障碍,其机制可能与其增加NE能神经递质活动有关。
黄芩苷;糖尿病小鼠;学习记忆;去甲肾上腺素
黄芩苷是从唇形科植物黄芩(Scutellaria baicalensis Georigi)中提取的一种黄酮类化合物,是黄芩的主要活性成分之一,具有抗炎、抗病毒、抗感染、抗氧化和抗脑缺血致学习记忆功能损伤等多种药理学作用[1-2]。近年来研究发现,黄芩苷具有降糖作用[3],同时能够有效防治糖尿病周围神经病变和糖尿病肾病等慢性并发症[4-7]。认知功能损害是糖尿病患者的主要并发症之一,主要表现为学习记忆功能的障碍[8]。但黄芩苷对糖尿病致学习记忆功能障碍的影响至今尚未见报道。本实验拟观察黄芩苷对四氧嘧啶致糖尿病小鼠学习记忆功能的影响并对其机制进行初步探讨。
1 材料与方法
1.1 实验动物 昆明种小鼠,雌雄各半,体质量24~28 g,由兰州大学动物实验中心提供,合格证号:SCXK(甘)2009-0004。
1.2 药物及试剂 黄芩苷 (纯度≥98%,批号130309-2,上海纯优生物科技有限公司);尼莫地平片 (20 mg,批号B131103015,四川科伦药业股份有限公司),四氧嘧啶(美国sigma公司);去甲肾上腺素 (NE)、间羟去甲肾上腺素酶联免疫试剂盒 (NMN)(美国BD公司)。
1.3 仪器 Morris水迷宫(上海移数信息科技有限公司);全波长Multiskan Spectrum酶标仪(美国Thermo公司);ACCU-CHEK血糖仪(瑞士罗氏公司)。
1.4 实验方法
1.4.1 模型建立及分组 参考文献方法[9-10],小鼠腹腔注射四氧嘧啶 (70 mg/kg)。于第3天腹腔取血测定禁食血糖,将空腹血糖浓度≥16 mmol/L的小鼠纳入实验,分为模型组、黄芩苷组 (12.5 mg/kg)和尼莫地平组 (15 mg/kg),每组动物均为12只。另设正常对照组,腹腔注射同体积的生理盐水。第4天起黄芩苷组和尼莫地平组每天灌胃给药一次,持续至第56天。模型组和正常对照组则灌服等体积生理盐水。
1.4.2 Morris水迷宫测试 造模前5天对小鼠进行Morris水迷宫训练,每只小鼠每天训练6次。训练时将小鼠面向池壁放入水中,使其寻找水中的平台 (平台置于第Ⅰ象限,没于水面下1 cm),找到平台所用时间记为逃避潜伏期。设定寻找平台的最大时限为90 s(即在90 s内未找到平台者逃避潜伏期记为90 s)。移去平台,选取原平台正对象限 (第Ⅲ象限)的中点为入水点,将小鼠面向池壁放入水中,动物自由游泳90 s,记录90 s内小鼠穿过平台区的次数和在目标象限的游泳时间。取最后6次测试结果的平均值为造模前成绩。于造模后第4、28、56天分别进行上述测试并记录小鼠的逃避潜伏期、穿台次数和在目标象限的游泳时间。
1.4.3 神经递质含有量检测 待第56天测试结束后将小
鼠断头处死,于冰台上快速分离大脑双侧海马和额叶皮层,经液氮冷冻后移至-80℃保存备用。采用酶联免疫吸附法检测NE及其代谢物NMN水平,操作均按试剂盒说明书完成。
表1 黄芩苷对糖尿病小鼠血糖的影响

表1 黄芩苷对糖尿病小鼠血糖的影响
组别 血糖值/(mmol.L1)第3天 第56天正常对照组9.1±1.2 9.2±1.5模型组 28.7±6.5## 26.5±6.8##黄芩苷组 29.1±10.2## 14.1±6.6#**
2 结果
2.1 黄芩苷对糖尿病小鼠血糖的影响 如表1所示,小鼠注射四氧嘧啶后第3天模型组和黄芩苷组血糖值明显升高,分别与正常对照组相比较,差异均具有统计学意义 (P<0.01),模型组和黄芩苷组血糖值之间差异无统计学意义。第56天黄芩苷组血糖值与模型组相比明显降低,差异具有统计学意义 (P<0.01),但黄芩苷组血糖值仍然高于正常对照组 (P<0.05)。
2.2 黄芩苷对糖尿病小鼠水迷宫测试结果的影响 如表2所示,造模前水迷宫测试成绩各组间均差异无统计学意义。
注:与正常对照组比较,#P<0.05,##P<0.01;与模型组比较,**P<0.01造模后第4天,模型组、黄芩苷组和尼莫地平组潜伏期稍有延长,穿台次数和目标象限停留时间比稍有降低,分别与正常对照组相比较,差异均无统计学意义,三者之间差异也无统计学意义。造模后第28天和56天,与正常对照组相比,模型组潜伏期均明显延长 (P<0.01);穿台次数和目标象限停留时间比均显著性减少 (P<0.01)。与模型组比较,黄芩苷组和尼莫地平组潜伏期均缩短 (P<0.05,P<0.01),穿台次数和目标象限停留时间比均明显增加 (P<0.05),但黄芩苷组和尼莫地平组之间差异无统计学意义。
表2 黄芩苷对糖尿病小鼠水迷宫测试结果的影响
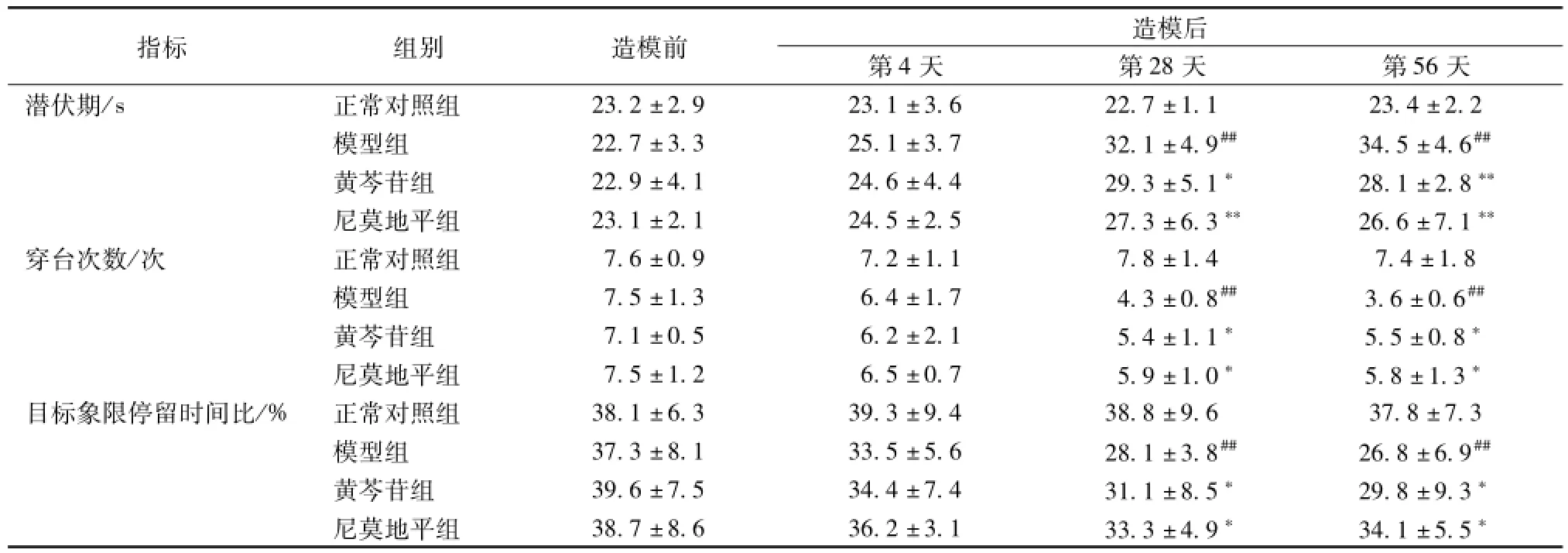
表2 黄芩苷对糖尿病小鼠水迷宫测试结果的影响
注:与正常对照组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01
指标 组别 造模前 造模后第4天 第28天 第56天潜伏期/s 正常对照组23.2±2.9 23.1±3.6 22.7±1.1 23.4±2.2模型组 22.7±3.3 25.1±3.7 32.1±4.9## 34.5±4.6##黄芩苷组 22.9±4.1 24.6±4.4 29.3±5.1* 28.1±2.8**尼莫地平组 23.1±2.1 24.5±2.5 27.3±6.3** 26.6±7.1**穿台次数/次 正常对照组 7.6±0.9 7.2±1.1 7.8±1.4 7.4±1.8模型组 7.5±1.3 6.4±1.7 4.3±0.8## 3.6±0.6##黄芩苷组 7.1±0.5 6.2±2.1 5.4±1.1* 5.5±0.8*尼莫地平组 7.5±1.2 6.5±0.7 5.9±1.0* 5.8±1.3*目标象限停留时间比/% 正常对照组 38.1±6.3 39.3±9.4 38.8±9.6 37.8±7.3模型组 37.3±8.1 33.5±5.6 28.1±3.8## 26.8±6.9##黄芩苷组 39.6±7.5 34.4±7.4 31.1±8.5* 29.8±9.3*尼莫地平组 38.7±8.6 36.2±3.1 33.3±4.9* 34.1±5.5*
2.3 黄芩苷对糖尿病小鼠大脑NE和NMN水平的影响如表3所示,与正常对照组相比,模型组海马区和额叶皮层区NE和NMN的量均呈显著性降低,差异具有统计学意义 (P<0.01)。与模型组比较,黄芩苷组NE和NMN的量均有升高,差异均具有统计学意义 (P<0.05,P<0.01)。
表3 黄芩苷对糖尿病小鼠大脑NE和NMN水平的影响

表3 黄芩苷对糖尿病小鼠大脑NE和NMN水平的影响
注:与正常对照组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01
组别额叶皮层区NE/(μg.L-1) NMN/(ng.L-1) NE/(μg.L-1) NMN/(ng.L-1海马区)96.2±22.5 241.4±96.1 132.7±24.6 387.8±48.3模型组 78.4±9.8## 102.5±26.4## 100.7±22.1## 201.6±55.4##黄芩苷组 90.1±10.6* 198.3±33.3** 117.5±18.9* 326.6±71.6正常对照组**
3 讨论
四氧嘧啶诱导的小鼠糖尿病模型是研究糖尿病并发认知障碍的常用模型。本研究参考文献方法共取40只小鼠腹腔注射四氧嘧啶 (70 mg/kg),第3天测定禁食血糖发现其中36只空腹血糖浓度≥16 mmol/L,并将其纳入实验,第56天测量发现,其高血糖依旧存在,表明本实验小鼠糖尿病模型是复制成功的。本研究造模后第4天Morris水迷宫测试发现各组动物学习记忆成绩没有明显差异,第28天和56天测试发现四氧嘧啶处理组动物水迷宫成绩均呈显著性下降,表明糖尿病学习记忆障碍模型成功建立。尼莫地平是目前临床上证实对改善糖尿病认知功能障碍患者的认知功能最为有效的药物[11],因此,本研究选用尼莫地平作为阳性对照。
糖尿病引起的中枢神经系统损害日益受到人们广泛关注和研究,其中学习记忆障碍是糖尿病中枢神经系统并发症的主要表现[12-13]。本实验结果显示,黄芩苷能够缩短四
氧嘧啶致糖尿病小鼠水迷宫潜伏期增加穿台次数和目标象限停留时间比,表明黄芩苷能够有效缓解糖尿病小鼠的学习记忆功能障碍。之前关于黄芩苷改善多种模型动物学习记忆功能损伤的研究屡有报道,但改善糖尿病小鼠的学习记忆功能障碍尚属本文首次报道。一直以来,黄芩苷在糖尿病领域主要用于降糖[3]、防治糖尿病周围神经病变和糖尿病肾病等慢性并发症[4-7]。本研究结果无疑为其在糖尿病领域的应用提供一种新的思路。
目前对糖尿病认知功能障碍的发病机制尚未阐明,普遍认为糖尿病认知障碍是多环节、多因素的致病过程[14]。海马和颞叶与记忆、学习密切相关,其超微结构的损害可能为糖尿病认知损害的结构基础。同时,糖尿病引起的神经递质异常也是糖尿病认知障碍发生的一主要因素。高血糖造成脑神经元损害,并影响一些神经递质的表达,从而导致脑结构破坏及脑功能的改变[15-16]。已有文献显示乙酰胆碱和多巴胺能神经传递的降低可导致糖尿病认知障碍[17]。本实验结果显示,四氧嘧啶致糖尿病小鼠大脑海马区和额叶皮层区NE和NMN水平均呈显著性降低,表明NE能神经递质活动受到抑制,而黄芩苷能够有效增加NE能神经递质活动,因此本研究认为,黄芩苷改善糖尿病小鼠的学习记忆功能障碍除了其本身的降糖作用外,可能更与其增加NE能神经递质活动有关。
总之,黄芩苷能够有效改善四氧嘧啶致糖尿病小鼠学习记忆功能障碍,其机制可能与其增加大脑海马区和额叶皮层区NE能神经递质活动有关。
[1] 辛文妤,宋俊科,何国荣,等.黄芩素和黄芩苷的药理作用及机制研究进展[J].中国新药杂志,2013,6(9):647-653 +659.
[2] 李园园,杨 晖,廖桂凤,等.黄芩苷抗脑缺血小鼠学习记忆功能损伤的保护作用[J].昆明医学院学报,2011,32(5):13-16.
[3] 李云巍,牛艳芬,黄年旭,等.黄芩苷对四氧嘧啶致小鼠糖尿病降糖作用的研究[J].昆明医学院学报,2009,30(6):5-8.
[4] 冯友根,郭丽敏.黄芩苷防治糖尿病并发症的作用与临床应用[J].医药导报,2004,23(8):572-573.
[5] 刘海霞.黄芩苷对早期糖尿病肾病肾功能及其抗氧化应激作用的影响[J].中国现代药物应用,2013,7(20):142-143.
[6] 刘长山,王秀军,孙丽萍,等.黄芩苷对2型糖尿病大鼠模型胰岛素抵抗的影响[J].中国老年学杂志,2010,30(23):3541-3542.
[7] 秦晓改,卢 威,牛艳芬,等.黄芩苷联合罗格列酮对糖尿病小鼠周围神经病变防治研究[J].医学综述,2011,17(21):3340-3341.
[8] Yamazaki Y,Miwa T,Sakurai H,et al.Clinical backgrounds and morbidity of cognitive impairment in elderly diabetic patients[J].Endocr J,2011,58(2):109-115.
[9] 黄彦峰,晋 玲,赵善民,等.四氧嘧啶糖尿病小鼠模型的复制与应用体会[J].时珍国医国药,2012,22(11):2784-2785.
[10] 田国庆,卢贺起,郭赛珊,等.补肾活血方对糖尿病小鼠学习记忆功能及中枢神经递质的影响[J].中医杂志,2009,50(5):460-462.
[11] 张 为,覃少东,吕泽平,等.尼莫地平对糖尿病认知功能障碍的临床研究[J].医学综述,2008,14(16):2539-2541.
[12] Sakurai T.Cognitive decline in elderly individuals with type 2 diabetes mellitus[J].Nihon Rinsho,2013,71(11):1960-1964.
[13] Ryan JP,Fine D F,Rosano C.Type 2 diabetes and cognitive impairment:contributions from neuroimaging[J].JGeriatr Psychiatry Neurol,2014,27(1):47-55.
[14] Bruce D G,Casey G P,Grange V,et al.Cognitive impairment,physical disability and depressive symptoms in older diabetic patients:the Fremantle Cognition in Diabetes Study[J]. Diabetes Res Glin Pract,2003,61(1):59-67.
[15] 边志杰,路承彪,罗建平,等.糖尿病诱发的认知功能损害研究[J].生物医学工程学杂志,2013,30(4):884-888.
[16] Dash SK.Cognitive impairment and diabetes[J].Recent Pat Endocr Metab Immune Drug Discov,2013,7(2):155-165.
[17] Luchsinger J A.Type 2 diabetes and cognitive impairment:linking mechanisms[J].J Alzheimers Dis,2012,30(Suppl 2):S185-S198.
R285.5
B
1001-1528(2015)11-2521-03
10.3969/j.issn.1001-1528.2015.11.042
2014-06-16
中央高校基本科研业务费专项资金(lzujbky-2013-46)
常 鹏(1991—),男,本科,研究方向为药理学。Tel:15193130829,E-mail:lzuchangp@163.com
*通信作者:李建雄(1976—),男,博士,副主任医师,研究方向为神经病学。E-mail:ldeyljx@163.com

