1-(4-硝基苯基)-3-(2-苯并噻唑)-三氮烯的合成及与钯的显色反应研究
邱丽琴
(泉州工艺美术职业学院材料工程系,福建泉州362000)
0 引言
三氮烯类试剂[1,2]是分子结构中含有(-N=N-NH-)或(-N=N-NOH-)分析功能团的一大类化合物的总称,是一种性能优良的分析试剂。目前的研究主要集中在含有分析功能团(-N=N-NH-)的非烃基类三氮烯试剂。由于具有与IB、IIB族元素的阳离子发生高灵敏度的显色反应的特性,该类试剂自20世纪30年代起就开始广泛用于 Cd2+、Hg2+、Ni2+、Cu2+、Co2+等金属阳离子的定性检验[3-5]。20世纪 80年代反应体系中表面活性剂的引入,近一步扩大了该类试剂的应用范围,目前该试剂已经可以用于Tl3+、Pt4+、CN-Pd2+以及表面活性剂的定量检验。
近年来三氮烯合成[2]的报道较多,但大部分都是两步合成法,即芳香族伯胺在酸性条件下重氮化,然后在适当条件下与另一芳胺偶合。常用的重氮化剂根据芳胺的碱性强弱而有所不同,碱性较强的芳胺以HCl-NaNO2为重氮化剂[6],大多数的杂环三氮烯试剂均是此种重氮化方法制得;而碱性较弱的芳胺则以H2SO4-NaNO2为重氮化剂。为了克服上述反应中反应不易完全、有NO2有毒气体放出、PH值难以调节以及产率低下的缺点,近年来也出现了以亚硝酸正丁酯为重氮化剂的合成方法[6]。
作者合成了一种新型三氮烯试剂[7]:1-(4-硝基苯基)-3-(2-苯并噻唑)-三氮烯,并研究了此试剂与Pd2+的显色反应条件[8]。结果表明,在pH11.0的Na2B4O7-NaOH缓冲溶液中,当有Tween100存在时,Pd2+能与显色剂形成稳定的配合物,其最大吸收波长位于537nm,表观摩尔吸光系数ε=1.94×105,钯的浓度在0.00~0.036μg/mL范围内符合比尔定律。并用该方法测定了自制的废水中的钯的含量,结果满意。
1 实验部分
1.1 主要仪器和试剂
主要仪器:UV-2000型紫外可见分光光度计、HS-3CT数字pH计(上海伟业仪器厂)、BS323S电子分析天平(北京赛多利斯仪器系统有限公司)、AVATAR 360FT-IR型红外光谱仪(Nicolet)、TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司)、DF-101S集热式恒温加热磁力搅拌器(巩义市英峪予华仪器制造)
主要试剂:对硝基苯胺、亚硝酸钠、2一氨基苯并噻唑、无水乙醇、丙酮、碳酸钠、浓硫酸、Na2B407-NaOH(pH=11)缓冲溶液、1.0mg/mL钯标准溶液(称取0.1000g金属钯和0.10gNaCl溶于10.0mL 新鲜王水中,溶液慢慢蒸发至近干后,加入2.0mL浓盐酸,再将此溶液蒸发至近干。重复此操作两次。最后用0.2mol/L盐酸溶解并定容至100mL)、0.2g/L三氮烯溶液(称取0.02g的三氮烯溶于100mL的乙醇-丙酮(体积比为 1∶1)混合液中)、表面活性剂[9](OP溶液:2%水溶液;Tween-80:2%水溶液;Tritonx-100:2%水溶液;Tween-20:2%水溶液;十二烷基硫酸钠:2%水溶液;十二烷基磺酸钠:2%水溶液;十六烷基溴化钠:2%水溶液)。
1.2 显色剂的合成原理

1.3 显色剂的合成方法[10][11]
首先称取1.38g对硝基苯胺溶于20mL 6 mol/L盐酸中,用冰浴冷却至0℃,同时在上述溶液中缓慢加入0.7g已冷却至1℃的NaNO2(溶于5mL水),使其温度保持在0~5℃之间重氮化2h,得澄清的重氮盐溶液。再将3.8g2一氨基苯并噻唑倾入上述溶液中,加2-3m1浓硫酸,搅拌0.5h后倾入800ml冰水中,析出黄色沉淀,搅匀,饱和Na2CO3溶液调节至pH 7~8,有沉淀出现,移去冰浴,室温下静置过夜。
最后将粗产品抽滤洗涤数次,再用乙醇-丙酮溶液重结晶2次,并在40℃下烘干产品,得到墨绿色的粉末状固体。
1.4 实验方法
准确移0.9mL的钯标准溶液(10μg/mL)到25mL的具塞比色管中,依次加入3.5mL Na2B407-NaOH缓冲溶液(pH 11.0),1.0mL 2%的 Tritonx-100 表面活性剂,1.5mL 0.2g/L 的显色剂[12]乙醇-丙酮溶液,加水稀释至刻度,摇匀后放置10min,用1cm比色皿,在最佳波长537nm处,以试剂空白为参比。
2 结果与讨论
2.1 产品结构的鉴定
对合成产品的C、H、N进行含量分析,所得结果表明,测定值与理论值一致。
理论值:C(52.17);H(3.03);N(23.40);O(10.69);S(10.71)。
实测值:C(52.14);H(3.06);N(23.36);O(10.65);S(10.68)。
通过产品的红外光谱图IR(KBr)表明:
在3284 cm-1有-NH-吸收峰;1592cm-1有-N=N-吸收峰;1509cm-1有苯环的骨架振动吸收峰,862 cm-1有苯环上的对位取代的吸收峰;1384 cm-1有-NO2吸收峰。
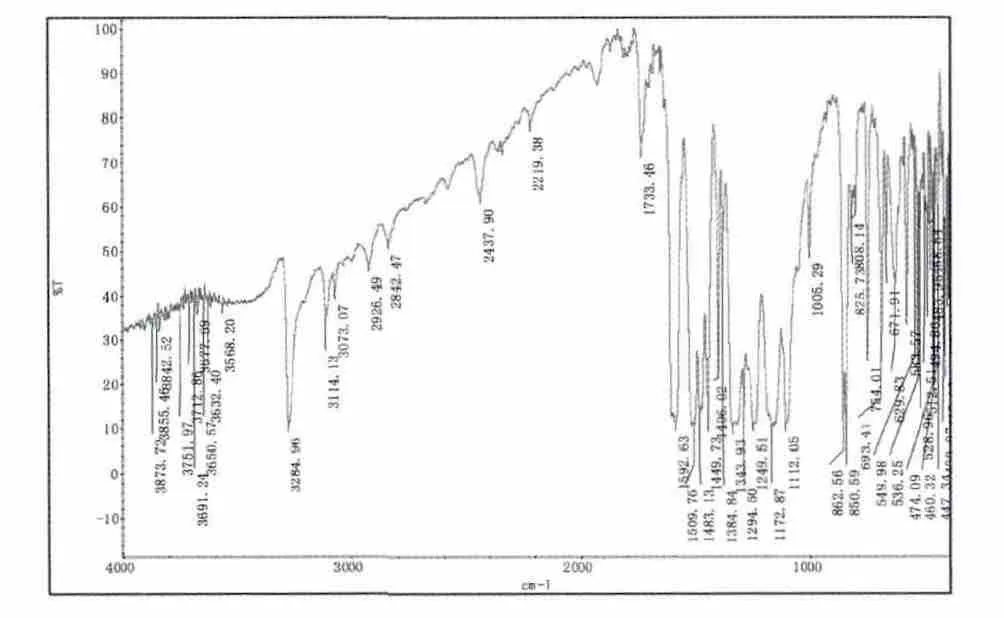
图2-1 红外光谱分析图
据此可以确定,三氮烯化合物为以下结构:

2.2 试剂物理性质
1-(4-硝基苯基)-3-(2-苯并噻唑)分子式:C13H9N5O2S,分子量:299,显色剂为墨绿色固体,微溶于水,易溶于乙醇、丙酮等有机溶剂,在不同的酸碱度下呈现不同的颜色,并且有不同的吸光度,在酸性介质中呈现浅黄色,在碱性介质中呈现红色。
2.3 试剂与 Pd(Ⅱ)的显色反应[11][12]
2.3.1 配合物的吸收光谱
在实验条件下,显色剂与钯形成橙色的配合物,在537nm处有最大负吸收,试剂的吸收峰在530nm波长处,表观摩尔吸光系数为 ε=1.94×105L·mol-1·cm-1。吸收光谱见图2-2。
2.3.2 缓冲溶液的选择和酸度对吸光度的影响
固定缓冲溶液用量,在不同酸碱度的缓冲体系中进行试剂与钯离子的显色反应,结果表明体系的吸光度在pH10.50~11.50最大且稳定,本实验选用Na2B407-NaOH缓冲溶液,改变缓冲溶液的用量,实验结果表明:用量为2~4mL时,体系的吸光度最大。所以本实验选用3.0mL pH=11.00的 Na2B407-NaOH缓冲溶液。
2.3.3 表面活性剂的种类和用量的影响
不加表面活性剂时,体系显色正常,为了加强显色效果增加了表面活性剂。实验结果表明:阴离子表面活性剂如:十二烷基硫酸钠和十二烷基硫酸钠,对体系无增敏作用;非离子表面活性剂和阳离子表面活性剂如:OP,Tween-80,TritonX-100,十六烷基溴化胺等均可起增溶增敏作用;通过吸光度的对比得出TritonX-100的效果最佳。所以本实验选用TritonX-100。浓度为2%的TritonX-100水溶液的最佳用量为0.5~1.5,实验选用 1.0mL。
2.3.4 显色剂[13]用量的影响
实验表明,显色剂用量对吸光度的测定有较大的影响。对10μg/mL钯离子在考察了不同用量显色剂对反应的影响,结果表明,0.2g/L三氮烯溶液的最佳用量为1~2mL。实验用0.2g/L的三氮烯乙醇-丙酮溶液1.5mL。不同用量的显色剂的吸收光谱如图2-3。

图2-2 吸收光谱

图2-3 吸收光谱
2.3.5 显色时间及配合物的稳定性
试验结果表明,体系的显色较快且比较稳定,吸光度在显色15min后达到恒定最大值。
2.3.6 试剂加入顺序影响
按照如下6种顺序加入试剂:
①Pd(Ⅱ)→表面活性剂→缓冲溶液→显色剂;
②Pd(Ⅱ)→表面活性剂→显色剂→缓冲溶液;
③Pd(Ⅱ)→缓冲溶液→表面活性剂→显色剂;
④Pd(Ⅱ)→缓冲溶液→显色剂→表面活性剂;
⑤Pd(Ⅱ)→显色剂→表面活性剂→缓冲溶液;
⑥Pd(Ⅱ)→显色剂→缓冲溶液→表面活性剂。然后分别测定各显色体系对对应空白的A值。试验结果表明以第四种试剂加入顺序测得A值最大,所以实验选用试剂加入方法是Pd(Ⅱ)→缓冲溶液→显色剂→表面活性剂。
2.3.7 配合物的组成
在上述条件下,采用比摩尔法和直线法测定络合物中摩尔比 nPd∶n显色剂=1∶3。在室温下,在15 min以内络合物的吸光度可以达到最大值,具体数值如下:

表2-1 络合比测定结果
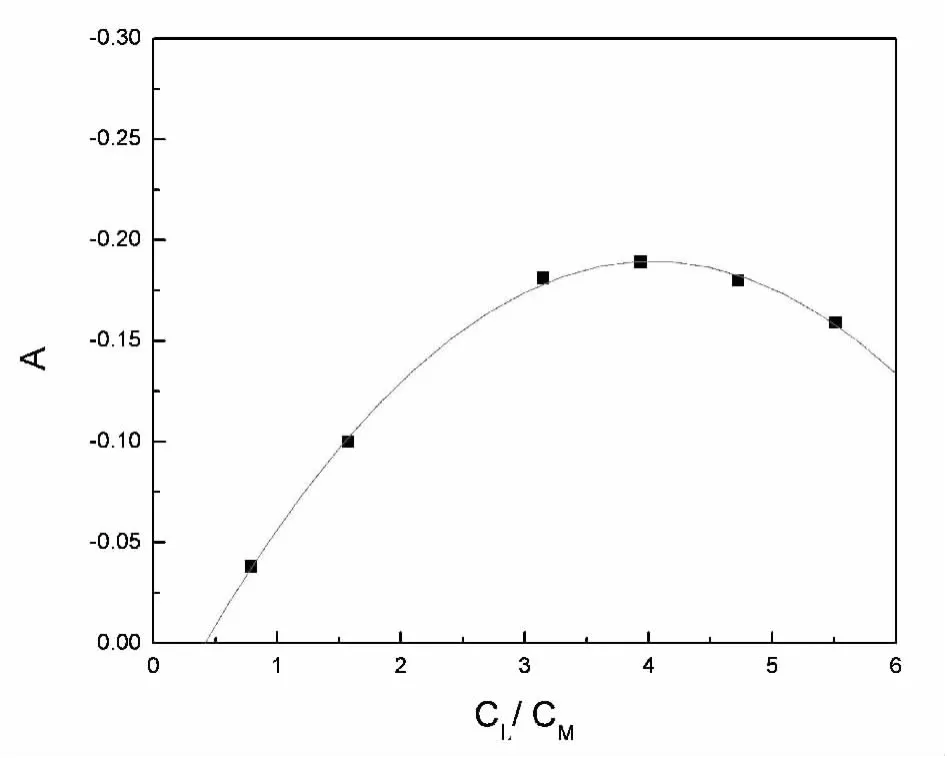
图2-4 络合比
2.3.8 工作曲线
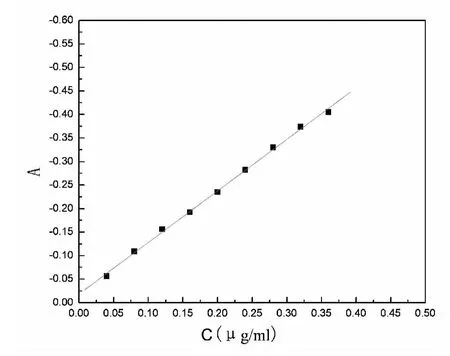
图2-5 工作曲线
在最佳实验条件下,钯离子的浓度在0~0.036μg/mL范围内符合比尔定律。由工作曲线求得直线的回归方程及相关系数如下:
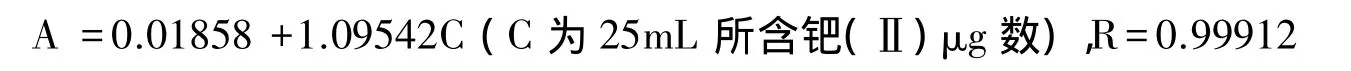
2.4 共存离子的影响
在实验操作条件下,测定含有9μg钯离子的吸光度,当允许相对误差在±5%范围,含如下离子无干扰(未测最高允存量):Hg2+、Cr3+、Al3+、Zn2+。而以下这几种离子有干扰:Cd2+、Ni2+、Co2+。加入 2ml 5.0%NaF与5.0%酒石酸钠混合掩蔽剂时可有效的消除共存干扰离子。
2.5 样品分析
取100mL的自来水,加入1mL钯标准溶液,搅拌均匀,制得合成水样。两次取此不同量的水样,然后按实验方法进行显色,并分别对他们同时进3次加标回收试验,根据标准曲线以及测得的吸光度计算平均回收率和标准偏差 ,测定结果如表2-2所示。

表2-2 样品钯含量测定结果
3 结论
本文合成了三氮烯类显色剂,并可用于微量钯元素的定量分析的方法。通过三氮烯类显色试剂和钯的显色反应条件的探讨,结果表明,该试剂对定量分析微量元素钯具有较好的选择性和较高的灵敏度的优良性能,测定方法简便快速。
[1]孙培培,王磊,等.三氮烯试剂的合成进展[J].化学试剂,1992,14(5):307-309.
[2]赵桂丹,郑云法.三氮烯试剂的合成进展[J].丽水师范专科学校学报,2001,23(5):22-26.
[3]堵锡华,刘长宁.1-(2-羟基-3,5-二硝基苯)-3-(4-苯基-2-噻唑)-三氮烯的合成及其与镍的显色反应[J].岩矿测试,2000,19(4):311-313.
[4]冯永兰.1-(2-羟基-3,5-二硝基苯基)-3-[4-(苯基偶氮)苯基]-三氮烯与汞的显色反应及其应用[J].分析化学,2000,28(3):311-313.
[5]张学军,夏心泉,等.4-甲醛基重氮氨基偶氮苯的合成及其与汞显色反应的研究[J].沈阳化工,1999,8(4):9-11.
[6]杨明华,龚楚儒,等.三氮烯试剂合成的新方法[J].化学世界 ,1998,9(9):478-479.
[7]王超,李杰,等.新型三氮烯试剂的合成及其性质[J].郑州大学学报(理学版),2011,43(4):81-83.
[8]杨明华,郑云法,等.1-(4-硝基苯基)-3-(5-硝基-2-吡啶)-三氮烯的合成及其与汞的显色反应研究[J].广东微量元素科学,2001,8(4):56-59.
[9]许琳,高美丽.三氮烯试剂的合成及其与Cd(Ⅱ)的显色反应研究进展[J].天津化工,2006,20(6):8-10.
[10]陈文宾,郑秋霜,等.一种新的三氮烯试剂的合成并应用于金(Ⅲ)离子的显色反应[J].理化检验-化学分册,2011,47(1):1-3.
[11]候林,等.新型新型三氮烯试剂的合成及其与痕量Pb(Ⅱ)的显色反应研究[J].北京农业大学学报,2011,42(5):130-132.
[12]龚楚儒,金传明,等.新试剂1-偶氮苯基-3-(5-硝基-2-吡啶)-三氮烯的合成及其与镉的显色反应[J].化学研究与应用,2001,13(5):532-533.
[13]杨海 ,徐军,等.两种含氟三氮烯显色剂FDNDAA与FFDAA的合成及其与镉显色反应的研究[J].理化检验-化学分册 ,2001,37(9):385-390.

