分子钳人工受体的研究进展
武运跃,石 浩,刘贵君
(浙江工业大学药学院,浙江杭州310032)
生物化工
分子钳人工受体的研究进展
武运跃,石 浩,刘贵君
(浙江工业大学药学院,浙江杭州310032)
分子识别是生物有机化学前沿富有挑战性的领域之一,分子钳作为一类新型的人工受体,因其在手性拆分、分子识别、传感器等方面具有的应用,受到广泛的关注,本文概括了分子钳受体的研究现状。
分子钳;人工受体;分子识别
0 前言
分子识别是生物体系的基本特征,酶选择性地催化生化反应、抗体与抗原的相结合等都是其精确的分子识别[1-3]。人工受体自上个世纪80年代以来,层出不穷,并对阴离子、阳离子、中性有机分子及生物分子表现出了一定的识别性能。钳形受体在结构上具有天然的空腔,可以根据识别不同的客体设计合成不同的类型,合成了一系列以胆甾、杯芳烃、芳杂环为隔离基的分子钳人工受体,引起人们的广泛关注,分子钳大致可分为以下几种。
1 芳杂环类分子钳
芳杂环类分子钳可望通过氢键、π-π stacking等作用产生识别作用,尽管单个氢键作用较弱,但当多个氢键协同作用就可能显示对客体分子强的选择性。
Fang等[4]合成了能选择性识别PO43-和HPO42-阴离子的分子钳1和2(Scheme 1),核磁滴定研究发现:主体酰胺与客体阴离子形成1:1型超分子配合物,其中分子钳2对PO43-和HPO42-的结合常数分别高达186300 mol/L,328400 mol/L,可用于磷酸根浓度测定的传感器。

Scheme 1
Kyne等[5]合成了手性分子钳3和4(Scheme 2),对主体3和4与多种氨基酸衍生物进行核磁滴定,滴定结果表明:主客体分子在破坏分子内氢键的同时,也形成了新的分子内氢键。其中,分子钳3对N-乙酰-L-谷酰胺阴离子有一定的对映选择性KL/KD=2,分子钳4对N-乙酰-D-谷酰胺阴离子选择性较好,KD/KL=2。
2005年,王健等[6]合成了以间苯二甲酸为隔离基,L-氨基酸甲酯为手性臂的手性分子钳5-10(Scheme 3),分子钳7对对硝基苯胺的结合常数高达2.622×103mol/L,分子钳6对丙氨酸甲酯具有较好的选择性,KD/KL高达7.6。

Scheme 2
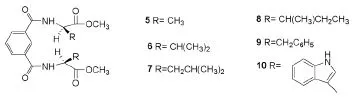
Scheme 3
彭游等[7]合成了对尿素、二苯甲酮、对硝基苯妥、戊二酰亚胺等具有一定识别性能的分子钳11-13(Scheme 4)。
曾碧涛等[8]合成了手性分子钳14~17(Scheme 4),分子钳14~17通过氢键作用对Cl-、Br-、I-和CH3COO-等都具有一定的识别性能,且形成了1:1型超分子配合物,选择性顺序为I->Br-> Cl->CH3COO-,分子钳15和16对I-的结合常数分别为1356.52 mol/L和7731.23 mol/L。
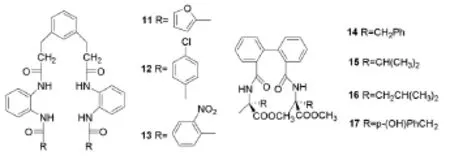
Scheme 4
高学祥等[9]合成了一类新型的三嗪类希夫碱分子钳18~20(Scheme 5),通过紫外滴定实验表明:分子钳19的紫外吸收强度随着Mg2+、Na+加入明显增强,铁离子使分子钳20的紫外吸收的峰型产生了明显的改变,表明了分子钳对金属离子有一定的选择性识别作用。
曾振亚等[10]合成了含有双蒽基团的新型酰胺阴离子受体21(Scheme 5),研究显示:该分子钳与对硝基苯酚形成1:1型超分子化合物,结合常数为1.24×103mol/L,对Br-、Cl-、I-等没有识别作用。

Scheme 5

Scheme 6
2 胆甾类分子钳
胆甾因其具有固有的不对称性及刚性结构,是构筑人工受体的理想单元。
2003年,陈淑华等[11]合成了一系列基于胆甾的手性分子钳22~46(Scheme 6),通过紫外滴定和核磁滴定实验表明,分子钳22~26对卤素阴离子均能形成1:1型超分子化合物,识别选择性为I->Cl->Br-,结合常数在102~103mol/L之间。分子钳27~32对氨基酸甲酯产生了一定的对映选择性,其中分子钳32对D/L-亮氨酸甲酯的KD/KL高达9.4,分子钳27对D/L-苯丙氨酸甲酯的KD/KL值达到4.5。分子钳28对D/L-苯丙氨醇的KD/KL达到了3.4,其它的手性分子钳都对氨基酸衍生物有一定的识别性能,分子钳44、46对苯胺、对硝基苯胺、对甲氧基苯胺有一定的选择性。
赵志刚等[12]合成了以脱氧胆酸甲酯为隔离基的分子钳47~51(Scheme 7),经紫外光谱实验表明:分子钳47~51对苯胺、邻甲氧基苯胺、间甲氧基苯胺和对甲氧基苯胺有良好的识别作用,主客体分子间形成1:1型超分子配合物,在氯仿中的选择性为苯胺>对甲氧基苯胺>间甲氧基苯胺>邻甲氧基苯胺,分子钳50对苯胺的结合常数高达14171.39 mol/L。

Scheme 7
曾碧涛等[13]合成了氨基甲酸酯型猪去养胆酸分子钳52~56(Scheme 8),紫外滴定表明:该类分子钳对卤素阴离子均具有较好的识别能力,选择性顺序为I->Br->Cl-。
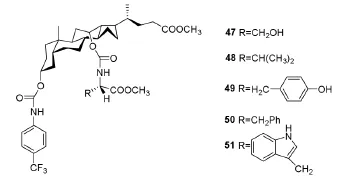
Scheme 8
赵志刚等[14]通过点击化学方法合成了鹅去氧胆酸类分子钳57~68(Scheme 9),经紫外滴定实验表明:主客体间形成了1:1型超分子化合物,对Hg2+的识别能力明显高于Cu2+,Mg2+,Pb2+。
Davis等[15]合成了胆甾胍盐分子钳受体69,70(Scheme 10),并研究了对外消旋体N-乙酰基氨基酸的手性拆分能力,结果显示:分子钳70对N-乙酰基氨基酸的对映选择性KL/KD高达10。
Liu等[16]在胆甾的3α和24α位上连接硫脲和氨基硫脲,形成了多重氢键的人工受体71(Scheme 11),受体71对L-谷氨酸有较好的识别能力,其结合常数高达5.57×106mol/L。

Scheme 9
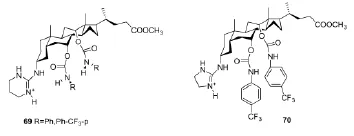
Scheme 10

Scheme 11
3 基于杯芳烃的分子钳
杯芳烃是具有三维结构的大环化合物,成为继环糊精和冠醚之后的又一类超分子主体化合物,受到大家的广泛关注[17-18]。由于其结构具有多变性、易于修饰的特点,所以可通过引入不同的官能团,得到满足条件的化合物[19-20]。如在杯芳烃上引入适当的基团形成人工受体,这类受体可望通过氢键、范德华力和π-π堆积等作用来识别客体分子。
Beer等[21]合成了对叔丁基杯[4]芳烃上含有吡啶鎓盐的分子钳72(Scheme 12),该分子钳对HPO42-具有一定的识别性能且结合常数远大于卤素等阴离子。
陆国元等[22-23]在杯[4]芳烃上引入了两个双胍基合成了手性杯芳烃衍生物73(Scheme 12),通过液-液竞争萃取实验表明,该分子钳选择性识别芳香族氨基酸,对L-苯丙氨酸的选择性高达90%。
Chen等[24-25]在杯芳烃冠醚的基础上合成了系列具有手性的杯芳烃衍生物74,75(Scheme 13),其中74对D-(+)葡萄糖酸内酯具有很好的识别性能,结合常数达1.8×104mol/L。
He等[26]在杯芳烃上引入光学活性基团L-色氨酸,合成了分子钳76~78(Scheme 13),并对N-取代丙氨酸阴离子有不同程度的手性识别性能。

Scheme 12
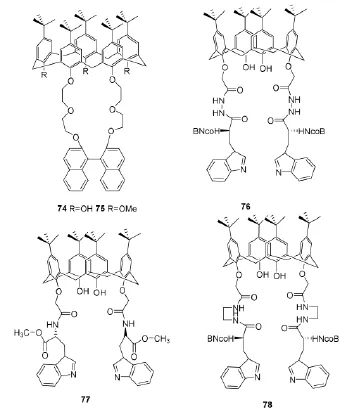
Scheme 13
Zheng等[27]在杯芳烃中引入甲基苄胺基团合成了手性杯芳烃分子钳79~80(Scheme 14),其中79展现了对D-二苯甲酰酒石酸的高选择性、专一性的特点,而分子钳80对D-二苯甲酰酒石酸没有识别性能。
Diamond等[28]在杯[4]芳烃下缘的四个酚羟基上引入了含有双萘荧光团的手性片段81(Scheme 14),通过光谱滴定实验发现其对R和S型苯乙胺有较好的选择识别性能。
随后Diamond等[29-30]又设计合成了82~83(Scheme 14),荧光淬灭实验表明:受体83在甲醇溶液中对短链的氨基醇、苯甘氨醇没有手性识别性能,但对长链的氨基醇、苯丙氨醇具有很好的手性识别性能。
何永炳等[31]合成了含有单磺酰基的杯[4]芳烃分子钳84(Scheme 14),通过光谱滴定实验发现其对R型的分子钳对N-乙酰基保护的天门冬氨酸阴离子具有较好的识别能力,KD/KL高达6.74;而S型的分子钳刚好呈现出相反的效果,KL/KD高达6.48。
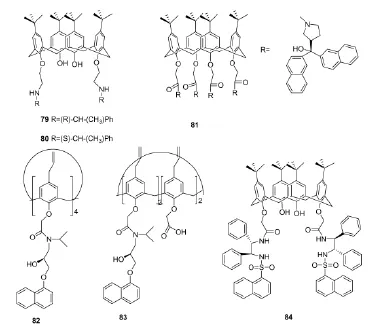
Scheme 14
4 基于异斯特维醇的手性分子钳
异斯特维醇是由甜菊糖苷经酸解(Scheme 15)之后得到的四环二萜类化合物[32],结构中含有多个手性中心且其结构稳定,因其具有刚性的凹面结构和固有的不对称性,是构筑分子识别人工受体的理想结构单元。该化合物于1955年由Mosetling E和Nes WR首次报导[33]。

Scheme 15
Katae V E等[34-35]在两分子的异甜菊醇的19位羧基上通过酯键或酰胺键的空间结构桥连得到了化合物85~88(Scheme 16),并以水-氯仿层模拟生物膜,测试了其对D、L-色氨酸等氨基酸的识别转移能力。实验发现:在以对D、L-色氨酸有识别转移能力的二苯骈-18-冠-6为实验对照的情况下,具有聚亚甲基二酯的空间结构的化合物85识别转移D、L-色氨酸的能力最强。而分子钳87和88对所测试的D/L-苯丙氨酸甲酯基本没有识别性能。
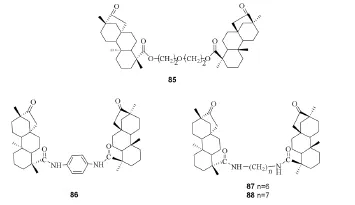
Scheme 16
5 结语
分子钳人工受体近些年来发展极为迅速,合成了一批对生物分子具有识别作用的受体,但是目前所报道的分子钳的手臂都是以非手性单元居多,而手性识别在生命过程中具有极其重要的作用,因此,设计合成隔离基和手臂都是手性单元的分子钳人工受体仍然有很大的发展前景。
[1]陈淑华,罗光荣.生物有机化学[M].成都:四川大学出版社,1991.
[2]DugasH.BioorganicChemistryFrontiers,Vol.2[M], Springer-Verlag,Berlin,1991.
[3]Dugas H.Bioorganic Chemistry;A Chemical Approach to Enzyme Action,3rd ed[M],Springer-Verlag,New York,1997.
[4]Liao J H,Chen C T,Fang J M.A novel phosphate chemosensor utilizing anion-induced fluorescence change [J].Org.Lett,2002,4:561-564.
[5]Kyne G M,Light M E,Kilburn J D.Enantioselective amino acid recognition using acylic thiourea receptors[J].J.Chem. Soc,Perkin Trans I,2001,11:1258-1263.
[6]王健,杨祖幸,张清华,等.手性芳酰胺类分子钳的设计与微波合成[J].有机化学,2005,25(7):850-853.
[7]彭游,陈淑华.芳杂环类分子裂缝对中性小分子的识别性能研究[J].四川大学学报,2006,43(1):175-178.
[8]曾碧涛,赵志刚.芳酰胺分子钳对阴离子的识别研究[J].化学研究与应用,2009,21(9):1279-1282.
[9]高学祥,赵军龙,李小安,等.三嗪类席夫碱分子钳化合物的合成与表征[J].应用化工,2013,42(12):2232-2236.
[10]曾振亚,吴进龙,隗兰华,等.含双蒽基团酰胺受体分子的合成及阴离子识别研究[J].高等学校化学学报,2003, 24(11):2005-2009.
[11]牟其明,陈淑华.手性不对称脲、胆甾和芳杂环类分子钳受体的设计合成及分子识别研究[D].成都:四川大学.
[12]杨学军,赵志刚等.脱氧胆酸手性分子钳的微波合成及其对中性分子的识别性能研究[J].化学研究与应用, 2008,20(11):1147-1152.
[13]曾碧涛,赵志刚,周黎军,等.氨基甲酸酯型猪去氧胆酸分子钳的微波合成及其对卤素阴离子的识别[J].合成化学,2011,19(5):614-618.
[14]赵志刚,王晓红,石治川,等.通过点击化学方法合成鹅去氧胆酸类分子钳及其识别性能研究[J].有机化学, 2014,34:1110-1117.
[15]Davis A P,Perry J J,Williams R P.Anion recognition by tripodal receptors derived from cholic acid[J].J.Am.Chem. Soc,1997,119:1793-1794.
[16]Shun-Ying Liu,Lei Fang,Yong-Bing,et al.Cholic-acidbased fluorescent sensor for dicarboxylates and acidic amino acids in aqueous solutions[J].Organic Letters,2005, 7:5825-5828.
[17]黄志镗,杨联明.杯芳烃研究进展[J].化学进展,1994,6(3): 173-177.
[18]Timmerma P,Verboom W,Reinhoudt D N.Resorcinarenes [J].Tetrahedron,1996,52:2663-2704.
[19]Bohmer V.Calixarenes,macrocycles with(almost)unlimited possibilities[J].Angew.Chem.Int.Ed.Engl,1995,34:713-745.
[20]Li X,Upton T G,Gibb C L D,et al.Resorcinarenes as templates:a general strategy for the synthesis of large macrocycles[J].J.Am.Chem.Soc,2003,125(3):650-651.
[21]Beer P D,Drew M G B,Gradwell K J.Synthesis and anion coordination chemistry of new calix[4]arene pyridinium receptors[J].Chem.Soc.Perkin Trans,2000,3,511-519.
[22]Liu F,Lu G Y,He W J,et al.Synthesis of calix[4]arene derivatives with alkyl guanidinium or chiral bicyclic guanidinium[J].Synthesis,2001,4:607-611.
[23]Liu F,Lu G Y,He W J,et al.Enantioselective recognition of calix[4]arene derivative bearing bicyclic guanidinium for D/L amino acid zwitterions[J].Chin.J.Chem,2001,19:317-320.
[24]Li S.Y,Zheng Q Y,Chen,C.F,et al.Fluorescent probes of d-(+)-gluconic acid δ-lactone based on binary hosts of chiral calix[5]arene[J].Tetrahedron:Asymmetry,2005,16: 2816-2820.
[25]Xu Z X,Zhang C,Zheng Q Y,et al.A new approach to enantiopure inherently chiral calix[4]arenes:determination of their absolute configurations[J].Org.Lett,2007,9:4447-4450.
[26]Qing G Y,He Y B,Wang F,et al.Enantioselective fluorescent sensors for chiral carboxylates based on calix[4]arenes bearing an l-tryptophan unit[J].Eur.J.Org.Chem,2007, 11:1768-1778.
[27]ZhengYS,JiA,ChenXJ,etal.Enantioselective nanofiber-spinning of chiral calixarene receptor with guest [J].Chem.Commun,2007,3398-3400.
[28]Grady T,Harris S J,Diamond D,et al.Determination of the enantiomeric composition of chiral amines based on the quenching of the fluorescence of a chiral calixarene[J]. Anal.Chem,1996,68:3775-3782.
[29]Lynam C,Jennings K,Diamond D,et al.Tuning and enhancing enantioselective quenching of calixarene hosts by chiral guest amines[J].Anal.Chem,2002,74:59-66.
[30]Lynam C,Diamond D.J.Varying solvent polarity to tune the enantioselective quenching of a calixarene host[J]. Mater.Chem,2005,15:307-314.
[31]Qing G Y,Qin H J,He Y B,et al.Enantioselective fluorescent recognition of amino alcohol based on calix[4]arenes bearing diphenylethylenediamine units[J].Supramol.Chem, 2008,20:265-271.
[32]Avent A G,Hanson J R,Ollveira B H.Hydrolysis of the diterpenoid glycoside,stevio-side[J].Phytochem,1990,29 (8):2712-2715.
[33]Mosetting E,Nes W R.SteviosideⅡthe structure of the aglycon[J].J.Org.Chem,1955,20:884-899.
[34]Kataev V E,Irina Y S,Militsina O I,et al.Isosteviol and some of its derivatives as receptors and carriers of amino acid picrates[J].Tetrahedron Letters,2006,47:2137-2139. [35]Kataev V E,Militsina O I,Strobykina I Y,et al.Synthesis and anti-tubercular activity of diesters on the basis of isosteviol and dicarboxylic acids[J].J.Pharm.Chem,2006, 40:473-475.
Progress in Research on Molecular Tweezers Artificial Receptors
WU Yun-yue,SHI Hao,LIU Gui-jun
(College of Pharmacy Science,Zhe Jiang University of Technology,Hangzhou Zhejiang 310032,China)
The study on molecular recognition of artificial receptors is one of the frontiers in bioorganic chemistry.Molecular tweezers as a new type of artificial receptor get widespread attention,it can be used in chiral separation,molecular recognition and sensors etc.This paper reviews the recent progress in molecular tweezers artificial receptors.
molecular tweezers;artificial receptor;molecular recognition
1006-4184(2015)8-0012-06
2015-03-11
武运跃(1989-),男,硕士研究生,专业方向:生物化工。E-mail:1229929609@qq.com。

