双(二苯基膦)烷烃的合成与表征
杨振强,孙敏青,周 铎,杨瑞娜
(河南省科学院 化学研究所有限公司,河南 郑州 450002)
双(二苯基膦)烷烃是一类重要的中间体和催化剂配体,可以与过渡金属化合物反应合成均相催化剂,广泛应用于工业催化领域,特别是应用于有机合成领域的偶联反应[1-3].偶联反应是有机合成中用于形成C-C,C-N,C-S等键的有效手段,其在合成天然产物、功能材料、药物、液晶分子以及生物活性化合物中有着非常广泛的应用[4-5].
本文作者采用三苯基膦为起始原料,经金属锂化制备二苯基膦锂后与二溴代烷烃(n=1~6)反应合成了目标化合物.该反应易于控制,减少了分离成本,使其更适合于工业化生产.1H NMR、31P NMR、MS和元素分析等确证了化合物的结构.合成路线见图1.
1 实验部分
1.1 仪器与试剂
Agilent 1120型液相色谱;Trance GC Ultra DSQⅡ型气质联用仪;Yanagimoto MFG CO型熔点测定仪(温度计未经校正);VARIO ELⅢ型元素分析仪;Bruker Avance 300型核磁共振仪(TMS为内标,氘代氯仿为溶剂).
实验所用的试剂均为分析纯.
1.2 合成过程
在氩气保护下,向干燥反应器中加入200mL四氢呋喃、78.7g(0.3mol)三苯基膦和2.5g叔丁醇钾,然后在水浴冷却下加入0.6mol锂,自然升温,搅拌过夜;液相色谱(HPLC)检测无三苯基膦后降温至0℃;分批加入0.3mol氯化铵,搅拌反应2h;控制反应温度并向反应体系滴加0.15mol二溴烷烃,保持温度-10~10℃反应5h,减压回收溶剂得到粘稠状固体,依次用稀盐酸、水、甲醇洗涤,氯仿和甲醇混合溶剂重结晶,得到类白色固体产品,含量大于98%(HPLC检测),收率为75%~86%.
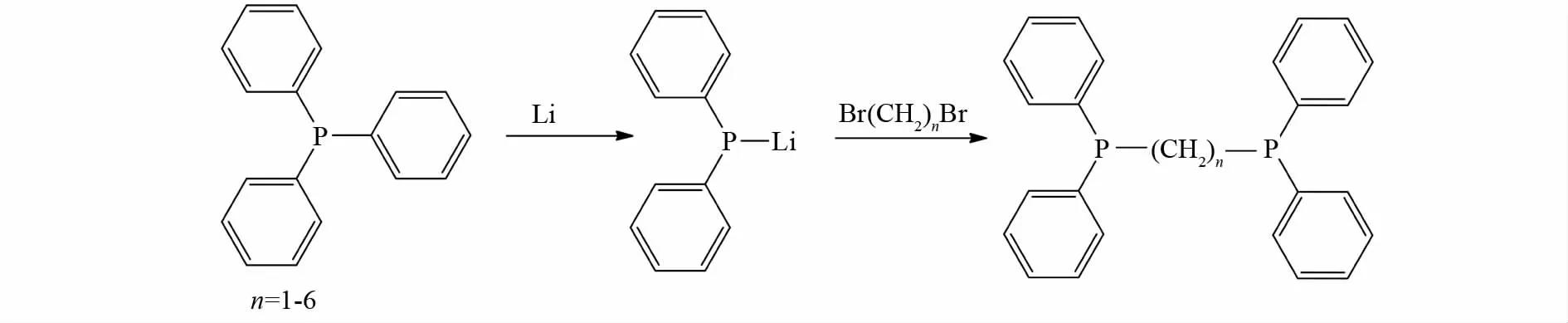
图1 合成路线Fig.1 Synthetic route
2 结果与讨论
2.1 反应条件
在合成双(二苯基膦)烷烃过程中,关键因素是控制滴加二溴烷烃时的反应温度,如果反应温度过高,产品收率会急剧降低,这可能是因为随着反应温度升高有聚合反应发生,导致产品产率下降.反应温度较低时,反应进行缓慢,氧化和水解等副反应增加.研究发现,使用二溴烷烃(n=1~6)烷基化过程中偶数碳链的最佳反应温度为10℃,奇数碳链的为-10℃.
2.2 物化性质
双(二苯基膦)烷烃随着烷基碳数的增大,偶数化合物或奇数化合物熔点均是依次降低.这可能是因为随着烷基的增大,分子极性降低,分子间取向力降低,相对分子质量增加,分子间色散力增加.当色散力的增加不足以弥补取向力的降低,熔点就会降低;当色散力的增加超过取向力的降低,熔点就会升高(表1).
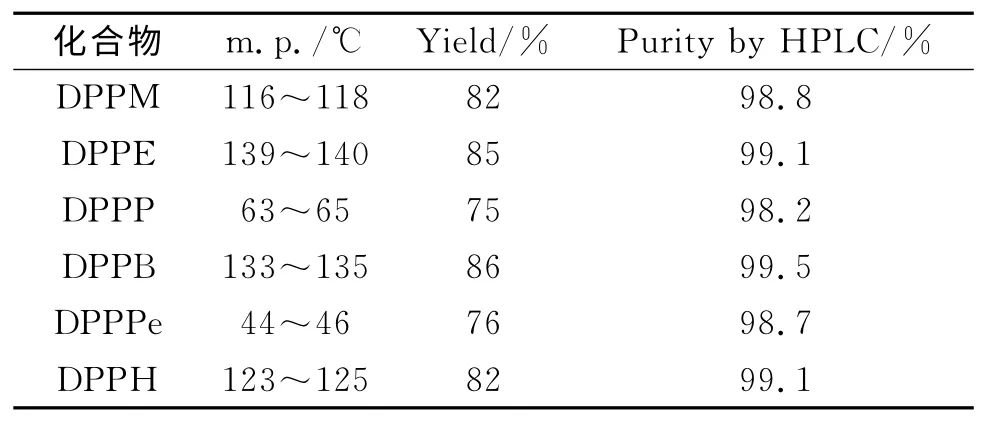
表1 化合物的收率和理化数据Table 1 Yield and physic-chemical data of the compounds
2.3 表征
在CDCl3溶剂中(氢谱使用TMS为内标,膦谱使用85%的磷酸为内标)测得各个化合物的NMR数据见表2.3以上高场为烷基碳链上氢的化学位移,7以下低场为苯环上氢的化学位移,各化合物中苯环上氢化学位移的个数与烷基碳链上氢化学位移个数一致.各化合物的膦谱数据虽然没有规律可循,但是均呈单峰,说明化合物的纯度和对称性均比较高.
利用VARIO ELⅢ元素分析仪和气质联用仪对各个化合物进行了分析,结果如表3所示.质谱、元素分析结果佐证了目标产物的结构.

表2 化合物的核磁数据(溶剂:CDCl3,300MHz,δ)Table 2 NMR data of compounds(solvent:CDCl3,300MHz,δ)
3 结论
合成的双齿膦配体可以通过单齿、双齿、螯合或桥连等方式与过渡金属配位,可广泛应用于偶联反应,特别是Suzuki偶联反应和Kumada反应.通过改变两个P原子之间的骨架长度,改变了其电子效应和立体效应,进而增强磷原子周围的电子云密度,增强其亲核性,加快了其氧化加成的速度,增大了膦配体脱离过渡金属的趋势,最终提高了其做为过渡 金属催化剂配体的活性.
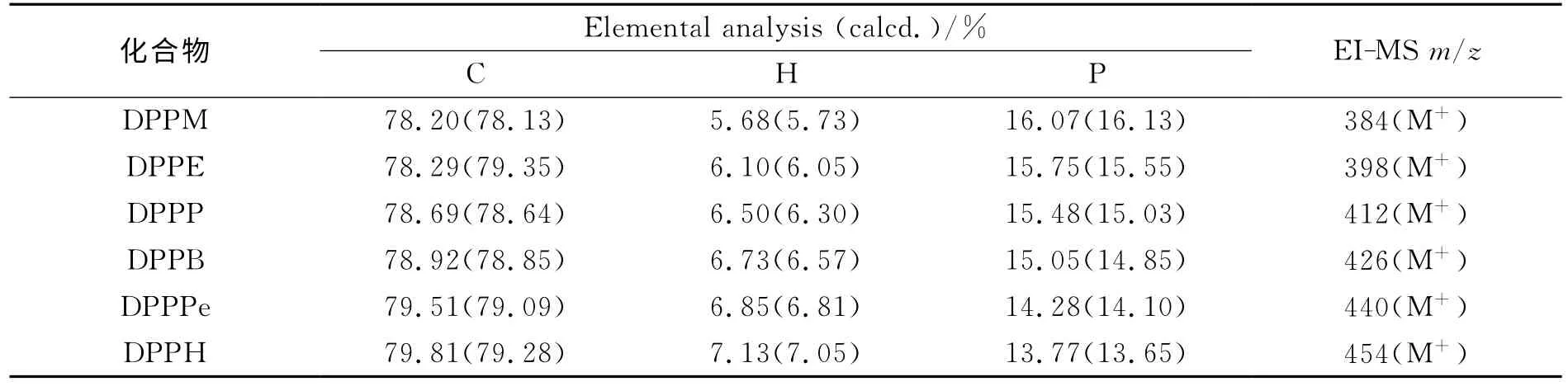
表3 化合物的元素分析和MS数据Table 3 MS and elementary analysis data of compounds
[1]IWASAWA N,SATOH H.A novel synthesis of 4,5-didehydrotropone—CO2(CO)4·dppm complexes[J].J Am Chem Soc,1999,121(34):7951-7952.
[2]BERA J K,ANGARIDIS P,COTTON F A,et al.Incorporating multiply bonded dirhenium species[Re2]n+(n=4or 5)into assemblies containing two or more such units[J].J Am Chem Soc,2001,123(7):1515-1516.
[3]HONAKER M T,SALVATORE R N.A mild and efficient csoh-promoted synthesis of ditertiary phosphines[J].Phosphorus,Sulfur and Silicon and the Related Elements,2004,179(2):277-284.
[4]ROBERT T H,SCOTT M Q.Hydrogenase enzyme reactivity modeling with a transition-metal dihydrogen complex[J].J Am Chem Soc,1994,116(5):2141-2142.
[5]BERTHOD M,ALAIN F R,MOHAMAD J,et al.A catalytic method for the reduction of secondary and tertiary phosphine oxides[J].Synlett,2007,10:1545-1548.