不同浓度生物活性玻璃对早期釉质龋再矿化的作用
方 谦, 穆 玉, 徐晓南, 周 雪, 彭 伟
(华北理工大学口腔医学院, 河北 唐山 063000)
·临床研究·
不同浓度生物活性玻璃对早期釉质龋再矿化的作用
方 谦, 穆 玉, 徐晓南, 周 雪, 彭 伟
(华北理工大学口腔医学院, 河北 唐山 063000)
目前: 探讨不同浓度生物活性玻璃促进早期釉质龋再矿化的效果。方法:收集新鲜拔除的牛切牙,制备釉质标本,随机分为显微硬度组(n=15)和能谱分析组(n=25)。各组标本在37 ℃人工脱矿液中脱矿72 h,然后用pH循环法模拟人的口腔环境,将标本分别浸泡在30、60、90 g/L生物活性玻璃溶液内,2次/d,5 min/次,循环15 d。用显微硬度仪在釉质块脱矿前及再矿化后分别测量其表面显微硬度,能谱分析仪对釉质表面的元素进行分析。结果: 脱矿处理后各组样本显微硬度均明显降底,生物活性玻璃溶液处理后显微硬度均明显提高,其中60 g/L 组的显微硬度差值最高,30 g/L组最低(P﹤0.05)。钙磷比以90 g/L组最高,60 g/L 组次之。结论:60 g/L生物活性玻璃促进早期釉质龋再矿化的疗效较好,90 g/L生物活性玻璃抗酸性最强。
生物活性玻璃; 早期釉质龋; 再矿化; 显微硬度
[DOI] 10.15956/j.cnki.chin.j.conserv.dent.2015.12.006
[Chinese Journal of Conservative Dentistry,2015,25(12): 729]
龋病初期的白垩斑的形成主要是釉质脱矿与再矿化动态平衡被破坏的结果。 再矿化是使钙、磷和其他矿物离子沉积在脱矿的釉质中,从而恢复脱矿釉质的硬度,终止或消除早期龋损。氟化物能较好的促进早期釉质龋再矿化,但其具有一定局限性:只能用于易清洁的平滑面,且需要多次涂擦[1]。生物活性玻璃(45S5)是由多种无机离子组成的具有优良的生物相容性和成骨活性的生物活性材料[2],其属于第3代生物活性玻璃,是一种以钙钠磷硅酸为活性成分的矿物质,最初用于骨再生[3],其安全性已得到认可,在口腔医学中的应用较为广泛,尤其在牙本质过敏、牙周炎治疗及牙槽骨重建等领域有较好的疗效。诸多学者证实了生物活性玻璃具有促进脱矿组织再矿化的作用,但其最适浓度未见报告。本实验通过观察在不同浓度生物活性玻璃干预下脱矿牛牙釉质的显微硬度和钙磷比的变化,探讨不同浓度生物活性玻璃促进早期釉质龋再矿化的作用,为临床应用提供理论依据。
1 材料和方法
1.1 主要材料和仪器
生物活性玻璃粉体(45S5)(北京大清):加入去离子水中配成30、60、90 g/L溶液;人工脱矿液配方:2.2 mmol/L硝酸钙,2.2 mmol/L磷酸二氢钾,50 mmol/L冰醋酸,pH值4.5;人工唾液配方(ISO/TR10271标准):氯化钠0.4 g,氯化钾0.4 g,无水氯化钙0.795 g,磷酸二氢钠0.78 g,硫化钠0.005 g,尿素1 g,去离子水稀释至1 000 mL,pH值7.0;Noran7 X射线能谱仪(Thermo Fisher,美国);HVST-1000ZA 显微硬度计(上海研润光机);DH-250型电热恒温培养箱(北京科伟永兴)。
1.2 样本制备
选择新鲜拔除的牛切牙,从中选取釉质发育良好,无脱钙、龋损、划痕和裂纹的牛牙20个,冠根分离后,低速双面金刚砂片将牙冠切成5 mm×5 mm×2 mm釉质块40个,流水下用600、800、1 000、1 200、2 400目碳化硅砂纸依次磨平、抛光唇侧釉质面,置于4 ℃去离子水中备用。
1.3 方法
1.3.1 实验分组
将制备的40个釉质块样本随机分为2个大组:显微硬度组(n=15)和能谱分析组(n=25)。显微硬度组分为3个小组:30、60、90 g/L生物活性玻璃处理组(n=5),每组用不同颜色抗酸指甲油标记。能谱分析组分为5个小组:正常组、脱矿组和30、60、90 g/L生物活性玻璃处理组(n=5),正常组不做任何处理。脱矿前2大组除釉质面外均涂上双层抗酸指甲油。
1.3.2 早期釉质龋模型的建立
将所有釉质块(正常组除外)浸泡在37 ℃人工脱矿液中72 h,釉质表面成白垩色,即为早期釉质龋形成,取出釉质块,用去离子水冲洗1 min。
1.3.3 再矿化处理(24 h pH循环)
将经过脱敏矿处理的釉质块(脱矿组除外)进行再矿化处理:脱矿液中浸泡10 min→再矿化液中(30、60、90 g/L生物活性玻璃溶液)浸泡5 min→人工唾液中浸泡8 h→脱矿液中浸泡10 min→再矿化液中(30、60、90 g/L生物活性玻璃溶液)浸泡5 min→人工唾液中浸泡过夜。循环15 d,均在37 ℃电热恒温培养箱中进行。浸泡后用去离子水冲洗牙面 1 min。
1.3.4 釉质表面的元素分析
将能谱分析组标本固定在扫描电镜载物台上,抽真空喷金,在各小组样本的观察界面上随机选取3个点,用X射线能谱分析仪进行点扫描,分析釉质表面的元素含量,计算钙磷质量和摩尔比值(Ca/P)。
1.3.5 釉质显微硬度测量
显微硬度组用显微硬度计测量釉质块矿化前、矿化后、再矿化后釉质表面的显微硬度值,分别计为SMH、SMH1、SMH2,负荷1.961 N,作用10 s,每个标本随机测量3个点,取平均值, 并计算显微硬度差值(△SMH=SMH2-SMH1)。
1.4 统计学分析
采用SPSS 17.0软件进行统计分析。再矿化前后数据的比较选用配对t检验,组间比较用单因素方差分析,两两比较采用LSD法,检验水准α=0.05。
2 结果
2.1 不同浓度组显微硬度检测结果
釉质标本采用组内标本自身脱矿及再矿化前后的对比,不同浓度组内再矿化前后显微硬度值比较差异有统计学意义(P﹤0.05);单因素方差分析显示, 各浓度组间显微硬度差值具有统计学意(F=32.26,P<0.05)。两两比较显示,各浓度组间显微硬度差值的比较均有统计学意义(P﹤0.05), 60 g/L组的显微硬度差值最高,90 g/L 组次之,30 g/L组最低(表1)。
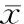
表1 不同浓度组再矿化前后显微硬度值比较(MPa, ±s)
不同字母组间相比P﹤0.05
2.2 不同浓度组能谱分析结果
能谱分析组随着生物活性玻璃浓度增加,Ca/P 摩尔比和质量比随之增加,与正常组的比值接近。单因素方差分析显示各组间质量比和摩尔比差异均有统计学意义(F=26.53,P﹤0.05;F=27.08,P<0.05)。两两比较显示,正常组的钙磷比与脱矿组、30 g/L和90 g/L组相比差异均有统计学意义(P﹤0.05),与60 g/L组相比差异无统计学意义(P﹥0.05);脱矿组的钙磷比与正常组、60 g/L 和90 g/L组相比差异均有统计学意义(P﹤0.05),与30 g/L组相比差异无统计学意义(P﹥0.05);90 g/L组的钙磷比与其余组相比差异均有统计学意义(P﹤0.05)(表2)。
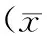
表2 不同浓度组钙磷比值比较 ±s)
a与正常组相比P﹤0.05;b与脱矿组相比P﹤0.05;c与30 g/L 组相比P﹤0.05;d与60 g/L组相比P﹤0.05;e与90 g/L组相比P﹤0.05
3 讨论
本实验采用的是化学致龋法中的脱矿溶液法,虽然未与自然龋损病程完全一致,但模拟了龋病主要的发生发展过程,对生物活性玻璃促进釉质龋再矿化作用的研究有一定的意义。早期釉质龋的临床表现为釉质表面呈现白垩色不透明区,其不透光性是由于釉质的脱钙使其光折射率的改变[4],该现象提示釉质发生了脱矿。本实验中不同浓度组釉质块标本经人工脱矿液处理后在肉眼观察下均成白垩色,提示了早期人工龋的形成。
釉质是人体中最硬的组织,主要由含钙磷离子的磷灰石晶体和少量其他磷酸盐晶体等组成[4]。釉质显微硬度的变化与矿物质的含量有关, Feagin等[5]发现在缓慢脱矿中,釉质表面显微硬度的减少与矿物质的丧失呈线性关系。而显微硬度测量是目前测量釉质硬度的主要方法,优点在于试验力小,对薄形样品可以测试;压痕小,可认为无损检测。正常人釉质的维氏硬度为242~339 VHN[6],本实验中的脱矿前牛牙釉质标本的显微硬度值符合正常人釉质的维氏硬度值。不同浓度生物活性玻璃处理组的釉质抗脱矿能力不同,其再矿化的能力也可能不同,因而本实验采用再矿化前、后的显微硬度的差值来说明不同浓度的药物促进脱矿釉质再矿化的效果。影响釉质再矿化的因素除了生物活性玻璃外,还可能与釉质本身相关,本实验对釉质标本自身脱矿前、后及再矿化后的显微硬度值进行检测,其差值更具有说服力,显微硬度差值越高,再矿化程度越高。本结果显示,60 g/L组的显微硬度差值较大,相对其他浓度组促进釉质再矿化的效果较好。
在釉质的再矿化实验中可通过X线能谱量化表面钙、磷的相对含量从而评估再矿化结果[7]。本结果显示,正常组和脱矿组中釉质表面元素主要由C、O、Ca、P等元素组成,而生物活性玻璃处理组中釉质表面元素主要由C、O、Ca、P、Si等元素组成。正常釉质表面的Ca/P质量比和摩尔比为2.1~2.3、1.61~1.8[8-9], 与实验前的釉质表面Ca/P离子比例接近。釉质发育不全的牙面较正常牙面钙离子含量低,且其抗酸溶解的能力也下降,从而推测釉质发育不全者更易患龋[10]。本实验在体外pH循环下进行,釉质标本浸泡在脱矿液中的时间相对较长,最后形成的Ca/P离子比例较高; 提示, 经过生物活性玻璃溶液处理过的釉质表面的抗酸能力增强,对釉质具有保护作用。生物活性玻璃抗酸性能的增强可能与其促进早期釉质龋再矿化的作用机制有关,即颗粒中的钠离子与溶液中的氢离子置换,使pH值升高; 颗粒中钙、磷酸离子释放,与唾液中的钙磷离子沉积在牙表面,形成富含钙磷的多孔网状矿化层,最后形成类羟基磷灰石[11-12]。本结果显示,30 g/L组的钙磷比相对偏低,60 g/L组的钙磷比与正常组的值接近,说明60 g/L 组的抗酸性较好;而90 g/L组的钙磷比高于正常组,这可能与以下因素有关:①诱导形成的釉质磷灰石晶体所含钙磷的比例较高;② 90 g/L生物活性玻璃溶液的钙磷离子浓度较高,未完全形成磷灰石晶体。推测90 g/L生物活性玻璃的抗酸性最强,60 g/L组次之。
综上所述,釉质发育不全者可选用90 g/L的生物活性玻璃溶液增强患牙的抗酸性,而早期釉质龋者可选用60 g/L的生物活性玻璃溶液促进早期釉质龋的再矿化。
[1]孙皎,赵信义.口腔生物材料学[M]. 北京:人民卫生出版社,2011:137.[2]Hench LL.The story of Bioglass[J].JMaterSciMaterMed,2006,17(11):967-978.
[3]Walsh LJ.Contemporary technologies for remineralization therapies: A review[J].InterDentSa, 2009,4(4):34-46.
[4]于世凤.口腔组织病理学[M]. 6版 . 北京:人民卫生出版社, 2007:53-156.
[5]Feagin F,Koulourides T,Pigman W.The characterization of enamel surface demineralization, remineralization,and associated hardness changes in human and bovine material[J].ArchOralBiol,1969,14(12):1407-1417.
[6]李东育,石四箴.牙釉质显微硬度测定及应用[J]. 上海铁道大学学报, 2000,21(3):96-98.
[7]Lou L,Nelson AE,Heo G,etal. Surface chemical composition of human maxillary first premolar as assessed by X-ray photoelectron spectroscopy (XPS)[J].ApplSurfSci,2008,254: 6706-6709.
[8]边专,王松灵.口腔生物学[M]. 4版 . 北京:人民卫生出版社, 2012:42.
[9]周学东.口腔生物化学[M]. 成都: 四川大学出版社, 2002:1-16.
[10]郑树国,邓辉,高学军,等.发育不全乳牙釉质的化学成分和晶体结构的初步研究[J]. 中华口腔医学杂志,1997,32(6):366-368.
[11]Wefel JS.NovaMin: likely clinical success[J].AdvDentRes,2009,21(1):40-43.
[12]Stoor P,Sderling E, Salonen JI. Antibacterial effects of a bioactive glass paste on oral microorganisms[J].ActaOdontalStandv,1998,56(3):161.
The effects of bioactive glass of different concentrations on the remineralization of the enamel with early caries
FANG Qian, MU Yu, XU Xiao- nan, ZHOU Xue, PENG Wei
(CollegeofStomatology,NorthChinaUniversityofScienceandTechnology,Tangshan063000,China)
AIM: To evaluate the effects of different concentrations of bioactive glass (BG) on remineralization of the enamel with early caries. METHODS: Freshly extracted bovine incisors were selected and used for enamel specimen preparation. After preparation, the specimens were placed in demineralization solution at 37 ℃ for 72 h to establish early enamel caries. Then pH cycle method was used for remineralization using 30, 60 and 90 g/L of bioactive glass respectively. After 15 d of pH cylcle, enamel micro hardness(MH) was measured by micro hardness tester(n=15),and the elements of the enamel were analyzed by X- ray energy spectrometer (EDX) (n=25). RESLUTS: After demineralization the MH of all the samples was decreased (P<0.05). After BG treatment the MH was increased(P<0.05), in 60 g/L group was the highest followed by that in 90 g/L group and 30 g/L group respectively(P<0.05). The molar ratio of Ca and P in 90 g/L group was the highest,followed by 60 g/L group(P﹤0.05). CONCLUTION: 60 g/L BG is most effective in remineralization of the enamel with early caries . 90 g/L BG is most resistant to the acid challenge.
bioactive glass; early enamel caries; remineralization; microhardness
2015-04-07;
2015-07-10
方 谦(1988-),女,汉族,浙江人。硕士生(导师:彭伟 )
彭 伟, E-mail:pengwei1968@sina.com
R781.1
A
1005-2593(2015)12-0729-04

