单亲灭活保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株融合子的选育
王慕华,潘佩平,赵玉明,2,苏槟楠,蔡颖慧,李海涛,2(.山西省生物研究所,山西太原030006;2.山西维尔生物乳制品有限公司,山西太原030006)
单亲灭活保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株融合子的选育
王慕华1,潘佩平1,赵玉明1,2,苏槟楠1,蔡颖慧1,李海涛1,2
(1.山西省生物研究所,山西太原030006;2.山西维尔生物乳制品有限公司,山西太原030006)
为获得具有抗噬菌体功能且发酵性能优良的乳酸菌酸奶生产菌株,将生产用保加利亚乳杆菌制备原生质体后高温灭活,灭活后的原生质体与嗜热链球菌抗噬菌体菌株的原生质体通过PEG6000诱导进行融合,并对融合子性能进行研究。结果从20株融合子中挑选出3株具有噬菌体抗性且发酵性能优良的乳酸菌融合子。融合条件为:以PEG6000(浓度为400 g/L,添加0.01 mol/L CaCl2、0.02 mol/L MgCl2)为促融剂,40℃融合2 min。此条件下,融合率可达1.85×10-6。获得的融合子在凝乳、产酸、产粘性物质、产香气成分及抗噬菌体方面性能优越,适合于酸奶生产。
单亲灭活,保加利亚乳杆菌,嗜热链球菌抗噬菌体菌株,原生质体融合,融合子选育
被誉为“美味食品”的酸奶因具有减缓人体乳糖不耐受性、减轻便秘、增强机体免疫力、降低血清胆固醇等功能而广受关注,需求量不断增大[1]。随着需求的增加,乳制品企业生产规模的扩大,生产菌株性能不稳定、常受噬菌体污染等问题也就日益凸显出来[2-3]。在发酵工业中,抗噬菌体乳酸菌的选育对于提高发酵效率,改善产品风味等起着非常重要的作用[4]。在发达国家,评价或筛选发酵剂优良菌株的重要标准就是抗噬菌体特性[5],目前我国在抗性乳酸菌的研究方面还停留在菌株的初步选育阶段,在工业化生产中应用很少,其生物学特性及发酵稳定性有待于进一步研究。
酸奶发酵通常采用保加利亚乳杆菌和嗜热链球菌作为主要发酵菌株。传统上,研究者普遍认为嗜热链球菌与保加利亚乳杆菌存在互惠共生关系[6]。这两种菌在牛奶中混合发酵会提高产酸速度,减弱后酸化程度,促进风味物质产生,产生更多的胞外多糖[7-8]。但近年来也有研究表明,某些嗜热链球菌与保加利亚乳杆菌株之间也存在拮抗抑制作用[9],混合发酵时比例不合适、条件控制不当就会直接影响到酸奶的生产时间与质量。因而研究嗜热链球菌与保加利亚乳杆菌菌株之间的共生关系,进行抗噬菌体菌株的选育,实现优良性状发酵菌株与抗噬菌体菌株的融合,可为工业化生产筛选出性状优良且质量稳定的酸奶生产菌株。与传统诱变或基因工程菌相比,原生质体融合可集中双亲优良性状且遗传稳定、安全可靠[10]。常用的合胞体杂种鉴定的方法有:菌体形态、大小等方面的形态特征分析;染色体核型、DNA含量、分子杂交等方面的遗传物质分析;同功酶谱、酶活性测定等方面的生理特性分析等[11]。本实验通过将已有的嗜热链球菌抗噬菌体菌株与具有优良生产性状的保加利亚乳杆菌进行融合,以期筛选出适合酸奶生产的乳酸菌生产菌株。
1 材料与方法
1.1材料与仪器
嗜热链球菌抗噬菌体菌株(Streptococcus thermophilus,S.t)由本所选育、保藏;保加利亚乳杆菌(Lactobacillus bulgaricus,L.b)酸奶生产厂家提供,本所保藏;噬菌体3种噬菌斑形态不同的噬菌体混合液,由本所分离、保藏[12];牛奶山西维尔生物乳制品有限公司提供,食品级;溶菌酶(22800 U/mg)BBI 购于生工生物工程(上海)有限公司;其他常规试剂均为国产分析纯。
PHS-3C雷磁pH计上海精密科学仪器有限公司;NDJ-1型旋转黏度计上海天平仪器厂;SLJ-Ⅰ型离心机沈阳理化仪器厂;WS2-84-64手提式高压蒸汽消毒器上海医用核子仪器厂;722PC可见分光光度计上海佑科仪器仪表有限公司;WS2-134-75电热恒温培养箱连云港医疗器械设备厂;FA1004电子天平上海舜宇恒平科学仪器有限公司;XMTD-4000电热恒温水浴锅北京市永光明医疗仪器厂;JT-型超净工作台常州第二航海仪器厂。
1.2实验方法
1.2.1试剂及培养基配制高渗溶液(原生质体稳定液):10 mmol/L Tris-HCl中加入0.5 mol/L蔗糖和0.02 mol/L MgCl2,用4 mol/L HCl溶液调节pH至6.5。
聚乙二醇(PEG6000):高渗溶液配制为400 g/L,并向其中加入0.01 mol/L CaCl2、0.02 mol/L MgCl2。
溶菌酶液:高渗溶液配制为10 mg/mL的酶原液,现用现配,过滤除菌。
MRS培养基[13]:蛋白胨10 g,牛肉膏10 g,酵母提取物5 g,柠檬酸二铵2 g,乙酸钠5 g,葡萄糖20 g,吐温80 1 mL,MgSO4·7H2O 0.58 g,MnSO4·4H2O 0.25 g,蒸馏水1000 mL,pH6.2~6.4,固体培养基添加1.5%的琼脂,用于保加利亚乳杆菌的培养。
M17培养基[13]:植物蛋白胨5.0 g,聚蛋白胨5.0 g,酵母提取物5.0 g,牛肉浸膏2.5 g,抗坏血酸0.5 g,β-甘油磷酸二钠19.0 g,1.0 mol/L MgSO4·7H2O 1.0 mL,蒸馏水1000 mL,pH6.8,固体培养基添加1.5%的琼脂,用于嗜热链球菌抗噬菌体菌株的培养。
原生质体再生培养基[14]:MRS、M17再生培养基为在其原有配方的基础上添加0.5 mol/L蔗糖,0.02 mol/L MgCl2。
脱脂乳培养基:牛乳脱脂后115℃灭菌15 min,冷却后置于冰箱冷藏备用,用于菌种的活化和菌株发酵性能的研究。
1.2.2指标检测
1.2.2.1噬菌体效价测定采用双层琼脂平板法[15]。
1.2.2.2酸奶酸度测定按GB/T 5409-85中滴定酸度的测定方法。
1.2.2.3pH测定采用酸度计于室温测定。
1.2.2.4粘度测定采用旋转粘度计,取牛乳发酵后4℃冷藏12 h的样品进行测定。
1.2.2.5乙醛含量测定乙醛在酸性条件下与亚硫酸氢钠发生加成反应生成乙醛亚硫酸氢钠,其剩余的亚硫酸氢钠被碘氧化。在碱性条件下,乙醛亚硫酸氢钠与碘定量反应,根据当量关系计算乙醛含量[16]。
1.2.2.6发酵活力测定酸度测定法:向灭菌脱脂乳中加3%发酵剂(菌体牛乳培养物),在适宜温度下(42℃)培养3.5 h,滴定其酸度。以乳酸酸度值来表示发酵活力,具体测定步骤如下:称取10 g(精确到0.001 g)已混匀的试样,置于150 mL锥形瓶中,加20 mL新煮沸冷却至室温的水,混匀,用氢氧化钠标准溶液电位滴定至pH8.3为终点;或于溶解混匀后的试样中加入2.0 mL酚酞指示液,混匀后用氢氧化钠标准溶液滴定至微红色,并在30 s内不褪色,记录消耗的氢氧化钠标准滴定溶液毫升数,代入下面公式中进行计算。结果以两次平行实验的平均值表示。
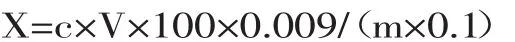
式中:X—试样的酸度,°T;c—氢氧化钠标准溶液的摩尔浓度,mol/L;V—滴定时消耗氢氧化钠标准溶液体积,mL;m—试样的质量,g;0.1—酸度理论定义氢氧化钠的摩尔浓度,mol/L;0.009—相当于乳酸(90%)的量。
1.2.3保加利亚乳杆菌及嗜热链球菌抗噬菌体菌株的培养将菌株从保存管中取出,以3%的接种量接种于脱脂乳培养基中,嗜热链球菌抗噬菌体菌株42℃培养4~6 h,保加利亚乳杆菌40℃培养10~12 h,连续活化2代。菌种活化后,嗜热链球菌抗噬菌体菌株接入M17液体培养基中,42℃培养10 h;保加利亚乳杆菌接入MRS液体培养基中,40℃培养12 h。
1.2.4保加利亚乳杆菌及嗜热链球菌抗噬菌体菌株的原生质体制备保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株培养到对数期后,收集菌体。30 mL高渗溶液洗涤2次后,15 mL高渗溶液悬浮,以溶菌酶作为去壁酶系进行原生质体的制备,酶解后再用15 mL高渗溶液悬浮得原生质体液。原生质体制备条件如表1。

表1 保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株原生质体制备条件Table 1 Protoplast preparation conditions of Lactobacillus bulgaricus and the bacteriophage-resistant mutants of Streptococcus thermophilus
1.2.5保加利亚乳杆菌的原生质体灭活保加利亚乳杆菌原生质体液于60℃水浴中恒温灭活50 min,取灭活前与灭活后的原生质体液适当稀释后涂MRS再生培养基平皿,40℃培养3~5 d后计数。

式中:A1为灭活前长出的菌落数;A2为灭活后长出的菌落数。
1.2.6保加利亚乳杆菌和嗜热链球菌抗噬菌体菌株的原生质体融合灭活的保加利亚乳杆菌原生质体液与嗜热链球菌抗噬菌体菌株原生质体液等量混合,取样分别涂M17、M17再生平皿,混合后放置5 min,2500 r/min离心10 min,收集原生质体,于沉淀中加入0.2 mL高渗溶液充分悬浮,再加入1.8 mL PEG6000溶液,混匀后分别于30、35、40、45℃处理1、2、5、10 min,2500 r/min离心10 min后悬浮于2 mL高渗溶液中,将悬浮液适当稀释后涂MRS再生平皿。M17平皿42℃,培养48 h后计数;M17、MRS再生平皿42℃,培养3~5 d后计数。

式中:D为融合子数,即融合后在MRS再生培养基上长出的菌落数;E为融合前在M17再生培养基上长出的菌落数;F为融合前在M17培养基上长出的菌落数。
1.2.7融合子的抗噬菌体性能检测
1.2.7.1融合子的噬菌体抗性检测采用双层琼脂平板法进行检测[12]:噬菌体增殖液(浓度为109PFU/mL)稀释到10-4,取稀释液0.1 mL和融合子的MRS培养液0.3 mL于20 mL灭菌小三角瓶中,再加入50℃左右的上层培养基,混匀后倒双层平板,42℃培养48 h后观察有无噬菌斑出现。
1.2.7.2融合子的抗噬菌体稳定性检测融合子抗噬菌体能力的稳定性通过传代稳定性实验来验证[12]:将获得的融合子以3%接种量在牛乳培养基中传代15代,取第5、10、15代以双层琼脂平板法检测有无噬菌斑出现;将融合子以3%接种量与噬菌体增殖液(109PFU/mL)在牛乳培养基中共同传代15代,观察牛乳的凝固情况。
1.2.7.3融合子的溶源性检测将筛选出来的融合子以3%接种量接种到MRS培养基中,1 h后加入0.4 ng/mL的丝裂霉素(mmc)诱导,继续培养,16 h后向菌液中加几滴氯仿剧烈振荡、3500 r/min离心15 min,取上清液做双层平板检查,观察有无噬菌斑出现[12]。
1.2.8融合子发酵性能的初步筛选测定将所获得的遗传稳定的融合子分别以3%的接种量接入150 mL灭菌牛乳中,42℃培养,每隔2 h测定其活菌数及pH。发酵结束后,统计融合子的凝乳时间、粘度、乙醛含量及滴定酸度,并测定融合子的发酵活力。
1.2.9融合子在高噬菌体环境下的发酵性能测定将初步鉴定生长、发酵性能优越的融合子与敏感菌株以3%的接种量接入150 mL灭菌牛乳中,向其中加入最佳感染复数(0.01)的噬菌体,每2 h测定其活菌数及pH,待发酵结束后,测定粘度、乙醛含量、凝乳时间并滴定酸度,结合感官评价挑选优良抗性菌株。感官评价方法为:10位食品研究人员品尝,并描述产品的口感、滋气味、乳清析出、组织状态等感官性状;气味在封盖打开后马上检测,乳清析出通过观察凝乳表面评定,组织状态用勺子在凝乳中轻轻搅拌均匀后观察;根据描述撰写感官风味评价。
1.2.10融合子Rh6的富集培养培养选用MRS培养基,培养过程中以Na2HPO4-柠檬酸(pH6.5)为缓冲液,42℃静置培养,每隔2 h晃动并取样测定其活菌数及pH。
1.3数据处理与统计分析
所有测定数据,采用Office Excel 2003(美国微软公司)整理、绘图,采用SPSS19.0软件(美国IBM)统计分析,数值以均值±标准差表示。
2 结果与讨论
2.1保加利亚乳杆菌及嗜热链球菌抗噬菌体菌株的培养及原生质体制备
嗜热链球菌抗噬菌体菌株培养10 h进入对数生长期,保加利亚乳杆菌培养12 h进入对数生长期,菌体量均可达109CFU/mL。按表1的原生质体制备条件,保加利亚乳杆菌的原生质体形成率为91.5%± 2.62%,嗜热链球菌抗噬菌体菌株的原生质体形成率为99.15%±0.23%。
2.2保加利亚乳杆菌的原生质体灭活
保加利亚乳杆菌原生质体液于60℃水浴中恒温灭活50 min,灭活率为98.64%±1.33%。
2.3灭活保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株原生质体融合条件的确定
灭活保加利亚乳杆菌与嗜热链球菌抗噬菌体菌株的原生质体进行融合,在高渗溶液中由PEG6000促融,融合温度及融合时间对融合率的影响如图1所示。
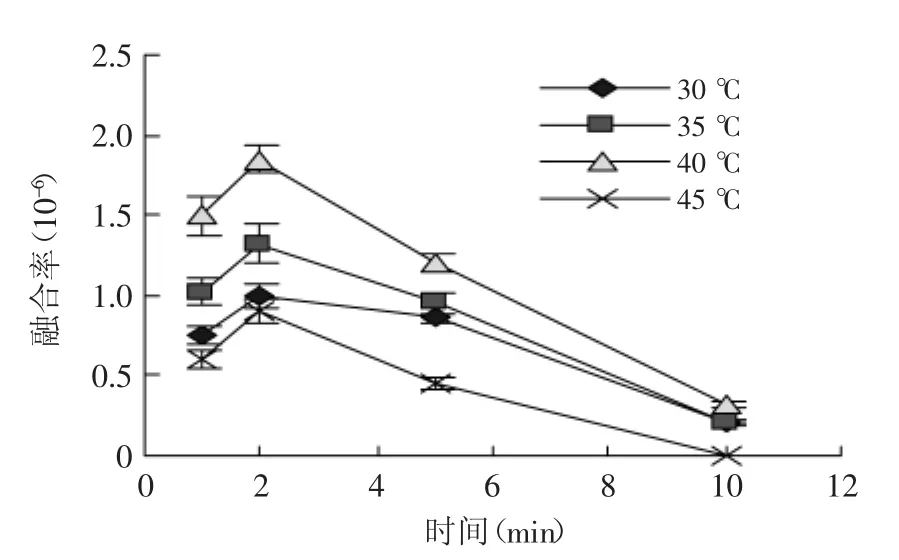
图1 融合温度和融合时间对原生质体融合率的影响Fig.1 Effect of temperature and time on protoplast fusion rate
由图1可知,原生质体融合时,时间不宜太长,这可能与融合时PEG6000会对原生质体造成一定的损伤有关[17]。最佳融合条件为:40℃,融合2 min,此条件下,融合率为1.85×10-6。
2.4融合子的检出及融合子的菌体形态
保加利亚乳杆菌可以在MRS、M17培养基上生长,而本实验用到的嗜热链球菌抗噬菌体菌株在MRS培养基上非厌氧培养时不生长,融合前保加利亚乳杆菌原生质体几乎全部灭活,因而可以认为融合后在MRS再生平皿上普通培养时生长的菌落即为融合子。将融合后再生于原生质体再生培养基上的20株菌的菌落标记并接入牛乳培养基中保存。通过凝乳时间检测挑选出3株凝乳较快的融合子,分别命名为Rh1、Rh6、Rh9,其中以Rh6凝乳最快,其菌体形态如图2所示,融合子Rh6呈椭圆形近似短杆,而出发菌株保加利亚乳杆菌为长杆状,嗜热链球菌为圆形。
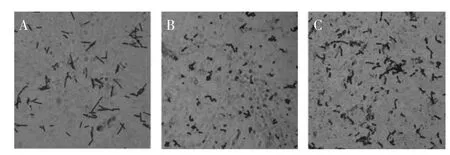
图2 融合前后菌体形态(×1000)Fig.2 Micrographs of Lactobacillus bulgaricus(A),the bacteriophage-resistant mutants of Streptococcus thermophilus(B)and their fusants(C)(×1000)
2.5融合子的抗噬菌体性能检测
对筛选到的3株性能优良的融合子进行抗噬菌体能力检测,采用双层琼脂平板法42℃培养48 h后观察均无噬菌斑出现,说明3株融合子对噬菌体具有抗性。进行溶源性检测,结果发现3株融合子所对应的双层平板上都没有噬菌斑出现,说明此3株融合子为非溶源菌。进行传代稳定性实验,结果为在第5、10、15代时都没有噬菌斑出现,且融合子以3%接种量与噬菌体增殖液(109PFU/mL)在牛乳培养基中共同传代,到第15代时仍可实现牛乳的正常凝固。说明融合子的抗噬菌体能力在遗传上是稳定的。
筛选到的融合子非厌氧培养时可以在MRS培养基上生长且具有噬菌体抗性,菌体形态有别于出发菌株保加利亚乳杆菌和嗜热链球菌抗噬菌体菌株,因此虽未作遗传物质方面的深入研究,但从融合子的生长特征、形状大小等表观特征看,确为区别于双亲的融合子。
2.6融合子发酵性能初步测定
对具有遗传稳定性的3株融合子进行发酵性能初步测定。每隔2 h在无菌的环境下取发酵样本,测定融合子的活菌数及pH,结果如图3、图4所示。
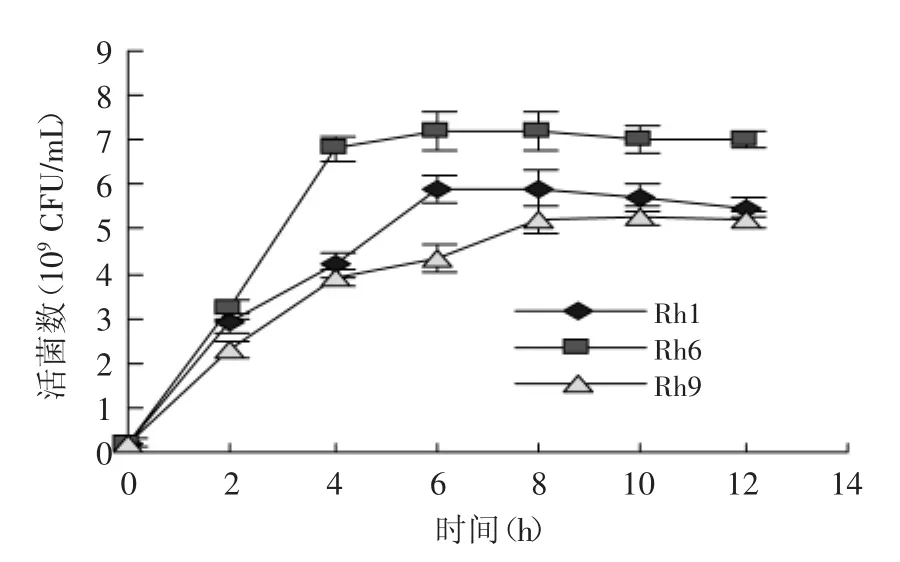
图3 融合子发酵过程活菌数Fig.3 The number of fusant in the fermentation process
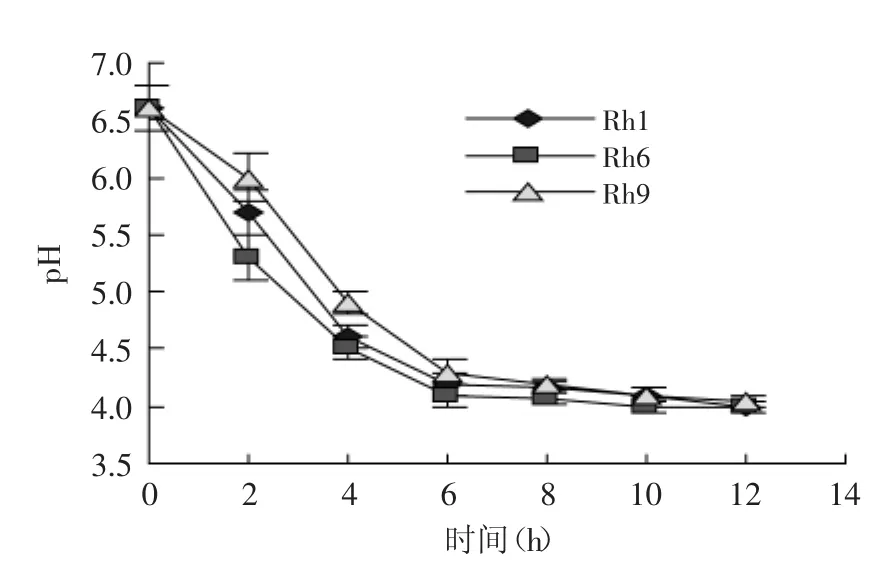
图4 融合子发酵过程pHFig.4 The pH in the fermentation process
由图3可见,Rh6生长较快,Rh1、Rh9相对较缓慢。由图4可知,Rh6的产酸能力较好。因此,初步判断Rh6较适宜发酵生产。
发酵结束后,统计融合子的凝乳时间、粘度、乙醛含量及滴定酸度,并测定融合子的发酵活力,结果如表2所示。
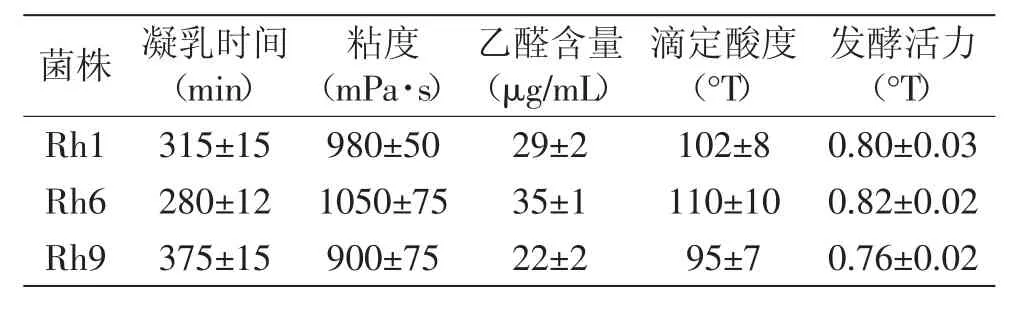
表2 融合子发酵结果(平均值±标准偏差)Table 2 The fermentation results of fusants(mean±SD)
由表2可知,Rh6的各项性能比较优越,综合以上融合子的特性及发酵能力,初步筛选出Rh6做进一步的研究,它的抗性稳定,生长能力、产酸能力较强,凝乳时间较短,粘度及乙醛含量较高,比较适合发酵生产。
2.7融合子在高浓度噬菌体条件下的发酵实验
对融合子Rh6及通常酸奶发酵时使用的保加利亚乳杆菌L.b与嗜热链球菌S.t的混合发酵剂进一步在高浓度噬菌体条件下(噬菌体浓度为109PFU/mL)进行牛乳发酵,测定各项指标。
2.7.1活菌数及pH结果每隔2 h取样涂平板测定活菌数及pH,结果如图5所示。
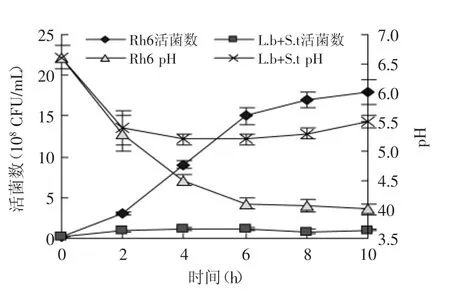
图5 高浓度噬菌体条件下活菌数及pHFig.5 The number of fusant and pH under high concentrations of phage
由图3及图5可知,Rh6在高浓度噬菌体发酵过程中,生长速度较无噬菌体时有所减慢,菌体量有所减少,但变化不是很大,4~6 h菌体量可达109CFU/mL,达到酸奶发酵标准;而保加利亚乳杆菌L.b与嗜热链球菌S.t的混合发酵剂为噬菌体的敏感菌株,在噬菌体存在的情况下明显生长缓慢,产酸能力下降,无法满足酸奶发酵的需要。
2.7.2发酵凝乳时间、滴定酸度、乙醛含量、粘度及感官风味评价结果菌株在高浓度噬菌体存在的条件下的发酵凝乳时间、滴定酸度、乙醛含量、粘度结果见表3,风味感官评价见表4。

表3 高浓度噬菌体条件下的菌株发酵情况(平均值±标准偏差)Table 3 The fermentation results of fusants and susceptible strain under high concentrations of phage(mean±SD)

表4 高浓度噬菌体发酵后酸奶的感官风味评价Table 4 Sensory flavor evaluation of yoghourt under high concentrations of phage
由表3、表4可知,保加利亚乳杆菌L.b与嗜热链球菌S.t的混合发酵剂在高浓度噬菌体条件下发酵的酸奶粘度大幅降低,凝乳时间变长,异常凝乳中检测发现有杂菌污染;Rh6整体发酵性能较好,粘度有所下降、凝乳时间有所延长,但变化不是很大,高浓度噬菌体的存在对酸奶发酵基本没有影响。
2.8融合子Rh6的富集培养
对筛选到的融合子Rh6进行富集培养,培养结果如图6。
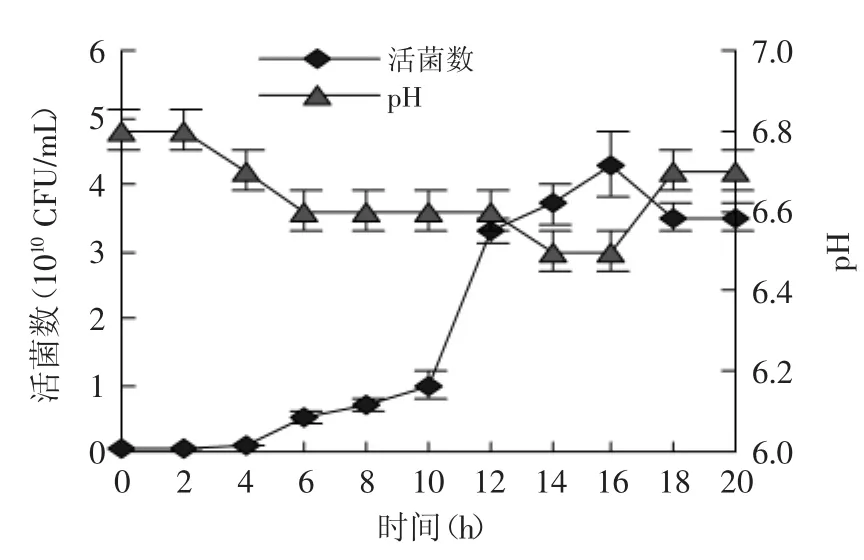
图6 融合子富集培养时的活菌数及pHFig.6 The number of bacteria and pH of fusants enrichment culture
由图6可知,培养过程中通过缓冲盐调控pH,融合子的活菌数可达1010CFU/mL,富集培养活菌数达到了制备酸奶发酵剂的要求[18],可用于工业化生产。
3 结论
通过单亲灭活、原生质体融合筛选到一株具有优良酸奶发酵特性及抗噬菌体功能的乳酸菌融合子。经培养条件优化,富集培养时菌体浓度可达1010CFU/mL,适合酸奶发酵工业。
通过对选育到的融合子的发酵特性研究表明:融合子性能优良且可实现酸奶生产单菌株发酵。融合子单独进行酸奶发酵时,产酸、产粘性物质、产香气成分等特性均可达到保加利亚乳杆菌与嗜热链球菌混合发酵的标准;在噬菌体存在的情况下,对噬菌体敏感的混合发酵剂无法完成酸奶发酵,而融合子虽然在菌体生长量方面有所下降(菌体生长量下降原因还不明确),但对酸奶发酵影响不大,完全可以完成酸奶发酵。
[1]Elizabeth W Ng,Marie Yeung,Phillip S Tong.Effects of yogurt starter cultures on the survival of Lactobacillus acidophilus[J]. International Journal of Food Microbiology,2010,145(1):169-175.
[2]任江红,秦立虎.酸奶生产中噬菌体的危害及控制[J].中国奶牛,2012(17):37-40.
[3]马成杰,吴正钧,程国军.酸奶生产中的噬菌体污染[J].江西农业学报,2007,19(7):90-91.
[4]黄海燕,陈萍.抗噬菌体乳酸菌的研究进展[J].中国酿造,2008,15(16):8-11.
[5]Mcgrath S,Sinderen D V,Fitzgerald G F.Bacteriophage derived genetic tools for use in lacticacid bacterial[J].International Dairy Journal,2002(12):3-15.
[6]Courtin P,Rul F.Interactions between Microorganisms in a Simple Ecosystem:Yogurt Bacteria as a Study Model[J].Le Lait,2004,84(1-2):125-134.
[7]Tamime A Y,Robinson R K.Yoghurt:Science and Technology[M].2nd edition.Cambridge:Woodhead Publishing Limited,1999.
[8]包维臣,陈霞,邵玉宇,等.保加利亚乳杆菌与嗜热链球菌共生机理的研究进展[J].中国乳品工业,2011,39(12):20-23.
[9]吴荣荣,马静,裴家伟,等.保加利亚乳杆菌和嗜热链球菌相互作用的研究[J].中国乳品工业,2003,31(4):9-13.
[10]王登宇,臧威,孙剑秋,等.细菌原生质体融合育种技术及其应用进展[J].中国酿造,2008,15(7):1-6.
[11]王成涛,牛天贵.构建高效降解胆固醇的融合乳酸菌的研究——融合子的鉴定及其在食品中应用[J].食品科学,2002,23(3):27-30.
[12]王慕华,潘佩平,赵玉明,等.嗜热链球菌抗噬菌体菌株的选育及其发酵特性的研究[J].食品与发酵工业,2014,40(3):92-96.
[13]杨洁彬,郭新华,张篪,等.乳酸菌—生物学基础及应用[M].北京:中国轻工业出版社,1996:78.
[14]杜连祥.工业微生物学实验技术[M].天津:天津科学技术出版社,1992:229.
[15]赵峰梅,孙文敬,王慕华,等.2-酮基-D-葡萄糖酸产生菌荧光假单胞菌K1005抗噬菌体菌株的选育[J].工业微生物,2000,30(4):45-49.
[16]刘鹏,任新宇.酸奶中乙醛含量测定方法的初步探讨[J].中国乳品工业,1992,20(2):151-154.
[17]李丽,房杰,黄洁洁,等.单亲灭活德氏乳杆菌和乳酸乳球菌原生质体融合条件优化[J].食品科学,2012,33(5):193-198.
[18]吴荣荣,张柏林.直投式酸奶发酵剂的发酵工艺及其优化[J].食品科学,2006,27(2):178-181.
Breedingoffusantbetweensingleinactivated Lactobacillusbulgaricus and bacteriophage-resistant mutant of Streptococcus thermophilus
WANG Mu-hua1,PAN Pei-ping1,ZHAO Yu-ming1,2,SU Bin-nan1,CAI Ying-hui1,LI Hai-tao1,2
(1.Shanxi Institute of Biology,Taiyuan 030006,China;2.Shanxi Veal Biological Dairy Products Co.Ltd.,Taiyuan 030006,China)
To obtain yogurt production strains with functions of phage resistant and good fermentation performance,protoplast fusion between single inactivated Lactobacillus bulgaricus and bacteriophage-resistant mutant of Streptococcus thermophilus was performed by the induction of PEG6000 and the performances of fusant were studied.Finally,three lactic acid bacteria fusants with functions of phage resistant and good fermentation performance were selected from 20 fusants that were obtained through fusion.The fusion rate reached 1.85× 10-6after 2 min of infusion at 40℃in the PEG6000.The performances of the fusant were superior at producing acid,solidifying milk,producing good smell and resisting phage,so it was applicable to yoghurt production.
single inactivation;Lactobacillus bulgaricus;bacteriophage-resistant mutant of Streptococcus thermophilus;protoplast fusion;fusant breeding
TS201.2
A
1002-0306(2015)20-0229-06
10.13386/j.issn1002-0306.2015.20.040
2015-01-20
王慕华(1975-),女,硕士,副研究员,研究方向:工业微生物、乳品发酵,E-mail:wang_muhua@126.com。
山西省农业科技攻关项目(20120311030)。

