基于苯甲酸受体的咔唑染料敏化剂的合成和光电性能
郝学良 赵金鸽 高建荣 韩 亮
(浙江工业大学化学工程学院,杭州 310032)
基于苯甲酸受体的咔唑染料敏化剂的合成和光电性能
郝学良 赵金鸽 高建荣 韩 亮*
(浙江工业大学化学工程学院,杭州 310032)
选择N-正丁基咔唑作为电子给体, 芴酮作为桥键, 苯甲酸作为受体, 通过桥键芴酮与给体和受体连接位置的改变, 设计合成了两个咔唑染料4-(6-(N-正丁基咔唑-3-基)-9-氧-9H-芴-3-基)苯甲酸(HXL-3W)和4-(7-(N-正丁基咔唑-3-基)-9-氧-9H-芴-2-基)苯甲酸(HXL-4Z). 对咔唑染料的光谱性能、电化学性能和光电转换性能进行了研究, 并运用密度泛函理论(DFT)方法对其几何结构和紫外-可见光谱进行了优化计算. 结果表明, HXL-4Z的吸收光谱呈现两个明显的π→π*跃迁吸收峰和一个较小的对应于分子内电荷转移的吸收峰, 而HXL-3W的吸收光谱则仅呈现一个π→π*跃迁吸收峰, 且摩尔吸光系数远小于HXL-4Z. 可能是HXL-3W分子结构中给体和受体距离较近, 张力较大, 导致较差的分子平面性和分子内电荷转移. 因而HXL-4Z的光吸收能力和电子注入效率较优, 从而具有较好的光电转换效率(2.03%) (短路电流(JSC) = 3.88 mAcm-2, 开路电压(VOC) = 700 mV, 填充因子(FF) = 0.75).
咔唑; 染料敏化剂; 苯甲酸受体; 合成; 光电性能
1 引 言
太阳能作为替代化石燃料的新能源,具有清洁无污染、可再生且用之不竭等特点. 将太阳能转换为电能是开发利用太阳能的重要途径之一,因而太阳能电池的研发和推广备受关注. 在各类太阳能电池中,染料敏化太阳能电池(DSSCs)由于具有原材料丰富易得、工艺简单,可弱光发电等优点,应用前景广阔. 染料敏化太阳能电池主要由导电玻璃、TiO2多孔纳米膜、染料敏化剂、电解质溶液以及Pt对电极组成,其中染料敏化剂的光谱响应范围以及量子产率是DSSCs光伏性能高低的重要影响因素.1-4
染料敏化剂的研究主要分两类,一类为有机金属配合物染料,典型结构为功能性多吡啶钌化合物,其光电转换效率高,但摩尔吸光系数低,且制备工艺复杂;5第二类为非金属有机染料,具有较高的摩尔吸光系数、宽的吸收光谱和可通过结构修饰调变产生优良电化学性能等优点,是近年来研究的热点. 经典的非金属染料敏化剂通常为“给体-π桥-受体(D-π-A)”结构,富电子的给体基团通过π桥将电子转移到受体,受体则通过羧基、磷酸基等特定官能团与TiO2进行化学吸附,提供电子转移通道,从而使光生电子顺利注入TiO2半导体中.6给体在很大程度上决定了染料敏化剂的光谱性质,根据给体的不同类型,目前已有咔唑型、7,8香豆素型、9,10吲哚啉型、11,12三芳胺型13,14等非金属染料敏化剂得以设计和开发. 咔唑及其衍生物具有强发射和吸收性质、良好的空穴传输能力以及宽带隙等优点,被应用于电致发光、光致折变和有机发光二极管(OLED)等材料.15-17咔唑类染料分子由于在可见光区域内响应度高、在太阳光照射下稳定性好,使得其作为一类发展前景良好的染料敏化剂而倍受关注. 本课题组18利用苯并噻二唑作为额外受体,设计合成了D-A-π-A型咔唑类染料敏化剂分子,光电转换效率最高达到5.40%; Han等19以咔唑为给体,引入环状π桥,获得了9.20%的光电转换效率. 另外,咔唑也被用作额外给体,与三芳胺或香豆素给体相结合,设计合成双给体型敏化剂,获得了较高的光电转换效率.20,21
与给体比较,受体相对研究较少. 最常用的受体为氰乙酸,其中的羧酸基团能与TiO2进行化学键连,使染料分子的最低未占据分子轨道(LUMO)与TiO2中钛的3d轨道发生电子云重叠形成电子转移通道,从而使光生电子顺利注入TiO2导带中. 因而很多高效的非金属染料敏化剂均采用氰乙酸为受体.22,23但氰乙酸引入染料敏化剂分子后,产生顺反两种异构体,顺式异构体中给体靠近TiO2导带,使氧化态染料与光生电子复合几率增大,将削弱开路电压.24相比较而言,另一苯甲酸受体的引入,不仅能进一步扩大染料敏化剂的共轭体系,而且羧酸官能团直接与共轭π系统相连,更有利于电子注入TiO2导带中.12012年,Zakkeruddin等25合成了一系列以苯甲酸为受体的三芳胺类染料敏化剂,并进一步在苯环上引入氰基,光电转换效率由2.87%提高到4.50%. 同样以三芳胺为给体,苯甲酸为受体,Wang等26引入噻吩并环戊二烯-苯并噻二唑为桥键,光电转换效率最高达到11.5%.
本文以N-丁基咔唑为电子给体,芴酮为π桥,苯甲酸为受体,设计合成了两个咔唑类染料,测定了光谱性能、电化学性能和光电转换性能,具体合成路线如示意图1所示.
2 实验部分
2.1 主要试剂与仪器
咔唑、N-溴代丁二酰亚胺、溴代正丁烷、正丁基锂、硼酸三甲酯、2,7-二溴-9-芴酮、3,6-二溴芴酮)、4-羧基苯硼酸、四三苯基膦钯等均为分析纯,上海阿拉丁生物科技股份有限公司. 数字显示显微熔点测定仪(X-4型,巩义市予华仪器有限责任公司); Bruker-500MHz型核磁共振谱仪(AvanceIII型,Bruker,瑞士); SHIMADZU紫外-可见分光光度计(UV-2500型,岛津公司,日本); Hitachi spectrofluorometer三维荧光光谱仪(FL-2500型,日立公司,日本); Thermo Finnigan LCQ Series,Agilent 6210 Series Time-of-Flight 质谱(MS)仪 (ESI/APCI)(LCQ DECA XP PLUS型,ThermoFisher/Finnigan,美国).
2.2 咔唑类染料敏化剂的合成
2.2.1 3-溴-6-(9-正丁基-9H-咔唑-3-基)-9H-芴-9-酮和2-溴-7-(9-正丁基-9H-咔唑-3-基)-9H-芴-9-酮的合成
溴代丁基咔唑(1.96 g,6.40 mmol)溶于四氧呋喃(THF,30 mL),-78 °C N2保护下搅拌,缓慢注入正丁基锂(3.0 mL,7.2 mmol,2.5 molL-1)反应1 h,之后加入硼酸三甲酯(2.24 mL,8.40 mmol). 升至室温搅拌20 h. 加入二溴芴酮(7.04 mmol,2.38 g),四三苯基膦钯(0.74 g,0.67 mmol)和碳酸钾水溶液(2 molL-1,13 mL),加热回流12 h. 冷却,加水稀释,乙酸乙酯萃取3次,合并有机层,无水Na2SO4干燥. 柱层析(Ia,VPE: VCH2Cl2= 1 : 1; Ib,VPE: VCH2Cl2= 5 : 1)分离得产物I.

示意图1 基于苯甲酸受体的咔唑染料的合成Scheme 1 Syntheses of carbazole dyes based on benzoic acid acceptor
Ia: 深红色固体; 收率 87.5%; m.p. 193-195 °C;1H NMR (CDCl3,500 MHz) δ: 8.42 (d,J = 1.5 Hz,1H,ArH),8.30 (dd,J = 4.7,3.1 Hz,2H,ArH),8.22(d,J = 7.2 Hz,2H,ArH),8.07 (d,J = 8.3 Hz,1H,ArH),7.83 (dd,J = 8.3,1.5 Hz,2H,ArH),7.63 (dd,J = 8.3,1.5 Hz,1H,ArH),7.54 (dd,J = 7.9,5.5 Hz,2H,ArH),7.48 (d,J = 8.1 Hz,1H,ArH),7.31 (t,J = 7.4 Hz,1H,ArH),4.38 (t,J = 7.2 Hz,2H,CH2CH2CH2CH3),1.95-1.89 (m,2H,CH2CH2CH2CH3),1.49-1.43 (m,2H,CH2CH2CH2CH3),1.00 (d,J = 7.4 Hz,3H,CH2CH2CH2CH3); C29H22BrNO的高分辨电喷雾质谱(HR-ESI-MS)分析结果: 实测值,480.0960 [M + 1]+,482.0919 [M + 1]+; 计算值,479.0885.
Ib: 深橙色固体; 收率 85.0%. m.p. 196-198 °C;1H NMR (CDCl3,500 MHz) δ: 8.34 (d,J = 1.6 Hz,1H,ArH),8.16 (d,J = 7.7 Hz,1H,ArH),8.03 (d,J = 1.5 Hz,1H,ArH),7.86 (dd,J = 7.7,1.8 Hz,1H,ArH),7.79 (d,J = 1.8 Hz,1H,ArH),7.73 (dd,J = 8.5,1.8 Hz,1H,ArH),7.63 (dd,J = 7.9,1.9 Hz,1H,ArH),7.59 (d,J = 7.7 Hz,1H,ArH),7.51 (dd,J = 7.5,1.1 Hz,1H,ArH),7.48 (d,J = 8.5 Hz,1H,ArH),7.45 (d,J = 8.2 Hz,1H,ArH),7.41 (d,J = 7.41 Hz,1H,ArH),7.31-7.28 (m,1H,ArH),4.35 (t,J = 7.2 Hz,2H,CH2CH2CH2CH3),1.94-1.86 (m,2H,CH2CH2CH2CH3),1.48-1.40 (m,2H,CH2CH2CH2CH3),0.98 (t,J = 7.4 Hz,3H,CH2CH2CH2CH3); C29H22BrNO的HR-ESIMS分析结果: 实测值,480.0945 [M + 1]+,482.0922[M + 1]+; 计算值,479.0885.
2.2.2 4-(6-(9-正丁基-9H-咔唑-3-基)-9-氧-9H-芴-3基))苯甲酸和4-(7-(9-正丁基-9H-咔唑-3-基)-9-氧-9H-芴-2基))苯甲酸的合成
化合物I (0.6 mmol,0.3 g),4-羧基苯硼酸(0.72 mmol,0.12 g)和四三苯基膦钯(0.06 mmol,0.07 g)溶于四氢呋喃(10 mL)中,N2保护下加入碳酸钾溶液(2 molL-1,1.2 mL),回流24 h. 冷至室温,加水稀释后,CH2Cl2萃取3次,合并有机层,无水Na2SO4干燥. 柱层析(VCH2Cl2: VCH3OH: VHAc= 400 : 2 : 1)分离得到产物.
HXL-3W: 深红色固体; 收率 76.0%. m.p. 316-318 °C;1H NMR (DMSO,500 MHz) δ: 13.13 (s,1H,COOH),8.87-8.80 (m,3H,ArH),8.33 (d,J = 7.7 Hz,1H,ArH),8.18 (dd,J = 8.1,3.9 Hz,2H,ArH),8.14-8.10 (m,5H,ArH),8.02 (dd,J = 8.1,1.4 Hz,1H,ArH),7.93 (dd,J = 8.1,1.2 Hz,1H,ArH),7.79 (dd,J = 8.3,2.6 Hz,1H,ArH),7.67 (d,J = 7.6 Hz,1H,ArH),7.51 (t,J = 8.5 Hz,1H,ArH),7.27 (t,J = 7.4 Hz,1H,ArH),4.48 (t,J = 6.9 Hz,2H,CH2CH2CH2CH3),1.85-1.77 (m,2H,CH2CH2CH2CH3),1.38-1.27 (m,2H,CH2CH2CH2CH3),0.90 (t,J = 7.2 Hz,3H,CH2CH2CH2CH3); C36H27NO3的HR-ESI-MS分析结果:实测值,522.2088 [M]+; 计算值,522.2064.
HXL-4Z: 橙红色固体; 收率 91.0%. m.p. 320-322 °C;1H NMR (DMSO,500 MHz) δ: 13.06 (s,1H,COOH),8.66 (d,J = 1.7 Hz,1H,ArH),8.33 (d,J = 7.7 Hz,1H,ArH),8.10 (dd,J = 7.8,1.8 Hz,1H,ArH),8.08-8.04 (m,4H,ArH),8.00-7.97 (m,3H,ArH),7.93 (d,J = 8.5 Hz,2H,ArH),7.89 (dd,J = 8.6,1.8 Hz,1H,ArH),7.72 (d,J = 8.6 Hz,1H,ArH),7.64 (d,J = 8.3 Hz,1H,ArH),7.49 (t,1H,J = 8.5 Hz,2H,ArH),7.24 (t,1H,J = 8.5 Hz,2H,ArH),4.45 (t,J = 7.0 Hz,2H,CH2CH2CH2CH3),1.83-1.76 (m,2H,CH2CH2CH2CH3),1.37-1.29 (m,2H,CH2CH2CH2CH3),0.90 (t,J = 7.4 Hz,3H,CH2CH2CH2CH3); C36H27NO3的HR-ESI-MS分析结果:实测值,522.2045 [M]+; 计算值,522.2064.
2.3 染料敏化剂电化学性能测试
染料溶液的循环伏安曲线通过IviumStat电化学工作站(IviumStat,荷兰)进行测定,采用三电极体系,玻碳电极为工作电极,铂片电极为辅助电极,Ag/ AgNO3电极为参比电极; 电解液为0.1 molL-1四丁基高氯酸铵(TBAP)的乙腈溶液.
2.4 染料敏化纳米电极的制备及电池器件的组装
利用丝网印刷制备的双层TiO2纳米粒子膜作为光电极: 首先在掺氟SnO2(FTO)导电玻璃上印一层12 μm厚的20 nm的TiO2粒子(OPV-TiO2,营口奥匹维特新能源科技有限公司),450 °C下马弗炉内煅烧 30 min. 在浸染料之前将烧好的膜浸入 40 mmolL-1的TiCl4水溶液中70 °C预处理30 min,然后分别用水和乙醇冲洗,电吹风吹干. 经马弗炉450 °C下再次煅烧30 min后,冷却至80 °C后浸入3 × 10-4molL-1染料的N,N-二甲基甲酰胺(DMF)溶液室温24 h敏化. 对电极的制备: 采用丝网印刷方法,将一定浓度的H2PtCl6溶液印刷在FTO导电玻璃上,然后在400 °C马弗炉中烧结 20 min. 吸附染料的 TiO2电极和铂对电极组装成三明治结构开放电池,所用电解液为OPV-AN-I型(营口奥匹维特新能源科技有限公司).
2.5 电池器件光电性能的测试
单色光光电转换效率(IPCE)使用PEC-S20 IPCE测试系统(Peccell,日本)测定. 光电压-电流特性曲线的测试是利用Keithley数字源表(Keithley 2601,美国)采集数据,白光光源为AM 1.5G太阳模拟器(Peccell-L15,日本),电池的有效面积为0.159 cm2.
3 结果与讨论
3.1 咔唑染料的合成
选择N-正丁基咔唑作为电子给体,芴酮作为桥键,苯甲酸作为受体,设计了两个咔唑染料. 通过桥键芴酮与给体和受体连接位置的改变,合成了4-(6-(N-正丁基咔唑-3-基)-9-氧-9H-芴-3-基)苯甲酸(HXL-3W)和4-(7-(N-正丁基咔唑-3-基)-9-氧-9H-芴-2-基)苯甲酸(HXL-4Z).
N-正丁基-3-溴代咔唑在正丁基锂作用下用硼酸三甲酯转变为N-正丁基咔唑硼酸酯,与相应的二溴芴酮进行Suzuki偶联,得到中间体I. 中间体I与4-羧基苯硼酸再一次发生Suzuki偶联得到目标产物.该类染料合成路线短,每步收率较高.
3.2 咔唑染料的光谱性质
图1是咔唑类染料在DMF溶液以及TiO2电极上的紫外-可见吸收光谱,反映了染料在溶液中以及负载到TiO2膜上对太阳光的吸收能力. 表1列出了咔唑类染料的光学性质参数. DMF溶液中,HXL-4Z的紫外光谱呈现两个明显的最大吸收峰,出现在299 nm处的峰摩尔吸光系数为8.3 × 104Lmol-1cm-1,出现在346 nm处的摩尔吸光系数为4.5 × 104Lmol-1cm-1,均为π→π*电子跃迁产生的吸收峰. 值得注意的是,在466 nm左右,还有一个较小的吸收峰,摩尔吸光系数较低,源于分子内电荷转移(ICT)吸收. 而HXL-3W的紫外光谱图只观察到了一个吸收峰,出现在288 nm,对应于分子的π→π*电子跃迁,其摩尔吸光系数也较HXL-4Z小. 可能是由于两者芴酮桥键连接方式不一样,HXL-3W中电子给体和受体之间距离近,张力大,整个分子扭成蝴蝶构象,导致分子平面性差,不利于分子内电荷转移,因而其紫外光谱中观察不到ICT吸收峰.
负载到TiO2上后,染料会发生聚集,形成J-聚集和H-聚集,使得紫外吸收光谱变宽并伴随着最大吸收波长的变化. J-聚集是一维头尾相邻排列结构的分子集合,其形成主要由于分子间的氢键、静电引力作用和疏水作用所致,导致吸收光谱红移; H-聚集则是一维面面相对结构的分子集合,主要由分子间较强的π-π堆积作用造成,导致吸收光谱蓝移. 与溶液中的紫外光谱相比,HXL-3W和HXL-4Z在TiO2膜上的紫外吸收光谱明显变宽,最大吸收波长发生红移,推测形成了J-聚集体. HXL-3W吸收光谱范围增大到650 nm,最大吸收峰移至393 nm 处;HXL-4Z吸收光谱范围增大到600 nm,呈现两个最大吸收峰. 一个出现在375 nm处,为原液体紫外光谱中346 nm处吸收峰红移所致; 另一个则出现在477 nm处,此峰对应于原液体紫外吸收光谱中466 nm处吸收峰,可以看出由于形成聚集体,导致此峰不仅发生了红移,其吸收强度也明显增大.
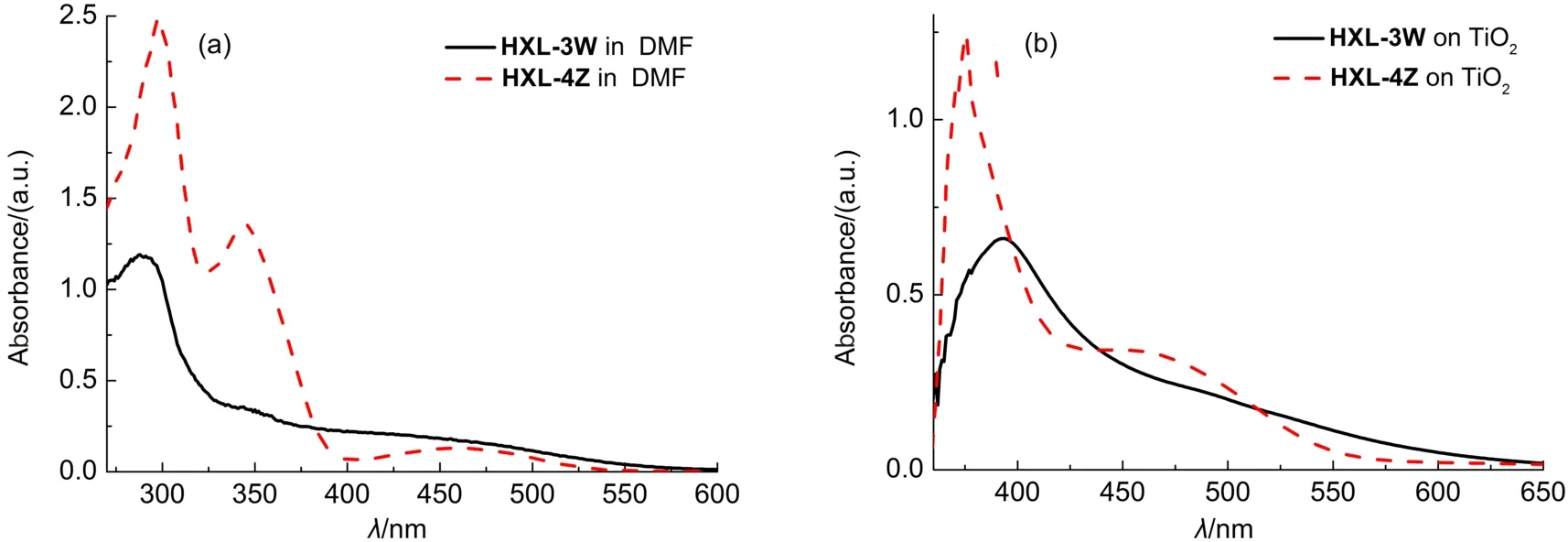
图1 咔唑类染料的紫外-可见吸收光谱Fig.1 UV-Vis absorption spectra of carbazole dyes

表1 咔唑类染料的光学性质Table 1 Optical properties of carbazole dyes
3.3 咔唑染料的电化学性质
在DSSC中,染料敏化剂吸收太阳光,激发后产生的电子注入到TiO2半导体导带中,流入外电路形成电流; 失去电子后形成的氧化态染料从电解质接受电子还原再生,完成光电化学反应循环. 因此要求染料敏化剂除了具有优良的吸光性能外,还要具备合适的氧化还原电势,保证电子的传递和染料分子的还原再生. 染料敏化剂的LUMO能量(ELUMO)高于半导体的导带(CB)能级(ECB),激发态电子才能顺利注入TiO2导带中; 其最高占据分子轨道(HOMO)能量(EHOMO)低于电解质的氧化还原电位,氧化态染料才能从电解质接受电子还原再生. 对HXL-3W和HXL-4Z在溶液中的循环伏安曲线进行了测试,HOMO能级由循环伏安曲线的第一氧化还原电位(Eox)得到. 测试时,以Ag/Ag+作为参比电极,获得氧化还原电位(EP),将其换算为相对于标准氢电极(NHE)的电位后,再转换为真空能级,即Eox= -(EP+ 0.197 eV + 4.4 eV) (Ag/Ag+作为参比电极相对于标准氢电极电位为0.197 eV,标准氢电极相对于真空电极为-4.4 eV). LUMO能级由ELUMO= Eox- E0-0计算得到,其中分子跃迁能(E0-0)由E0-0= 1240/λint求得,λint为归一化的染料吸收光谱和荧光发射光谱相交处的波长,数据列于表2. 从表2中可以看出,HXL-3W和HXL-4Z的LUMO能级分别为-2.10和-2.22 eV,高于TiO2的导带能级(-0.5 V (vs NHE)),因而其激发态染料能顺利将电子注入到TiO2导带中; HXL-3W和HXL-4Z的HOMO能级分别为-5.49和-5.24 eV,低于的能级(0.4 V (vs NHE)),表明氧化态染料分子可被电解质(I-)还原再生.
3.4 咔唑染料的光电转换性能
采集300-800 nm单色光辐照度以及电池的电流I,得到单色光转化效率(IPCE),见图2中插图. IPCE与光捕获效率、电子注入量子效率和注入电子在纳米晶膜与导电玻璃的后接触面上的收集效率三部分相关. 由图2可知,HXL-4Z的IPCE曲线主要分布于300-650 nm 之间,与其在TiO2电极上的吸收光谱相似,于366和488 nm处各有一个IPCE峰值,分别为33%和27%. HXL-3W的IPCE曲线则仅分布于300-400 nm之间,最大值仅为18%,其IPCE响应范围以及峰值均远不如HXL-4Z. 由于无论在溶液中还是在TiO2薄膜上HXL-3W的吸收光谱均延伸到400 nm以上,而IPCE曲线却在400 nm以上无响应,推测原因可能是其尽管在400 nm以上具有一定的光捕获率,但其分子平面性差,使得分子内电子传输弱,导致电子注入量子效率低,表现为400 nm以上无IPCE响应.

表2 咔唑染料的电化学性质Table 2 Electrochemical properties of carbazole dyes

图2 咔唑染料的电流密度-电压(J-V)曲线和光电转换效率(IPCE)曲线(插图)Fig.2 Current density-potential (J-V) curve and incident photo-to-current conversion efficient (IPCE) curve (inset)of carbazole dyes
3.5 密度泛函理论研究
为了进一步分析咔唑染料的吸收光谱特征,采用密度泛函理论(DFT),在B3LYP/6-31G(d)水平上对分子的几何构型进行优化; 同时采用含时密度泛函理论(TD-DFT)计算了染料的紫外-可见吸收光谱.

表3 咔唑类染料的光学性质Table 3 Optical properties of carbazole dyes
图3是N-正丁基咔唑染料分子基态的空间几何结构. 由图3可以看出,HXL-3W分子结构中芴酮桥与咔唑给体以及苯甲酸受体之间均存在比较大的二面角,分别为56°和37°,使得整个分子成扭曲状态. 可能由于在HXL-3W中,咔唑给体和苯甲酸受体分别位于芴的3位和6位,距离比较近,如处于共平面构型两者张力大,因而整个分子扭转成蝴蝶构象. HXL-3W由于平面性差,导致分子共轭性差,仅在288 nm处出现最大吸收峰,且摩尔吸光系数较小.而HXL-4Z分子结构中咔唑给体、芴酮桥和苯甲酸受体共平面,整个分子共轭较好,因而其最大吸收波长较HXL-3W长.

图3 咔唑染料的优化构型(侧视图)Fig.3 Optimized geometries (side view) of carbazole dyes
图4列出了HXL-3W和HXL-4Z的前线轨道的三维透视图. HXL-3W和HXL-4Z的前线轨道类似,给体对HOMO电子云分布的贡献最大,而LUMO电子云主要分布在芴酮桥和苯甲酸受体上. 由于HOMO和LUMO的跃迁不是禁阻的,因此在400 nm以上有弱的紫外-可见吸收.
图5是用B3LYP/6-31G(d)优化计算的咔唑染料分子前线轨道能级图,相关数据列于表2,并与实验值相比较. 从图5中可以看出,两种染料分子的HOMO能级分别为-5.44和-5.41 eV,低于电解质的能级(-4.9 eV),而染料分子的LUMO能级分别为-2.36和-2.48 eV,高于TiO2的导带能级(-4.0 eV),从而可见染料的激发态电子可以有效注入到光阳极,同时氧化态染料可从还原态电解质获得电子而再生.
为了更深入地了解构效关系,在基态几何结构优化的基础上进一步对HXL-3W和HXL-4Z的紫外-可见光谱吸收进行了含时密度泛函理论(TDDFT)计算,如图6所示. HXL-3W和HXL-4Z在400 nm以上有弱吸收,分别为532.8和608.4 nm,这和HOMO-LUMO能量差的分析结果是一致的. HXL-3W的吸收光谱主要分布在250-400 nm,最大吸收峰在313 nm处,对应为HOMO - 2至LUMO + 1的电子跃迁. HXL-4Z的吸收光谱主要分布在250-450 nm,呈现两个较强的吸收(311和384 nm),其中最强吸收峰在311 nm处,对应为HOMO - 2至LUMO + 1的电子跃迁; 而384 nm处的吸收峰则主要对应电子从HOMO到LUMO + 1的跃迁. 总之,TD-DFT计算得到的紫外光谱图与实测光谱图吻合较好.
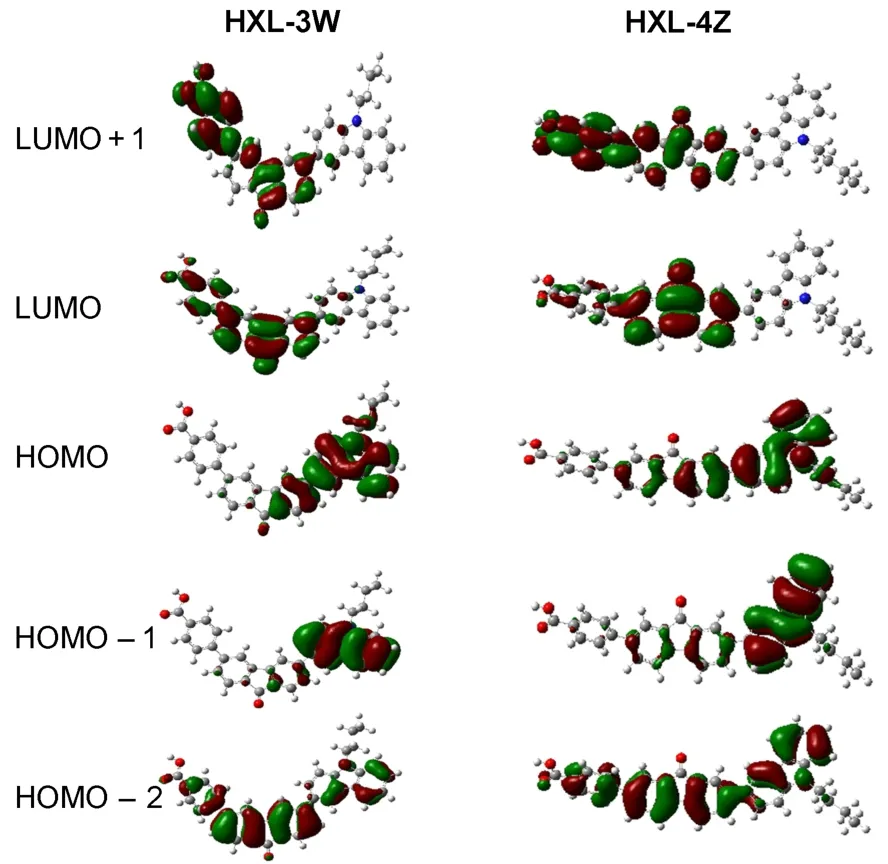
图4 咔唑染料分子的前线轨道(HOMO,LUMO)Fig.4 Frontier molecular orbitals (HOMO,LUMO) of carbazole dyes
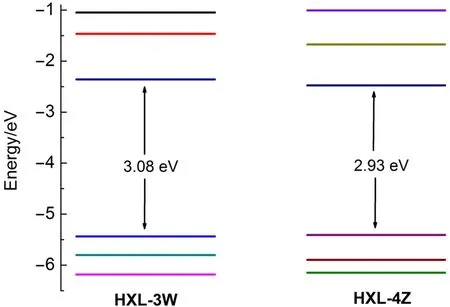
图5 用B3LYP/6-31G(d)优化计算的咔唑染料分子前线轨道能级Fig.5 Optimized energy level of the frontier molecular orbitals of carbazole dyes calculated at B3LYP/6-31G(d)
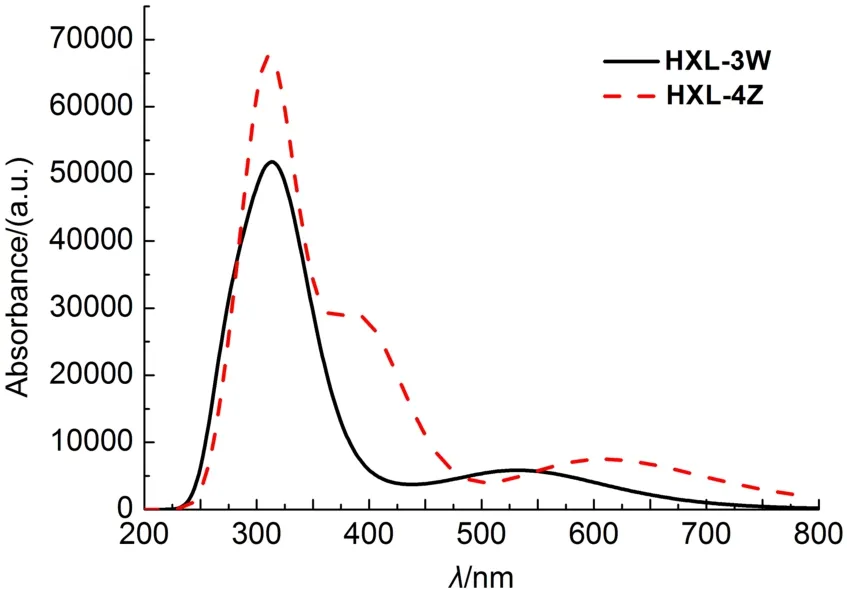
图6 含时密度泛函理论(TD-DFT)计算得到的咔唑染料的紫外-可见光吸收光谱Fig.6 UV-Vis absorption spectra of carbazole dyes by time-dependent density functional theory (TD-DFT)calculation
4 结 论
以N-正丁基咔唑为给体,芴酮为桥键,苯甲酸为受体,通过改变桥键与给体及受体的连接方式,设计合成了两个咔唑染料HXL-3W和HXL-4Z. 在HXL-3W分子中给体和受体距离较近,导致两者张力较大,扭曲成蝴蝶构象,从而使得分子平面性差,紫外吸收波长短,吸收强度弱. 而HXL-4Z分子中给体和受体距离远,分子平面性好,因而光吸收性能较佳,其光电转换性能为2.03%. 尽管如此,以苯甲酸为受体的HXL-4Z的光电转换效率偏低,主要是由于其光吸收能力仍较弱,导致单色光电转换效率偏低,短路电流不高. 苯甲酸受体与氰乙酸受体相比,虽共轭体系增大,但吸电子能力降低,如能在苯环上引入吸电子基团,有望加强分子内电荷转移,提高光电转换效率. 因而在我们进一步对染料分子结构优化工作中,将考虑在苯环上引入类似硝基或氰基等强吸电子基团,帮助分子内电荷转移,改善染料光吸收能力.
(1)Mishra,A.; Fischer,M. K. R.; Bäuerle,P. Angew. Chem. Int. Edit. 2009,48,2474. doi: 10.1002/anie.v48:14
(2)Hou,L. M.; Wen,Z.; Li,Y. X.; Hu,H. Y.; Kan,Y. H.; Su,Z. M. Acta Phys. -Chim. Sin. 2015,31,1504. [候丽梅,温 智,李银祥,胡华友,阚玉和,苏忠民. 物理化学学报,2015,31,1504.]doi: 10.3866/PKU.WHXB201505211
(3)Li,H. X.; Zuo,G. F.; Li,Z. F.; Wang,X. F.; Zheng,R. H. Acta Phys. -Chim. Sin. 2015,31,866. [李会学,左国防,李志峰,王晓峰,郑仁慧. 物理化学学报,2015,31,866.] doi: 10.3866/PKU.WHXB201503254
(4)Zhan,W. S.; Li,R.; Pan,S.; Guo,Y. N.; Zhang,Y. Acta Phys. -Chim. Sin. 2013,29,255. [詹卫伸,李 睿,潘 石,郭英楠,张 毅. 物理化学学报,2013,29,255.] doi: 10.3866/PKU.WHXB201211221
(5)Polo,A. S.; Itokazu,M. K.; Iha,N. Y. M. Coordin. Chem. Rev. 2004,248,1343. doi: 10.1016/j.ccr.2004.04.013
(6)Zhang,S. F.; Yang,X. D.; Numata,Y. H.; Han,L. Y. Energy Environ. Sci. 2013,6,1443. doi: 10.1039/c3ee24453a
(7)Gupta,K. S. V.; Suresh,T.; Singh,S. P.; Islam,A.; Han,L. Y.;Chandrasekharam,M. Org. Electron. 2014,15,266. doi: 10.1016/j.orgel.2013.11.020
(8)Li,T.; Cui,Y. H.; Zhong,C. J.; Ye,Q.; Han,L. J. Photochem. Photobiol. A: Chem. 2015,303,91.
(9)Seo,K. D.; Choi,I. T.; Park,Y. G.; Kang,S.; Lee,J. Y.; Kim,H. K. Dyes Pigm. 2012,94,469. doi: 10.1016/j.dyepig.2012.02.015
(10)Han,L.; Wu,H. B.; Cui,Y. H.; Zu,X. Y.; Ye,Q.; Gao,J. R. J. Photochem. Photobiol. A: Chem. 2014,290,54.
(11)Wang,L.; Liang,M.; Zhang,Y.; Cheng,F.; Wang,X.; Sun,Z.;Xue,S. Dyes Pigm. 2014,101,270. doi: 10.1016/j.dyepig.2013.10.016
(12)Liang,G. J.; Zhong,Z. C.; Chen,M. H.; Xu,J.; Xu,W. L.; He,P.; Hou,Q. F.; Li,Z. F. Acta Phys. -Chim. Sin. 2012,28,1885.[梁桂杰,钟志成,陈美华,许 杰,徐卫林,和 平,候秋飞,李在房. 物理化学学报,2012,28,1885.] doi: 10.3866/PKU.WHXB201205301
(13)Liang,M.; Chen,J. Chem. Soc. Rev. 2013,42,3453. doi: 10.1039/c3cs35372a
(14)Zhong,C. J.; Gao,J. R.; Cui,Y. H.; Li,T.; Han,L. J. Power Sources 2015,273,831.
(15)Tang,J.; Hua,J. L.; Wu,W. J.; Li,J.; Jin,Z. G.; Long,Y. T.;Tian,H. Energy Environ. Sci. 2010,3,1736. doi: 10.1039/c0ee00008f
(16)Li,P. P.; Chen,Y.; Zhu,J.; Feng,M.; Zhuang,X.; Lin,Y.; Zhan,H. Chem. -Eur. J. 2010,17,780.
(17)Duan,T. N.; Fan,K.; Zhong,C.; Peng,T. Y.; Qin,J. G.; Chen,X. G. RSC Adv. 2012,2,7081. doi: 10.1039/c2ra20777j
(18)Han,L.; Zu,X. Y.; Cui,Y. H.; Wu,H. B.; Ye,Q.; Gao,J. R. Org. Electron. 2014,15,1536. doi: 10.1016/j.orgel.2014.04.016
(19)Liu,J.; Yang,X. D.; IsIam,A.; Numata,Y. H.; Zhang,S. F.;Salim,N. T.; Chen,H.; Han,L. Y. J. Mater. Chem. A 2013,1,10889. doi: 10.1039/c3ta12368e
(20)Liu,B.; Wang,R.; Mi,W. J.; Li,X. Y.; Yu,H. T. J. Mater. Chem. 2012,22,15379. doi: 10.1039/c2jm32333h
(21)Venkateswararao,A.; Justin Thomas,K. R.; Lee,C. P.; Ho,K. C. Tetrahedron Lett. 2013,54,3985. doi: 10.1016/j.tetlet.2013.05.069
(22)Wang,X. Z.; Yang,J.; Yu,H.; Li,F.; Fan,L.; Sun,W.; Liu,Y.;Koh,Z. Y.; Pan,J.; Yim,W. L.; Yan,L.; Wang,Q. Chem. Commun. 2014,50,3965. doi: 10.1039/c4cc00577e
(23)Liu,B.; Wang,B.; Wang,R.; Gao,L.; Huo,S.; Liu,Q.; Li,X.;Zhu,W. J. Mater. Chem. A 2014,2,804. doi: 10.1039/C3TA13993J
(24)Yu,H. H. Synthesis and Properties of Novel Organic Sensitizers Based on Indoline for Dye-Sensitized Solar Cells. Master Dissertation,East China University of Science and Technology,Shanghai,2012. [于晖晖. 新型含吲哚啉纯有机太阳能电池敏化染料的合成与性能研究[D]. 上海: 华东理工大学,2012.]
(25)Katono,M.; Bessho,T.; Wielopolski,M.; Marszalek,M.; Moser,J. E.; Baker-Humphry,R.; Zakkeruddin,S. M.; Grätzel,M. J. Phys. Chem. C 2012,116,16876. doi: 10.1021/jp304490a
(26)Zhang,M.; Wang,Y.; Xu,M.; Ma,W.; Li,R.; Wang,P. Energy Environ. Sci. 2013,6,2944. doi: 10.1039/c3ee42331j
Synthesis and Photoelectric Properties of Carbazole Sensitizing Dyes Based on a Benzoic Acid Acceptor
HAO Xue-Liang ZHAO Jin-Ge GAO Jian-Rong HAN Liang*
(College of Chemical Engineering,Zhejiang University of Technology,Hangzhou 310032,P. R. China)
4-(6-(N-butylcarbazole-3-yl)-9-oxo-9H-fluoren-3-yl)benzoic acid (HXL-3W) and 4-(7-(N-butylcarbazole-3-yl)-9-oxo-9H-fluoren-2-yl)benzoic acid (HXL-4Z), were designed and synthesized through the linking position variation of the fluorenone π-bridge with the N-butylcarbazole donor and a benzoic acid acceptor. The spectra, electrochemistry and photoelectric conversion properties of these carbazole dyes were investigated and their geometric structure and UV-Vis spectra were optimized and calculated using the density functional theory (DFT) method. The results show two distinct absorption peaks, ascribed to the π→π* transition, along with a small peak corresponding to intramolecular charge transfer in the absorption spectrum of HXL-4Z. However, only one π→π* transition absorption peak is found in the spectrum of HXL-3W and its molar extinction coefficient is far smaller than that of HXL-4Z. The reason for this may be a closer distance between the donor and acceptor of HXL-3W leading to a large tension, causing inferior molecular planarity and intramolecular charge transfer. Therefore, HXL-4Z which possesses superior light absorptivity and electron injection efficiency, shows an enhanced photoelectric conversion efficiency of 2.03% (short-circuit photocurrent density (Jsc) = 3.88 mAcm-2, open-circuit photovoltage (Voc) = 700 mV, fill factor (FF) = 0.75).
Carbazole; Sensitizing dye; Benzoic acid acceptor; Synthesis; Photoelectric property
July 13,2015; Revised: September 4,2015; Published on Web: September 7,2015.
. Email: hanliang814@163.com; Tel: +86-571-88320891.
O646
10.3866/PKU.WHXB201509075
The project was supported by the National Natural Science Foundation of China (21406202,21176223) and Natural Science Foundation of Zhejiang Province,China (LY13B020012).
国家自然科学基金(21406202,21176223)和浙江省自然科学基金(LY13B020012)资助项目