壳聚糖基复合海绵的制备及性能研究
蓝春媛,曾丽璇,卢 平,张秋云,罗继文
(华南师范大学化学与环境学院,教育部环境理论化学重点实验室,广州510006)
壳聚糖基复合海绵的制备及性能研究
蓝春媛,曾丽璇,卢平,张秋云*,罗继文*
(华南师范大学化学与环境学院,教育部环境理论化学重点实验室,广州510006)
以壳聚糖(CS)和海藻酸钠(SA)为材料,研究了两者不同质量比合成复合海绵(CS/SA)的效果,在此基础上,再加入羧甲基纤维素钠(CMC)进行改性,制备了改性复合海绵(CS/SA/CMC),用FTIR和SEM对其结构进行表征、形貌观察及吸水率分析.结果表明,在复合反应温度为25℃、冷冻干燥时间为24 h、氯化钙浓度为0.5%、壳聚糖与海藻酸钠按质量比为1∶3,复合海绵的孔径最大,吸水率高达900%以上,改性后吸水率提高了约400%.
壳聚糖;海藻酸钠;羧甲基纤维素钠;复合海绵
近年来,利用高分子的生物相容性、无毒无副作用等特点制备的复合海绵在药物缓释、伤口敷料、细胞培养和组织工程等领域得到广泛的应用[1-2].海绵医用敷料[3-5]是医用敷料的一种,是一类弹性、多孔的固体材料,目前主要有海藻酸盐/壳聚糖海绵[6]、壳聚糖/海藻酸钠/明胶海绵[7]、壳聚糖/透明质酸/纳米银复合海绵[8]、壳聚糖海绵[9]、海藻酸钠/纳米银复合海绵[10]、壳聚糖复合海绵[11]等,但大部分复合海绵在制备过程采用的交联剂大多数具有毒性(如甲醛、戊二醛、环氧氯丙烷等),并抑制细胞生长[7],直接限制了其在生物医学及其他领域的应用.因此,研究具有无毒、抗菌性[3]、抗氧化性、可生物降解及生物相容性好的复合海绵将是复合海绵的未来研究趋势.复合海绵因制备过程复杂、工艺中较多不可控因素,使很多理想型的医用复合海绵材料仅限于实验室理想条件下制备.
本文利用壳聚糖的氨基正离子和海藻酸钠的羧酸根负离子之间的聚电解质作用,制备出新型聚电解质海绵,利用羧甲基纤维素钠与海藻酸钠在一定比例范围内具有很好的相容性,与壳聚糖分子链上的氨基作用的特性,在真空冷冻干燥技术下,以CaCl2为固化剂,制备羧甲基纤维素钠/海藻酸钠/壳聚糖复合海绵,并通过吸水率分析复合海绵的吸附性.本研究避免了有毒交联剂的使用,成功制备了无毒、吸湿性较强、可生物降解及生物相容性好的复合海绵,扩大复合海绵在其他领域的使用,同时为复合海绵的开发利用提供理论指导以及制作新型无毒医用止血材料提供参考.
1 实验部分
1.1材料与仪器
壳聚糖(简称CS,相对分子量2.0×105,脱乙酰度为88%);海藻酸钠(简称SA,天津市大茂化学试剂厂);羧甲基纤维素钠(简称CMC,天津市大茂化学试剂厂);冰醋酸(天津市大茂化工有限公司);氯化钙(上海凌峰化学药品有限公司);氢氧化钠(天津化学试药厂);LABCONCO真空冷冻干燥箱(广州科桥实验技术设备有限公司);电动搅拌器(D-8401WZ天津市华兴科学仪器厂);电子分析天平(FA2004,上海梁平仪器有限公司).
1.2复合海绵的制备
将壳聚糖溶于1%的醋酸水溶液得到质量分数为2%的壳聚糖溶液,然后将其按一定比例与2%海藻酸钠溶液混合,充分搅拌得到聚电解质复合物,匀浆后倒入模具内冷冻干燥.依次在CaCl2和NaOH溶液中浸泡后用蒸馏水洗涤,再冷冻干燥,得到壳聚糖/海藻酸钠海绵.复合海绵中壳聚糖与海藻酸钠的质量比为(1∶1、1∶3、3∶1),并标记为CS/SA11、CS/ SA13、CS/SA31.
1.3复合海绵的改性制备
复合海绵的制备流程见图1,称取一定量的壳聚糖加入100 mL玻璃烧瓶中,加入体积分数为1%的醋酸溶液,充分搅拌,直至完全溶解,溶液呈浅黄色,配制得到质量分数为2%的壳聚糖溶液.称量一定量的海藻酸钠,加入盛有一定体积的去离子水的100 mL玻璃烧瓶中,充分搅拌,直到海藻酸钠充分溶解,即配制得2%的海藻酸钠溶液.将上述配制的溶液,按质量比为CS∶SA=1∶3的比例混合,充分机械搅拌,混合均匀后,分别加入与海藻酸钠相对质量为5%、10%、15%的羧甲基纤维素钠,搅拌使羧甲基纤维素钠充分溶解,并与壳聚糖和海藻酸钠2种溶液完全混合.并标记为 CS/SA/CM1、CS/SA/ CM2、CS/SA/CM3.将混合液倒入预先准备的干净模具内,密封并放于冰箱冷冻过夜,隔天取出后在-54℃下冷冻干燥24 h.冷冻后将其依次浸泡于0.5%CaCl2溶液3 h、1%NaOH溶液2 h,然后用大量去离子水洗涤直至中性,再次冷冻干燥24 h,即可得到多孔结构改性复合海绵(图2).

图1 改性复合海绵的流程图Figure 1 Preparation process of modified compound sponge

图2 改性复合海绵样品Figure 2 Photograph of the modified compound sponge
1.4复合海绵的表征
用Nicolet 6700型(美国热电尼高力)傅立叶变换红外光谱仪测得样品的红外光谱.通过JEM-2100HR型(日本电子)扫描电子显微镜观察海绵的表面形貌并拍照.
1.5复合海绵吸水率测定
将复合海绵置于有无水氯化钙的干燥器中,于室温下每隔3 h称质量1次,直到恒质量为止,称试样质量ddry,再将干燥过的试样浸入到蒸馏水中,2min后将材料取出,以滤纸将表面水吸除后称湿态质量dwet,按下式计算吸水率[12]:

2 结果与讨论
2.1复合海绵的表征、形貌与吸水率
2.1.1复合海绵的表征图3中,CS显示位于1 557 cm-1处的—NH2特征弯曲振动峰,此外,由于壳聚糖分子中含有一定量的乙酰氨基,所以在1 633 cm-1出现酰胺I峰[CO伸缩振动吸收峰],随着SA的加入壳聚糖的—NH2特征弯曲振动向高波移动,吸收峰变窄,说明了CS上的—NH3+与海藻酸钠上的COO-之间相互存在静电作用形成了聚电解质复合物.CS与SA之间的静电吸引导致CS在3 251 cm-1处的—OH和—NH2的伸缩振动峰向高波数移动并变窄,说明了静电作用削弱了原本较强的CS分子内氢键.在未交联和交联的FTIR谱图对比中,可以看到2 931 cm-1处的吸收峰减弱,原因是由于Ca2+引入,与海藻酸钠分子链上的官能团络合形成了网状的egg-box结构,限制了分子中六元环上C—H键的伸缩振动,使得偶极矩变化较小,吸收峰变得不明显,同时也表明Ca2+与COO-发生作用.
2.1.2复合海绵的形貌图4表明复合海绵具有多孔结构,壳聚糖和海藻酸钠形成的聚电解质复合物呈不定型态.CS/SA31的表面比较密实,孔隙较小,而随着海藻酸钠含量的增加,两者形成的复合物孔隙逐渐增大,CS/SA13形成的孔隙最大.而海绵的制备过程采用冷冻干燥方法,聚合物溶液低温冷冻时,在聚集的高分子链周围充满了水冷冻形成的冰,这些冰在冷冻干燥过程中升华而形成孔,最终形成海绵的多孔结构.相对于单独CS来说,引入SA后复合海绵的孔径增大[6].

图3 壳聚糖(CS)、未浸泡的海绵以及复合海绵的红外图谱Figure 3 FTIR spectra of CS,without soaking sponge and compound sponge

图4 不同复合海绵样品的扫描电镜照片Figure 4 SEM images of different compound sponges
2.1.3复合海绵的吸水率壳聚糖和海藻酸钠本身都具有良好的吸湿性,两者形成的聚电解质复合物也具有良好的吸水率(图5).随着SA含量的增加吸水率明显增加,CS∶SA=1∶3的吸水率最好,原因SA是高吸湿性大分子聚合物,分子链上含有大量的COO-和OH-,大分子吸收大量的水分,使得其亲水性大于CS,随着海藻酸钠量的增加,复合海绵的吸水率也增加.从吸水率的测定可见复合海绵具有良好的吸水溶胀性.
2.2复合海绵的改性
2.2.1复合海绵的改性原理壳聚糖具有良好的生物相容性、无毒性、无刺激性,其分子链上含有大量的伯氨基[13-14],为天然的聚阳离子化合物,其结构式为图6.
图7、图8分别为海藻酸钠和羧甲基纤维素钠的化学结构式,海藻酸钠与羧甲基纤维素钠两者为聚阴离子化合物,当羧甲基纤维素钠的质量百分含量在5%~15%范围时,羧甲基纤维素钠与海藻酸钠相容[15].海藻酸钠、羧甲基纤维素钠和壳聚糖可以通过正、负电荷吸引形成聚电解质复合海绵,海藻酸钠是典型的离子交联水凝胶,G单元上的Na+易与某些二价阳离子(Cu2+、Zn2+、Ca2+、Sr2+、Ba2+等)发生离子交换反应络合形成水凝胶纤维而析出,其中Ca2+的离子空间大小最适合与海藻酸钠大分子形成紧密络合,G单元与Ca2+形成蛋盒结(图9),G单元堆积而形成网络结构,而CMC与Ca2+也进行离子交联[16](图10).

图5 不同复合海绵的吸水率Figure 5 Water absorption of different compound sponges
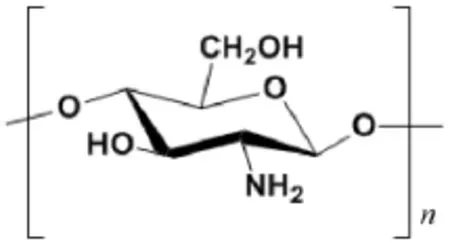
图6 壳聚糖化学结构式Figure 6 Structure of chitosan

图7 海藻酸钠化学结构式Figure 7 Structure of sodium alginate
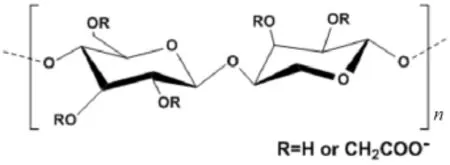
图8 羧甲基纤维素钠化学结构式Figure 8 Structure of carboxymethylcellulose sodium

图9 G单元与Ca2+交联Figure 9 G unit crossed with Ca2+

图10 羧甲基纤维素钠与Ca2+交联Figure 10 Carboxymethylcellulose sodium crossed with Ca2+
2.2.2改性复合海绵的表征高聚物相容时,分子间便存在相互作用,这种相互作用在红外谱图上明显表现出来[17].从图11看出,复合海绵在3 358 cm-1表现为分子氢键O—H伸缩振动峰,随着CMC含量的增加,羟基伸缩振动峰变宽且向低波偏移,这是因为CMC与SA大分子上的羟基之间形成氢键所致的,如果2种多糖共混后羟基伸缩振动峰增值并向低波数发生移动,那么分子间氢键一定增强[18],表明SA与CMC两种聚阴离子化合物在一定的范围内相容;复合海绵在1 567 cm-1出现了—NH3+的特征吸收峰,加入CMC,吸收振动峰由低波数向高波数移动约40 cm-1,表明羧甲基纤维素钠 COO-与 CS的—NH3+通过静电作用结合.
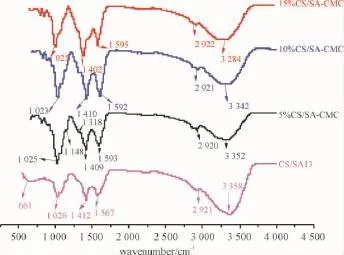
图11 改性复合海绵的红外光谱Figure 11 FTIR spectra of the modified compound sponges
2.2.3改性复合海绵的形貌CS/SA随着CMC含量的增加孔隙变小(图12).CMC含量为5%时,孔隙较大,当CMC含量为15%孔径小而密,原因是CMC分子结构中羧甲基比SA分子结构中的羧基的空间体积要大很多,CMC含量较低时,CMC大分子上的羧甲基伸展穿插于SA大分子间,再通过静电作用与CS结合,在冷冻干燥方法形成大孔径的复合物,而随着CMC含量的增加,其在水溶液中伸展穿插于CMC大分子间[15],CMC大分子自身之间形成强烈的氢键作用,限制了其与SA大分子间的相互作用,在静电作用下与CS结合,其形成的孔隙较CMC含量低的小而密.

图12 不同改性复合海绵样品的扫描电镜照片Figure 12 SEM images for different modified complex sponges
2.2.4改性复合海绵吸水率基于复合海绵CS∶SA=1∶3的比例上添加CMC对复合海绵进行改性.不同CMC含量的CS/AS/CMC海绵的吸水率示于图13.随着CMC含量的增加,复合海绵的吸水率增加,与未改性的复合海绵相比,吸水率增加约400%.改性复合海绵吸水率增加的主要原因是具有吸湿特性的CMC,CMC分子自身能形成一个三维空间网状结构,能结合住大量的水[18],而且CMC大分子中—CH2OCH2COO-比SA大分子中—COO-体积大得多,—CH2OCH2COO-的空间效应使得共混后的海绵大分子之间的作用力减弱,降低了复合海绵结晶区尺寸,提高了柔韧性和吸湿性[19].由于止血材料要求较高的吸水性能,聚电解质海绵具有优良的吸水性能,制备过程简单,使用无毒的交联剂,在该领域具有一定的应用价值,值得深入研究.
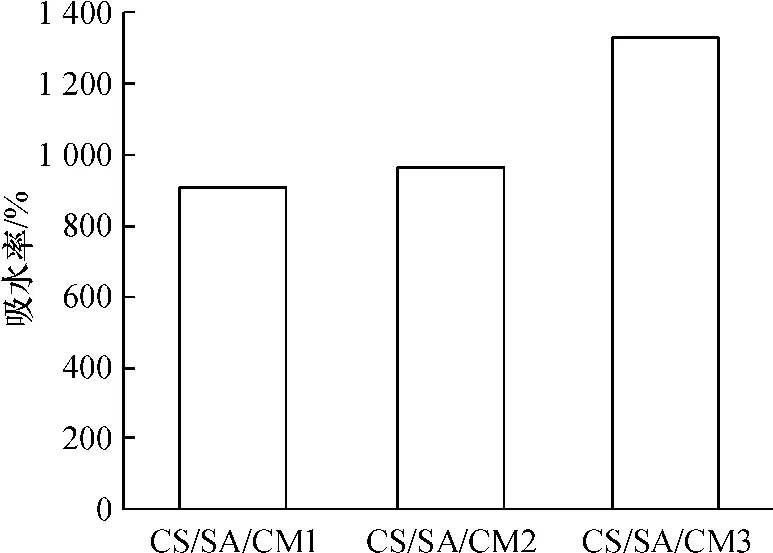
图13 不同改性复合海绵吸水率Figure 13 Water absorption of different modified compound sponges
3 结论
本文充分利用3种材料的相容性、无毒性、可降解性等优点成功的制备了复合海绵,通过FTIR、SEM、吸水率测试研究表明,复合海绵中的壳聚糖、海藻酸钠和羧甲基纤维素钠之间相互穿插、缠绕并通过静电相互作用,使制备的海绵表现出良好的吸水性.羧甲基纤维素钠的加入提高了壳聚糖和海藻酸钠复合海绵的吸水率,同时也提高复合海绵的柔韧性.壳聚糖、海藻酸钠和羧甲基纤维素钠对人体无毒,生物相容性好,易被生物降解,并有一定的止血作用,可望成为一种较理想的止血材料.
[1]Wu Y B,Mi F L,Shyu S S.Asymmetric chitosan membranes prepared by drywet phase separation a new type of wound dressing for controlled antibacterial release[J]. Journal of Membrane Science,2003,212(1):237-254.
[2]何小维,陈巍,李忠彦.羧甲基纤维素钠/壳聚糖复合海绵制备工艺研究[J].化工新型材料,2007,35(7): 59-64. He X W,Chen W,Li Z Y.Research on the preparation of carboxymethylceulose sodium/chitosan complex sponge[J].New Chemical Materials,2007,35(7):59-64.
[3]Rossi S,Faccendini A,Bonferoni M C,et a1.“Spongelike”dressings based on biopolymers for the delivery of platelet lysate to skin chronic wounds[J].International Journal of Pharmaceutics,2013,440(2):207-215.
[4]Min S J,Gao X,Han C M,et al.Preparation of a silk fibroin spongy wound dressing and its therapeutic eficiency in skin defects[J].Journal of Biomaterials Science,2012,23(1-4):97-110.
[5]Sionkowska A,Ptanecka A.Preparation and characterization of silk fibroin/chitosan composite sponges for tissue engineering[J].Journal of Molecular Liquids,2013,178: 5-14.
[6]樊李红,赵吉,黄进,等.壳聚糖/海藻酸钠聚电解质海绵及抗菌功能[J].武汉理工大学报,2006,28(11):25 -28. Fan L H,Zhao J,Huang J,et al.Polyelectrolyte sponges with antimicrobial functions based on chitosan and sodium alginate[J].Journal of Wuhan University of Technology,2006,28(11):25-28.
[7]莫名月,李国明,孔志玲,等.壳聚糖负载利福平微囊的制备及其性能研究[J].华南师范大学学报:自然学报版,2006(1):87-91. Mo M Y,Li G M,Kong Z L,et al.The preparation and properties of rifampicin-laded chitosan microcapsules[J]. Journal of South China Normal University:Natural Science Edition,2006(1):87-91.
[8]Anisha B S,Raja B,Chennazhi K P,et al.Chitosan-hyaluronic acid/nano silver composite sponges for drug resistant bacteria infected diabetic wounds[J].International Journal of Biological Macromolecules,2013,6(2):310-320.
[9]Ana P,Desirée T O,María J A,et al.Development of chitosan sponges for buccal administration of insulin[J]. Carbohydrate Polymers,2007,68(4):617-625.
[10]Song Y S,Ga H L,Se G L,et al.Alginate-based composite sponge containing silver nanoparticles synthesized in situ[J].Carbohydrate Polymers,2012,90(1):109-115.
[11]刘传荣,陈思浩,郑玉林.响应面分析法优化壳聚糖复合海绵的制备工艺[J].化工进展,2014,33(2):463-469. Liu C R,Chen S H,Zheng Y L.Optimizing the preparation technology of chitosan composite sponge by response surface method[J].Chemical Industry And Engineering Progress,2014,33(2):463-469.
[12]Ma J B,Wang H J,He B L,et al.A preliminary in vitro study on the fabrication and tissue engineedng applications of a novel chitosan bilayer material as a scaffold of human neofetal dennal fibroblasts[J].Biomaterials,2001,22(4):331-336.
[13]刘群,薛伟明,于炜婷,等.海藻酸钠-壳聚糖微胶囊膜强度的研究[J].高等学校化学学报,2003,23(7): 1417-1420. Liu Q,Xue W M,Yu W T,et al.Study of microcapsule membrane strength of sodium alginate chitosan[J]. Chemical Journal of Chinese University,2003,23(7): 1417-1420.
[14]蒋挺大.壳聚糖[M].北京:化学工业出版社,2001,127.
[15]朱平,张传杰.羧甲基纤维素钠与海藻酸钠的相容性研究[J].武汉科技学院学报,2008,21(8):78-81. Zhu P,Zhang C J.Compatibility of carboxymethyl cellulose and sodium alginate[J].Journal of Wuhan University of Science and Engineering,2008,21(8):78-81.
[16]展义臻,赵雪,朱平.新型海藻酸共混纤维的制备及性能综述[J].丝绸,2009,4(3):46-50. Zhang Y Z,Zhao X,Zhu P.Review of synthesis and properties of a novel Alginate Blend Fibers[J].Silk,2009,4(3):46-50.
[17]张传平.海藻酸钠/狡甲基纤维素钠共混纤维的制备及结构与性能研究[D].青岛:青岛大学,2008.
[18]伊洪坤,卢平.壳聚糖改性TiO2光催化剂的制备及其光催化性能研究[J].华南师范大学学报:自然科学版,2009(2):70-74. Yi H K,Lu P.The preparation of chitosan modified TiO2photocatalyst and its photocatalytic performance[J]. Journal of South China Normal University:Natural Science Edition,2009(2):70-74.
[19]Yi M Q.Fibers of cospun alginate:USA,6080420[P]. 2000-06-27.
【中文责编:成文英文责编:李海航】
Preparation and Performance of Chitosan-Based Compound Sponge
Lan Chunyuan,Zeng Lixuan,Lu Ping,Zhang Qiuyun*,Luo Jiwen*
(School of Chemistry and Environment,South China Normal University;Key Laboratory of Theoretical Chemistry of Environment,Ministry of Education,Guangzhou 510006,China)
With different mass ratios of chitosan(CS)and sodium alginate(SA)as the main raw materials,the chitosan-based compound sponge(CS/SA)was successfully synthesized and modified by carboxymethyl cellulose sodium(CMC).The structure and morphology of the sponge were characterized by FTIR and SEM and its physical property was measured.The optimum conditions of the preparation were as follow:reaction temperature is 298 K,time of lyophilization is 24 hours and the concentration of calcium chloride is 0.5%.The result shows that the compound sponge has the highest pore size when the mass ratio of chitosan to sodium alginate was 1∶3.The water absorption of sponge of about 900%was further increased by about 400%after modification.
chitosan;sodium alginate;carboxymethylcellulose sodium;sponge
O636.1
A
1000-5463(2015)03-0074-06
2014-07-07《华南师范大学学报(自然科学版)》网址:http://journal.scnu.edu.cn/n
国家自然科学基金项目(21147003)
张秋云,副教授,Email:hnsdhks@163.com;罗继文,讲师,Email:holdit@126.com.

