CT引导下气管前腔静脉后间隙病变穿刺活检术的临床应用
梁力嵩, 席建东, 王显龙, 俞志坚, 温志波, 江永焰
·非血管介入Non-vascular intervention·
CT引导下气管前腔静脉后间隙病变穿刺活检术的临床应用
梁力嵩,席建东,王显龙,俞志坚,温志波,江永焰
目的探讨CT引导下气管前腔静脉后间隙结节穿刺活检术的临床可行性和应用。方法回顾性总结2008年1月至2014年7月于南方医科大学珠江医院46例行CT引导下气管前腔静脉后间隙病变穿刺活检术资料,穿刺结束后立即行CT平扫及临床短期随访,了解并发症情况,评估穿刺安全性;行穿刺术所取得标本,均行细胞病理学及组织学检查,以手术标本病理结果或治疗效果作为标准,评估活检术准确性及其临床应用价值。结果本组患者并发症发生率15.6%(1例液气胸,6例少量气胸(肺压缩10%以下),余均未出现明显并发症;46例患者中2例取得的组织较为细碎,未获得确切病理结果,1例穿刺组织病理结果与术后病理结果不相符;43例(93.5%)患者获得病理学诊断。结论CT引导下气管前腔静脉后间隙病变穿刺活检术,在操作者熟悉气管前腔静脉后解剖的基础上,术前认真阅读患者影像资料,根据实际情况制定合适的穿刺路径,能够安全、准确地取得组织病理结果。这一技术对指导临床医师进一步制定诊疗计划极有帮助。
穿刺活检;计算机断层成像;引导;纵隔病变;气管前间隙
气管前腔静脉后(pretracheal retrocaval,PTRC)间隙按照Felson[1]的纵隔三分法属于中纵隔,其病变种类繁多,影像表现复杂,鉴别诊断较困难[2-4]。该处位置较深,且周围有较多重要脉管走行,尽管CT引导下穿刺活检术能够直接取得病变组织病理结果,对于临床工作中制定下一步诊疗计划具有重要意义,但穿刺活检术具有较高风险。本研究回顾性收集本院CT引导下经PTRC间隙病变活检穿刺术病例,并介绍该区域病变穿刺技术经验及总结其临床应用价值。
1 材料与方法
1.1材料
1.1.1资料来源回顾性收集2008年1月至2014年7月共46例于我院影像诊断中心行CT引导下PTRC间隙病变穿刺活检术患者,其中男28例,女18例,年龄18~82岁。入选条件:肺内病变或胸腔积液均未找到异常细胞患者且PTRC病变最短径均大于20 mm。
1.1.2器材飞利浦16排螺旋CT,扫描条件120 kV 80 mAs层厚5 mm层间距5 mm根据病灶内部有无坏死及坏死区域大小,选择切割活检针或抽吸活检针,切割针型号:德国OptiMed 1399-1210 18 G-150 mm,抽吸活检针型号:Precisa PRE1815 18 G-150 mm。
1.2方法
1.2.1术前准备患者术前均于本院或外院行CT平扫及增强扫描检查,观察病灶形态、影像学特点及寻找最大截面积所在层面,病变最长径(31.6±8.5)mm,最短径(27.2±6.8)mm。活检前与患者签订知情同意书,常规检查凝血时间、血小板计数和凝血酶原,若有长期服用抗凝药病史,需停药2周以上,复查出、凝血时间、血小板计数和凝血酶原,在患者凝血功能正常之后方可进行穿刺。
1.2.2穿刺过程根据患者年龄、自身情况、病变大小确定患者体位。协助患者摆放自身感觉较为舒适体位,嘱患者自由平静呼吸。取金属标记物贴于体表,扫描定位后确定穿刺点及角度,在穿刺针进入胸膜腔之前,在体壁肌肉组织内调整方向及角度,确定角度无误后刺入已测得预定深度,本研究平均刺入深度(96.5±9.3)mm,根据肿块情况及所选针类型不同,对病灶切割1~2次。在穿刺结束后,穿刺点局部按压2 min止血,并用无菌敷贴保护穿刺点,再次行CT平扫观察肺部及纵隔情况,注意有无气胸及纵隔出血。穿刺所得组织均行病理学、细胞学检查,并辅以免疫组化进一步辅助观察。在穿刺结束后行CT平扫以及短期临床监测观察其并发症发生率及发生情况。
2 结果
2.1穿刺与病理结果
45例在首次进入胸膜腔后,顺利到达PTRC间隙,并取得标本,1例在首次失败后,患者返回病房观察3 d,在确定无并发症之后,再次行穿刺活检,顺利取得标本。穿刺成功率100%(46/46),首次穿刺成功率97.8%(45/46)。
46例患者中,2例因取得组织过于细碎,无法观察,1例活检组织病理报告为原始神经外胚层细胞瘤(primitive neuroectodermal tumor,PNET),病变经胸腔镜切除后,手术标本病理活检为浆母细胞瘤,余43例均取得较满意活检组织,阳性率95.7%(44/46),特异性97.7%(43/44)。其中4例采取抽吸针进行穿刺活检,3例成功获取组织;切割针阳性率97.6%(41/42),特异性100%(41/41)(图1、2)。未取得组织病理结果患者在简单对症治疗后转至他院继续就诊。在取得病理结果的43例患者中,均在我院治疗均取得一定效果。
2.2并发症
在穿刺活检术后复扫CT,短期内临床随诊复查观察,并发症发生率15.6%(7/46),其中气胸6例,气胸量均不足10%,给予吸氧等助肺扩张对症处理后,均自行吸收,大量液气胸1例,在经过抽气引流等对症治疗6 d之后好转。余39例患者均未出现气胸、纵隔血肿、感染等并发症。

图1 左下叶外侧基底段结节,病灶较小
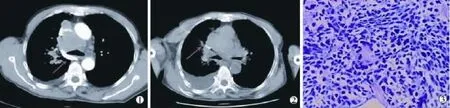
图2 因右肺下叶多枚栗粒灶,而气管前腔静脉后淋巴结明显肿大
3 讨论
3.1PTRC间隙应用解剖及其意义
PTRC间隙由Schnyder等[5]通过对CT影像资料的观察总结,提出这一解剖位置的概念。该间隙由气管前壁、主动脉弓内侧壁、升主动脉的后面、上腔静脉的后内侧缘及奇静脉弓的内侧缘所围而成。由于该间隙并非简单的筋膜间隙,而是由结缔组织、脂肪和淋巴结等充填[5-6],该区域病变对周围脉管及组织结构易推压而导致该间隙形态改变。该间隙正常情况下较狭小,周边大血管较多,在行CT引导下穿刺时,具有较高风险。因此在活检穿刺之前,强调患者行胸部增强扫描,甚至多排螺旋CT增强薄层扫描,重建出该区域的脉管,对于穿刺点、穿刺路径的选择具有重要意义。
3.2CT引导下PTRC间隙病变穿刺路径及技术分析
根据其周围脉管走行特点及对于增强CT扫描图像的仔细观察分析,PTRC间隙其右壁及右后壁由纵隔胸膜构成,无重要脉管走行,因此进针点选择有侧胸壁及后胸壁2种选择。侧胸壁作为进针点,其入路路径要经过较多肺组织,因此该方案作为次要选择方案。本研究中主要选用从胸椎右侧横突旁作为进针点,从PTRC间隙右后壁进入,选择该路径的原因是因为从此路径进针时,能够避开重要脉管,特别是上腔静脉、奇静脉,降低产生严重并发症的概率,且背部肌肉组织较侧胸壁厚,利于穿刺针在软组织内调整方向。在穿刺过程中采取“三步法”:①局部浸润麻醉,穿刺针进入局部肌肉,仔细核对方向、角度及所选择层面;②穿刺针进入肺内后,再行CT平扫观察,确定方向及选择层面;③一次性穿过纵隔胸膜,到达病变组织,根据病变的大小选择合适的切割长度进行取材。
本组有2例患者采取从前胸壁进针,其原因:①患者自身情况及肺部条件较其他患者差,无法耐受俯卧位;②病变较大(穿刺时所选层面截面积分别为33 cm×27 cm、51 cm×38 cm),上腔静脉受病变严重压迫变窄,奇静脉及奇静脉弓增宽,以后胸壁作为进针点,路径上有扩张迂曲的奇静脉弓,无法规避;③从前胸壁进针,其路径避免了对叶间胸膜的损伤,降低了气胸的发生概率。该2例患者在穿刺术后未发生并发症,穿刺组织经过病理检查后均取得与术后病理相符合结果。
针对未取得标本及所取得标本病理与手术病理不吻合不同的病例分析,发现该3例患者穿刺时,2例使用抽吸针,1例使用切割针,标本病理与手术结果不同原因是因为术前增强扫描示病灶内较多坏死灶,如果用切割针,较可能取得坏死组织,对病理观察影响较大,因此选用了抽吸针进行穿刺活检[7]。尽管术前和术后免疫组化有相似性,但是由于穿刺标本所取得组织较少,且挤压变形和坏死,镜下观察局限,免疫组化表达辅助诊断意义不大,因此造成了该例患者的误诊。因此在病灶坏死不多时,尽量择切割针,穿刺1~2次,以增加获取组织量;而在病变坏死灶较多时,可选择抽吸针,多次进行取材,且在穿刺结束时以4%甲醛固定液冲洗套管,增加获得细胞量[8],但须特别指出,在多次穿刺抽吸过程中,应严格掌握抽吸过程中进针距离,避免进入过深损伤周围重要脉管。
3.3并发症
在纵隔活检中并发症以气胸、咯血及纵隔血肿较为多见[9-10]。尤其以大咯血导致气管阻塞及纵隔血肿较为凶险,因此在术前认真阅片,合理规划穿刺路径就显得尤为重要。在背部或者前胸壁皮下及肌肉中正确调整角度之后不在肺组织内调整方向,而是一次性就进入PTRC间隙,这样做的优点是避免了对于脏层胸膜及纵隔胸膜的反复穿刺,从而降低并发症的发生率[10-11]。在穿刺针进入肺组织后观察,若穿刺针角度或层面不正确时,应将穿刺针退出胸膜腔,行CT平扫,在确认患者无气胸、咯血等并发症之后方可重复穿刺,否则应与临床医师沟通,建议中止穿刺术,嘱患者回病房充分休息,并行影像学复查,确认无明显并发症之后方可再次行穿刺术。15%并发症发生率数据表明“三步法”的操作安全性值得肯定。
3.4总结
CT以其良好空间分辨率,扫描快速,定位精确,其引导纵膈病变的被认为具有重要意义[12-14],尽管随着超声引导的针吸活检术(endoscopic ultrasound with fine needle aspiration,EUS-FNA)或近来与气管镜结合的经气管镜超声引导针吸活检术(endobronchial ultrasound-guided transbronchial needle aspiration,EBUS-TBNA)技术的在临床上的广泛开展,特别是EBUS-TBNA的发展,但因其均采用22 G细针,取得标本较为细碎,病理医师根据穿刺组织仅能做出细胞学观察。本组研究中大多采用直径为18 G的穿刺活检针,获得组织较为完整,文献报道EUSFNA及EBUS-TBNA灵敏度及特异度波动浮动较大[15-16]。本研究中对肿瘤转移性淋巴结活检阳性率均达100%(19/19),符合NACC2015非小细胞肺癌分期中提出的“同步分期”的观点[17-18],穿刺所得标本足够供病理科在常规细胞及组织观察后,对有疑难或较难诊断的组织进一步行免疫组化检测,从而分辨细胞类型及组织来源,特别是针对非小细胞肺癌转移性淋巴结,可以对EGFR,ALK等基因进行检测,这对非小细胞肺癌患者的化疗方案制定具有重要意义[19-21];本研究在操作者熟悉PTRC间隙解剖的前提下,仔细阅读患者术前增强CT扫描资料,根据病变及周围脉管情况合理选择穿刺进针点及所选穿刺针类型,以“三步法”的穿刺模式,不仅能够准确定位,还能根据病变增强扫描,合理选择所需活检针。因本院尚未开展EUS-FNA或EBUS-TBNA检查,因此有待进一步更多临床数据对本研究及EUS-FNA和(或)EBUS-TBNA进行统计学分析及观察研究比较,分析不同技术之间优劣性。
[1]Felson B.Chest Roentgenology[M].Philadelphia:Saunoders,1973:50-100.
[2]PriolaAM,PriolaSM,CardinaleL,etal.Theanterior mediastinum:diseases[J].Radiol Med,2006,111:312-342.
[3]滑炎卿,郑向鹏,张国桢.纵隔解剖“三分区”在占位病变诊断中的应用[J].中华放射学杂志,2001,35:339-341.
[4]张星,何国祥.纵隔肿瘤影像学特点的探讨 (附58例分析)[J].实用放射学杂志,2004,20:907-909.
[5]Schnyder PA,Gamsu G.CT of the pretracheal retrocaval space[J].AJR Am J Roentgenol,1981,136:303-308.
[6]许仕全,韩景茹,姜均本.纵隔内气管前间隙的断面解剖及其临床意义[J].中国临床解剖学杂志,1999,17:46-47.
[7]Capalbo E,Peli M,Lovisatti M,et al.Trans-thoracic biopsy of lung lesions:FNAB or CNB?Our experience and review of the literature[J].Radiol Med,2014,119:572-594.
[8]李辉,武明辉,宁培刚,等.CT引导下胸部经皮切割针与抽吸针穿刺活检效果比较[J].郑州大学学报·医学版,2009,44:862-864.
[9]吴达明,陆勇,杜联军,等.CT导引下的纵隔病变穿刺活检[J].介入放射学杂志,2006,15:421-423.
[10]袁小冬,汪建华,左长京,等.CT引导下隆突下淋巴结穿刺活检术的临床应用[J].介入放射学杂志,2011,20:311-314.
[11]杨肖华,黄新宇,汪国祥.CT引导下经皮肺穿刺活检术并发症的影响因素分析[J].介入放射学杂志,2013,22:658-662.
[12]Herman SJ,Holub RV,Weisbrod GL,et al.Anterior mediastinal masses:utility of transthoracic needle biopsy[J].Radiology,1991,180:167-170.
[13]Priola AM,Galetto G,Priola SM.Diagnostic and functional imaging of thymic and mediastinal involvement in lymphoproliferative disorders[J].Clin Imaging,2014,38:771-784.
[14]De Kerviler E,Benet C,Brière J,et al.Image-guided needle biopsy for diagn osis and molecular biology in lymphomas[J]. Best Pract Res Clin Haematol,2012,25:29-39.
[15]Agarwal R,Srinivasan A,Aggarwal AN,et al.Efficacy and safety of convex probe EBUS-TBNA in sarcoidosis:a systematic review and meta-analysis[J].Respir Med,2012,106:883-892.
[16]王栋,马卫霞,姜淑娟,等.经支气管镜超声引导针吸活检术在纵隔病变诊断中的应用价值[J].中华医学杂志,2013,93:1563-1566.
[17]Travis WD,Brambilla E,Noguchi M,et al.Diagnosis of lung cancer in small biopsies and cytology:implications of the 2011 International Association for the Study of Lung Cancer/American Thoracic Society/European Respiratory Society classification[J]. Arch Pathol Lab Med,2013,137:668-684.
[18]Travis WD,Brambilla E,Noguchi M,et al.International association for the study of lung cancer/American thoracic society/European respiratory society international multidisciplinary classification of lung adenocarcinoma[J].J Thorac Oncol,2011,6:244-285.
[19]Suda K,Mizuuchi H,Maehara Y,et a l.Acquired resistance mechani sms to tyrosine kinase inhibitors in lung cancer with activating epidermal growth factor receptor mutation:diversity,ductility,and destiny[J].Cancer Metastasis Rev,2012,31:807-814.
[20]Oxnard GR.Strategies for overcoming acquired resistance to epidermal growth factor receptor:targeted therapies in lung cancer[J].Arch Pathol Lab Med,2012,136:1205-1209.
[21]Gainor JF,Shaw AT.Emerging paradigms in the development of resistance to tyrosine kinase inhibitors in lung cancer[J].J Clin Oncol,2013,31:3987-3996.
Clinical application of CT-guided percutaneous puncturing biopsy for the lesions located in the pretracheal retrocaval space
LIANG Li-song,XI Jian-dong,WANG Xian-long,YU Zhi-jian,WEN Zhi- bo,JIANG Yong-yan.Medical Imaging Center,Zhujiang Hospital of Southern Medical University,Guangzhou,Guangdong Province 510280,China
WEN Zhi-bo,E-mail:zhibowen@163.com
ObjectiveTo discuss the clinical feasibility and application of CT-guided percutaneous puncturing biopsy for the lesions located in the pretracheal retrocaval space.MethodsThe clinical and biopsy data of 46 patients with lesions in the pretracheal retrocaval space,who had received CT-guided percutaneous puncturing biopsy at Zhujiang Hospital of Southern Medical University during the period from January 2008 to July 2014,were retrospectively analyzed.When the puncture was finished,plain CT scan was immediately performed to check the complication and to evaluate the safety of the procedure;the patients were followed up for a short time.All the specimens obtained by puncture were sent for pathological cytology and histological examination.Taking the pathological results of the surgical specimens or the therapeutic effect as the standard,the diagnostic accuracy of biopsy and its clinical application were evaluated.ResultsIn this series,the complication incidence was 15%,including hydropneumothorax(n=1)and mild pneumothorax(lung compression<10%,n=6);and no other obvious complications were observed.In two patients,the specimens obtained by biopsy were broken bits and no exact pathological diagnosis could be made.In one patient,the pathological findings of biopsy specimen were not consistent with the postoperative pathological results.In the remaining 43 patients,pathological diagnosis was successfully obtained.ConclusionThe pathological results of the lesions located in the pretracheal retrocaval space can be safely and correctlyobtained by CT-guided percutaneous puncturing biopsy when the operator is quite familiar with the anatomy of pretracheal retrocaval space,reads the patient's imaging materials before procedure carefully and formulates the puncturing path properly according to the actual situation,This technique is very helpful in guiding clinicians to make a further treatment plan.(J Intervent Radiol,2015,24:974-978)
puncture biopsy;computed tomography;guidance;mediastinal lesion;pretracheal space
R735
A
1008-794X(2015)-11-0974-05
2015-03-05)
(本文编辑:俞瑞纲)
10.3969/j.issn.1008-794X.2015.11.011
510280广州南方医科大学珠江医院影像诊断科
温志波E-mail:zhibowen@163.com

