颅内动脉瘤相关糖蛋白标志物的蛋白组学研究
许璟 马费强 陈贤谊 周峰 朱国伟 张建民


DOI:10.3760/cma.j.issn.1671-0282.2015.03.013
基金項目:浙江省卫生厅平台骨干项目(2011RCB022);浙江大学横向科技项目(11-491020-290)
作者单位:310009 杭州,浙江大学医学院附属第二医院神经外科
通信作者:张建民,Email:zjm135@vip.sina.com
【摘要】目的 在脑脊液(cerebrospinal fluid, CSF)中筛选与颅内动脉瘤(intracranial aneurysm, IA)相关的糖蛋白标志物,对其灵敏度和特异性加以评价。方法 采用定量蛋白质组学和质谱技术,平行比较随机选取的4组研究对象即正常对照组(healthy control, HC)、疾病对照组(disease control, DC)、未破裂IA组(unruptured IA, UIA)和破裂IA组(ruptured IA, RIA)各10例的CSF中糖蛋白的表达差异,筛选出其中的一个差异蛋白——受体酪氨酸激酶Axl,并在另一相同分组各20例患者基础上,用受试者工作特征曲线(receiver operating characteristic curve,ROC曲线)对候选标志物的灵敏度和特异性做出评价。数据分析采用GraphPad Prism5软件,多组之间比较采用单因素方差分析中的Newman-Keuls多重比较法;相关性分析采用Pearson相关分析。以P<0.05为差异具有统计学意义。结果 首先,在人CSF中一共鉴定了294个糖蛋白。其次,通过HC、DC、RIA以及UIA四组之间的比较,鉴定和定量了59个仅在RIA组中发生特异性改变的蛋白、24个仅在UIA组中发生特异性改变的蛋白以及33个在RIA组和UIA组中均发生改变的蛋白。最后,选取了其中一个仅在RIA组中表达增高的蛋白-酪氨酸受体激酶Axl,在独立CSF和血浆中进一步加以验证,ROC曲线分析表明在95%特异性时,CSF中Axl 区分RIA和UIA的灵敏度为60%。血浆Axl在区分RIA和正常对照的灵敏度为40%,区分RIA和UIA的灵敏度为25%。结论 CSF Axl可以作为预测IA破裂的潜在标志物,深入研究其与IA形成和破裂的关系将有助于揭示IA发病机制和寻找新的治疗靶点。
【关键词】颅内动脉瘤;脑脊液;定量蛋白质组学;受体酪氨酸激酶Axl;生物标志物
Identify the glycoproteins as biomarkers for intracranial aneurysm with a proteomics approach
Xu Jing,Ma Feiqiang,Chen Xianyi,Zhou Feng,Zhu Guowei,Zhang Jianmin.Neurosurgery Department, Second Affilated Hospital Zhejiang University College of Medicine, Hangzhou 310009, China
Corresponding author: Zhang Jianmin, Email: zjm135@vip.sina.com
【Abstract】Objective To screen the glycoproteins as biomarkers for intracranial aneurysm (IA) in cerebrospinal fluid (CSF) and evaluate the specificity and sensitivity of the biomarker candidates. Methods A complementary proteomic approach integrated with multidimensional chromatography was employed to simultaneously measure relative changes in the gylcoproteins of cerebrospinal fluid (CSF) obtained from patients with ruptured IA (RIA) and unruptured IA (UIA) compared to the healthy controls (HC) and disease controls (DC). One protein-receptor tyrosine kinase Axl with a unique change in RIA was validated in CSF and plasma. The sensitivity at 95% specificity of Axl in CSF and plasma was evaluated with receiver operating characteristic curve (ROC curve). Results Firstly, a total of 294 glycoproteins were identified in human CSF with believable evidence. Secondly, the proteomic findings showed the quantitative changes in RIA and UIA as compared to HC and DC. Of 294 identified CSF proteins, 59, 24 and 33 proteins displayed quantitative changes unique to RIA, UIA or IA, respectively. At last, one of these unique proteins-receptor tyrosine kinase Axl with unique increase in RIA was confirmed both in CSF and plasma. ROC curve analysis showed that the sensitivity at 95% specificity of Axl in CSF to differentiate RIA from UIA was 60%. When compared to CSF, the sensitivity at above setting in plasma to differentiate RIA from HC was 40% and to differentiate RIA from UIA was 25%. Conclusions A glycoprotein biomarker Axl might be used as a promising biomarker to predict the rupture of IA. The further investigation of the relations between Axl and IA formation as well as rupture might help to elucidate the underlying pathogenesis and find new therapeutic targets.
【Key words】Intracranial aneurysm; Cerebrospinal fluid; Quantitative proteomics; Receptor tyrosine kinase Axl; Biomarker
颅内动脉瘤(intracranial aneurysm, IA)在人群中的发病率相当高,据估计在成人中可以达到1%~5%[1-3]。一旦发生破裂引起蛛网膜下腔出血,病死率可高达50%以上[4]。而通过及时的治疗未破裂IA的病死率却很低[5],但对无症状的UIA是否要进行治疗仍存在很大争议[6]。临床上制定了一些所谓的“标准”来判断无症状的UIA是否需要进行治疗,如IA的大小、位置等[7]。但是这些标准并没有坚实的科学依据,IA的破裂和大小可能没有直接关系[8]。迄今为止,IA的病因和发病机制还不清楚[9-10],国内外学者仍未找到一种有效的生物标志物。本研究利用定量蛋白质组学技术筛选差异表达的糖蛋白,发现了一个仅在RIA中表达增高的蛋白——酪氨酸受体激酶Axl,其可能成为非常有前景的预测IA破裂的生物标志物。
1 资料与方法
1.1 一般资料
本课题研究对象为2010年1月1日到2012年12月31日就诊于浙江大学医学院附属第二医院神经外科的患者。本研究获得了医院伦理委员会的批准,且均获得研究对象的同意并签署书面知情同意书。
入选标准:(1)正常对照(HC) 从脑外伤完全恢复至少两个月以上入院行颅骨修补的患者中选取。入选标准为:①各项常规和实验室检查的指标均在正常范围;②无严重肝肾心肺病史;③无遗传性家族疾病史;④无严重抽烟、酗酒史(抽烟<40 支/周,饮酒<150 g酒精/周);⑤经CTA检查排除IA。(2)其他神经系统疾病对照(DC) 从非出血性疾病相关的脑肿瘤患者或其他神经系统疾病患者中选取,并且经CTA或MRA证实排除IA。(3)未破裂IA患者(UIA) 经DSA或CTA、MRA检查后确诊,并且无任何IA相关症状的患者。(4)破裂IA患者(RIA) 经DSA检查确诊是由于IA破裂引起蛛网膜下腔出血的患者。破裂动脉瘤脑脊液的采集在手术或栓塞后的一个月进行。用于脑脊液和血液标志物筛选的4组患者(RIA, UIA, 正常对照和疾病对照,每组各10 例)在年龄(52.4±9.0)岁 vs.(55.2±3.9)岁vs.(52.8±6.9)岁vs.(54.6±4.2)、性别(男/女:8/2 vs. 8/2 vs. 8/2 vs. 8/2 vs. 8/2)等方面差异无统计学意义。而用于验证的4组患者(RIA, UIA, 正常对照和疾病对照,每组各20 例)在年龄(51.7±8.4)岁vs.(51.2±10.2)岁vs.(50.8±7.6)歲vs.(49.5±7.7)岁和性别(男/女:7/13 vs. 7/13 vs .7/13 vs. 7/13)亦差异无统计学意义。
1.2 实验方法
1.2.1 脑脊液和血液标本的采集 腰穿由熟练的医生操作,统一在清晨(7:00-8:00)采集。患者平躺侧卧位,腰3~4椎间隙为进针位置,第一管2~5 mL送脑脊液常规。第二管收集约10 mL作为实验标本,分装成0.5 mL/管。血液在空腹下采集,每个病例采集1 mL左右血液至肝素抗凝管中;离心分离得到的血浆分装成0.1 mL/管。所有标本收集后均立即放在-80 ℃低温冰箱备用。
1.2.2 使用凝集素亲和柱分离脑脊液中的糖蛋白 将等分的脑脊液样本(2 mL)用Qproteome糖蛋白试剂盒(Qiagen,Valencia,CA)进行糖蛋白的分离和富集。使用SpeedVac (Thermo, Asheville, NC)将样品干燥至约200 μL,在1000 g下离心5 min后,把上清液转移到另一新管中,沉淀则用凝集素亲和试剂盒中的去污剂100 μL进行溶解后与上清液合并。处理好的样品与1500 μL结合缓冲液以及蛋白酶抑制剂(100×)混和,旋转震荡充分混匀。将糖蛋白用100 μL带有蛋白酶抑制剂溶液的洗脱缓冲液洗脱6次。洗脱液则通过添加4倍体积的冰冷丙酮沉淀,在-20 ℃下孵育2 h洗脱沉淀池,然后4 ℃12 000g下,在预冷微离心机离心10 min。去除上清液,沉淀后的蛋白样品加入100 μL 0.5 mol/L TEAB(triethylammonium biocarbonate)溶解。最后使用BCA法测定蛋白浓度(Thermo, Rockford, IL)。
1.2.3 iTRAQ标记和二维液相色谱及串联质谱分析 来自四个比较组的100 μg蛋白质用胰蛋白酶消化后分别用四种iTRAQTM试剂的一种来标记(Applied Biosystems, Foster City, CA)。然后,把iTRAQ标记的样本混合后(共400 μg),用PolySulfoethyl ATM 强阳离子交换色谱柱将样品分成6个部分,分别用SpeedVac真空离心干燥,溶解于0.5%三氟乙酸中,然后通过毛细管C18反相柱,线性梯度设置5%~95%流动相B(80% 乙腈/0.08TFA/HPLC 级纯水)85 min,洗脱后的组分与重结晶的α-cyano-4-hydroxycinnamic acid (7 mg/mL 溶解于60% 乙腈/2.6% 醋酸铵,sigma)以及内参(4700 Mass Standard Kit, Applied Biosystems)混合,用ProbotTM自动点样器点至不锈钢MALDI 24×24 矩阵的点样板上,每板一共有576个点,用MALDI-TOF/TOF质谱仪(4700 Proteomics Analyzer withTOF/TOF OpticsTM,Applied Biosystems)进行蛋白鉴定,通过比较不同组与对照组的比值进行定量分析。
1.2.4 血浆和脑脊液中可溶性Axl(sAxl)的ELISA验证 根据制造商的说明书,在人ELISA试剂盒(Abcam, Cambridge, MA)测定血浆和脑脊液中sAxl。在测定前脑脊液和血浆样品分别为1∶100和1∶1000稀释。在微孔板上读出450 nm处的吸光度。用标准曲线测定血浆和脑脊液中sAxl浓度。
1.3 统计学方法
数据分析采用GraphPad Prism 5 软件,多组之间比较采用单因素方差分析中的Newman-Keuls Multiple Comparison Test;相关性分析采用Pearson相关分析;灵敏度和特异性评价采用受试者工作特征曲线(receiver operating characteristic curve,ROC)分析。以P<0.05 为差异具有统计学意义。
2 结果
2.1 脑脊液糖蛋白质组的鉴定
结合糖蛋白分离和定量蛋白质组学技术,本研究在脑脊液中一共鉴定了294个糖蛋白质,这些被鉴定的蛋白通过Uniprot数据库(http://www.uniprot.org)的搜索,主要涉及以下11类:(1)与免疫或炎症反应相关;(2)与细胞黏附相关;(3)与细胞外基质组成相关;(4)与蛋白合成和降解相关;(5)与转运相关;(6)与细胞凋亡或抗凋亡相关;(7)与细胞增殖、分化和迁移相关;(8)与信号转导途径相关;(9)与物质代谢相关;(10)与细胞结构和细胞骨架相关;(11)功能未知。在这些蛋白中,除了有相当一部分蛋白(21%)功能未知,其他最常见的是与免疫及炎症反应相关的蛋白(13%)、与细胞黏附相关的蛋白(12%)以及与蛋白合成及降解相关的蛋白(13%),其在动脉瘤的形成和破裂过程中发挥了重要作用。
2.2 在破裂和未破裂动脉瘤中发生改变的脑脊液糖蛋白
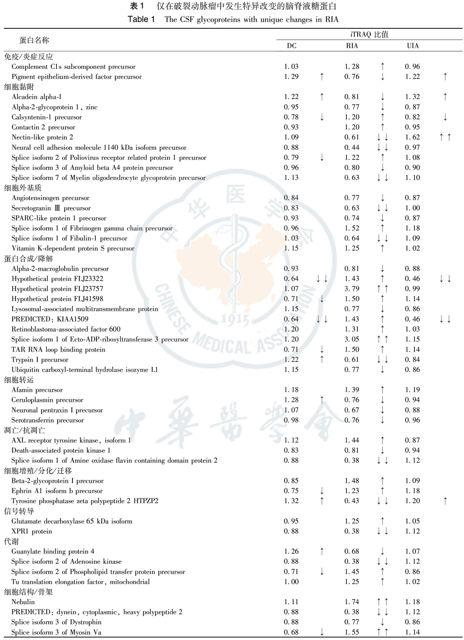
利用同时可以标记四组样品的iTRAQ试剂分别标记HC(iTRAQ-114)、DC(iTRAQ-115)、RIA(iTRAQ-116)和UIA (iTRAQ-117),然后分别比较115/114、116/114和117/114的比值,找出以下三组感兴趣的蛋白:(1)仅在RIA组中发生变化或者特异性改变(变化的方向有别于其他组)的蛋白;(2)仅在UIA组中发生变化或者特异性改变的蛋白;(3)同时在RIA组和UIA组中发生变化的蛋白。利用这些标准,笔者分别鉴定了59个、24个和33个在RIA组、UIA组或IA组中发生特异改变的蛋白(见表1~3)。
2.3 候选糖蛋白标志物Axl在脑脊液和血浆中
验证
在本研究中优先选择了受体酪氨酸激酶Axl进行验证,因为该蛋白仅在RIA的脑脊液中表达增加44%;数据库中显示有N-linked糖基化位点;大量的文献支持Axl介导的信号通路在各种类型细胞的存活、生长、聚集、迁移以及在抗炎症反应中发挥重要的调节作用;目前可方便地对其进行定量。
首先在4组合并的脑脊液样品中Axl的含量分别为:HC组(65.89±12.89)ng/mL; DC组(95.99±16.51)ng/mL; RIA组(152.64±12.52)ng/mL;UIA组(61.87±22.18)ng/mL(每组样品重复三次,如图1)。
然后,每组单独10个样品的Axl质量浓度分别为:HC组 (52.27±29.00)ng/mL; DC组 (93.51±38.45)ng/mL; RIA组 (140.90±28.59) ng/mL;UIA组 (55.34±34.80)ng/mL(图1B)。由此可见,单独检测10个样品的Axl均数与合并样品基本接近。单因素方差分析显示,与HC组相比,RIA组的Axl质量浓度显著增加(q=3.956, P<0.01);但UIA组差异无统计学意义(P>0.05)。虽然DC组与HC组相比,Axl质量浓度也显著增加(P<0.05),但是RIA组与DC组相比,Axl质量浓度也显著增加(q=4.547, P<0.01),因此Axl在RIA中的增加具有特异性。
然后在另一批性别、年龄匹配的患者和对照,每组20个样品同时采集脑脊液和血液标本,检测4组的Axl质量浓度:HC组 (71.18±42.74)ng/mL; DC组(81.75±45.66)ng/mL; RIA组(107.30±41.49)ng/mL;UIA组(54.90±31.86)ng/mL(图2A)。单因素方差分析显示,与HC组相比,RIA组的Axl质量浓度显著增加(q=4.254, P<0.05);DC组和UIA组差异无统计学意义(P>0.05)。虽然RIA组Axl的均数略高于DC组,但差异无统计学意义(P>0.05)。血浆中的Axl质量浓度比脑脊液高10倍以上,但是4组的变化趋势与脑脊液中定量结果基本一致。血浆中Axl质量浓度分别为:HC组(804.5±345.1)ng/mL; DC组(976.0±402.6)ng/mL; RIA组(1252.0±601.4)ng/mL;UIA组(835.9±494.2)ng/mL(图2B)。单因素方差分析显示,与HC组和UIA组相比,RIA组Axl质量浓度显著增加(q=4.254和3.956, P<0.05);但與DC组相比,RIA组Axl的均数略高,但差异无统计学意义(P>0.05)。Pearson相关性分析表明,血浆与脑脊液中的Axl质量浓度显著相关(P<0.01),相关性系数r2=0.774(图3)。
最后,笔者利用ROC分析,评价CSF和血浆中Axl的质量浓度作为候选的生物标志物的灵敏度和特异度。CSF中Axl质量浓度的ROC分析结果显示,RIA能较好地和UIA区分,AUC为0.83,95%特异性时的灵敏度为60%,P<0.01;同时RIA也能够较好地与HC区分,AUC为0.732 5,但95%特异度时的灵敏度仅为15%,P<0.05(表4)。血浆中Axl质量浓度的ROC分析结果显示,RIA能够较好地与HC区分,AUC为0.72, 95%特异度时的灵敏度为40%,P<0.05。同时RIA也能够较好地与UIA区分,AUC为0.705, 95%特异度时的灵敏度为25%,P<0.05(表5)。
3 讨论
蛋白质的糖基化是最重要的翻译后修饰之一,目前发现的蛋白质中有一半以上有糖基化修饰[11]。尤其是存在于细胞外环境的蛋白如各种体液、分泌蛋白和细胞外基质蛋白等。并且,糖基化修饰对蛋白质的功能有重要影响,如蛋白质的折叠和运输等[12];丝氨酸、苏氨酸残基的乙酰氨基葡萄糖化与信号转导密切相关[13];蛋白质的糖基化程度以及糖链结构的异常变化常常与肿瘤等疾病相关[14-15];参与免疫或炎症反应的几乎所有的关键性分子都是糖蛋白[16]。笔者在4组人CSF中鉴定的294个蛋白中有142个蛋白有明确的糖基化修饰位点,并包含了各种形式的糖基化修饰。另外,132个蛋白在数据库中明确注释为细胞外基质蛋白、分泌蛋白或是细胞膜相关蛋白。其余的蛋白大部分定位不明。
本研究一共鉴定了116个在RIA和(或)UIA中发生特异改变的蛋白,其功能涉及免疫与炎症反应、细胞黏附和细胞外基质的组成、重建与降解等,均与IA的形成和破裂相关[17-18]。在这发生改变的116个蛋白中,既有原来已经有报道的与IA或其他动脉瘤如腹主动脈瘤相关的蛋白,如蛋白酶抑制剂α2微球蛋白(α2-microglobin);也有在血管内皮细胞的损伤修复和再生等过程中发挥重要作用的蛋白,如色素上皮衍生因子(Pigment epithelium-derived factor,PEDF))和Axl等。
Axl最初在肿瘤细胞中被发现,在各种细胞中(如血管内皮细胞和平滑肌细胞等)都有广泛表达,并且在许多慢性疾病中有表达增高或活性增加[19-20]。它的两个主要配体是生长休止特定蛋白6(growth-arrest-specific protein 6, Gas6)和蛋白S(protein S)。Axl介导的信号通路在各种类型细胞的存活、生长、聚集、迁移以及抗炎症反应中发挥调节作用。目前认为,Axl信号通路主要有四种激活形式:(1)配体(聚化,引起细胞内酪氨酸激酶结构域的自身磷酸化,使得Axl能与PI3K、PLC、Grb2等结合,调节细胞的存活和增殖等[19]。Gas6/Axl信号通路能够通过激活SHP-2(Src homolog 2 domain containing protein tyrosine phosphatase 2)抑制血管内皮生长因子受体2的激活[21-22]。(2)两个相邻细胞的Axl受体的细胞外结构域可以互相结合而激活,但不依赖其酪氨酸激酶活性。(3)配体非依赖的Axl二聚化和自身磷酸化激活。有研究报道,活性氧在血管平滑肌细胞(vascular smooth muscle cell,VSMC)中通过Gas6不依赖的方式促进Axl的磷酸化,这种方式在氧化应激或Axl受体过量表达的病理情况下更有意义[23]。(4) Gas6与Axl 结合后还可导致Axl的细胞外结构域被剪切,形成可溶性的sAxl-Gas6复合物,而抑制配体依赖的激活信号。Gas6/Axl信号通路在生理性的固有免疫反应中发挥关键的调节作用,干扰素α/β受体能激活Gas6/Axl信号通路,通过激活促炎信号的抑制因子如Twist等进而抑制Toll样受体和细胞因子发挥抗炎作用[24]。但是,在乳腺癌中却发现抑制Axl降低了促炎性细胞因子的表达。可见,在病理条件下,Axl依赖的信号在炎症中可能有不同于生理稳态中的调节作用。Gas6/Axl信号通路还在心血管系统尤其在病理状态下发挥重要作用。在Axl基因敲除的小鼠中发现Axl在血管重建中发挥作用[22]。VSMC损伤时,能通过自分泌机制诱导多种生长因子(包括PDGF和Gas6)以及生长因子受体(包括PDFGR和Axl)的表达,Gas6/Axl能激活PI3K/Akt促进VSMC和内皮细胞的存活。有研究发现,Gas6的血浆浓度与腹主动脉瘤的大小呈正相关而与sAxl则呈负相关,提示Axl信号可能与其发病机制相关,而且血浆中的Gas6/sAxl的比例可作为该病的生物标志物[25]。本研究发现Axl特异性地在RIA的CSF和血浆中增高,提示Axl可能成为RIA的生物标志物,而且Axl依赖的信号通路可能在IA的形成和破裂中发挥了关键性的作用。
总之,本研究在人CSF和血浆中的蛋白质组学定量研究,发现Axl可成为非常有前景的预测IA破裂的生物标志物,并且深入研究Axl介导的信号通路在IA形成和破裂的作用有助于揭示IA的发病机制和寻找新的治疗靶点。
参考文献
[1]Deruty R, Pelissou-Guyotat I, Mottolese C, et al. Management of unruptured cerebral aneurysms[J]. Neurol Res, 1996, 18(1): 39-44.
[2]谭显西, 钟鸣, 吴近森, 等. 急性破裂性颅内动脉瘤血管内治疗的围手术期处理[J]. 中华急诊医学杂志, 2003, 12(3): 186-187.
[3]吴群, 吴盛, 凌晨晗, 等. 颅内动脉瘤破裂急性期与非急性期手术184例分析[J]. 中华急诊医学杂志, 2010, 19(8): 858-861.
[4]Nahed BV, Bydon M, Ozturk AK, et al. Genetics of intracranial aneurysms[J]. Neurosurgery, 2007, 60(2): 213-226.
[5]Wiebers DO, Whisnant JP, Huston J 3rd, et al. Unruptured intracranial aneurysms: natural history, clinical outcome, and risks of surgical and endovascular treatment[J]. Lancet, 2003, 362(9378): 103-110.
[6]Raymond J, Meder JF, Molyneux AJ, et al. Unruptured intracranial aneurysms: the unreliability of clinical judgment, the necessity for evidence, and reasons to participate in a randomized trial[J]. J Neuroradiol, 2006, 33(4): 211-219.
[7]Weir B. Unruptured intracranial aneurysms: a review[J]. J Neurosurg, 2002, 96(1): 3-42.
[8]Salary M, Quigley MR, Wilberger JE Jr. Relation among aneurysm size, amount of subarachnoid blood, and clinical outcome[J]. J Neurosurg, 2007, 107(1): 13-17.
[9]Frosen J, Tulamo R, Paetau A, et al. Saccular intracranial aneurysm: pathology and mechanisms[J]. Acta Neuropathol, 2012, 123(6): 773-786.
[10]Hashimoto T, Meng H, Young WL. Intracranial aneurysms: links among inflammation, hemodynamics and vascular remodeling[J]. Neurol Res, 2006, 28(4): 372-380.
[11]Hagglund P, Bunkenborg J, Elortza F, et al. A new strategy for identification of N-glycosylated proteins and unambiguous assignment of their glycosylation sites using HILIC enrichment and partial deglycosylation[J]. J Proteome Res, 2004, 3(3): 556-566.
[12]Jimenez D, Roda-Navarro P, Springer TA, et al. Contribution of N-linked glycans to the conformation and function of intercellular adhesion molecules (ICAMs)[J]. J Biol Chem, 2005, 280(7): 5854-5861.
[13]Halim A, Ruetschi U, Larson G, et al. LC-MS/MS characterization of O-glycosylation sites and glycan structures of human cerebrospinal fluid glycoproteins[J]. J Proteome Res, 2013, 12(2): 573-584.
[14]Durand G,Seta N. Protein glycosylation and diseases: blood and urinary oligosaccharides as markers for diagnosis and therapeutic monitoring[J]. Clin Chem, 2000, 46(6 Pt 1): 795-805.
[15]Ungar D. Golgi linked protein glycosylation and associated diseases[J]. Semin Cell Dev Biol, 2009, 20(7): 762-769.
[16]Rabinovich GA, van Kooyk Y, Cobb BA. Glycobiology of immune responses[J]. Ann N Y Acad Sci, 2012, 1253: 1-15.
[17]Chalouhi N, Ali MS, Jabbour PM, et al. Biology of intracranial aneurysms: role of inflammation[J]. J Cereb Blood Flow Metab, 2012, 32(9): 1659-1676.
[18]Krings T, Mandell DM, Kiehl TR, et al. Intracranial aneurysms: from vessel wall pathology to therapeutic approach[J]. Nat Rev Neurol, 2011, 7(10): 547-559.
[19]Korshunov VA. Axl-dependent signalling: a clinical update[J]. Clin Sci (Lond), 2012, 122(8): 361-368.
[20]OBryan JP, Frye RA, Cogswell PC, et al. Axl, a transforming gene isolated from primary human myeloid leukemia cells, encodes a novel receptor tyrosine kinase[J]. Mol Cell Biol, 1991, 11(10): 5016-5031.

