探讨门控SPECT心肌灌注显像在慢性心衰患者心脏再同步化治疗中的临床应用价值
李 婷,徐文贵,李剑明,卢如明,梁 钰
(1.天津医科大学肿瘤医院分子影像及核医学诊疗科 国家肿瘤临床医学研究中心 天津市肿瘤防治重点实验室,天津 300060;2.泰达国际心血管病医院,天津 300457)
探讨门控SPECT心肌灌注显像在慢性心衰患者心脏再同步化治疗中的临床应用价值
李婷1,徐文贵1,李剑明2,卢如明2,梁钰2
(1.天津医科大学肿瘤医院分子影像及核医学诊疗科 国家肿瘤临床医学研究中心 天津市肿瘤防治重点实验室,天津300060;2.泰达国际心血管病医院,天津300457)
目的:探讨门控SPECT心肌灌注显像(GSMPI)在慢性心力衰竭(CHF)患者心脏再同步化治疗(CRT)及其预后评估中的临床应用价值。材料和方法:2012年1月—2014年6月行CRT植入且术前行GSMPI的CHF患者21例,经显像获得相位直方图带宽(PHB)、相位标准差(PSD)、左心室射血分数(LVEF)、左室舒张末容积(EDV)、静息灌注评分(SRS)及疤痕面积(SS)等功能参数。所有患者于CRT后半年复查心脏超声,以左室舒张末期内径缩小、LVEF增高(差值>5%),且半年内无再住院记录为CRT有效,将入选患者分为有效组及无效组。比较两组患者各项参数间的差异、分析其对CRT疗效的预测价值。同时记录左室内最迟激动部位。结果:CRT有效组15例(71.4%),无效组6例(28.6%),两组患者各参数之间均有统计学差异(P均<0.05),其中以PSD、PHB差异最显著(P<0.01)。左室内最迟激动部位位于心尖部、前壁、间壁者10例(47.6%),下壁者6例(28.6%),侧壁者5例(23.8%)。结论:GSMPI能够“一站式”提供多项功能参数,心脏收缩同步性定量参数及心肌梗死疤痕面积等可应用于预测术后疗效,其中PSD、PSW具有更高的预测价值;参考左室内最迟激动点及心梗疤痕部位,可应用于指导CRT电极植入。
心力衰竭,充血性;体层摄影术,发射型计算机,单光子;门控血池显像
心脏再同步化治疗(CRT)在慢性心力衰竭(CHF)上的临床疗效已得到肯定,它通过纠正心脏机械收缩失同步,逆转心脏重构,改善心功能,进而延缓心衰进展。但是,严格按照CRT指南筛选的患者中仍有20%~40%表现为低反应或无反应,CRT的低反应率问题已成为心电生理领域的研究难点[1-2]。因此,分析CRT的影响因素并找到能有效预测疗效的最佳指标对于指导临床早期干预、优化治疗方案,提高CRT的反应率至关重要。
应用门控SPECT心肌灌注显像(GSMPI)指导CRT已成为国际上的研究热点,该方法的优势在于可通过一次成像 “一站式”评价心脏机械收缩失同步、定位心脏最迟收缩部位、定量心肌血流受损范围、定位及定量心脏疤痕负荷,同时测定左室容积及射血分数,能够为CRT术前筛选患者、术中电极植入及预后判断提供十分有效的指导。本研究旨在探讨GSMPI法在慢性心衰患者心脏再同步化治疗及预测疗效上的临床应用价值。
1 材料与方法
1.1临床资料
2012年1月—2014年6月本院收治的行CRT治疗的慢性心力衰竭患者21例,其中男16例,女5例,平均(60.5±6.2)岁,所有患者心功能NYHA分级为Ⅲ~Ⅳ级,超声心动图示左心室舒张末期内径>55mm,左室射血分数<35%。其中,缺血性心肌病17例,扩张型心肌病4例。因采用心电图门控采集技术,持续性心房颤动心律绝对不齐者不被入组。
1.2扫描技术
患者于静息状态下,行静脉注射显像剂99mTc-MIBI 740~925 MBq(放化纯度>95%,由原子高科股份有限公司提供)。约40 min后行GSMPI,采用美国GE Millennium VG-5双探头扫描仪,运用门控采集技术,以心电图R波做为触发电位,在每个心动周期内,探头共旋转180°,每6°采集一帧,每25 s/帧,共采集30帧。将若干个心动周期的同一时间点的信号叠加在一起,通过计算机处理获得各种功能图像。
1.3图像后处理方法
将原始数据经Emory Cardiac Toolbox软件进行处理,心脏同步性分析应用位相分析技术,经计算机自动重建后得到左室短轴、水平长轴及垂直长轴三轴面心肌灌注断层显像及极坐标靶心图,半定量法计算总静息灌注评分(SRS)(灌注正常为0分;放射性计数轻度减低为1分;中度减低为2分;重度减低为3分;灌注缺损为4分)(图1)。以低于左室心肌内最高计数50%的区域为心肌梗死疤痕区,获得疤痕面积(SS)(图2)。
应用位相分析技术,得到心脏各个位点的收缩时相分布,按收缩先后以不同的色阶显示出来,即相位图、相位直方图(图3),计算机自动测定相位直方图带宽(PHB)、相位标准差(PSD),同时自动获得心脏收缩时相电影,动态观察并定位心脏最迟收缩部位。同时获得心室功能曲线及左室舒张末期容积(EDV)、左室射血分数(LVEF)等定量参数。
1.4图像及数据的评价方法
入选患者CRT术前均行GSMPI,获得PHB、PSD、SRS、SS、EDV、LVEF。术后半年行心脏超声,以左室舒张末期内径缩小、左室射血分数增高(差值>5%),且半年内无再住院记录为CRT有效,将入选患者分为有效组及无效组。比较两组患者各项参数的差异、分析其对CRT疗效的预测价值。相关数据采用SPSS 19.0版软件包统计分析,单样本计量资料以均数±标准差表示,组间比较采用独立样本t检验,P<0.05为差异有统计学意义。统计左室内最迟收缩部位的分布情况。
2 结果
CRT有效组及无效组各项参数相比,P值均<0.05,表明两组患者各项参数间有统计学差异,P值排序依次为PSD<PHB<SS<SRS<EDV<LVEF。其中,PSD、PHB两组间差异最显著(P<0.01)(表1)。
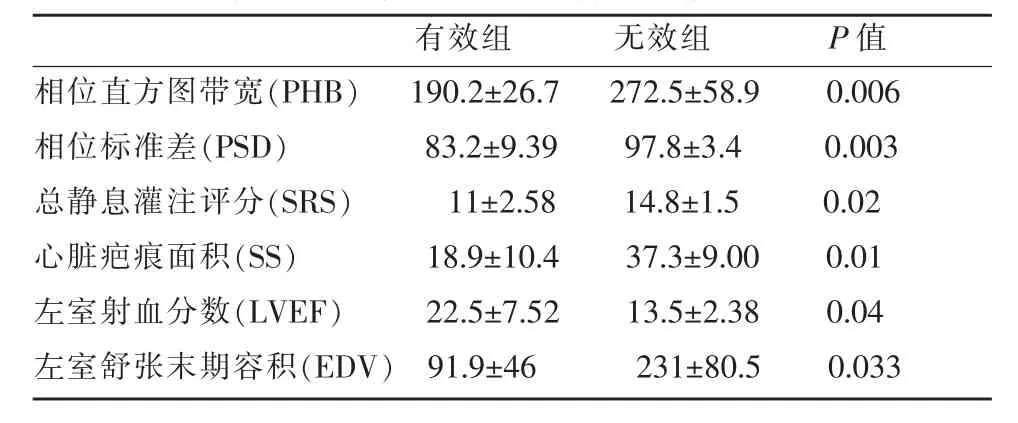
表1 有效组及无效组GSMPI各项参数间差异比较表
左室内最迟收缩部位分别位于心尖、前壁、间壁10例(47.6%)、下壁6例(28.6%)及侧壁5例(23.8%)。
GSMPI对心肌血流灌注及疤痕负荷的显示见图1~2。
GSMPI评价心脏收缩同步性的功能图像见图3。
3 讨论
CRT的无反应率问题仍持续存在[2-3],已成为目前临床治疗的一大挑战。其主要原因包括:①CRT前能否准确筛选左室机械收缩失同步的患者;②瘢痕心肌的定位及定量:左室电极植入处是否避开疤痕区,坏死心肌范围是否已失去植入CRT的意义;③明确心脏最迟收缩部位,是否将最迟激动点作为电极植入点等。研究表明,左室电极植入处远离最迟收缩部位会导致CRT无反应,甚至明显增加术后患者的死亡率[4]。因此,如果能够准确评估上述定性及定量指标,并将其结果应用于指导CRT实施,无疑将改善CRT无应答,使更多的患者从中受益。
评价心脏收缩同步性的方法有超声组织多普勒技术(TDI)及心电图。尽管一些单中心的研究证实TDI所得参数与CRT疗效间具有较好的相关性[5],但迄今最大的多中心研究——“再同步治疗应答预测因子试验(PROSPECT)[6]”提示,任何单一的TDI参数均不能评估心脏同步性及预测CRT疗效,原因在于其测量时具有角度和帧频的依赖性[7],对操作者经验要求较高,测量方法缺乏统一的标准。并且TDI无法定量心肌血流灌注减低的范围、程度。

图1 (左图)短轴、垂直长轴及水平长轴三轴面心肌灌注显像图,可见下壁中段及基底段、下间壁基底段及下侧壁显像剂分布明显稀疏、缺损;(右图)总静息灌注评分示33分。 图2 显示心肌梗死疤痕面积。阈值设定为50%,梗死疤痕面积占左心室面积的42%,其中右冠状动脉(RCA)供血区域内灌注缺损面积为95%,提示RCA为“罪犯”血管。Figure 1. The left image shows the myocardial perfusion imaging in the short axis,the vertical long axis and the horizontal long axis. The distribution of the imaging agent is obviously sparse or defects in the middle and the base of the inferior wall,the base of the inferiorseptal wall and the inferior-lateral wall.The right image shows the summed rest score is 33. Figure 2. The size of the myocardial infarction scar(SS).We make 50%as the threshold value,the SS is 42%of the area of the left ventricle,within which the right coronary artery(RCA)regional blood perfusion defect area is 95%,so the RCA is the“criminal”vessel.

图3 男,45岁,临床诊断为陈旧性下壁心肌梗死;经GSMPI显像获得相位图(左图)及相位直方图(右图)。色阶条蓝、紫、红、白,依次代表收缩由早至晚。左图红色箭头处为最迟收缩部位,位于左室下间壁,其次为黄色箭头所指处,位于左室下壁。Figure 3. Male,45y.The clinical diagnosis is old myocardial infarction in the inferior wall.The phase image and the phase histogram image are acquired through the GSMPI.The color blue,purple,red,white,followed by representatives of contraction early to late systolic.In the left image,the red arrow indicates the latest contraction area is located in the inferior-septal wall of the left ventricular.Addition to it,the latest contraction is the inferior wall which is indicated by the yellow arrow.
GSMPI位相分析技术应用于评估心脏收缩同步性近年来开始见诸报道。该法是通过门电路技术,以不同的色阶代表心脏开始收缩及其传导的顺序,从而观察心室内是否存在局部收缩延迟、定位最迟收缩部位。同时获得一系列定量参数,主要包括:PHB,其值越小提示心脏收缩同步性越好;PSD,其绝对值越小代表相位分布越集中,心脏收缩协调性越好;二者的应用价值已得到证实[8]。所有定量参数均由计算机软件自动获得,不受人为因素干扰,可重复性好。研究证实,采用心脏专用软件全自动处理所得心脏收缩失同步参数与有经验操作者手动计算的结果相关性很好,结果具有很高的特异度及灵敏度[9-10]。
GSMPI法同时能够显示心肌血流灌注情况,定位及定量心肌疤痕负荷。Schinkel等[11]研究表明,对显像中出现的不可逆性缺损区作定量分析,可准确识别心肌梗死区内的疤痕组织。研究证实,硝酸酯药物介入后行GSMPI,对于存活心肌的测定结果与“金标准”-18F-FDG PET显像具有很好的相关性,且花费低、便于操作,具有更加广泛的实用价值[12-13]。研究发现,缺血性心肌病与非缺血性心肌病患者因心肌疤痕负荷程度不同,植入CRT的预后也不同:非缺血性心肌病组生存率更高;缺血性心肌病组中,GSMPI所示疤痕负荷少者对CRT具有和非缺血性心肌病患者相似的反应。反之,疤痕负荷重者植入CRT后,左室功能无明显改善,生存率亦相对较差[14]。
本研究结果显示心脏疤痕负荷定量指标可用于判断CRT的预后,存在大面积心梗疤痕者对CRT的反应较差,甚至无法从中获益。这与以往的研究结果一致,原因可能为CRT不能完全纠正大量疤痕及组织纤维化所导致的心脏室壁运动障碍[15]。研究也证实了心脏收缩失同步的程度与CRT疗效密切相关,21例患者中15例有效,其定量指标相位直方图带宽及相位标准差较无效组小,失同步程度较无效组低,结果与Henneman等[16]研究结果一致。同时,本研究通过GSMPI位相动态电影所显示的心脏激动传导顺序,直接定位左室内最迟收缩部位,为CRT术中选择电极植入点提供依据。
GSMPI的最大优势在于通过一次显像即可获得多项信息,综合分析心脏最迟收缩部位及梗死疤痕区的位置,可用于指导CRT电极的植入,即在避开疤痕区的前提下,选择最迟激动点作为左室电极植入点,以最大程度地发挥起搏器的作用,强化患者对CRT的反应。而GSMPI所显示的心脏收缩失同步及心脏疤痕负荷的程度又可用于指导CRT筛选合适患者,判断CRT预后。实践表明,应用GSMPI法联合心肌血流灌注及心脏收缩同步性可明显提高对CRT预后判断的敏感性[17]。此外,GSMPI所得定量参数还能够用于评价CRT术前术后心脏收缩失同步及心功能的变化,评估CRT疗效,且具有很好的重复性。
综上,SPECT门控心肌灌注显像从理论及方法学上都具备了在CRT及其预后判断乃至疗效评估中的实际应用价值,优于其他方法的是它的 “一站式”多功能性以及良好的可重复性,能够合理利用医疗资源,减少重复检查。尽管核素显像具有少量的放射性,但其辐射量完全符合国家放射防护相关标准,且药物仅需数小时即可衰变、排出,因此与GSMPI产生的诊断效益相比,其辐射量十分微小,检查相当安全。
[1]Chinitz JS,d'Avila A,Goldman M,et al.Cardiac resynchronization therapy:who benefits?[J].Ann Glob Health,2014,80(1):61.
[2]Bordachar P,Eschalier R,Lumens J,et al.Optimal Strategies on avoiding CRT nonresponse[J].Curr Treat Options Cardiovasc Med,2014,16(5):299.
[3]孙茜,李晶洁.机械不同步评价临床心脏再同步化治疗的进展[J].中华临床医师杂志:电子版.2013,9(7):158.
[4]Ypenburg C,Bommel RJ,Delgado V,et al.Optimal left ventricular lead position predicts reverse remodeling and survival after cardiac resynchronization therapy[J].J Am Coll Cardiol,2008,52(17):1402.
[5]戴玫,张盛翠.超声心动图在慢性心力衰竭的再同步治疗中的应用[J].心血管病学进展,2009,30(2):328.
[6]Chung ES,Leon AR,Tavazzi L,et al.Results of the predictors of response to CRT(PROSPECT)Trial[J].Circulation,2008,117(20):2608.
[7]巩雪,,宿燕岗,潘文志,等.常用临床和超声指标对心脏再同步化治疗效果的预测价值[J].中华临床医师杂志:电子版,2011,5(2):34.
[8]Boogers MM,Van Kriekinge SD,Henneman MM,et al.Quantitative gated SPECT-derived phase analysis on gated myocardial perfusion SPECT detects left ventricular dyssynchrony and predicts response to cardiac resynchronization therapy[J].J Nucl Med,2009,50(5):718.
[9]Zhou Y,Faber TL,Patel Z,et al.An automatic alignment tool to improve repeatability of left ventricular function and dyssynchrony parameters in serial gated myocardial perfusion SPECT studies[J]. Nucl Med Commun,2013,34(2):124.
[10]Lalonde M,Birnie D,Ruddy TD,et al.SPECT blood pool phase analysis can accurately and reproducibly quantify mechanical dyssynchrony[J].J Nucl Cardiol,2010,17(5):803.
[11]Schinkel AF,Valkema R,Geleijnse ML,et al.Single-photon emission computed tomography for assessment of myocardial viability[J].Eur Interv,2010,6(Suppl G):G115.
[12]Tsai JP,Yun CH,Wu TH,et al.A meta-analysis comparing SPECT with PET for the assessment of myocardial viability in patients with coronary artery disease[J].Nucl Med Commun,2014,35(9):947.
[13]Raja S,Singh B,Rohit MK,et al.Comparison of nitrate augmented Tc-99m tetrofosmin gated SPECT imaging with FDG PET imaging for the assessment of myocardial viability in patients with severe left ventricular dysfunction[J].J Nucl Cardiol,2012,19(6):1176.
[14]Evan C,Hidekazu T,Prem S,et al.Impact of scar burden by single-photon emission computed tomography myocardial perfusion imaging on patient outcomes following cardiac resynchronization therapy[J].Eur Heart J,2011,32(1):93-103.
[15]Keida T,Morishima I,Tsuchiya T,et al.Detection of regional low myocardial perfusion helps predict a response to cardiac resynchronization therapyinpatientswithnon-ischemiccardiomyopathy:find index by nuclear imaging for dyssynchrony(find)study[J].JACC,2010,55(10-Sup1):A24.E225.
[16]Henneman MM,Chen J,Dibbets-Schneider P,et al.Can LV dyssynchrony as assessed with phase analysis on gated myocardial perfusion SPECT predicts response to CRT?[J].J Nucl Med,2007,48(7):1104-1111.
[17]Chalil S,Foley PWX,Muyhaldeen SA,et al.Late gadolinium enhancement cardiovascular magnetic resonance as a predictor of response to cardiac resynchronization therapy in patients with ischemic cardiomyopathy[J].Europace,2007,9(11):1031-1037.
Clinical application value of gated SPECT myocardial perfusion imaging on cardiac resynchronization therapy in patients with chronic heart failure
LI Ting1,XU Wen-gui1,LI Jian-ming2,LU Ru-ming2,LIANG Yu2
(1.Tianjin Medical University Cancer Institute and Hospital,National Clinical Research Center of Cancer,Laboratory of Cancer Prevention and Therapy,Tianjin 300060,China;2.TEDA International Cardiovascular Hospital,Tianjin 300457,China)
Objective:To investigate the clinical value of gated SPECT myocardial perfusion imaging on cardiac resynchronization therapy(CRT)and evaluate their prognosis in patients with chronic heart failure(CHF).Methods:Twenty one patients with CHF in 2012 January to 2014 June were assigned to CRT,and underwent gated SPECT myocardial perfusion imaging(GSMPI)before operation.Functional parameters including phase histogram bandwidth,phase standard deviation,left ventricular ejection function,end diastolic volume,summed rest scores and scar size were acquired by imaging.All patients underwent a second-time cardiac ultrasonography at the sixth month after operation.Effective therapy was considered when left ventricular end diastolic diameter decreased,LVEF increased,and no hospitalization records existed within half a year.Then,the patients were divided into effective and ineffective groups.The differences between the functional parameters of the two groups were compared,the predictive value for the efficacy of CRT was analyzed,and the latest systolic area in the left ventricule was recorded.Results:Fifteen cases(71.4%)were effective after CRT,and 6 cases(28.6%)were irresponsive.All parameters between the two groups showed significant differences(P<0.05),and PSD and PHB were the most significant(P<0.01).The latest systolic area of the left ventricle was located in the apex,the anterior wall and the septal wall in 10 patients'(47.63%),in the inferior wall in 6 patients(28.6%),and in the lateral wall in 5 patients(23.8%).Conclusion:GSMPI can provide“onestop”multiple functional parameters,which can be used to guide CRT electrode implantation and predict curative effect.PSD and PSW might have a higher predictive value.
Heart failure,congestive;Tomography,emission-computed,single-photon;Gated blood-pool imaging
R541.61;R817.4
A
1008-1062(2015)05-0325-04
2014-10-09;
2015-01-15
李婷(1984-),女,天津人,主治医师。
徐文贵,天津医科大学肿瘤医院分子影像及核医学诊疗科,300060。

