茯苓中多糖含量的测定方法研究*
张文芳,陈丹红
(福建省测试技术研究所, 福建 福州 350003)
茯苓中多糖含量的测定方法研究*
张文芳,陈丹红
(福建省测试技术研究所, 福建 福州 350003)
筛选分光光度法测定茯苓中多糖含量的最优条件,以便快速准确地进行茯苓产品质量评价。方法:采用苯酚—浓硫酸比色法测定茯苓中总糖含量;采用3,5-二硝基水杨酸(DNS)比色定糖法测还原糖含量,相减得多糖含量;同时分别从水浴时间,苯酚和浓硫酸用量等方面考察最优条件;进行了精密度、重复性、稳定性、加样回收率等方面试验。结果:茯苓总糖测定的最优条件为6%苯酚1.0ml,浓硫酸5.0ml,沸水浴15 min;回归方程为回归的标准曲线方程为y=0.0056x,R2=0.9943;测茯苓还原糖的回归的标准曲线方程为y=0.7720x,R2=0.9903。方法操作简便,结果准确可靠,重复性好,可用作茯苓中多糖含量的测定。
茯苓;总糖; 还原糖; 多糖;紫外分光光度法
茯苓为多孔菌科真菌茯苓Poria cocos(Schw.) Wolf的干燥菌核,为我国传统的常用中药材,具有祛湿利尿、健脾和胃、补体强身、安神宁心的作用。茯苓主要化学成分为茯苓多糖、三萜类、树胶、蛋白质和脂肪酸等化合物等。中外学者对茯苓的化学成分及生物活性进行研究,发现其所含的多糖与免疫功能的调节、细胞与细胞的识别、细胞间物质的运输、癌症的诊断与治疗等,都有着密切的关系。大量研究表明植物多糖具有增强机体免疫功能、抗肿瘤、抗病毒、抗衰老、降血糖、刺激造血等多种生物学功效,而且对机体几乎没有毒性。天然多糖化合物作为一种免疫调节剂已越来越多地用于肿瘤、肝炎等疾病的治疗和康复。而艾滋病的肆虐更使天然多糖化合物特别是它的强抗病毒活性的衍生物,成为科学家们尤其是药物学家们高度重视的对象。茯苓中多糖的含量与药效的关系极大,建立茯苓多糖的分析测定体系对于茯苓药材的内在质量控制具有重要意义。文章与以前仅采用采用苯酚—浓硫酸体系测总糖的方法不同,扣除了还原糖的含量,得到茯苓多糖的真实含量。该方法简便、快速,可为进一步研究茯苓种植质量和药理活性提供分析数据。
1 仪器与试剂
1.1 仪器(表1)
1.2 试剂
苯酚,浓硫酸:上海化学试剂有限公司,分析纯;其余均为化学纯,市售。

表1 实验仪器
2 方法及结果
2.1 茯苓多糖测定方法的研究
2.1.1 原理
提取液中不仅含有多糖,还含有一些还原糖如单糖和寡糖,由于无法直接测得溶液中多糖的含量,因此用苯酚-硫酸法测得总糖含量,DNS法测得还原糖含量,然后两者相减即得多糖含量。
茯苓多糖=茯苓总糖-茯苓还原糖
2.1.2 茯苓总糖测定---采用苯酚硫酸法
2.1.2.1 实验原理
苯酚-硫酸试剂可与游离的单糖或寡糖、多糖中的己糖、糖醛酸(或甲苯衍生物)起显色反应,己糖在490 nm(戊糖以及糖醛在480 nm)处有最大吸收,吸收值与糖含量呈线性关系。多糖在硫酸的作用下先水解成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚生成橙黄色化合物。再以比色法测定。
2.1.2.2 标准曲线制作
(1)取9支干净的试管,然后按照表2提供的数据加样。
(2)加完样后静置20min,待显色稳定
(3)以0号试管为空白对照,于490 nm下测溶液的吸光值。
(4)样品含量的测定:取一定量的待侧样品,加水补足2 mL,按上述步骤,测490 nm的光密度,以标准曲线计算总糖含量。
2.1.2.3 苯酚硫酸法测总糖含量的标准曲线(图1)回归的标准曲线方程为y=0.0056x,R2=0.9943。
2.1.3 还原糖含量测定
采用3,5-二硝基水杨酸(DNS)比色定糖法
2.1.3.1 实验原理
还原糖是指含自由醛基或酮基的单糖(如葡萄糖)和某些具有还原性的双糖(如麦芽糖)。它们在碱性条件下,可变成非常活泼的烯二醇。遇氧化剂时,具有还原能力,烯二醇本身则被氧化成糖酸及其他产物。黄色的3,5-二硝基水杨酸(DNS)试剂与还原糖在碱性条件下共热后,自身被还原为棕红色的3-氨基-5-硝基水杨酸。在一定范围内,反应液里棕红色的深浅与还原糖的含量成正比,在波长为540 nm处测定溶液的吸光度,查对标准曲线并计算,便可求得样品中还原糖的含量。(DNS溶液共热后被还原成棕红色的氨基化合物,在一定的范围内还原糖的量和棕红色物质颜色深浅的程度成一定的比例关系。(该方法操作简单,快速,杂质干扰较少)。
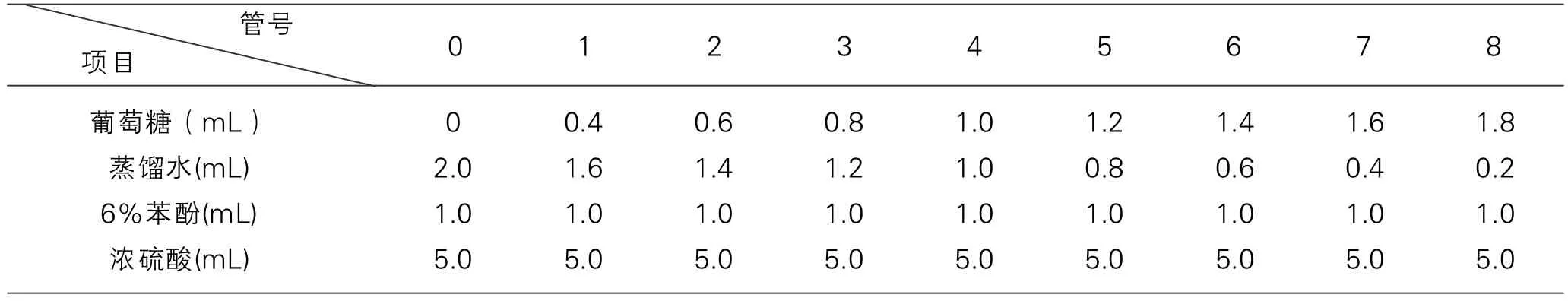
表2
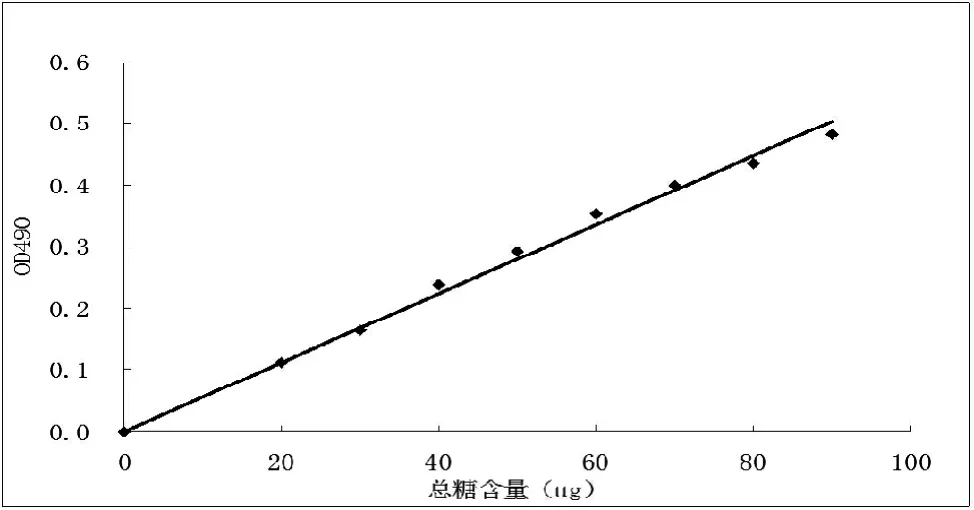
图1 苯酚硫酸法测总糖含量的标准曲线
2.1.3.2 实验试剂
3,5-二硝基水杨酸(DNS)试剂:
甲液:溶解6.9 g结晶酚于15.2 mL10%氢氧化钠溶液中,并用水稀释至69 mL,在此溶液中加6.9 g亚硫酸氢钠。
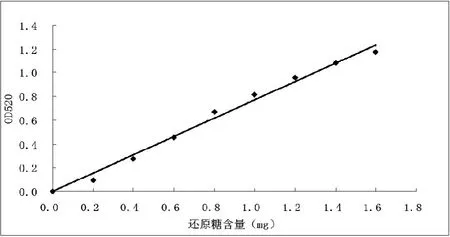
图2 3.5-二硝基水杨酸比色定糖法(DNS)测还原糖含量的标准曲线
乙液:称取255 g酒石酸钾钠加到300 mL10%氢氧化钠溶液中,再加入880 mL1%3,5-二硝基水杨酸溶液。
将甲乙二溶液相混合即得黄色试剂,贮于棕色瓶中备用。在室温放置7~10d以后使用。
2.1.3.3 标准曲线制作
(1) 取9支干净的试管,编号0~8,分别按照表3加入试剂。
(2)加完样后在沸水浴中加热5min,取出,然后立即用流动冷水冷却。
(3)待样品冷却完全后每管中加入21.5 mL蒸馏水,充分摇匀。
(4)以0号管为空白对照,于520 nm下测光吸收值。
(5)样品含量的测定:取一定量的待侧样品加水补足2 mL,按上述步骤,测得其520 nm的光吸收值。根据标准曲线方程即可算出还原糖含量。
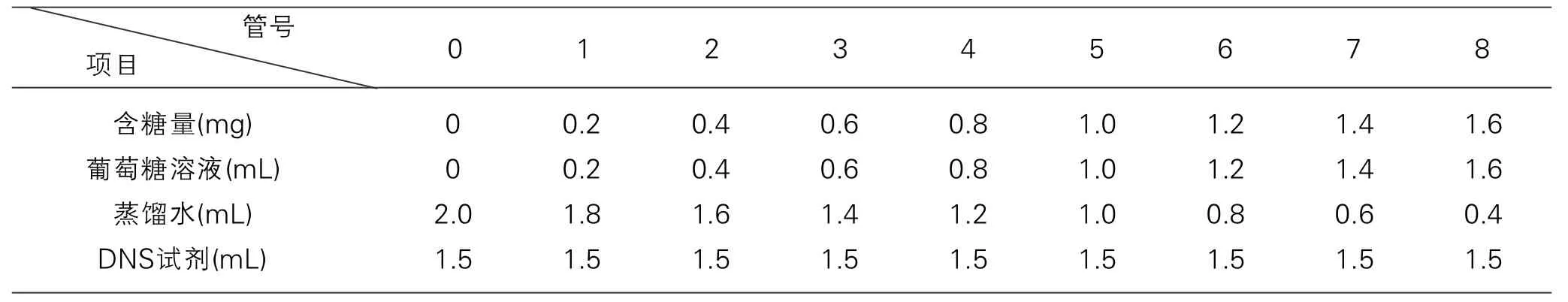
表3
2.1.3.4 3.5-二硝基水杨酸比色定糖法(DNS)测还原糖含量的标准曲线(图2)
回归的标准曲线方程为y=0.7720x,R2=0.9903。
2.2 茯苓多糖测定方法的优化
2.2.1 对照品溶液制备:精密称取105℃干燥 恒重的葡萄糖50mg与50ml容量瓶中用水溶解并定容,摇匀。精密吸取5ml于50ml容量瓶中,加水至刻度,摇匀,即得 0.1mg.mL-1的对照品溶液。
2.2.2 苯酚用量选择:精密称取对照品溶液各1.0ml的5份,分别加入6%苯酚0.6、0.8、1.0、1.2、 1.4 mL,混匀,每份分别缓慢加入浓硫酸5 mL并搅拌,充分摇匀,静至5min后再置沸水浴中 加热15min,取出,冷却至室温,在490nm处测吸光度。结果如表4。选择6%苯酚用量为1.0 mL。
2.2.3 浓硫酸用量选择:精密称取对照品溶液1.0ml的5份,各加入6%苯酚1.0ml,分别缓慢加入浓硫酸4.0,4.5 , 5.0,5.5,6 mL,并搅拌,充分摇匀,静至5min后再置沸水浴中 加热15min,取出,冷却至室温,在490nm处测吸光度。结果如表5。选择浓硫酸用量为5.0 ml。
2.2.4 水浴时间选择:精密称取对照品溶液1.0mL的5份,各加入6%苯酚1.0mL,分别缓慢加入浓硫酸5.0 mL 并搅拌,充分摇匀,静至5min后再置沸水浴中加热分别为5、10、15、20、25min,取出,冷却至室温,在490nm处测吸光度。结果如表6。选取水浴时间为15min。
2.2.5 样品的测试及精密度实验: 称取同一批茯苓粉末(过60目筛)各1.0g 6份,按上述测定总糖和还原糖方法测定后相减得多糖含量,平行测定茯苓多糖含量为0.725 mg.mL-1,RSD为1.07%(n=6),结果见表7,表明精密度良好。
2.2.6 加样回收率实验及标准偏差: 称取同一批茯苓粉末(过60目筛)各1.0g 3份,分别加入葡萄糖供试品10 mL(1 mg.mL-1)的母液。按最优的测定条件测总糖和还原糖,测定后相减得多糖含量,平行测定3次茯苓多糖的回收量,计算得平均回收率为:102.39%,RSD为0.36%(n=3),表明回收率良好,结果见表8。
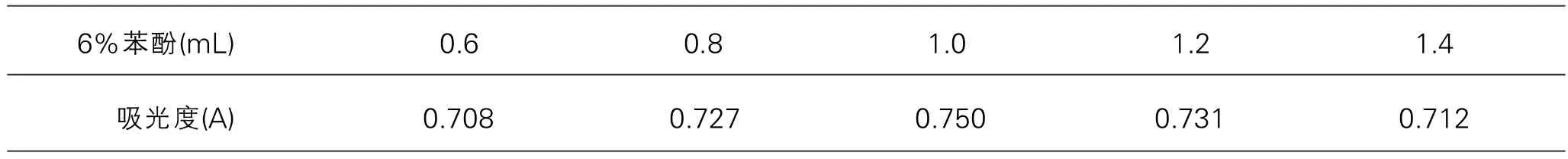
表4 6%苯酚不同用量实验结果

表5 浓硫酸不同用量实验结果

表6 水浴不同时间实验结果
2.2.7 稳定性试验:精确称取同一供试液1 mL,按含量测定方法的最佳条件操作,以试剂空白作对照,每隔30min 测一次吸光度,考察样品3h内的稳定性,结果表明供试样品在3小h内显色稳定。
3 结论
采用苯酚—浓硫酸比色法测定茯苓中总糖含量;采用3,5-二硝基水杨酸(DNS)比色定糖法测还原糖含量,相减得多糖含量;建立的这个方法体系测量结果比用苯酚—浓硫酸比色法算多糖的结果更精确;方法的重现性,稳定性,精密度,回收率都达到了检测要求,该方法未见报道可作为茯苓产品质量监控的有效方法。
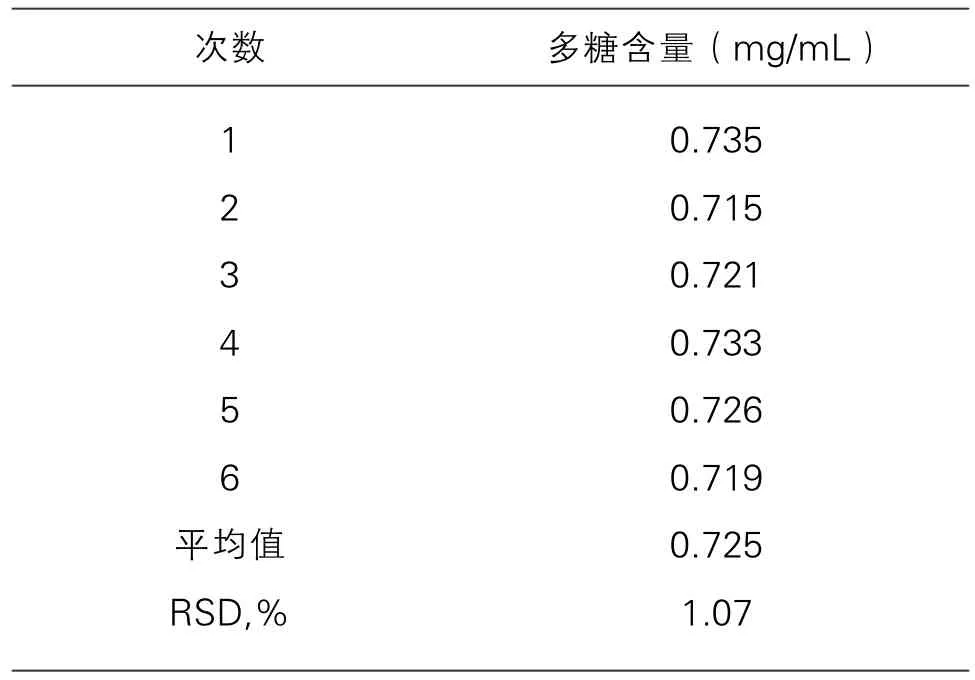
表7 精密度实验结果
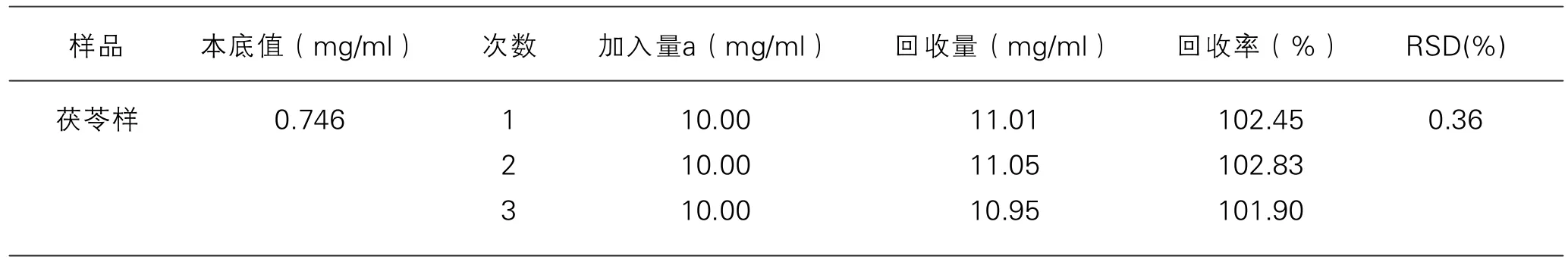
表8 回收率及相对标准偏差(RSD)
[1]国家中医药管理局《中华本草》编委会.中华本草上册[M].上海:上海科学技术出版社,1999,554.
[2]仲兆金,刘浚.分光光度法测定茯苓有效成分的最优条件研究[J].亚太传统医药,2014,1.10(2):17-18.
[3]张思番,刘静涵,蒋建勤,周咏梅.茯苓化学成分和药理作用及开发利用[J].中华实用中西医杂志,2005,18(2):227-230.
[4]丁诚实.分光光度法测定茯苓活性成分的含量[J].食品工程,2008,33(4):26-28.
[5]胡明华,梁永威,彭川丛 .不同产地不同规格的茯苓水溶性多糖含量比较[J].中国药业,2012,21(7):10-11.
[6]沈玉萍,李军,贾晓斌.中药茯苓化学成分的研究进展[J].南京中医药大学学报,2012,28.(3):297-300.
[7]周燕霞,唐明林,殷辉安,等.茯苓中多糖的提取及含量测定[J].天然产物研究与开发,2013,15(4):330-333.
O652
A
1007-550X(2015)05-0035-05
10.3969/j.issn.1007-550X.2015.05.002
*福建省科技厅项目----‘茯苓产品质量标准的研制 ’(2011R1007-4)资助。
2015-04-13
张文芳(1963-),女,工程师。

