基于高内涵分析的何首乌对肝窦内皮细胞损伤的配伍减毒研究△
庞晶瑶,李雨萌,柏兆方,赵艳玲,赵奎君,马致洁*,王伽伯*,肖小河
(1.首都医科大学附属北京友谊医院,北京 100050;2.解放军302医院 全军中药研究所,北京 100039;3.云南中医学院 中药学院,云南 昆明 650500)
·基础研究·
基于高内涵分析的何首乌对肝窦内皮细胞损伤的配伍减毒研究△
庞晶瑶1,2,李雨萌3,柏兆方2,赵艳玲2,赵奎君1,马致洁1*,王伽伯2*,肖小河2
(1.首都医科大学附属北京友谊医院,北京 100050;2.解放军302医院 全军中药研究所,北京 100039;3.云南中医学院 中药学院,云南 昆明 650500)
目的:观察何首乌对肝窦内皮细胞损伤的配伍减毒情况,为其临床合理用药提供参考。方法:采用高内涵分析技术,检测何首乌与茯苓、甘草、三七在肝窦内皮细胞上的配伍减毒情况。结果:何首乌对肝窦内皮细胞的损伤呈剂量依赖性,在IC50的剂量下,分别配伍不同浓度的茯苓、甘草、三七都有显著的减毒作用,且呈剂量依赖性。何首乌配伍茯苓减毒的效果较好,甘草次之,三七稍差。结论:采用高内涵分析方法更加直观、具体地反映何首乌与茯苓、甘草、三七的配伍减毒效果,为临床用药的安全性、合理性提供依据。
何首乌;配伍减毒;肝窦内皮细胞;高内涵分析
近年来,临床上服用何首乌致肝损伤的病例日益增多,作为“四大仙草”之一的常用补益类中药,何首乌的安全性受到质疑。2013年10月、2014年7月我国食品药品监督管理总局(CFDA)相继出台关于何首乌及其相关制剂的通告,提示口服何首乌及其成方制剂可能有引起肝损伤的风险。我国传统的中药减毒方法有两种,分别为炮制减毒和配伍减毒。本文拟从配伍减毒的角度出发,在细胞水平上对何首乌配伍减毒情况进行研究。
何首乌作为保健类中药,在中国历史上有广泛的应用,但古人对其导致肝损伤的记载很少。据本草考证:“首乌以茯苓为使”,古人多强调首乌与茯苓配伍使用。2013年CFDA提示关注的5个含何首乌的制剂(养血生发胶囊、首乌丸、首乌片、首乌延寿片、首乌延寿颗粒)皆没有与茯苓配伍使用。文献研究发现,何首乌配伍茯苓的现代研究较少。合适的配伍方法是否有助于降低何首乌的肝毒性,值得我们去深入研究。在临床上被广泛使用的解百药毒、调和诸药的甘草与何首乌配伍使用是否有助于缓和何首乌的毒性,也未见报道。另外,近期课题组在研究何首乌的肝毒性时发现,其能导致肝脏微循环灌注障碍[1]。活血药(三七)是否能改善首乌引起的微循环障碍,达到减毒的作用,也未见相关报道。肝窦内皮细胞作为肝脏代谢的屏障,大部分药物经肝脏代谢时会首先受累。为此,本研究以原代肝窦内皮细胞为模型,采用高内涵分析方法[2],考察首乌与茯苓、甘草、三七的配伍减毒情况,寻找合适的配伍减毒方法,为临床何首乌的合理用药提供参考。
1 试药和仪器
1.1 试药
肝窦内皮细胞特制基础培养基(武汉原生原代生物医药科技有限公司,批号:Med-0002);胎牛血清、胰蛋白酶(Gibco公司);青霉素;链霉素;磷酸盐缓冲液;96孔板(Costar 3599,康宁公司);二甲基亚砜(DMSO);除菌滤器(25 mm,0.22 μm);细胞培养瓶(430720,康宁公司);Hochest 33342(H3570,生命科学);SYTOX®Orange Nucleic Acid Stain(S11368,生命科学);水为超纯水。茯苓、甘草、三七由解放军第三〇二医院中药房提供;何首乌(北京绿野药业有限公司,批号:13101701)经解放军第三〇二医院肖小河研究员鉴定为蓼科植物何首乌的干燥块根。
1.2 仪器
高内涵筛选系统(Molecular Devices公司);TC10TM自动细胞计数器(Bio-Rad公司);恒温二氧化碳培养箱(NAPCO公司);常规倒置显微镜(上海泽权仪器设备有限公司);台式低速离心机(湖南赫西仪器装备有限公司);超净工作台(苏州净化设备有限公司);回流提取装置、旋转蒸发仪(上海申生科技有限公司);ZK-82B 型真空干燥箱(上海市实验仪器总厂);AL204微量分析天平(Mettler Toledo公司);LGJ-18型冷冻干燥机(北京西四环科学仪器厂);高压蒸汽灭菌器(SN510C,重庆雅马拓科技有限公司)。
2 方法
2.1 样品制备
首乌制备方法:采用50%乙醇冷浸提取2次,每次24 h,提取溶剂为8倍,过滤,合并滤液,减压蒸发浓缩,冷冻干燥得净膏,出膏率为15.7%[3]。
茯苓制备方法:采用加热回流,固液比为1∶12,提取次数为2次,提取时间为100 min,水浴蒸发浓缩,冷冻干燥得净膏,出膏率为2.28%[4]。
甘草制备方法:采用加热回流,加10倍量水,回流提取2次,提取时间分别为1.5、1 h,合并滤液并减压浓缩,冷冻干燥得净膏,出膏率为23.58%[5]。
三七制备方法:10倍量水,加热回流提取2次,提取时间分别为2、1 h,合并滤液并减压浓缩,冷冻干燥得净膏,出膏率为37.17%。
2.2 肝窦内皮细胞毒性评价方法
正常人肝窦内皮细胞购自武汉原生原代生物医药科技有限公司。在含有10%的胎牛血清、100 U·mL-1的青霉素、100 μg·mL-1的链霉素的肝窦内皮细胞特制基础培养基中,37 ℃、5% CO2条件下进行常规培养,实验均在细胞生长对数期进行。细胞均匀接种在96孔板中,每孔5000个细胞,铺板24 h后给药,给药24 h后进行荧光染色。本实验采用二重荧光标记法,用质量浓度为1 μg·mL-1的Hochest 33342(Ex/Em:350/461 nm)标记所有细胞的细胞核显蓝色;用浓度为1 μmol·L-1的SYTOX®Orange Nucleic Acid Stain(Abs/Em:547/570 nm)标记死细胞的细胞核显橙色。于37 ℃避光孵育15 min,细胞被标记好后,由高内涵仪器直接对细胞进行成像分析。统计结果,并分析各孔的细胞存活情况。精确称量何首乌总提物50 mg,溶于DMSO中作为储液备用。
2.3 统计方法
用ImageXpress Micro XL高内涵软件对图像进行处理分析,实验数据以GraphPad Prism 5.0、IBM SPSS Statistics 20、OriginPro 8.5软件处理,所有数据采用独立样本t检验进行统计学处理。P<0.05设为有统计学意义。
3 结果
3.1何首乌总提取物对肝窦内皮细胞毒性检测结果及IC50值
本实验设6个浓度梯度,3倍稀释,最高质量浓度为2 mg·mL-1(相当于生药量12.74 mg·mL-1),用ImageXpress Micro XL高内涵仪器,采用二重荧光标记法(Hochest 33342标记所有的细胞,SYTOX®Orange Nucleic Acid Stain标记死细胞),以每孔活细胞的百分比作为评价指标,用GraphPad Prism 5.0 软件处理,结果:LogIC50值为-0.12,计算IC50为0.76 mg·mL-1(相当于生药量4.84 mg·mL-1)。见图1。
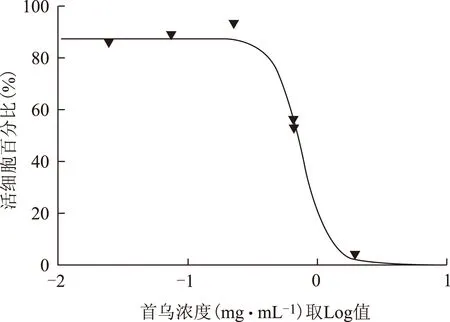
图1 何首乌总提取物作用于肝窦内皮细胞的IC50值
3.2基于高内涵分析评价何首乌与茯苓、甘草、三七的配伍减毒情况
3.2.1首乌与茯苓、甘草、三七的配伍减毒情况高内涵成像结果,见图2~3。实验取IC50值作为何首乌的配伍实验用量,分别配伍不同浓度的茯苓、甘草、三七,复6孔,分别作对照。用ImageXpressMicroXL高内涵仪器分析,采用二重荧光标记法(Hochest33342标记所有细胞显蓝色,SYTOX®OrangeNucleicAcidStain标记死细胞显橙色),以每孔活细胞的百分比作为评价指标,用OriginPro8.5软件作图。

注:A.首乌;B.首乌+茯苓;C.首乌+甘草;D.首乌+三七;茯苓质量浓度为2 mg·mL-1;甘草质量浓度为4 mg·mL-1;三七质量浓度为1 mg·mL-1。图2 首乌与茯苓、甘草、三七的配伍减毒高内涵成像结果
图2显示,单纯何首乌组死细胞数很多,大约占细胞总数的45%;首乌+茯苓组的死细胞数很少,约占3%;首乌+甘草组的死细胞数较少,约占10%;首乌+三七组的死细胞数较多,约占20%。从染色结果来看,首乌配伍茯苓的减毒效果最好。
3.2.2高内涵软件统计分析各孔的活细胞数及其百分比,综合评价何首乌与不同浓度的茯苓、甘草、三七在肝窦内皮细胞上的配伍减毒情况,见图3~5。

注:*P<0.05;**P<0.01。下同。图3 何首乌与不同浓度的茯苓配伍减毒结果

图4 首乌与不同浓度的甘草配伍减毒结果

图5 首乌与不同浓度的三七配伍减毒结果
结合图3~5可以看出:首乌浓度为4.84mg·mL-1(生药量)时,对肝窦内皮细胞表现出明显的抑制作用,配伍茯苓提取物质量浓度为0.07~2mg·mL-1,合生药首乌∶茯苓为1∶(1.58~0.055);配伍甘草提取物质量浓度为0.15~4mg·mL-1,合生药首乌∶甘草为1∶(7.61~0.285);三七提取物质量浓度为0.037~1mg·mL-1,合生药首乌∶三七为1∶(48.89~1.80)。三者都能明显地降低何首乌对肝窦内皮细胞的毒性作用,且茯苓的减毒效果相对较好。
4 讨论
古代本草记载“首乌以茯苓为使”,现在何首乌的使用较少见规范的配伍减毒应用,而其肝毒性屡见报道,为明确首乌的肝毒性是否与合理的配伍有关,本研究在细胞水平上分别考察了茯苓、甘草、三七与何首乌配伍使用对其肝毒性的影响。结果显示三者都能明显地降低何首乌的肝细胞毒性,且茯苓的效果较好,在一定程度上佐证了古代首乌与茯苓相使为用的科学性。
尽管现在对何首乌的肝毒性报道很多,但我们要对此有客观全面的认识,从不同角度探索何首乌的毒性问题。前期课题组从炮制减毒的角度探讨了何首乌的毒性情况,结果显示,合理的炮制方法能在一定程度上降低其肝毒性。本文从配伍减毒的角度探讨了首乌的减毒情况,表明在细胞水平上首乌与茯苓、甘草、三七配伍确实能降低其毒性作用。虽然体外细胞实验不能完全模拟人体的自身代谢,但却能给临床上首乌的配伍减毒提供参考。本文没有在中医的理论指导下应用,今后需要紧密结合临床,在动物水平上进行更加深入的研究,寻求最好的配伍解毒方法和最佳的配伍比例。
[1] 常青,赵海娟,李春,等.制首乌联合定量运动对大鼠肝脏微循环及肝功能的影响[J].中国药物警戒,2014,11(4):193-197.
[2]DragunowM.High-contentanalysisinneuroscience[J].NatRevNeurosci,2008,9(10):779-788.
[3] 吕旸.基于肝细胞毒价检测的何首乌质量控制方法研究[D].北京:北京化工大学,2013.
[4] 赵子剑.茯苓多糖的提取方法优选[J].时珍国医国药,2009,20(9):2207-2208.
[5] 孙付军,周倩,王春芳,等.甘草炮制前后药效学比较[J].中国实验方剂学杂志,2010,16(14):115-118.
CompatibilityAttenuatedDetoxificationstudyonRadixPolygoniMultiflori-causedHepaticSinusEndothelialCellInjuryBasedonHighContentAnalysis
PANGJingyao1,2,LIYumeng3,BAIZhaofang2,ZHAOYanLing2,ZHAOKuijun1,MAZhijie1*,WANGJiabo2*,XIAOXiaohe2
(1.BeijingFriendshipHospital,CapitalMedicalUniversity,Beijing100050,China;2.ChinaMilitaryInstituteofChineseMedicine,302MilitaryHospital,Beijing100039,China;3.YunnanUniversityOfTCM,CollegeofTraditionalChineseMedicine,Kunming650500,China)
Objective:To observe the compatibility attenuated detoxification of Radix Polygoni Multiflori-caused hepatic sinus endothelial cell injury,and provide reference for the further study of the clinical rational medication.Methods:The High Content Analysis was applied to detect the compatibility attenuated detoxification of Radix Polygoni Multiflori-caused hepatic sinus endothelial cell injury with Poria cocos,Radix Glycyrrhizae and Radix notoginseng.Result:A dose dependent relation existed between Radix Polygoni Multiflori and hepatic sinus endothelial cells injury,which was embedded significantly in compatibility attenuated detoxification with different concentration of Poria cocos,Radix Glycyrrhizae and Radix notoginsen under the dose of IC50.Compatibility attenuated detoxification with Poria cocos effected better,of which with Radix notoginseng was the least potent.Conclusion:Compatibility attenuated detoxification effect of Radix Polygoni Multiflori and Poria cocos,Radix Glycyrrhizae and Radix notoginsen was specifically reflected through High Content Analysis,which may provide a scientific basis for the safety and rationality of clinical medication.
Radix Polygoni Multiflori;compatibility attenuated detoxification;hepatic sinus endothelial cells;High Content Analysis
2014-11-30)
国家重大新药创制专项课题(2015ZX09501-004-001-008);国家公益性行业专项课题(201507004-04);国家自然科学基金项目(81373984,81403126)
*
王伽伯,博士,助理研究员,研究方向:中药药性与毒性评价;Tel:(010)66933325,E-mail:pharm_sci@126.com 马致洁,博士,药师,研究方向:中药药理与毒理研究;E-mail:13811647091@163.com
10.13313/j.issn.1673-4890.2015.4.008

