超细晶纯钛种植体表面微弧氧化处理的实验研究
贾晓瑞,辛海涛,张 强,宋鑫磊,安佰利
(1.第四军医大学口腔医院修复科,军事口腔医学国家重点实验室,陕西西安710032 2.兰州军区空军机关医院,甘肃兰州730020)
纯钛材料具有良好的生物相容性和耐腐蚀性,且能与牙槽骨组织形成良好的骨结合,因此作为种植体材料已广泛应用于临床[1]。但纯钛的机械强度比钛合金低,将纯钛种植体应用于临床时会因种植体折断而影响种植修复寿命[2]。另有文献报道,钛合金的机械强度虽相对较高,但由于该合金中所含的铝和钒元素会对人体产生毒副作用,也在一定程度上限制了其作为种植体材料在口腔临床中的应用[3-4]。因此,需要对纯钛材料的组织与结构进行研究,以提高其机械性能来满足临床种植需要。
晶粒细化是一种通过改变金属材料的晶粒大小和结构来提高其机械性能的方法,而且在细化过程中不会形成任何有害元素[5]。本课题组前期研究发现,采用等通道挤压技术对纯钛材料的晶粒进行细化处理后,可使其晶粒直径由40 μm减小到300 nm;细化后的材料硬度值由1 496 MPa上升到2 458 MPa,动态、静态压缩屈服强度分别从900、300 MPa 上升到1 240、772 MPa[6]。Park 等研究也证明,超细晶纯钛能促进成骨细胞在其表面的黏附和繁殖[7]。以上研究结果提示,具有更高强度和良好生物相容性的超细晶纯钛更适合作为种植体的材料用于临床。
为了提高种植体的骨结合率和减少种植失败的风险,现有的纯钛种植体都要进行表面处理[8-10]。表面处理技术主要有物理方法、电化学方法和化学方法[11-13],其中微弧氧化(MAO)是目前应用较广,改性效果好并且技术成熟的方法[14-16]。为了能将超细晶纯钛应用于口腔种植修复,本实验采用微弧氧化技术在超细晶纯钛表面制备氧化涂层,并通过测量氧化涂层的组成及其相关性能评价,以探讨微弧氧化技术用于超细晶纯钛材料表面处理的可行性。
1 材料和方法
1.1 试件制备
取直径10 mm、长10 cm的圆柱状商业纯钛(99.5%,2级)(西北工业大学)用等通道挤压(ECAP)模具常温下挤压4道次,然后进行热处理将其制成超细晶纯钛材料(图1)。分别取上述制备的超细晶纯钛和普通纯钛,将其线切割成直径6 mm、厚3 mm的圆盘状试件后,用SiC砂纸抛光至1 500目;然后再依次用丙酮、无水乙醇、去离子水各超声震荡清洗3次备用。

图1 等通道挤压技术示意图和制备的超细晶纯钛
1.2 制备微弧氧化涂层
取上述制备的超细晶纯钛试件和普通纯钛试件(作为对照)各12个,分别置于微弧氧化设备(MAO-100D,长安大学提供)中的阳极处;然后以不锈钢板作为阴极,混合性水溶液作为电解液,并在电压450 V、单脉冲、频率500 Hz、循环周期为15%的条件下进行微弧氧化处理15 min。
1.3 微弧氧化涂层性能测定
微弧氧化处理结束后,将两种试件各随机分为2组(每组6个试件)。一组采用X射线能谱仪(ZEISS SUPRATM55,徳国)分析各试件氧化涂层的元素组成,场发射扫描电子显微镜(SEM)(ZEISS SUPRATM55,徳国)观察并测量各试件氧化涂层表面和横断面的形貌及其厚度;另一组采用三维形貌扫描仪(NANOVEA,美国)测量各试件氧化涂层的表面粗糙度、涂层附着力自动划痕仪(WS-2005,兰州)测量各试件氧化涂层与基体的结合力强度。每种测量方法均在每个试件上各随机测量3个部位,并取其平均值。
1.4 统计学分析
2 结果
2.1 各组微弧氧化涂层的元素组成
超细晶纯钛实验组和普通纯钛对照组微弧氧化涂层的元素组成(图2)。超细晶纯钛表面涂层的各元素比例分别为:O(47.12%)、Ti(35.53%)、P(6.98%)、Si(10.35%)、C(0.02%),普通纯钛表面涂层的各元素比例分别为:O(47.45%)、Ti(35.75%)、P(9.61%)、Si(7.17%)、C(0.02%),两组各元素的比例均无显著性差异(P>0.05);提示,超细晶纯钛经微弧氧化处理后其表面的元素组成未发生明显变化。
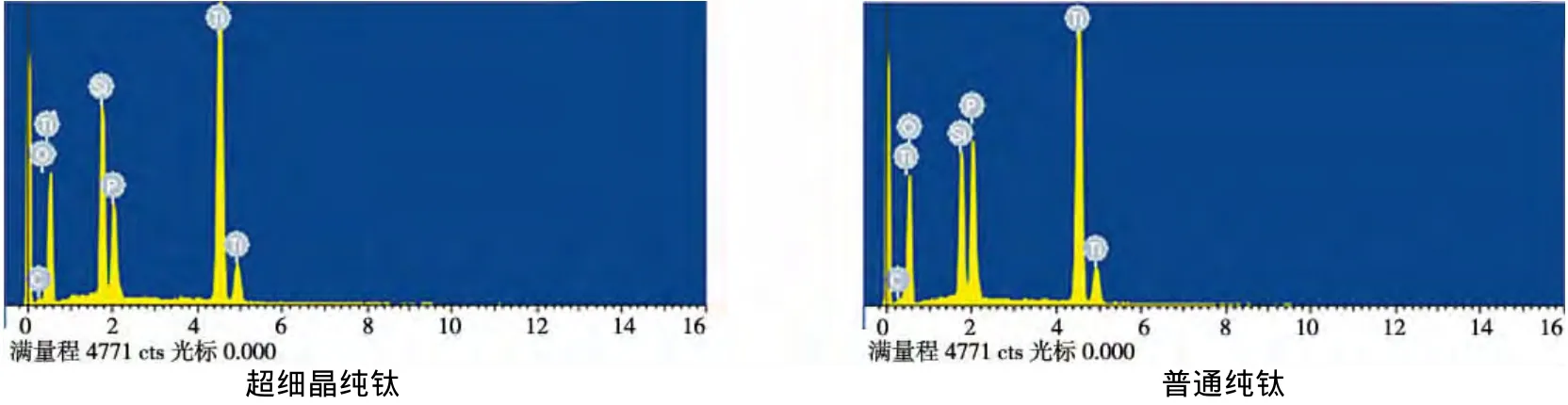
图2 两种材料表面涂层的元素组成
2.2 各组氧化涂层表面和横截面的形貌及其厚度
SEM观察显示:微弧氧化处理后,超细晶纯钛和普通纯钛表面均形成了疏松多孔的氧化涂层,两组试件的涂层表面均分布有火山口状圆形或椭圆形微孔,其中超细晶纯钛表面氧化涂层的孔隙率大于普通纯钛的氧化涂层(图3);通过观察各试件表面涂层的横截面形貌可见,两组试样表面的涂层均由两部分组成,分别为:接触底物结构致密的内层和含释放通道疏松而多孔的外层(图4)。涂层厚度:超细晶纯钛组为(7.833±0.771)μm,普通纯钛组为(4.775±0.558)μm,二者相比有显著差异(P<0.05)(表1)。

图3 两种材料表面形貌(SEM,×5 000)

图4 超细晶纯钛和普通纯钛涂层的横截面(SEM,×5000)
2.3 各组微弧氧化涂层的粗糙度
三维形貌扫描仪显示:超细晶纯钛和普通纯钛两种材料经微弧氧化处理后所形成的氧化涂层均呈现出高低不平的粗糙界面(图5),其粗糙度值分别为(1.391±0.143)μm 和(1.346±0.091)μm(P>0.05)(表1)。

图5 超细晶纯钛和普通纯钛氧化涂层表面的三维形貌
2.4 各组微弧氧化涂层的结合力
涂层附着力自动划痕仪测定结果显示,超细晶纯钛和普通纯钛经微弧氧化处理后所形成的氧化涂层与其基体之间的结合力值分别为:(23.900±1.267)N、(23.867±1.134)N(P>0.05)(表1)。
表1 各组微弧氧化涂层的厚度、粗糙度和结合力比较(s)
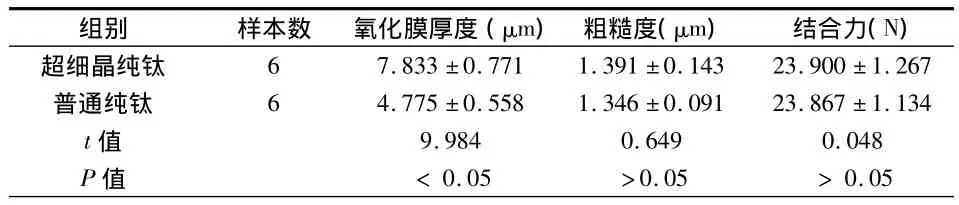
表1 各组微弧氧化涂层的厚度、粗糙度和结合力比较(s)
组别 样本数 氧化膜厚度(μm)粗糙度(μm)结合力(N)超细晶纯钛6 7.833±0.771 1.391±0.143 23.900±1.267普通纯钛 6 4.775±0.558 1.346±0.091 23.867±1.134 t值 9.984 0.649 0.048 P值 <0.05 >0.05 >0.05
3 讨论
钛因其优异的生物相容性和耐腐蚀性,现已被广泛应用于口腔种植修复中。但由于纯钛材料的机械强度相对较低,如何提高其力学性能是近年来口腔种植研究的热点。等通道挤压是Segal等[17]20世纪80年代提出的一种制备纳米材料的加工方法,所用模具由两个成一定角度的等径通道组成,材料受压后可通过纯剪切应力改变晶粒结构和大小,且能在不改变试样尺寸的前提下进行多次挤压变形,以增大总应变量,并使晶粒得到进一步细化。本课题组前期研究表明,通过等通道挤压可使纯钛的晶粒明显细化、硬度和屈服强度明显提高,且不会明显改变其弹性模量,从而有利于纯钛与骨组织发生骨结合;生物安全性试验也表明,超细晶纯钛无毒性反应、不含抑制细胞生长成分、不会引起溶血(溶血率为1.6%),并且对黏膜无刺激性[6]。以上研究结果提示,晶粒细化后的纯钛材料具有更好的机械性能和生物安全性,更适合作为牙科种植体材料应用于临床。
为了使超细晶化纯钛材料能应用于口腔种植修复,还要对其表面进行处理,使之能与骨组织形成良好的骨结合。目前,用于纯钛材料表面处理的方法主要有物理方法、电化学方法和化学方法。微弧氧化是近年来在阳极氧化的基础上建立起来的一种在有色金属表面原位生长陶瓷膜的新技术,其过程和机制包括热析出、元素扩散、等离子化学反应和电泳效应等。对纯钛表面进行微弧氧化处理,可将其表层的Ti原子转化为内层致密、外层多孔的稳定的TiO2活性陶瓷层,有利于提高钛植入体的生物活性[18-19]。本实验选用微弧氧化技术对试件进行表面处理,通过元素分析可知,超细晶纯钛实验组和普通纯钛对照组表面氧化涂层中的主要元素均为 O、Ti、P、Si、C,两种材料表面涂层的各组成元素比例基本相同;其中Ti为基体成分,O为微弧氧化过程中产生,而少量P、Si和C的存在则说明:在微弧氧化过程中,有电解液中的离子沉积到试件表面,并参与了氧化膜的形成,从而形成了含有不同元素的氧化层。涂层表面形貌观察结果显示,微弧氧化处理后的两组试件表面均形成了疏松多孔的氧化涂层,从而为成骨细胞的黏附提供了结构基础。Akin等[20]发现,钛种植体表面粗糙度的增加可以增加磷酸钙盐的沉积,并能提高成骨细胞造蛋白质和提取钙离子的能力;而疏松多孔的表面则有利于成骨细胞的黏附和增殖,并增强种植体与骨组织间的结合力。本实验发现,普通纯钛组涂层表面的粗糙度为(1.346±0.091)μm,超细晶纯钛组涂层表面的粗糙度为(1.391±0.143)μm,均可为成骨细胞的黏附和骨组织的结合提供较为理想的表面形貌。有研究发现,涂层的厚度小于10 μm时,涂层和基体间可形成较牢固的结合。本实验发现,超细晶和普通纯钛的涂层厚度分别为(7.833±0.771)μm、(4.775±0.558)μm,而两者的结合强度分别为(23.900±1.267)N、(23.867±1.134)N,无明显差异。该结果表明,虽然超细晶纯钛组和普通纯钛组的氧化涂层厚度有差异,但涂层与其基体间仍形成了较高的结合力;提示机械性能优越的超细晶纯钛经微弧氧化后,可以作为种植体材料并在临床中应用。关于其生物安全性、生物相容性尚需进一步研究。
本实验采用微弧氧化技术分别在超细晶纯钛和普通纯钛表面制备氧化涂层,并通过测定氧化层的组成及其相关性能评价,探讨微弧氧化技术用于超细晶纯钛材料表面处理的可行性。结果表明,超细晶和普通纯钛表面生成的氧化涂层在元素组成、表面形态和粗糙度等方面,均未见明显差异;虽然超细晶纯钛组表面的涂层厚度明显高于普通纯钛组,但两者的涂层与其基体的结合强度均较高,且无显著性差异,均能满足临床种植体的使用要求。提示,机械性能良好的超细晶纯钛经微弧氧化处理后,可在其表面形成性能良好的氧化涂层,从而为超细晶纯钛的后续生物学研究及其在口腔种植中的应用提供了实验室依据。
[1]Rack HJ,Qazi JI.Titanium alloys for biomedical applications[J].Mat Sci Eng C ,2006,26(8):1269-1277.
[2]Hao YL,Li SJ,Sun BB,et al.Ductile titanium alloy with low Poisson's ratio[J].Phys Rev Lett,2007,98(21):216405-216408.
[3]Latysh V,Krallics G,Alexandrov I,et al.Application of bulk nanostructured materials in medicine[J].Curr Appl Phys ,2006,6(2):262-266.
[4]Moskalyk RR,Alfantazi AM.Processing of vanadium:a review[J].Miner Eng,2003,16(9):793-805.
[5]Ko YG,Shin DH,Park KT,et al.An analysis of the strain hardening behavior of ultra-fine grain pure titanium[J].Scripta Mater,2006,54(10):1785-1789.
[6]张强,辛海涛,李恺,等.等通道挤压超细晶纯钛材料生物安全性研究[J].实用口腔医学杂志,2014,30(3):302-305.
[7]Park JW,Kim YJ,Park CH,et al.Enhanced osteoblast response to an equal channel angular pressing-processed pure titanium substrate with microrough surface topography[J].Acta Biomater,2009,5(8):3272-3280.
[8]Liu XY,Chu PK,Ding CX.Surface modification of titanium,titanium alloys and related materials for biomedical applications[J].Mater Sci Eng R,2004,47:49-121.
[9]Xie YT,Liu XY,Huang AP,et al.Improvement of surface bioactivity on titanium by water and hydrogen plasma immersion ion implantation[J].Biomaterials,2005,26(31):6129-6135.
[10]Kim HW,Kim HE,Knowles JC.Fluor-hydroxyapatite sol-gel coating on titanium substrate for hard tissue implants[J].Biomaterials,2004,25(17):3351-3358.
[11]Pham MT,Matz W,Reuther H,et al.Ion beam sensitizing of titanium surfaces to hydroxyapatite formation[J].Surf Coat Technol,2000,128-129:313-319.
[12]Feng B,Chen JY,Qi SK,et al.Carbonate apatite coating on titanium induced rapidly by precalcification[J].Biomaterials,2002,23(1):173-179.
[13]Toworfe GK,Composto RJ,Shapiro IM,et al.Nucleation and growth of calcium phosphate on amine-,carboxyl-and hydroxyl-silane self-assembled monolayers[J].Biomaterials,2006,27(4):631-642.
[14]Wang YM,Liang BL,Lei TQ,et al.Microarc oxidation coating formed on Ti6Al4V in Na2SiO3system solution:microstructure,mechanical and tribological properties[J].Surf Coat Technol,2006,201(1-2):82-89.
[15]Li LH,Kong YM,Kim HW,et al.Improved biological performance of Ti implants due to surface modi?cation by microarc oxidation[J].Biomaterials ,2004,25(14):2867-2875.
[16]Ryu HS,Song WH,Hong SH.Biomimetic apatite induction of P-containing titania formed by micro-arc oxidation before and after hydrothermal treatment[J].Surf Coat Technol ,2008,202(9):1853-1858.
[17]Segal VM,Reznikovv VI,Drobyshevskiy AE,et al.Plastic working of metals by simple shear[J].Russian Metallurgy,1981(1):99-105.
[18]Wei DQ,Zhou Y,Jia DC,et al.Characteristic and in vitro bioactivity of a microarc-oxidized TiO2-based coating after chemical treatment[J].Acta Biomater,2007,3(5):817-827.
[19]Song WH,Jun YK,Han Y,et al.Biomimetic apatite coating on micro-arc oxidized titania[J].Biomaterials,2004,25(17):3341-3349.
[20]Akin FA,Zreiqat H,Jordan S,et al.Preparation and analysis of macroporous TiO2films on Ti surfaces for bone-tissue implants[J].Biomed Mater Res,2002,57(4):588-596.

