干湿交替对湖滨带不同高程沉积物磷释放的影响研究
宋中奇 姜 霞 王金枝 张彩云 李 炟
(1.哈尔滨商业大学生命科学与环境科学研究中心,黑龙江 哈尔滨150076;2.中国环境科学研究院 环境基准与风险评估国家重点实验室,北京100012)
水位变化引起的湖滨带土壤干湿交替过程能够显著影响磷的迁移转化[1],主要是干燥、再湿润过程通过影响土壤的物理、化学特征(如氧化还原状态、pH值和矿物结构)及微生物群落结构和活性[2][3]来实现。由于湖水侵蚀时间和地表植被类型等不同,湖滨带内不同高程的土壤表现出不同的粒径分布和分形特征[4],进而表现出不同的比表面积和理化性质,从而影响N、P等营养物质在泥水界面交换的过程[5]。对于水位变化对湖滨带土壤性质的影响作用,一些学者认为沉积物/土壤干燥显著增加了其对PO43-的吸附[6],而另外的研究发现干燥降低了沉积物的吸附性能[7][8]。
为了揭示干湿交替作用对湖滨带不同高程土壤理化性质及对P的吸附/解吸作用的影响,取贡湖湖滨带最高水位点的出露土壤、泥水界面沉积物及覆水沉积物,分析不同高程沉积物的粒径分布特征和磷的吸附解吸能力。并进行淹水实验,研究湖滨带不同高程沉积物磷的吸附解吸特性及释磷量的不同。
1 材料与方法
1.1 研究区域
贡湖位于太湖东北部,水体处于轻度富营养化状态。本试验以贡湖湖滨缓冲带为研究对象,采样点位于贡湖北部华庄镇,水位受降雨影响较大,湖滨带坡度较小,最高水位与最低水位相差20cm左右。采样点处水质清澈洁净,植被以草型为主。
1.2 样品采集与处理
采样时间为2013年12月,采样方法参照参考文献[9]。在垂向岸边的一条样带上纵向取三点,包括最高水位点(A)、取样时水位点处沉积物(B)、水面下0.5m处淹水沉积物(C)(如图1)。在落干土壤A点采集表层10cm土样,B点取表层10cm沉积物,C点用抓泥斗采集水下0.5m处沉积物样品。样品采集后捡掉砾石、动植物残体等,混合均匀装入密封袋中运回实验室,置于-20℃冰箱保存待用。

图1 采样点剖面示意图
1.3 实验方法
1.3.1 磷的吸附热力学实验

图2 A(湖滨带最高水位点土壤)、B(泥水界面沉积物)、C(覆水沉积物)对磷的等温吸附曲线
实验所用沉积物/土壤样品均经冷冻干燥、研磨、过100目筛。磷的吸附热力学实验和分析方法参见参考文献[10]。
1.3.2 沉积物/土壤淹水实验
取A、B、C三点干燥沉积物10g加入1L蒸馏水置于具塞容器内震荡24h,之后置于敞口容器内静置15天[11]。分析实验前后沉积物磷形态含量,及试验后水体磷素浓度。每个处理设置3个重复,实验结果以平均值表示(3次分析结果的误差范围<5%)。
1.4 分析方法
粒度分析所用样品为沉积物鲜样,采用Malvern公司生产的Mastersizer2000激光粒度分析仪,粒径测量范围为0.02μm~2000μm,可提供每一粒度组分的百分含量、累积曲线及其他各种粒度参数。
溶解性总磷(DTN)采用过硫酸钾消解-钼锑抗比色法测定;无机磷(DIP)采用磷钼蓝比色法;溶解性有机磷(DOP)采用差值法,DOP=DTP-DIP;沉积物磷形态分析采用SMT法测定[11]。
采用Excel2010、SPSS19.0以及Sigmplot12.0软件对实验数据进行处理,进行统计检验和图表绘制。
2 结果与分析
2.1 沉积物粒度分布特征
从表1的粒度分布可以看出,不同采样点表现出不同的粒度分布特征。A点中位粒径为30.02μm,显著高于B点和C点中位粒径15.59μm和15.78μm,且黏土粒级含量明显较低,粉砂粒级含量也低于B、C两点,而细砂粒级和粗砂粒级的含量占27.87%,显著高于其他两点。C点组成以粉砂粒级和黏土粒级为主,粒径主要集中在63μm以下,占比达90.76%,与李青芹[12]等对我国其他湖泊的研究结果一致。
于试验鹅14、42、70日龄清晨8:00,以重复为单位,空腹称重。从每个重复中随机选取2只接近平均体重的试验鹅,称重、记录。
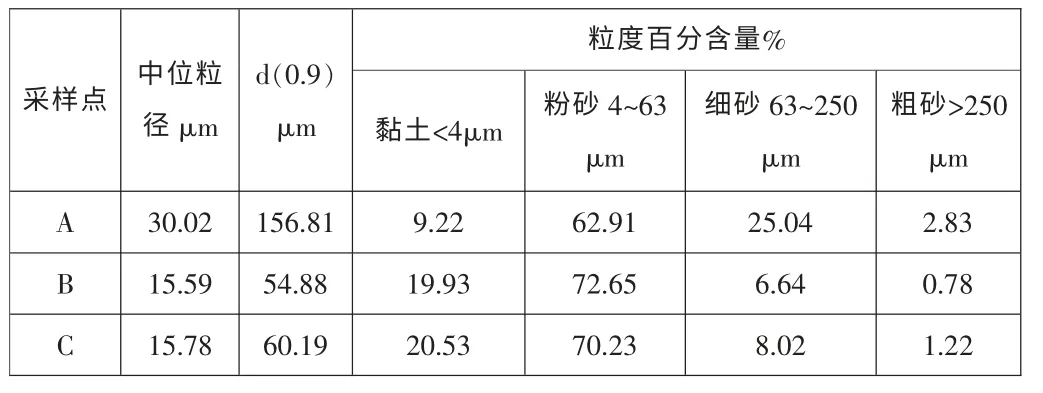
表1 湖滨带沉积物粒度特征
*d(0.9)表示粒径在该数值以下的组分占90%。
A为湖滨带最高水位点土壤,B为泥水界面沉积物,C为覆水沉积物。
2.2 磷的吸附/解吸特征
采样点A、B、C磷的吸附量与溶液初始浓度C0的线性回归结果见图2,C0与磷的吸附量呈很好的线性关系(R2>0.96)。在初始磷浓度较低时,沉积物表现出解吸磷,随着溶液磷浓度的增加,沉积物逐渐吸附上覆水体中的DIP。
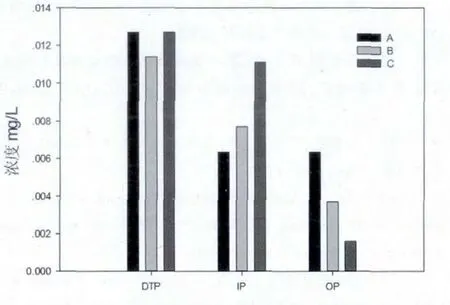
图3 实验后水体磷浓度
采样点A、B、C的磷的吸附等温方程见表2,等温方程中斜率较高的对磷的吸附能力较强。沉积物对磷的吸附能力强弱表现为C>B>A,A点吸附性能弱于B和C点。
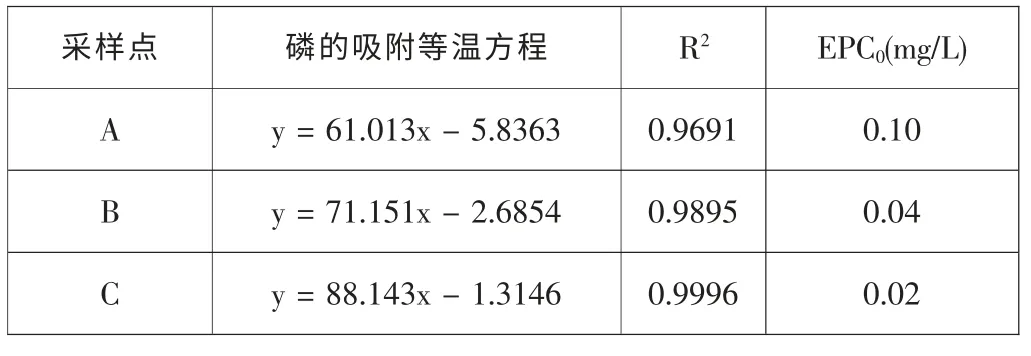
表2 A(湖滨带最高水位点土壤)、B(泥水界面沉积物)、C(覆水沉积物)
*y为平均吸附量,g/kg;x为初始溶液浓度,mg/L。
一般来讲,吸附颗粒中粘粒级颗粒含量越高,比表面积越大,则表面能越强,对磷的吸附量就越大[13]。结合沉积物粒度分析结果,A、B、C三点中A点的粘粒级颗粒含量最低,其结果与吸附解吸实验相一致。
2.3 再淹水对上覆水磷浓度的影响
如图3所示,淹水15天后采样点A、B、C的上覆水DTP含量无显著差别,分别为0.013、0.011和0.013mg/L。A点水体IP和OP含量占DTP比例相等,而C点水体以IP为主,占DTP比例达87.2%,OP仅占12.8%。A、B、C三点水体中IP浓度依次升高,OP浓度则依次递减。Qiu和McComb[14]的研究结果显示干燥沉积物/土壤再润湿,会导致生物可利用性磷含量增加,有利于增加微生物的数量和活性。淹水后A点OP含量较高,可能是因为微生物活动较强,繁殖过程中利用环境中较多的磷素合成自身有机物。
2.4 淹水前后沉积物磷变化
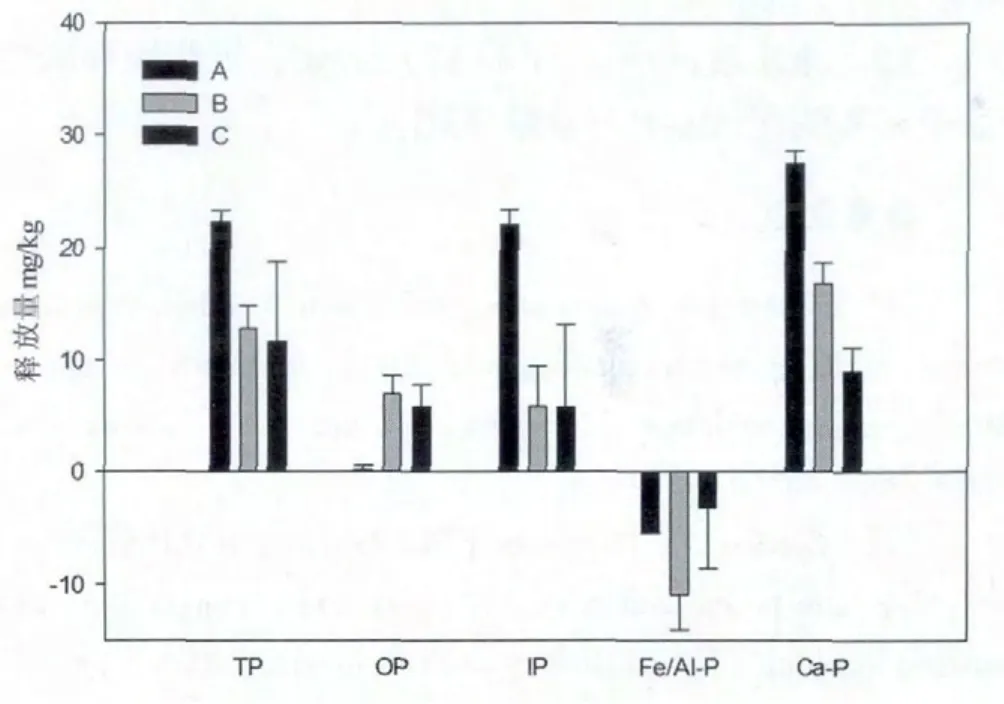
图4 A、B、C各形态磷释放量
表3为沉积物各形态磷初始含量,实验前A、B、C三点TP含量无明显差异。沉积物中磷素以Ca-P为主要赋存形态,其次为OP、Fe/Al-P,平均占比分别为62.5%、22.5%和15.0%。A点Ca-P含量略高于B、C两点,Fe/Al-P和OP含量稍低。OP含量稍低可能是由于在水位较低时,湖滨土壤长时间暴露于空气中,在风干过程中土壤的有机磷分解[15]。

表3 A(湖滨带最高水位点土壤)、B(泥水界面沉积物)、C(覆水沉积物)
图4所示为实验前后A、B、C三点各形态磷含量差值,实验后三点TP含量出现不同程度的降低,降幅为A>B>C。TP含量的减少是各形态磷综合作用的结果,其中OP和Ca-P含量有所下降,Fe/Al-P含量有所升高,各磷形态含量实验前后差值大小总体为Ca-P>OP>Fe/Al-P,Ca-P含量的减少是导致TP含量下降的主要原因。Ca-P包含Ca2-P、Ca8-P、Ca10-P,马利民等[16]研究干湿交替对三峡库区土壤磷释放的影响,发现Ca2-P在水土界面的释放活性最大,马利民的研究支持本实验结果。
采样点A、B、C的OP含量在试验后均出现较小幅度的下降,其中A点降幅极小,而水体中OP含量较高,相应的IP含量降幅显著高于B、C两点。这一结果再次印证了A点的生物可利用性磷含量较高,再淹水后微生物活性增强,相比于B、C两点,A点微生物会利用IP合成更多的OP。
3 结论
3.1湖滨带高位沉积物与淹水沉积物相比黏土级颗粒含量较低,中位粒径较大,湖滨带高位沉积物对磷的吸附能力弱于淹水沉积物。
3.2淹水后沉积物TP降幅A>B>C,沉积物释磷以Ca-P形态为主,Ca-P释放量A>B>C。
[1]Gilbert J.D.,Guerrero F.,de Vicente I.Sediment desicca tion as a driver of phosphate availability in the water column of Mediterranean wetlands[J].Science of the Total Environment.2014,466–467(0):965-975.
[2]Gordon H.,Haygarth P.M.,Bardgett R.D.Drying and rewetting effects on soil microbial community composition and nutrient leaching[J].Soil Biology and Biochemistry.2008(2):302-311.
[3]Foulquier A.,Volat B.,Neyra M.,Bornette G.,Montuelle B.Long-term impact of hydrological regime on structure and functionsofmicrobial communities in riverinewetland sediments[J].FEMSMicrobiology Ecology.2013(2):211-226.
[4]熊平生,谢世友,莫心祥.长江三峡库区水土流失及其生态治理措施[J].水土保持研究,2006(2):272-273.
[5]金相灿,屠清瑛.湖泊富营养化调查规范(第2版)[M].北京:中国环境科学出版社,1990.
[6]De Groot,C.J.,Fabre,A.The impact of desiccation of a freshwatermarsh(Garcines Nord,Camargue,France)on sedimentwater-vegetation interactions.Hydrobiologia.1993,252(1):105-116.
[7]Baldwin,D.S.Effects of exposure to air and subsequent drying on the phosphate sorption characteristics of sediments from a eutrophic reservoir.Limnology and Oceanography.1996,41(8):1725-1732.
[8]de Vicente,I.,Andersen,F.,Hansen,H.C.B.,Cruz-Pizar ro,L.,Jensen,H.S.Water level fluctuationsmay decrease phosphate adsorption capacity of the sediment in oligotrophic high mountain lakes.Hydrobiologia.2010,651(1),253-264.
[9]C.J.Watts.Seasonal phosphorus release from exposed,reinundated littoral sediments of two Australian reservoirs[J].Hydrobiologia,2000,431(1):27-39.
[10]姜霞,王书航.沉积物质量评估手册[M].北京:科学出版社,2012.
[11]国家环境保护总局.水和废水监测分析方法(第四版)[M].北京:中国环境科学出版社,2002.
[12]李青芹,霍守亮,等.我国湖泊沉积物营养盐和粒度分布 及 其 关 系 研 究[J].农 业 环 境 科 学 学 报,2010(12):2390-239 7.
[13]周孝德,环境因素对滇池底泥磷吸附的影响[J].水利学报,1998(增刊):12-17.
[14]Qiu,S.,McComb,A.Drying-induced stimulation of ammonium release and nitrification in reflooded lake sediment.Marine and FreshwaterResearch.1996(3),531-536.
[15]Liu M.,Hou L.,Xu X.,et al.Adsorption of phosphate on tidal flat surface sediments from the Yangtze Estuary[J].EnvironmentalGeology,2002(42):657-665.
[16]马利民,张明,滕衍行,等.三峡库区消落区周期性干湿交替环境对土壤磷释放的影响[J].环境科学,2008(4):103-1039.

