实验室条件下氧化铋的制备过程中所涉各因素的研究分析
易 宇
(长沙有色冶金设计研究院有限公司,长沙410011)
铋在自然界中以游离金属和矿物的形式存在,自身具有低熔点、质脆易粉碎、导电导热性差等性质。铋的化学性质较稳定,除了应用于医药治疗中,也广泛应用于冶金添加剂、易熔合金、阻燃剂、化工应用、电子陶瓷、半导体、核工业中,因此,铋被公认为是安全的“绿色”金属[1]。根据铋的存在形式,通常情况下,铋的获取途径主要通过以下两个途径:一是在铜、铅等有色金属冶炼过程中回收;二是通过冶炼钨矿等矿物实现铋精矿的回收,进而获取铋金属。以上两种方法中,第一种是国内外主要的铋的获取方式[3]。
本文利用某铜业公司生产的4NBi为原料,在一定温度下,使固体铋熔化为铋熔体后再蒸发为蒸汽,采用适当的减压氧化实现β-型球状超细Bi2O3粉末的制备。本文系统地介绍了β-型球状超细Bi2O3粉末制备过程,以及在实验室条件下制备对Bi2O3粉末粒度的影响。
1 实验方法
1.1 实验原料
纯度为99.99%的铋原料;纯度为99.99%的氮气和氧气。
1.2 仪器设备
图1为制备超细Bi2O3的实验装置图。
超细Bi2O3的制备实验装置含有5个重要的组成部分:(1)等离子体发生器;(2)氧化室;(3)冷却室;(4)收尘布袋;(5)铜坩埚。
1.3 实验过程
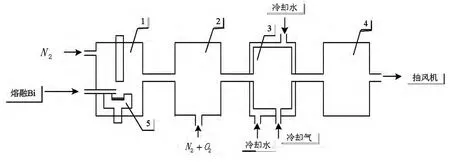
图1 超细Bi2O3制备实验装置图
根据图1可知制备Bi2O3的的核心过程如下:将高纯度的熔融Bi送入等离子体发生器的铜坩埚中气化后,利用氧化室中充入的纯氧将气化后的Bi氧化,在冷却室中将生成的Bi2O3冷却后,最后在收尘布袋中实现Bi2O3收集。
2 铋溶体的蒸发速率的理论分析
考虑到固体铋挥发性差的特性,本文采用的实现铋气化的主要方式是将固体铋熔化后,再蒸发为铋蒸汽。然而,在实际的生成过程中,固体铋转化为铋蒸汽必须保证一定的速率,否则无法保证Bi2O3的生产。为了定性地了解铋熔体的蒸发速率,本节以锌的蒸发速率作为比较对象进行研究。
公式1和公式2分别表示了铋和锌的饱和蒸汽压与温度的关系。
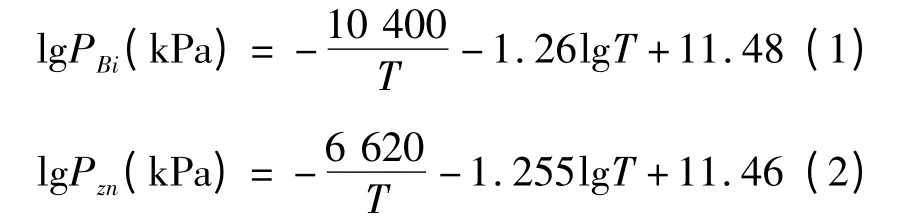
根据公式1和公式2可绘制出铋和锌的饱和蒸汽压与温度的关系图,如图2所示。
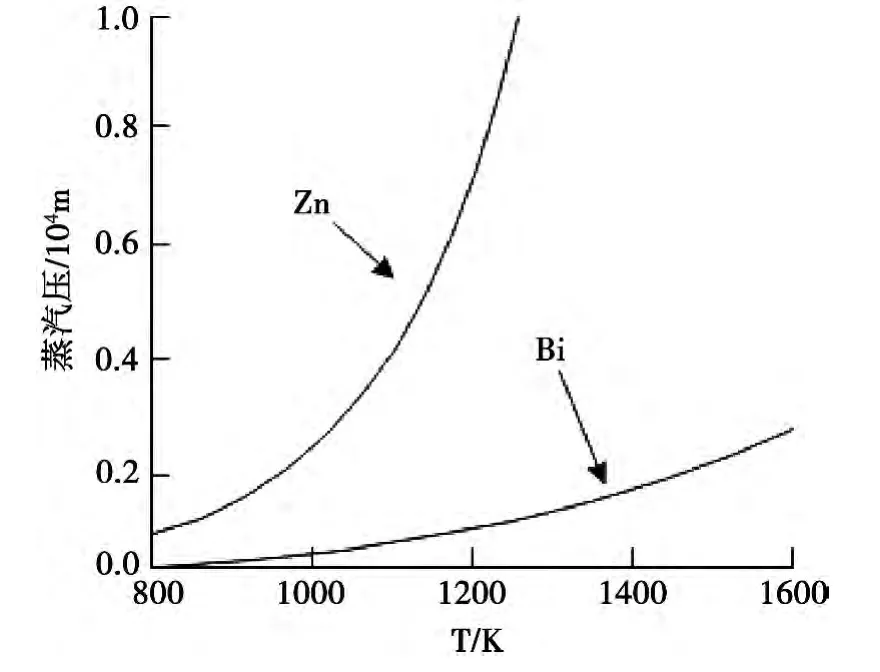
图2 铋和锌的蒸汽压与温度的关系图
通过图2所示的铋和锌的蒸汽压与温度的关系对比图可以看出,在相同的温度下,铋的饱和蒸汽压明显低于锌的饱和蒸汽压,也就是说,在相同的温度下,铋的蒸发速率要慢很多。利用蒸汽氧化法制备氧化锌的温度范围界于600℃和907℃间,当温度为600℃时,锌的饱和蒸汽压为1 534.5Pa,为达到近似的蒸汽压,铋所需的温度值为1 148℃。
此外,通过研究金属的蒸发速率公式可知,金属的蒸发速率受到温度、蒸发面、真空度等因素的影响。
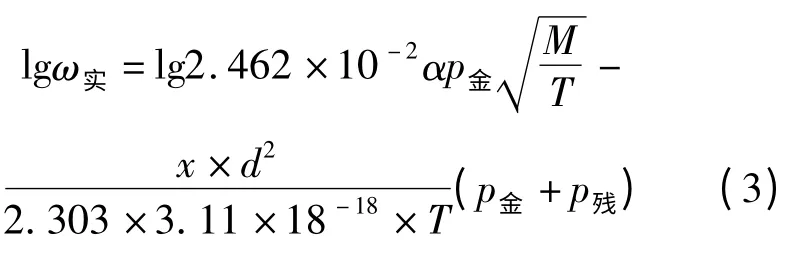
其中,公式3中所涉的主要因子含义如下:
ω实表示金属蒸发的实际测试速率;
α表示为金属的凝聚系数,本文采用默认值为1;
p金表示为金属的饱和蒸汽压;
p残表示剩余气体的压力;
x表示金属的蒸发面和冷凝面的间距离。
根据公式3可分析出,在不同压力、温度和蒸发面值时铋的蒸发速率的变化情况,如图3所示。
图3分别展示了蒸发距离分别为0.013cm、0.008cm和0.003cm时,铋的蒸发率与压力、温度间的变化关系。下面分别进行阐述:
(1)在不同的蒸发距离和特定的温度下,从压力和蒸发速率两个方面分析,铋的蒸发速率随着压力的减小而不断增大,当压力低于某定值时,则铋的蒸发速率处于定值,也就是最大值。
(2)在不同的蒸发距离和特定的压力下,铋的蒸发速率并不一定随着温度的升高而降低,在图3(c)图中,铋的蒸发速率随着温度的升高而增大,这与文献2中所阐述的论点是一致的[2]。因此,图3(c)中的关系图应更能反映温度与蒸发速率的关系。
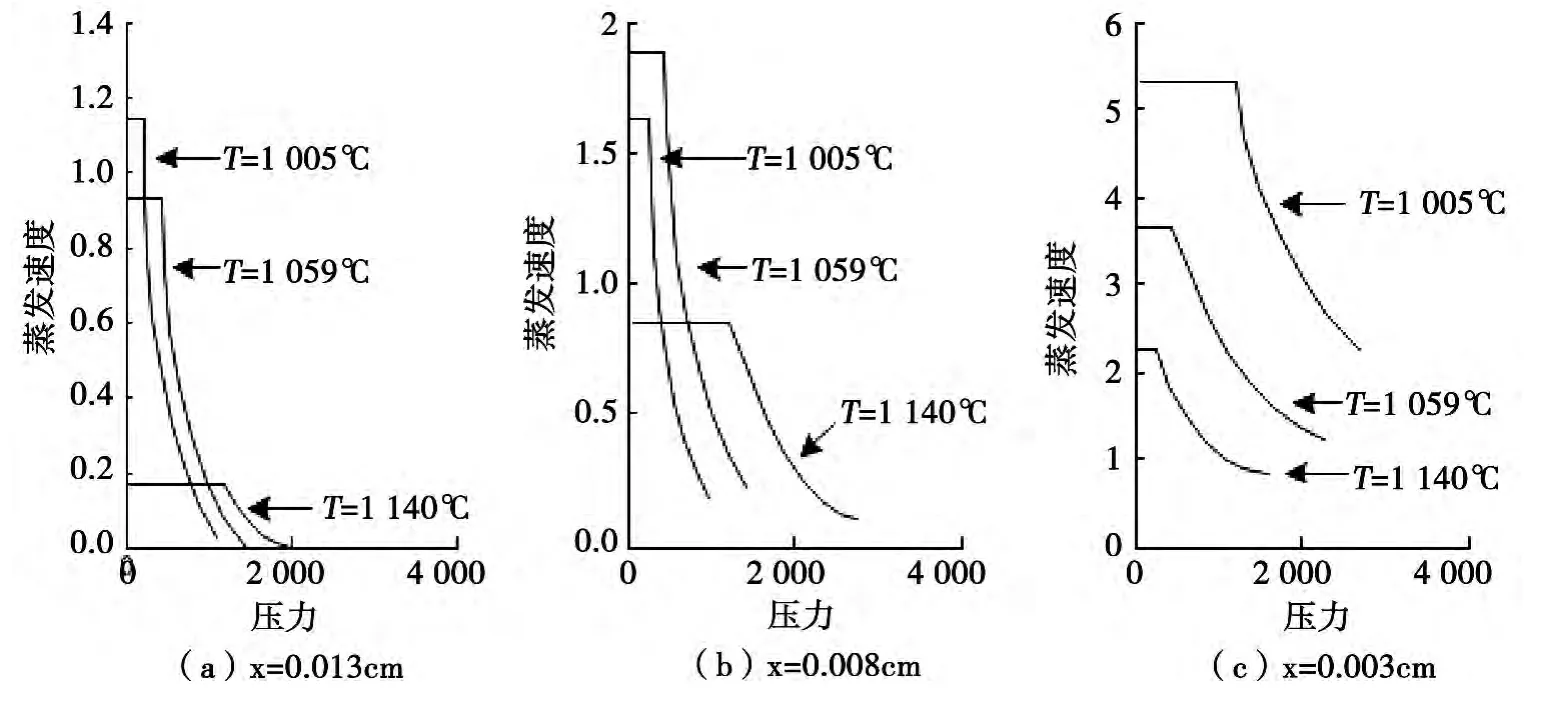
图3 不同压力、温度和蒸发面值时铋的蒸发速率的变化图
(3)通过研究图3(c)可以看出,在温度为1140℃时,配合以适当的压力,可获得铋最大的蒸发速率。
通过以上分析证明了前面所述的实验过程的理论可行性。
3 实验室条件下Bi2O3粉末制备结果与讨论
通过以上分析可知,利用气化减压氧化法制备Bi2O3粉末的过程中,等离子体发生器、氧化室、冷却室中的环境因素对Bi2O3粉末的制备具有明显的影响,因此,根据实验室制备Bi2O3粉末的结果进行逐项讨论。
3.1 等离子体发生器对Bi2O3粉末制备的影响
在等离子体发生器中对Bi2O3粉末制备产生影响的两个因素分别为等离子体发生器内的温度和压力。
当等离子体发生器内的环境为N2注入量为12L/min、压力为0.08MPa时,温度对Bi2O3粉末平均粒径的影响如图4所示。
根据图4所示,当等离子体发生器内的温度不断升高时,Bi2O3粉末的粒径会逐渐变大。随着温度的不断升高,铋的蒸发速率增大,使得等离子体发生器内Bi2O3的浓度增大,使Bi2O3粒子间碰撞机会增大,从而使Bi2O3粉末的粒径增大。从图4可以看出,在1 200℃时,铋的粒径明显增大,考虑到Bi2O3生产的需求及生产的能耗,可将Bi2O3粉末的生产温度设定为1 200℃。

图4 等离子体发生器内温度对Bi2O3粉末平均粒径的影响图
当等离子体发生器内的N2注入量为12L/min、温度为1 200℃时,等离子体发生器内的压力对Bi2O3粉末平均粒径的影响如图5所示。
根据图5所示,Bi2O3粉末的粒径随着等离子体发生器内的压力逐步增大而逐步减小。在前面的分析中可知铋的蒸发速率随着压力的增大而不断减小,因此,使等离子体发生器内的铋的蒸发速率减小,使Bi2O3的浓度降低,进而导致Bi2O3粉末的粒径变小。从图5中,可明显看出在压力为0.08MPa时,Bi2O3粉末的粒径明显变小,因此,可设定等离子体发生器内的压力值为0.08MPa。

图5 等离子体发生器内压力对Bi2O3粉末平均粒径的影响图
3.2 氧化室对Bi2O3粉末制备的影响
在氧化室中对Bi2O3粉末制备产生影响的两个因素分别为氧化室内的温度和气体流量。
当氧化室内的气体流量为12L/min时,氧化室中温度的变化对Bi2O3粉末平均粒径的影响如图6所示。

图6 氧化室内温度对Bi2 O3粉末平均粒径的影响图
根据图6所示,Bi2O3粉末粒径随着氧化室内温度的增加而逐渐降低。温度在900℃~1 200℃间时,Bi2O3粉末粒径的变化程度较大;温度在1 200℃~1 400℃间时,Bi2O3粉末粒径的变化程度较小,因此,可设定氧化室内的温度为1 200℃。
当氧化室内的温度为1 200℃时,氧化室内的气体流量的变化对Bi2O3粉末平均粒径的影响如图7所示。
根据图7所示,Bi2O3粉末粒径随着氧化室内氧气的气体流量的增大而逐步变大,但对Bi2O3粉末粒径大小的影响程度有限。在实际生产的过程中,氧化室内气体流量的大小对于Bi2O3的产量具有重要的影响作用,如果气体流量较大,则冷却室对产生的Bi2O3的冷却速率不够会导致Bi2O3的粒径较大;如果气体流量较小,会导致Bi2O3的产量明显下降,因此,可设定氧化室内氧气的气体流量为12L/min。

图7 氧化室内氧化气体流量对Bi2 O3粉末平均粒径的影响图
3.3 冷却室对Bi2 O3粉末制备的影响
冷却室对Bi2O3粉末制备产生影响的关键因素在于冷却速度是否与Bi2O3粉末生成的速率匹配。图8显示了冷却气体的流量对Bi2O3粉末平均粒径的影响。

图8 冷却室内冷却气体对Bi2O3粉末平均粒径的影响图
根据图8所示,Bi2O3粉末平均粒径随着冷却气体流量的增大而逐步减小。当冷却气体的流量在80L/min~120L/min的范围时,Bi2O3粉末粒径的变化程度较大;当冷却气体的流量在120L/min~140L/min的范围时,Bi2O3粉末粒径的变化程度较小,因此,可设定冷却气体的流量为120 L/min。
3.4 实验室条件下制备的Bi2 O3粉末的XRD分析
对实验室条件下制备的Bi2O3粉末的XRD分析图谱如图9所示。
通过比对Bi2O3粉末的XRD分析图谱与标准的PDF卡可知,实验室条件下制备的Bi2O3粉末为四方晶系的Bi2O3,所得产品为β-型球状超细Bi2O3粉末。

图9 Bi2 O3粉末的XRD分析图谱
4 结语
通过在实验室条件下对Bi2O3粉末的制备,并对制备Bi2O3粉末方法中所涉的各要素进行了深入的分析,总结如下。
(1)通过对铋溶体的蒸发速率的理论分析可知当温度1 140℃时,配合以适当的压力,可获得铋的蒸发速率为5g/(cm2·min),也就是说,该蒸发速率满足了制备Bi2O3粉末的要求。
(2)通过研究实验室条件下制备Bi2O3粉末过程中,等离子体发生器、氧化室、冷却室中等环境因素的影响,从而确定了制备β-型球状超细Bi2O3粉末所需的环境,即是等离子体发生器内的温度为1 200℃、压力为0.08MPa,氧化室内的气体流量为12L/min,冷却室内的气体流量为气体流量为120L/min。
[1]白猛,郑雅杰,洪波,张博亚,张传福.漂浮阳极泥中铋的提取与三氧化二铋的制备[J].中南大学学报(自然科学版),2012,43(5):1621-1627.
[2]丘克强,段文军,陈启元.金属在真空状态下的蒸发速率[J].有色金属,2002,54(2):48-54.
[3]郑雅杰,滕浩,白猛.以高砷精炼铋烟尘为原料制备高纯氯氧化锑[J].中南大学学报(自然科学版),2011,42(6):1549-1553.

