自身免疫性胰腺炎的多层螺旋CT表现(附5例分析)
1.中山大学肿瘤防治中心(中山大学附属肿瘤医院) (广东 广州 510060) 2.中山大学附属第一医院(广东 广州 510055)
周 健1 彭振鹏2 冯仕庭2李子平2
自身免疫性胰腺炎的多层螺旋CT表现(附5例分析)
1.中山大学肿瘤防治中心(中山大学附属肿瘤医院) (广东 广州 510060) 2.中山大学附属第一医院(广东 广州 510055)
周 健1彭振鹏2冯仕庭2李子平2
目的探讨自身免疫性胰腺炎(autoimmune pancreatitis,AIP)的多层螺旋CT表现。方法回顾性分析5例经病理证实或临床治疗后随访证实的自身免疫性胰腺炎的64层螺旋CT表现。结果5例自身免疫性胰腺炎中3例(60%)胰腺弥漫性肿大,呈“腊肠状”,其中1例(20%)胰头部明显肿大,疑似肿物形成。1例(20%)胰腺体尾部局限性肿大。1例(20%)胰腺未见明显肿大。3例(60%)胰周筋膜模糊,其中2例(40%)胰周见少许渗出性积液,1例(20%)胰周见低密度环状包膜影,即“胶囊征”。4例(80%)胰腺密度均匀。1例(20%)胰头部见斑点状钙化。5例(100%)胰腺中度均匀强化。4例(80%)胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变,其中2例(40%)伴有胰管轻度扩张。1例(20%)仅表现胰管轻度扩张。2例(40%)累及单侧肾周筋膜,肾周筋膜模糊。1例(20%)累及单侧肾盂,表现为肾盂增大,内见低密度软组织肿块影,增强扫描肿块轻度强化。结论多层螺旋CT可以用于诊断自身免疫性胰腺炎,可用于评估胰腺外病变及胰腺治疗后改变。
自身免疫疾病;胰腺炎;体层摄影术, X线计算机
自身免疫性胰腺炎(autoimmune pancreatitis,AIP)是由于自身免疫机制导致的一类特殊的慢性胰腺炎,1961年Sarles等首先报道,Yoshida等1995年将其正式命名为自身免疫性胰腺炎[1-2]。其使用糖皮质激素治疗有效,但术前易被误诊为胰腺癌而行手术切除。本文收集经病理证实或临床治疗后随访证实的自身免疫性胰腺炎5例,对其64层螺旋CT资料进行回顾性分析,旨在提高对本病多层螺旋CT表现的认识,指导临床治疗。
1 资料与方法
1.1 资料搜集2009年5月至2013年12月中山大学附属第一医院经病理证实或临床治疗后随访证实的自身免疫性胰腺炎5例,其中男性4例,女性1例,年龄22~61岁,平均年龄47岁,1例患者有系统性红斑狼疮病史。所有病例均行64层螺旋CT多期平扫及增强扫描。3例经超声内镜穿刺病理活检均提示:少量炎症细胞,未见恶性特征。2例经临床、实验室检查、影像学表现及激素规范治疗后随访确诊。
1.2 扫描方案采用Toshiba Aquilion64层螺旋CT扫描仪,扫描范围自膈顶至双侧肾脏下极,管电压120KV,管电流200mA,数据采集为64层×0.5mm薄层扫描,获得原始容积数据后,以层厚1mm进行重建。采用非离子型碘对比剂(碘普罗胺注射液,300mgI/ml),剂量为1.5~2.0ml/kg,经肘前静脉双筒高压注射器注射,注射流率3.5~4.0ml/s,自开始注射对比剂后分别于25s、60s对病灶进行动脉期、门脉期动态增强扫描。
1.3 图像分析所有图像均经两位经验丰富的放射诊断医师独立阅片,以一致的意见为分析结果,对以下方面内容进行评价:(1)胰腺形态改变;(2)胰周筋膜改变,是否可见“胶囊征”;(3)胰腺密度改变;(4)胰管改变;(5)胰腺外改变。
2 结 果
2.1 胰腺形态改变分为弥漫肿大型、局限肿大型和混合型。本组5例中,3例(60%)胰腺弥漫性肿大(图1),呈“腊肠状”,其中1例(20%)胰头部明显肿大,疑似肿物形成(图2)。1例(20%)胰腺体尾部局限性肿大。1例(20%)胰腺未见明显肿大。
2.2 胰周筋膜改变3例(60%)胰周筋膜模糊,其中2例(40%)胰周见少许渗出性积液,1例(20%)胰周见低密度环状包膜影,延迟扫描可见强化,即“胶囊征”(图3)。
2.3 胰腺密度改变4例(80%)胰腺密度均匀,1例(20%)胰头部见斑点状钙化(图4)。5例(100%)胰腺中度均匀强化(图5)。
2.4 胰管改变4例(80%)胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变(图6),其中2例(40%)伴有胰管轻度扩张。1例(20%)仅表现胰管轻度扩张。
2.5 胰腺外改变2例(40%)累及单侧肾周筋膜,肾周筋膜模糊(图7)。1例(20%)累及单侧肾盂,表现为肾盂增大,内见低密度软组织肿块影,增强扫描肿块轻度强化(图8、9)。经激素治疗后,5例均表现为胰腺体积缩小,胰周脂肪间隙清晰(图10)。1例胰腺尾部周围见少许条索影。2例累及单侧肾周筋膜的患者表现为肾周筋膜较前清晰。1例累及单侧肾盂的患者表现为肾盂软组织肿块较前减小。
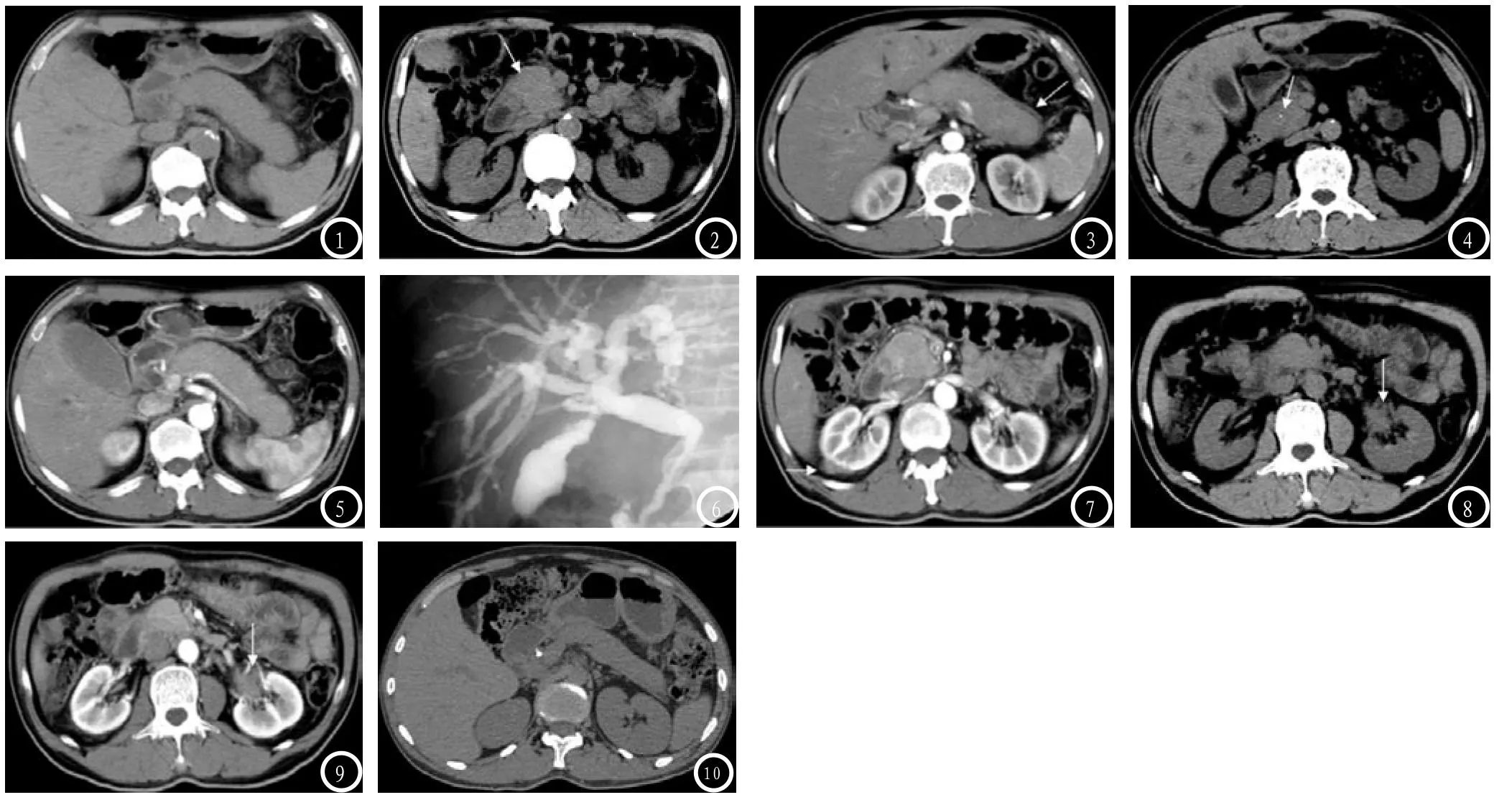
图1 胰腺弥漫性肿大,呈“腊肠状”。图2 胰头部明显肿大,疑似肿物形成。图3 胰周见低密度环状包膜影,增强扫描延迟期可见强化,即“胶囊征”。图4 胰头部见斑点状钙化。图5 增强扫描胰腺呈中度均匀强化。图6 胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变。图7 右后肾周筋膜模糊。图8 左侧肾盂增大,内见低密度软组织肿块影。图9 左侧肾盂内低密度软组织肿块增强扫描轻度强化。图10经激素治疗后,胰腺体积缩小,胰周脂肪间隙清晰。
3 讨 论
自身免疫性胰腺炎是胰腺对自身成分作为抗原由CD4阳性辅助细胞的识别产生免疫应答而造成胰腺的炎症性病变。由自身免疫性引起的慢性胰腺炎曾被称为原发性硬化性胰腺炎、淋巴浆细胞硬化性胰腺炎、非酒精性胆道退行性胰腺炎和自身免疫性胰腺炎[3]。自身免疫性胰腺炎好发于中老年男性患者,首发症状常表现为非特异性的上腹痛、梗阻性黄疸以及糖尿病,除胰腺受累外,还可伴发全身多器官受累,如胆道系统、肾脏、腹膜后、唾液腺、肺、纵隔等,分别表现为硬化性胆管炎、肾实质结节灶、腹膜后纤维化、涎腺炎、肺内间质性病变、纵隔及肺门淋巴结肿大等[4,5]。
3.1 临床表现与病理分型根据临床病理表现,自身免疫性胰腺炎可分为1、2两个亚型,1型(淋巴浆细胞硬化性胰腺炎)是以胰腺为表现形式的多器官疾病,属IgG4相关性疾病,对类固醇敏感,但易复发,长期应用小剂量类固醇可减少其复发,不伴粒细胞上皮损伤。2型(特发性导管中心性胰腺炎)与IgG4无关,常见于年轻患者,同样伴有阻塞性黄疸和胰腺炎症,对类固醇敏感,罕有复发,伴有粒细胞上皮损伤,可致中小胰管或腺泡的破坏和闭塞[6]。Kamisawa等研究显示,1型阻塞性黄疸较2型常见,而腹痛和急性胰腺炎较2型少见[7]。
3.2 自身免疫性胰腺炎的临床和影像特点,主要有:(1)血清丙种球蛋白或IgG升高。(2)自身抗体阳性。(3)胰腺弥慢性肿大。(4)主胰管弥漫性不规则狭窄,偶尔伴发胰内段胆管狭窄。(5)淋巴浆细胞浸润和纤维化改变。(6)没有症状或症状轻微。(7)几乎没有胰腺钙化或囊性改变。(8)偶尔伴发其它自身免疫性疾病。(9)对激素治疗敏感,激素治疗后胰腺功能及形态改变均可恢复正常[8]。本组5例病例中,临床症状主要表现为腹痛和身目黄染。3例IgG升高,2例自身抗体阳性,3例胰腺弥漫性肿大,4例胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变,其中2例胰管轻度扩张,3例经超声内镜穿刺病理活检提示淋巴浆细胞浸润和纤维化改变,1例胰头部见斑点状钙化,没有发现胰腺囊性变,1例患者伴发系统性红斑狼疮病史4年,所有患者行激素治疗后胰腺功能、形态及临床症状均明显好转,与自身免疫性胰腺炎的临床和影像特点相符。
3.3 自身免疫性胰腺炎的胰腺病变CT特征,主要表现为:胰腺弥漫性肿大,胰腺密度比较均匀,中度强化,边界模糊,病理检查见间质纤维增生,伴炎症细胞浸润,特别是淋巴浆细胞浸润。胰腺周围有时可见低密度环状包膜影,即“胶囊征”改变,增强扫描延迟期可见强化。Takahashi等人通过一组患者(25例自身免疫性胰腺炎,33例胰腺癌,16例正常胰腺)的双期增强CT扫描得出自身免疫性胰腺炎的CT征象主要包括:①胰腺弥漫性肿大②增强扫描时胰腺强化程度弥漫性减低③胰腺周围可见低密度环状包膜影(“胶囊征”)④增强时胆管壁可见强化⑤胰腺内可见钙化灶,通常表现为典型的1~2个斑点状钙化⑥肾脏受累[9]。“胶囊征”主要为胰腺周围组织淋巴细胞及浆细胞浸润和纤维化改变,其延迟强化是自身免疫性胰腺炎的特征性征象之一[10]。胰腺局限性肿大和胰腺内低密度肿块形成也常见于自身免疫性胰腺炎患者[3]。本组1例患者胰头部见1个斑点状钙化,与Takahashi报道一致。
3.4 自身免疫性胰腺炎的胰腺外病变CT特征肝内外胆管和胰管狭窄。Sahani等人认为肝内外胆管狭窄是自身免疫性胰腺炎患者最常见的胰腺外病变,可达到所有患者的68~90%[3],病理检查胰胆管周围可见大量炎症细胞浸润。本组4例(80%)患者表现为胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变,与文献报道一致。自身免疫性胰腺炎另一个常见的胰腺外病变特征是肾脏受累,在Takahashi报道的一组40例自身免疫性胰腺炎患者中,肾脏受累及的患者达到所有患者总数的35%,肾脏受累可以表现为肾周皮质内的小结节,呈圆形或楔形,或者呈散在的片状改变。Takahashi的报道中有3例病例做了肾脏病理活检,表现为淋巴浆细胞浸润和纤维化改变。本组2例患者均表现为单侧肾周筋膜模糊,未见肾周皮质内的小结节。1例患者表现为单侧肾盂低密度软组织肿块影。经激素治疗后,肾周筋膜较前清晰,肾盂软组织肿块较前减小。少数患者可有胰周淋巴结肿大和胰腺假性囊肿形成,本组病例均没有发现。
3.5 鉴别诊断自身免疫性胰腺炎最重要的是和胰腺癌鉴别,以及和其他慢性胰腺炎鉴别。当自身免疫性胰腺炎炎症比较局限时,很难和胰腺癌鉴别[10,11]。本组3例病例均表现为胰头部明显肿大,胆总管胰腺段逐渐变窄,肝内外胆管“串珠样”改变,可疑胰头部肿瘤。对于难以与胰腺癌鉴别的自身免疫性胰腺炎患者可以在短期内服用大量激素治疗后复查,如果胰腺体积较前减小,胰周脂肪间隙较前清晰,则诊断为自身免疫性胰腺炎而非胰腺癌,必要时需要进行穿刺活检病理检查明确诊断。弥漫性自身免疫性胰腺炎与淋巴瘤鉴别比较困难,它们都表现为胰腺实质弥漫性肿大,增强时强化程度较低,因此,鉴别诊断需要依靠其它的发现,如腹膜后和盆腔增大的淋巴结,或者是脾脏也发现病灶,必要时需要靠细针穿刺活检来明确诊断[12,13]。弥漫性自身免疫性胰腺炎还要和浆细胞瘤、转移瘤以及弥漫浸润性胰腺癌相鉴别[3]。
1. 陈赟,丁玖乐,邢伟.自身免疫性胰腺炎CT和MRI表现分析[J].中国CT和MRI杂志, 2013,11(3): 22-23.
2. Yoshida K, Toki F, Takeuchi T, et al. Chronic pancreatitis caused by an autoimmune abnormality: proposal of the concept of autoimmune pancreatitis[J].Dig Dis Sci, 1995, 40: 1561-1568.
3. Sahani DV, Kalva SP, Farrell J, et al. Autoimmune pancreatitis: imaging features[J].Radiology, 2004, 233: 345-352.
4. Kamisawa T, Egawa N, Nakajima H, et al. Extrapancreatic lesions in autoimmune pancreatitis[J].J Clin Gastroenterol, 2005, 39: 904-907.
5. Bodily KD,Takahashi N, Fletcher JG, et al. Autoimmune pancreatitis: pancreatic and extrapancreatic imaging findings[J].AJR,2009,192:431-437.
6. 黄颖秋.自身免疫性胰腺炎的研究进展[J].世界华人消化杂志,2013, 21: 3505-3513.
7. Kamisawa T, Chari ST, Giday SA, et al. Clinical profile of autoimmune pancreatitis and its histological subtypes: an international multicenter survey[J].Pancreas 2011,40: 809-814.
8. Okazaki K, Chiba T. Autoimmune related pancreatitis[J].Gut, 2002, 51:1-4.
9. Takahashi N, Fletcher JG, Fidler JL, et al. Dual-Phase CT of Autoimmune Pancreatitis: A Multireader Study[J].AJR, 2008, 190: 280-286.
10.崔庆周,郭宏强.CT应用于胰腺癌与自身免疫性胰腺炎的鉴别价值研究[J]中国CT和MRI杂志,2015,13(4): 73-75.
11.王静波,向子云,詹勇,等.自身免疫性胰腺炎与胰腺癌的CT鉴别诊断价值[J]中国CT和MRI杂志,2011,9(2): 45-48.
12.Riccardo M, Rossella G, Calogero C, et al. Autoimmune Pancreatitis: CT Patterns and Their Changes after Steroid Treatment[J].Radiology, 2008, 247: 435-443.
13.罗益贤,陆普选,乐晓华,等.艾滋病相关淋巴瘤的影像学表现[J]罕少疾病杂志,2015,(2): 58-61.
(本文编辑: 黎永滨)
MSCT Characteristics of Autoimmune Pancreatitis (Imaging Findings in Five Cases)
ZHOU Jian1, PENG Zhen-peng2, FENG Shi-ting2, LI Zi-ping2. 1 Medical Imaging and Minimally Invasive Interventional Center, Sun Yat-sen University Cancer Center; State Key Laboratory of Oncology in South China; Collaborative Innovation Center for Cancer Medicine, Guangzhou 510060, China; 2 Department of Radiology, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, China
ObjectiveTo evaluate the MSCT characteristics of autoimmune pancreatitis.MethodsFive autoimmune pancreatitis patients confirmed by pathology or clinical were retrospectively analyzed by the 64-slice spiral CT.ResultsDiffuse swelling of pancreas was found in three patients, just as sausage-shaped. Among them one case of the pancreatic head show obvious swelling, suspected neoplasm. Obvious pancreatic body and tail swelling in one patient. No significant swelling of the pancreas in one patient. Minimal peripancreatic stranding in three patients, peripancreatic fluid collection in two patients, focal enlargement with a capsule-like rim in one patient. Four patients showed homogeneous pancreatic density. One patient can be seen calification in the the pancreatic head . Pancreas showed mild homogeneous enhancement in all five patients.Distal common bile duct stricture can be seen in four patients as string-of-beads changes, with slight expansion of the pancreatic duct in two patients. One patient only showing pancreatic duct mild expansion. Two patients with extraparenchymal renal involment, showing perirenal stranding. One patient with renal pelvis involment, showing low density inflammatory mass and mild homogeneous enhancement.ConclusionsMSCT can be used for the diagnosis of autoimmune pancreatitis, and also can be used to assess extrapancreatic lesions and pancreatic changes after treatment.
Autoimmune Diseases; Pancreatitis; Tomography, X-ray Computed
10.3969/j.issn.1672-5131.2015.08.022
R814.42;R576
A
2015-07-08
李子平

